1 . (Ⅰ)已知A为常见的金属单质。B俗称磁性氯化铁。根据如图所示的关系:
B:_______ D:_______ 。
(2)写出③的离子方程式:_______ 。
(3)写出④的化学方程式:_______ 。
(4)写出⑤的化学方程式:_______ 。
(5)写出E→F的现象_______ 。
写出E→F的化学方程式_______ 。
(Ⅱ)某兴趣小组同学为探究黑木耳中的含铁量,进行如下实验。已知:
ⅰ.黑木耳富含蛋白质、糖类、卵磷脂、铁及一些还原性物质等。每100克黑木耳含铁高达185毫克。
ⅱ.紫色的 溶液在酸性条件下有强氧化性,其还原产物是无色的
溶液在酸性条件下有强氧化性,其还原产物是无色的 。
。
ⅲ. 与铁氰化钾(
与铁氰化钾(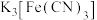 )溶液反应生成蓝色沉淀。
)溶液反应生成蓝色沉淀。
为确定黑木耳中含有铁元素,甲同学设计实验方案如图。_______ 。
(7)步骤④检验 所用试剂是
所用试剂是_______ 溶液。
(8)下列有关上述实验得出的结论正确的是_______ (填字母符号)。
a.黑木耳中一定含 和
和
b.滤液A中一定含 和
和
c.白色沉淀中一定含
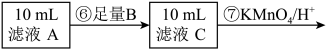
为测定黑木耳中铁元素的含量,乙同学设计实验方案如下。
(10)步骤⑦中观察到的实验现象是_______ ,反应的离子方程式是_______ 。

B:
(2)写出③的离子方程式:
(3)写出④的化学方程式:
(4)写出⑤的化学方程式:
(5)写出E→F的现象
写出E→F的化学方程式
(Ⅱ)某兴趣小组同学为探究黑木耳中的含铁量,进行如下实验。已知:
ⅰ.黑木耳富含蛋白质、糖类、卵磷脂、铁及一些还原性物质等。每100克黑木耳含铁高达185毫克。
ⅱ.紫色的
 溶液在酸性条件下有强氧化性,其还原产物是无色的
溶液在酸性条件下有强氧化性,其还原产物是无色的 。
。ⅲ.
 与铁氰化钾(
与铁氰化钾(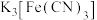 )溶液反应生成蓝色沉淀。
)溶液反应生成蓝色沉淀。为确定黑木耳中含有铁元素,甲同学设计实验方案如图。
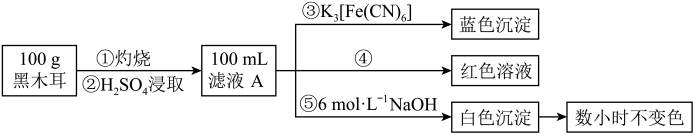
(7)步骤④检验
 所用试剂是
所用试剂是(8)下列有关上述实验得出的结论正确的是
a.黑木耳中一定含
 和
和
b.滤液A中一定含
 和
和
c.白色沉淀中一定含

为测定黑木耳中铁元素的含量,乙同学设计实验方案如下。
| A.Na | B.Zn | C.Fe | D.Cu |
(10)步骤⑦中观察到的实验现象是
您最近一年使用:0次
名校
解题方法
2 . 闽盐集团晾晒海水获得的粗盐中含有可溶性杂质 、
、 、
、 等。粗盐提纯的工艺流程如下,下列说法正确的是
等。粗盐提纯的工艺流程如下,下列说法正确的是
 、
、 、
、 等。粗盐提纯的工艺流程如下,下列说法正确的是
等。粗盐提纯的工艺流程如下,下列说法正确的是
A.“步骤I”中试剂1为 溶液,试剂2为 溶液,试剂2为 溶液 溶液 |
| B.“步骤I”生成的沉淀只能一次性过滤,不能分步过滤 |
| C.“步骤II”试剂3可以用稀硫酸代替稀盐酸 |
| D.“步骤II”从滤液中获得精盐的方法是蒸发结晶 |
您最近一年使用:0次
2024-02-04更新
|
139次组卷
|
5卷引用:天津市滨海新区田家炳中学2023-2024学年高一下学期第一次月考化学试题
名校
解题方法
3 . 黄铜灰渣(含有Cu、Zn、 、
、 及少量
及少量 、
、 、
、 )生产
)生产 溶液的流程如下图所示。
溶液的流程如下图所示。
(1)写出“浸取”时 反应的离子方程式:
反应的离子方程式:___________ 。
(2)过滤Ⅰ后所得滤液中___________ (填“含”或“不含”) ,用离子方程式解释为:
,用离子方程式解释为:___________ 。
(3)检验“滤液Ⅱ”中由铁元素形成的阳离子的方法是___________ 。该阳离子的溶液和氢氧化钠溶液反应的现象是___________ ;此现象对应的化学方程式是___________
(4)“反应Ⅱ”所用稀硝酸可由质量分数为63%、密度为 的浓硝酸稀释获得。
的浓硝酸稀释获得。
①该浓硝酸的物质的量浓度为___________  ,若要获得
,若要获得 的稀硝酸,需要用到浓硝酸的体积为
的稀硝酸,需要用到浓硝酸的体积为___________ mL。
② 是一种无色气体,依据信息写出“反应Ⅱ”的化学方程式:
是一种无色气体,依据信息写出“反应Ⅱ”的化学方程式:___________ 。
 、
、 及少量
及少量 、
、 、
、 )生产
)生产 溶液的流程如下图所示。
溶液的流程如下图所示。
(1)写出“浸取”时
 反应的离子方程式:
反应的离子方程式:(2)过滤Ⅰ后所得滤液中
 ,用离子方程式解释为:
,用离子方程式解释为:(3)检验“滤液Ⅱ”中由铁元素形成的阳离子的方法是
(4)“反应Ⅱ”所用稀硝酸可由质量分数为63%、密度为
 的浓硝酸稀释获得。
的浓硝酸稀释获得。①该浓硝酸的物质的量浓度为
 ,若要获得
,若要获得 的稀硝酸,需要用到浓硝酸的体积为
的稀硝酸,需要用到浓硝酸的体积为②
 是一种无色气体,依据信息写出“反应Ⅱ”的化学方程式:
是一种无色气体,依据信息写出“反应Ⅱ”的化学方程式:
您最近一年使用:0次
名校
解题方法
4 . 海水资源开发利用的部分过程如图所示。下列说法正确的是
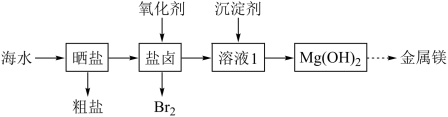
A.向盐卤中通入的氧化剂可以是 | B.工业生产中常选用NaOH作为沉淀剂 |
| C.粗盐可采用沉淀、过滤和结晶等过程提纯 | D.常用电解熔融氧化镁的方法制备金属Mg |
您最近一年使用:0次
名校
解题方法
5 . 硫酸亚铁晶体 在医药上做补血剂。某课外小组测定该补血剂中铁元素的含量,并检验该补血剂是否变质。实验步骤如下:
在医药上做补血剂。某课外小组测定该补血剂中铁元素的含量,并检验该补血剂是否变质。实验步骤如下:
(1)向操作①的滤液中滴加 溶液后变为红色,则该滤液中含有
溶液后变为红色,则该滤液中含有_______ (填离子符号)。
(2)操作②中反应的离子方程式:_______ 。
(3)操作③中反应的离子方程式:_______ 。
(4)操作④中系列操作的步骤:过滤、_______ 、_______ 、灼烧、冷却至室温、称量。
(5)假设实验中的损耗忽略不计,则每片补血剂含铁元素的质量为_______ g(用含a的代数式表示)。
 在医药上做补血剂。某课外小组测定该补血剂中铁元素的含量,并检验该补血剂是否变质。实验步骤如下:
在医药上做补血剂。某课外小组测定该补血剂中铁元素的含量,并检验该补血剂是否变质。实验步骤如下: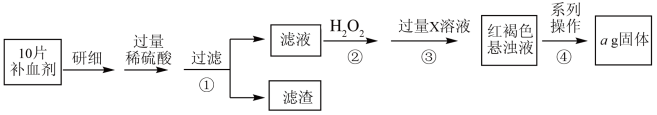
(1)向操作①的滤液中滴加
 溶液后变为红色,则该滤液中含有
溶液后变为红色,则该滤液中含有(2)操作②中反应的离子方程式:
(3)操作③中反应的离子方程式:
(4)操作④中系列操作的步骤:过滤、
(5)假设实验中的损耗忽略不计,则每片补血剂含铁元素的质量为
您最近一年使用:0次
2023-12-14更新
|
168次组卷
|
2卷引用:天津市新华中学2023-2024学年高一上学期第二次月考化学试卷
名校
解题方法
6 . 利用废旧镀锌铁皮制备 胶体粒子的流程如图所示,已知:
胶体粒子的流程如图所示,已知: 溶于强碱时生成易溶于水的
溶于强碱时生成易溶于水的 ,下列说法正确的是
,下列说法正确的是

 胶体粒子的流程如图所示,已知:
胶体粒子的流程如图所示,已知: 溶于强碱时生成易溶于水的
溶于强碱时生成易溶于水的 ,下列说法正确的是
,下列说法正确的是
| A.用氢氧化钠溶液处理废旧镀锌铁皮,主要目的是为了处理表面的油污 |
B.“酸溶”的离子方程式为 |
C.“氧化”后溶液中存在的阳离子有 、 、 、 、 |
D. 胶体粒子可通过过滤操作得到 胶体粒子可通过过滤操作得到 |
您最近一年使用:0次
2023-12-02更新
|
223次组卷
|
3卷引用:天津市第一中学2023-2024学年高一上学期期末考试化学试卷
解题方法
7 . 下列除去杂质的方法正确的是
①除去乙烷中少量的乙烯:光照条件下通入 ,气液分离;
,气液分离;
②除去 中少量的
中少量的 :气体通过盛饱和碳酸钠溶液的洗气瓶;
:气体通过盛饱和碳酸钠溶液的洗气瓶;
③除去乙醇中少量的乙酸:加足量生石灰,蒸馏。
④除去乙酸乙酯中少量的乙酸:用饱和碳酸钠溶液分液;
①除去乙烷中少量的乙烯:光照条件下通入
 ,气液分离;
,气液分离;②除去
 中少量的
中少量的 :气体通过盛饱和碳酸钠溶液的洗气瓶;
:气体通过盛饱和碳酸钠溶液的洗气瓶;③除去乙醇中少量的乙酸:加足量生石灰,蒸馏。
④除去乙酸乙酯中少量的乙酸:用饱和碳酸钠溶液分液;
| A.①② | B.②④ | C.③④ | D.②③ |
您最近一年使用:0次
名校
解题方法
8 . 已知海水中的溴含量约为65mg•L-1,从海水中提取溴的工业流程如图:

(1)请列举海水淡化的两种方法:_______ 、_______ 。
(2)上述步骤Ⅰ中已获得游离态的溴,步骤Ⅱ又将其转化成化合态的溴,目的是_______ 。
(3)步骤Ⅱ通入热空气吹出Br2,利用了溴的 _______。(填字母)
(4)步骤Ⅱ中涉及的离子反应如下,请在方框内填入正确的化学计量数:_______ 。
_______Br2+_______CO ═_______BrO
═_______BrO +_______Br-+_______CO2↑
+_______Br-+_______CO2↑
(5)上述流程中吹出的溴蒸气也可以先用二氧化硫的水溶液吸收,再用氯气氧化,然后进行蒸馏,则溴与二氧化硫的水溶液反应的离子方程式为_______ 。
(6)实验室分离溴还可以用萃取法,下列可以用作溴的萃取剂的有_______(填字母)。

(1)请列举海水淡化的两种方法:
(2)上述步骤Ⅰ中已获得游离态的溴,步骤Ⅱ又将其转化成化合态的溴,目的是
(3)步骤Ⅱ通入热空气吹出Br2,利用了溴的 _______。(填字母)
| A.氧化性 | B.还原性 | C.挥发性 | D.腐蚀性 |
_______Br2+_______CO
 ═_______BrO
═_______BrO +_______Br-+_______CO2↑
+_______Br-+_______CO2↑(5)上述流程中吹出的溴蒸气也可以先用二氧化硫的水溶液吸收,再用氯气氧化,然后进行蒸馏,则溴与二氧化硫的水溶液反应的离子方程式为
(6)实验室分离溴还可以用萃取法,下列可以用作溴的萃取剂的有_______(填字母)。
| A.乙醇 | B.四氯化碳 | C.裂化汽油 | D.苯 |
您最近一年使用:0次
名校
解题方法
9 . 某研究小组以工厂废渣(Fe3O4、Al2O3、SiO2)为原料制取Fe2O3工艺流程如图。回答下列问题:

(1)“碱浸”时可能发生反应的化学方程式为_______ 。“酸溶”时发生反应的化学方程式为_______ 。
(2)“操作a”的名称为_______ ,用到的玻璃仪器有玻璃棒、_______ 。
(3)“氧化”的目的是_______ 。_______ (填能或否)用H2O2代替O2。
(4)“沉铁”步骤可观察到现象是_______ 。
(5)操作c中所发生的化学反应方程式为_______ 。

(1)“碱浸”时可能发生反应的化学方程式为
(2)“操作a”的名称为
(3)“氧化”的目的是
(4)“沉铁”步骤可观察到现象是
(5)操作c中所发生的化学反应方程式为
您最近一年使用:0次
名校
10 . 下列实验操作不能达到实验目的的是
| 实验目的 | 实验操作、现象 | |
| A | 制备Fe(OH)3胶体 | 将饱和的FeCl3溶液滴入沸水中,并继续煮沸至生成红褐色液体 |
| B | 除去MgCl2溶液中的AlCl3 | 在MgCl2溶液中加入适量NaOH溶液搅拌、过滤 |
| C | 除去Cu粉中混有的CuO | 在混合物中加入稀硫酸,充分反应后过滤、洗涤、干燥 |
| D | 比较氯和碘的非金属性 | 将少量氯气通入碘化钾溶液中,溶液颜色加深 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



