名校
1 . 我国近代化学工业英基人侯德榜先生设计出“侯氏制碱法”,提高了食盐的转化率,缩短了生产流程,减少了对环境的污染。钢仁一中化学实验社团模拟“侯氏制碱法”开展如下项目式学习:
项目一:粗盐的提纯
粗盐中除了含有泥沙之外,还含有少量 等杂质离子,粗盐提纯的流程如图所示:
等杂质离子,粗盐提纯的流程如图所示: 分别为足量的
分别为足量的_____________ 、_____________ 。
(2)操作2的名称是_____________________ 。
(3)“滤液”中加入足量的试剂 生成气泡的离子方程式为
生成气泡的离子方程式为_____________________________ 。
项目二:模拟“侯氏制碱法“利用上述实验制得的 全部用于制备纯碱,工艺流程如图所示:
全部用于制备纯碱,工艺流程如图所示:

(4)氮化和碳酸化过程在如图所示装置中进行, 导管应通入的气体是
导管应通入的气体是_____________ (填化学式),仪器 的作用是
的作用是_____________________________________________ 。
(5)写出煅烧固体时发生的化学方程式:_________________________________________________ 。
(6)称取了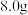 粗盐进行实验,最终制得
粗盐进行实验,最终制得 纯碱,假设完全转化,则粗盐的纯度是
纯碱,假设完全转化,则粗盐的纯度是_________  。(保留2位有效数字)
。(保留2位有效数字)
项目一:粗盐的提纯
粗盐中除了含有泥沙之外,还含有少量
 等杂质离子,粗盐提纯的流程如图所示:
等杂质离子,粗盐提纯的流程如图所示:
 分别为足量的
分别为足量的(2)操作2的名称是
(3)“滤液”中加入足量的试剂
 生成气泡的离子方程式为
生成气泡的离子方程式为项目二:模拟“侯氏制碱法“利用上述实验制得的
 全部用于制备纯碱,工艺流程如图所示:
全部用于制备纯碱,工艺流程如图所示:
(4)氮化和碳酸化过程在如图所示装置中进行,
 导管应通入的气体是
导管应通入的气体是 的作用是
的作用是(5)写出煅烧固体时发生的化学方程式:
(6)称取了
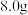 粗盐进行实验,最终制得
粗盐进行实验,最终制得 纯碱,假设完全转化,则粗盐的纯度是
纯碱,假设完全转化,则粗盐的纯度是 。(保留2位有效数字)
。(保留2位有效数字)
您最近一年使用:0次
解题方法
2 . 镁及其合金是用途很广泛的金属材料。大量的镁是从海水中提取的,从海水中提取镁的主要步骤如图所示。

回答下列问题:
(1) 在水中的电离方程式为
在水中的电离方程式为___________ 。
(2)氯化钠属于________ (填“离子”或“共价”)化合物,其形成过程可表示为_________ 。
(3) 与盐酸反应的离子方程式为
与盐酸反应的离子方程式为___________ 。
(4)在 、NaCl、NaOH的混合溶液中:
、NaCl、NaOH的混合溶液中:
①验证该混合溶液中含有 的方法及现象为
的方法及现象为___________ 。
②NaOH中存在的化学键为___________ 。
③将少量的氧化铝投入该混合溶液中,发生反应的化学方程式为___________ 。
(5)电解熔融氯化镁时,每生成1.2gMg,同时转移的电子数为____  。
。

回答下列问题:
(1)
 在水中的电离方程式为
在水中的电离方程式为(2)氯化钠属于
(3)
 与盐酸反应的离子方程式为
与盐酸反应的离子方程式为(4)在
 、NaCl、NaOH的混合溶液中:
、NaCl、NaOH的混合溶液中:①验证该混合溶液中含有
 的方法及现象为
的方法及现象为②NaOH中存在的化学键为
③将少量的氧化铝投入该混合溶液中,发生反应的化学方程式为
(5)电解熔融氯化镁时,每生成1.2gMg,同时转移的电子数为
 。
。
您最近一年使用:0次
解题方法
3 . 硫酸亚铁可用作农药防治小麦黑穗病、制造磁性氧化铁、铁催化剂等。工业上用赤铁矿(含 及
及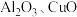 等杂质)制备
等杂质)制备 的工艺流程如图;
的工艺流程如图;

回答下列问题:
(1)赤铁矿在“碱浸”前先要粉碎,其目的是_____________ 。
(2)“碱浸”的作用是_____________ 。
(3)试剂a为_____________ (填化学式),“滤渣”的成分为_____________ (填化学式)。
(4)“还原”中涉及的离子反应方程式为_____________ 、_____________ 。
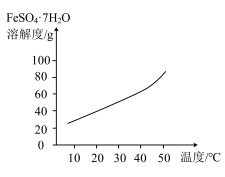
(5)已知 的溶解度曲线如图所示,为得到
的溶解度曲线如图所示,为得到 晶体,“一系列操作”为蒸发浓缩、
晶体,“一系列操作”为蒸发浓缩、_____________ 、过滤、洗涤、干燥。
(6) 溶液久置后会变质,原因是
溶液久置后会变质,原因是_____________ ,为了检验久置的 溶液是否变质,可选用的试剂是
溶液是否变质,可选用的试剂是_____________ (填化学式)溶液。
 及
及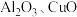 等杂质)制备
等杂质)制备 的工艺流程如图;
的工艺流程如图;
回答下列问题:
(1)赤铁矿在“碱浸”前先要粉碎,其目的是
(2)“碱浸”的作用是
(3)试剂a为
(4)“还原”中涉及的离子反应方程式为
(5)已知
 的溶解度曲线如图所示,为得到
的溶解度曲线如图所示,为得到 晶体,“一系列操作”为蒸发浓缩、
晶体,“一系列操作”为蒸发浓缩、
(6)
 溶液久置后会变质,原因是
溶液久置后会变质,原因是 溶液是否变质,可选用的试剂是
溶液是否变质,可选用的试剂是
您最近一年使用:0次
4 . 化学小组同学为研究氯气制备和氯水的成分及性质进行了如下实验。
【实验1】制备氯气。如图是实验室制取纯净、干燥氯气的装置图。
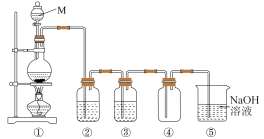
(1)M的名称是___________ ,①中反应的化学方程式是___________ 。
(2)③中存放的试剂是___________ 。(填“浓硫酸”或“饱和食盐水”)
(3)⑤中NaOH溶液的作用是___________ 。
【实验1】制备氯气。如图是实验室制取纯净、干燥氯气的装置图。

(1)M的名称是
(2)③中存放的试剂是
(3)⑤中NaOH溶液的作用是
您最近一年使用:0次
5 . 海洋是一个有待开发的巨大化学资源宝库,海水中元素种类很多,总储量很大,可以从海水中提取镁、溴,主要流程如下。

回答下列问题:
(1)通入的气体X是_______(填字母)。
(2)海水提取溴单质③~④的目的是使溴元素得到_______ 。工业生产中,用SO2吸收吹出的溴,化学方程式为: ,可改写为离子方程式
,可改写为离子方程式_______ 。
(3)从海水中也可以提取镁,将MgSO4转化成Mg(OH)2时,为了降低成本,试剂M最好选用_______(填字母)。
(4)加入试剂M后,分离得到Mg(OH)2沉淀的操作是_______ ,该操作必须用到的玻璃仪器有:烧杯、漏斗和_______ 。
(5)写出“虚线框”处的化学反应方程式:_______ 。

回答下列问题:
(1)通入的气体X是_______(填字母)。
| A.Cl2 | B.N2 | C.H2 | D.CO |
 ,可改写为离子方程式
,可改写为离子方程式(3)从海水中也可以提取镁,将MgSO4转化成Mg(OH)2时,为了降低成本,试剂M最好选用_______(填字母)。
| A.NaOH | B.Ca(OH)2 | C.Cu(OH)2 | D.KOH |
(5)写出“虚线框”处的化学反应方程式:
您最近一年使用:0次
解题方法
6 . 以废铁屑(含少量 、
、 、
、 等杂质)为原料制备硫酸亚铁晶体的流程如图所示:
等杂质)为原料制备硫酸亚铁晶体的流程如图所示:

已知:酸性溶液中的 容易被空气氧化
容易被空气氧化
(1)实验室需要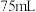 该硫酸,用质量分数为98%、密度为
该硫酸,用质量分数为98%、密度为 的浓硫酸进行配制,需要用到的玻璃仪器有烧杯、玻璃棒、量筒和
的浓硫酸进行配制,需要用到的玻璃仪器有烧杯、玻璃棒、量筒和___________ (填仪器名称),用量筒量取V(浓硫酸)=___________  。
。
(2)“滤渣”的主要成分是___________ (填化学式),“溶液Ⅰ”中的阳离子是___________ (填离子符号)。
(3)写出流程中生成 的反应的化学方程式:
的反应的化学方程式:___________ 。向“溶液Ⅰ”中加入过量 时发生反应的离子方程式为
时发生反应的离子方程式为___________ 。
(4)“操作Ⅲ”的过程是蒸发浓缩、___________ 、___________ 、洗涤、干燥,检验“溶液Ⅱ”中不存在 的试剂是
的试剂是___________ 。
 、
、 、
、 等杂质)为原料制备硫酸亚铁晶体的流程如图所示:
等杂质)为原料制备硫酸亚铁晶体的流程如图所示:
已知:酸性溶液中的
 容易被空气氧化
容易被空气氧化(1)实验室需要
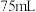 该硫酸,用质量分数为98%、密度为
该硫酸,用质量分数为98%、密度为 的浓硫酸进行配制,需要用到的玻璃仪器有烧杯、玻璃棒、量筒和
的浓硫酸进行配制,需要用到的玻璃仪器有烧杯、玻璃棒、量筒和 。
。(2)“滤渣”的主要成分是
(3)写出流程中生成
 的反应的化学方程式:
的反应的化学方程式: 时发生反应的离子方程式为
时发生反应的离子方程式为(4)“操作Ⅲ”的过程是蒸发浓缩、
 的试剂是
的试剂是
您最近一年使用:0次
名校
7 . I.如图是利用电化学装置将SO2转化为重要的化工原料H2SO4的原理示意图。
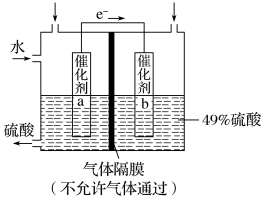
请回答下列问题:
(1)该装置将_______ 能转化为______ 能。
(2)催化剂b表面O2发生_______ 反应,其附近溶液酸性______ (填“增强”、“不变”或“减弱”)。
(3)催化剂a表面的电极反应式:_______ 。
II.某废料铁泥主要成分是Fe2O3、FeO和Fe,其他杂质不与硫酸反应。实验室用该废料提取Fe2O3,设计实验流程如图:

(4)步骤(I)充分反应后进行的实验操作名称是______ 。
(5)步骤(II)中加入H2O2溶液后需要适当加热但温度不能过高,原因是______ 。
(6)为了检验溶液B中是否有亚铁离子剩余,有同学提出只需要取少量溶液B于试管中并向其中滴加氢氧化钠溶液,然后观察现象即可证明。请你判断该同学的方法是否可行并说出理由______ 。
(7)步骤(III)中将NaOH溶液换成氨气也可以得到Fe(OH)3沉淀,反应的离子方程式为______ 。

请回答下列问题:
(1)该装置将
(2)催化剂b表面O2发生
(3)催化剂a表面的电极反应式:
II.某废料铁泥主要成分是Fe2O3、FeO和Fe,其他杂质不与硫酸反应。实验室用该废料提取Fe2O3,设计实验流程如图:

(4)步骤(I)充分反应后进行的实验操作名称是
(5)步骤(II)中加入H2O2溶液后需要适当加热但温度不能过高,原因是
(6)为了检验溶液B中是否有亚铁离子剩余,有同学提出只需要取少量溶液B于试管中并向其中滴加氢氧化钠溶液,然后观察现象即可证明。请你判断该同学的方法是否可行并说出理由
(7)步骤(III)中将NaOH溶液换成氨气也可以得到Fe(OH)3沉淀,反应的离子方程式为
您最近一年使用:0次
2023-05-19更新
|
710次组卷
|
2卷引用:贵州省遵义市仁怀市高中教育联盟2022-2023学年高一下学期5月期中考试化学试题
名校
解题方法
8 . 为不断满足人民群众对美好生活的需要,水资源保护已经成为我国生态建设的重要领域。水处理技术的目的在于使废水经过技术处理后达到再次使用或者排放的水质要求,被广泛应用于工业、农业、环保、餐饮等各个行业,与人们的日常生活密切相关。经检测,某工厂的酸性废水中所含离子及其浓度如下表所示:
回答下列问题:
Ⅰ.
(1)该工业废水中
___________  。
。
Ⅱ.为了减少污染并变废为宝,工程师们设计了如下流程,回收铜和绿矾( )。
)。
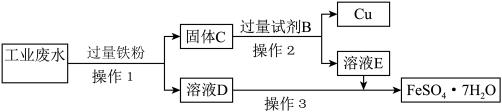
(2)在实验室完成操作1,需用到的玻璃仪器除烧杯、玻璃棒外,还有___________ 。
(3)工业废水中加入铁粉后,反应的离子方程式为 、
、___________ 、___________ 。
(4)试剂B是___________ 。
(5)操作3是蒸发浓缩、___________ 、过滤,最后用少量冷水洗涤晶体,在低温下干燥。
(6)证明溶液E中只含有 而不含
而不含 的实验方法:取少量溶液E于试管中,
的实验方法:取少量溶液E于试管中,___________ (填字母)。
a.先加氯水,再加KSCN溶液后显红色
b.先加KSCN溶液,不显红色,再加氯水后显红色
c.滴加NaOH溶液,只产生白色沉淀,且白色沉淀迅速变为灰绿色,最后呈红褐色
| 离子 |  |  |  |  |  |
浓度/( ) ) |  | 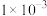 | 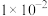 |  |
Ⅰ.
(1)该工业废水中

 。
。Ⅱ.为了减少污染并变废为宝,工程师们设计了如下流程,回收铜和绿矾(
 )。
)。
(2)在实验室完成操作1,需用到的玻璃仪器除烧杯、玻璃棒外,还有
(3)工业废水中加入铁粉后,反应的离子方程式为
 、
、(4)试剂B是
(5)操作3是蒸发浓缩、
(6)证明溶液E中只含有
 而不含
而不含 的实验方法:取少量溶液E于试管中,
的实验方法:取少量溶液E于试管中,a.先加氯水,再加KSCN溶液后显红色
b.先加KSCN溶液,不显红色,再加氯水后显红色
c.滴加NaOH溶液,只产生白色沉淀,且白色沉淀迅速变为灰绿色,最后呈红褐色
您最近一年使用:0次
2023-04-23更新
|
257次组卷
|
2卷引用:贵州省铜仁市2022-2023学年高一上学期期末考试化学试题
名校
解题方法
9 . 菠菜富含膳食纤维、胡萝卜素、维生素c、维生素e、钙、磷、铁、等矿物质。14~18岁青少年每日合理摄入铁量为20~25mg,某化学小组针对菠菜中含铁量进行如下实验。
(一)实验目的:菠菜含铁量是否满足青少年日常所需
(二)实验方案:取适量新鲜菠菜平均分成三份,实验操作和现象记录如下:
(1)灼烧菠菜时,除了酒精灯还需要下列仪器中的_______ (填选项)。
A. B.
B. C.
C. D.
D. E.
E.
(2)写出实验三中 参与的最主要反应的离子方程式
参与的最主要反应的离子方程式_______ 。
(3)检验试剂KSCN溶液中的 采用
采用_______ 的方法。
(4)由三组实验做出如下推断,其中合理的是:_______(填选项)。
(三)实验数据:菠菜中含铁量的测定,实验步骤如下:
①取 新鲜菠菜,充分灼烧,将灰分转移至干燥器中冷却。
新鲜菠菜,充分灼烧,将灰分转移至干燥器中冷却。
②向灰分中加入 盐酸和
盐酸和 ,浸泡
,浸泡 ,过滤并用少量盐酸洗涤烧杯和沉淀,滤液和洗涤液合并;
,过滤并用少量盐酸洗涤烧杯和沉淀,滤液和洗涤液合并;
③将合并液定容成 待测液,利用分光光度法测得铁的浓度为
待测液,利用分光光度法测得铁的浓度为 。
。
根据上述实验,回答下列问题:
(5)步骤②洗涤烧杯和沉淀的目的是_______ 。
(6)步骤③定容操作若仰视容量瓶刻度线,会造成菠菜样品含铁量测定结果_______ 。(填“偏高”、“偏低”或“无影响”)。
(7)根据实验数据计算菠菜含铁量为_______ 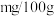 。
。
(四)实验结论:由于菠菜中含有大量草酸( )与铁元素形成沉淀影响铁元素吸收,所以不是理想的补铁剂。(附:猪肝每
)与铁元素形成沉淀影响铁元素吸收,所以不是理想的补铁剂。(附:猪肝每 中含铁量达到
中含铁量达到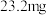 ,且容易被人体吸收。)
,且容易被人体吸收。)
(一)实验目的:菠菜含铁量是否满足青少年日常所需
(二)实验方案:取适量新鲜菠菜平均分成三份,实验操作和现象记录如下:
| 实验 | 操作步骤 | 检验试剂 | 现象 |
| 实验一 | 适量蒸馏水浸泡,过滤,取滤液,加检验试剂后加入适量 ,再次加入检验试剂 ,再次加入检验试剂 | KSCN溶液 | 均无明显现象 |
| 实验二 | 充分灼烧,加适量盐酸浸泡,取滤液,加检验试剂 | KSCN溶液 | 极浅的红色 |
| 实验三 | 充分灼烧,加适量盐酸、 浸泡,取滤液,加检验试剂 浸泡,取滤液,加检验试剂 | KSCN溶液 | 较深的红色 |
A.
 B.
B. C.
C. D.
D. E.
E.
(2)写出实验三中
 参与的最主要反应的离子方程式
参与的最主要反应的离子方程式(3)检验试剂KSCN溶液中的
 采用
采用(4)由三组实验做出如下推断,其中合理的是:_______(填选项)。
| A.菠菜样品中含铁量极低 | B.菠菜中的铁元素很难用蒸馏水直接溶出 |
| C.仅用盐酸无法溶出菠菜灰分中的铁元素 | D.灼烧的目的是将菠菜中的铁元素氧化 |
(三)实验数据:菠菜中含铁量的测定,实验步骤如下:
①取
 新鲜菠菜,充分灼烧,将灰分转移至干燥器中冷却。
新鲜菠菜,充分灼烧,将灰分转移至干燥器中冷却。②向灰分中加入
 盐酸和
盐酸和 ,浸泡
,浸泡 ,过滤并用少量盐酸洗涤烧杯和沉淀,滤液和洗涤液合并;
,过滤并用少量盐酸洗涤烧杯和沉淀,滤液和洗涤液合并;③将合并液定容成
 待测液,利用分光光度法测得铁的浓度为
待测液,利用分光光度法测得铁的浓度为 。
。根据上述实验,回答下列问题:
(5)步骤②洗涤烧杯和沉淀的目的是
(6)步骤③定容操作若仰视容量瓶刻度线,会造成菠菜样品含铁量测定结果
(7)根据实验数据计算菠菜含铁量为
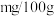 。
。(四)实验结论:由于菠菜中含有大量草酸(
 )与铁元素形成沉淀影响铁元素吸收,所以不是理想的补铁剂。(附:猪肝每
)与铁元素形成沉淀影响铁元素吸收,所以不是理想的补铁剂。(附:猪肝每 中含铁量达到
中含铁量达到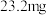 ,且容易被人体吸收。)
,且容易被人体吸收。)
您最近一年使用:0次
2023-03-02更新
|
605次组卷
|
4卷引用:贵州省遵义市南白中学2022-2023学年高一下学期第一次联考化学试题
10 . 工业上“侯氏制碱法”以NaCl、NH3、CO2及水等为原料制备纯碱,其反应原理为:NaCl +NH3+H2O+CO2 =NaHCO3↓+NH4Cl。生产纯碱的工艺流程示意图如下:

(1)上述沉淀池中发生反应的离子方程式_________ ,实验室分离出沉淀的操作名称是_________ ,煅烧炉里进行的化学反应方程式为:_________ 。
(2)写出上述流程中X物质的化学式_________ 。
(3)使原料氯化钠的利用率从70%提高到90%以上,主要是设计了_________ (填上述流程中的循环1或循环2)
(4)为检验产品碳酸钠中是否含有氯离子,可取少量试样溶于水后,还需要的试剂有_________ 。

(1)上述沉淀池中发生反应的离子方程式
(2)写出上述流程中X物质的化学式
(3)使原料氯化钠的利用率从70%提高到90%以上,主要是设计了
(4)为检验产品碳酸钠中是否含有氯离子,可取少量试样溶于水后,还需要的试剂有
您最近一年使用:0次



