名校
1 . 某工业废水中存在大量的H+、Na+、NO 、Cu2+、SO
、Cu2+、SO ,欲提取NaNO3,设计工艺流程如图所示。下列关于流程中物质与反应的说法,正确的是
,欲提取NaNO3,设计工艺流程如图所示。下列关于流程中物质与反应的说法,正确的是
 、Cu2+、SO
、Cu2+、SO ,欲提取NaNO3,设计工艺流程如图所示。下列关于流程中物质与反应的说法,正确的是
,欲提取NaNO3,设计工艺流程如图所示。下列关于流程中物质与反应的说法,正确的是
| A.过程i除去的离子为:Cu2+ |
| B.试剂a为BaCl2 |
| C.沉淀3为BaCO3 |
D.过程iv所涉及的离子反应为:CO +2H+=H2O+CO2↑ +2H+=H2O+CO2↑ |
您最近一年使用:0次
2024-03-01更新
|
183次组卷
|
4卷引用:北京九中2023-2024学年高一下学期开学测试化学试题
北京九中2023-2024学年高一下学期开学测试化学试题北京市中关村中学2023-2024学年高一下学期开学考化学试题(已下线)5.1.3 硫酸根离子检验、粗盐的提纯北京市第十五中学2023-2024学年高一下学期期中考试化学试题
2 . 海洋中有丰富的矿产、能源、水产……等资源,部分化学资源获取途径如下:
(1)下列有关实验室模拟步骤①的说法正确的是___________ 。
a.溶解粗盐时,尽量使溶液稀些,以保证食盐完全溶解
b.滤去不溶性杂质后,将滤液移到坩埚内加热浓缩
c.当蒸发到剩有少量液体时停止加热,利用余热蒸干
d.制得的晶体转移到新过滤器中,需用大量水进行洗涤
(2)“氯碱工业“通过电解饱和食盐水可制得NaOH溶液、Cl2和另一种无色无味的单质气体,该气体的化学式为___________ 。
(3)下列有关说法正确的是___________ (填字母序号)。
a.在第②、③、④步骤中,溴元素均被氧化
b.用澄清的石灰水可鉴别NaHCO3溶液和Na2CO3溶液
c.除去粗盐中Ca2+、 、
、 加入试剂的先后顺序为NaOH、BaCl2、Na2CO3
加入试剂的先后顺序为NaOH、BaCl2、Na2CO3
d.海水中还含有碘元素,将海水中的碘升华可直接制备单质碘
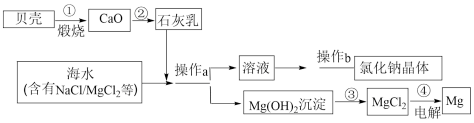
(4)海水获取氯化钠和金属镁的实验流程如图所示,请你根据题意回答下列问题。___________ 。
(二)第①步的化学方程式___________ 。
(三)第③步加入的化学试剂为___________ (填名称)。
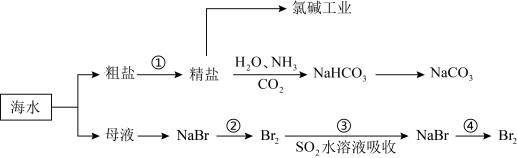
(1)下列有关实验室模拟步骤①的说法正确的是
a.溶解粗盐时,尽量使溶液稀些,以保证食盐完全溶解
b.滤去不溶性杂质后,将滤液移到坩埚内加热浓缩
c.当蒸发到剩有少量液体时停止加热,利用余热蒸干
d.制得的晶体转移到新过滤器中,需用大量水进行洗涤
(2)“氯碱工业“通过电解饱和食盐水可制得NaOH溶液、Cl2和另一种无色无味的单质气体,该气体的化学式为
(3)下列有关说法正确的是
a.在第②、③、④步骤中,溴元素均被氧化
b.用澄清的石灰水可鉴别NaHCO3溶液和Na2CO3溶液
c.除去粗盐中Ca2+、
 、
、 加入试剂的先后顺序为NaOH、BaCl2、Na2CO3
加入试剂的先后顺序为NaOH、BaCl2、Na2CO3d.海水中还含有碘元素,将海水中的碘升华可直接制备单质碘
(4)海水获取氯化钠和金属镁的实验流程如图所示,请你根据题意回答下列问题。
(二)第①步的化学方程式
(三)第③步加入的化学试剂为
您最近一年使用:0次
名校
3 . 草酸亚铁( )常用作照相显影剂,新型电池材料等。
)常用作照相显影剂,新型电池材料等。
(1)以 溶液制备草酸亚铁晶体的实验流程如下:
溶液制备草酸亚铁晶体的实验流程如下:

①配制 溶液时往往加入少量铁粉的原因是
溶液时往往加入少量铁粉的原因是___________ 。
②“转化”步骤的化学方程式为___________ 。
③若该流程中需要使用480mL 0.2000 的草酸溶液,则需要称取
的草酸溶液,则需要称取___________ g草酸晶体( ;配制过程中需要使用的玻璃仪器有玻璃棒、胶头滴管、量筒及
;配制过程中需要使用的玻璃仪器有玻璃棒、胶头滴管、量筒及___________ ,若定容时俯视刻度线,则所配溶液中
___________ 0.2000 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(2)用草酸亚钦晶体在700℃下焙烧反应制备纳米零价铁,反应的化学方程式:
 。当生成1mol Fe时,转移电子的物质的量为
。当生成1mol Fe时,转移电子的物质的量为___________ 。
(3)写出草酸亚铁溶于足量稀硫酸的离子方程式___________ 。
(4)已知: (M=180g/mol)受热分解时,固体质量随温度变化的曲线如图所示。加热到400℃时,固体的成分是
(M=180g/mol)受热分解时,固体质量随温度变化的曲线如图所示。加热到400℃时,固体的成分是___________ (填化学式)。

 )常用作照相显影剂,新型电池材料等。
)常用作照相显影剂,新型电池材料等。(1)以
 溶液制备草酸亚铁晶体的实验流程如下:
溶液制备草酸亚铁晶体的实验流程如下:
①配制
 溶液时往往加入少量铁粉的原因是
溶液时往往加入少量铁粉的原因是②“转化”步骤的化学方程式为
③若该流程中需要使用480mL 0.2000
 的草酸溶液,则需要称取
的草酸溶液,则需要称取 ;配制过程中需要使用的玻璃仪器有玻璃棒、胶头滴管、量筒及
;配制过程中需要使用的玻璃仪器有玻璃棒、胶头滴管、量筒及
 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。(2)用草酸亚钦晶体在700℃下焙烧反应制备纳米零价铁,反应的化学方程式:

 。当生成1mol Fe时,转移电子的物质的量为
。当生成1mol Fe时,转移电子的物质的量为(3)写出草酸亚铁溶于足量稀硫酸的离子方程式
(4)已知:
 (M=180g/mol)受热分解时,固体质量随温度变化的曲线如图所示。加热到400℃时,固体的成分是
(M=180g/mol)受热分解时,固体质量随温度变化的曲线如图所示。加热到400℃时,固体的成分是
您最近一年使用:0次
名校
解题方法
4 . 早在战国时期,《周礼·考工记》就记载了我国劳动人民制取氢氧化钾以漂洗丝帛的工艺,其过程如图所示。下列说法错误的是


| A.操作a为分液 | B.草木灰主要成分属于盐 |
| C.反应过程中未涉及的基本反应类型为置换反应 | D.反应过程中能够循环利用的物质是碳酸钙 |
您最近一年使用:0次
解题方法
5 . 食盐是生活必需品,也是一种工业原料。粗盐含有 、
、 、
、 等杂质。
等杂质。
(1)“粗盐→精盐”过程:
①“除杂1”中反应的离子方程式为____ 。
②试剂X为____ (填化学式)。
③该过程中不涉及的实验操作是____ (填标号)。
A.溶解 B.过滤 C.蒸发 D.渗析
(2)用精盐配制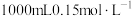 生理盐水的过程:
生理盐水的过程:
①用托盘天平称取 固体的质量为
固体的质量为____ g。
②下列关于配制溶液过程中操作不正确的是_______ (填标号)。 ”过程:
”过程:
①将电解过程发生反应的化学方程式补充完整:______ ,__ ___
___ __
__ __
__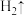 。
。
②在一定条件下 与盐酸反应生成消毒剂
与盐酸反应生成消毒剂 。“有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是:每克含氯消毒剂的氧化能力相当于多少克
。“有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是:每克含氯消毒剂的氧化能力相当于多少克 的氧化能力。则
的氧化能力。则 的有效氯含量为
的有效氯含量为______ g。
 、
、 、
、 等杂质。
等杂质。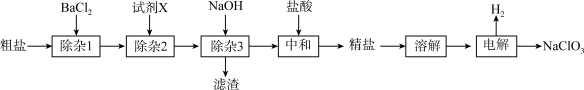
(1)“粗盐→精盐”过程:
①“除杂1”中反应的离子方程式为
②试剂X为
③该过程中不涉及的实验操作是
A.溶解 B.过滤 C.蒸发 D.渗析
(2)用精盐配制
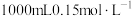 生理盐水的过程:
生理盐水的过程:①用托盘天平称取
 固体的质量为
固体的质量为②下列关于配制溶液过程中操作不正确的是
 ”过程:
”过程:①将电解过程发生反应的化学方程式补充完整:
 ___
___ __
__ __
__ 。
。②在一定条件下
 与盐酸反应生成消毒剂
与盐酸反应生成消毒剂 。“有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是:每克含氯消毒剂的氧化能力相当于多少克
。“有效氯含量”可用来衡量含氯消毒剂的消毒能力,其定义是:每克含氯消毒剂的氧化能力相当于多少克 的氧化能力。则
的氧化能力。则 的有效氯含量为
的有效氯含量为
您最近一年使用:0次
解题方法
6 . 下列有关海水资源综合利用的说法错误的是
| A.蒸馏海水可获得淡水 |
| B.在制溴工业中,涉及氧化还原反应 |
C.在制镁工业中,可用贝壳为原料生产石灰乳以沉淀 |
D.为除去粗盐中的 、 、 、 、 ,可依次加入足量的 ,可依次加入足量的 、 、 、 、 溶液 溶液 |
您最近一年使用:0次
名校
7 . 下图为粗盐的提纯工艺,先将粗盐溶于水并过滤出泥沙等难溶性杂质,再依次加入过量的 、
、 、
、 试剂除去
试剂除去 、
、 、
、 等可溶性杂质。
等可溶性杂质。 、
、 、
、 为
为 、
、 、
、 ,下列试剂的添加顺序不合理的是
,下列试剂的添加顺序不合理的是
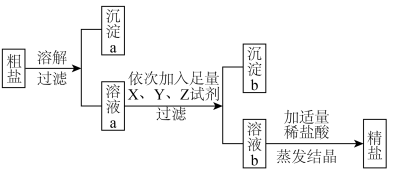
 、
、 、
、 试剂除去
试剂除去 、
、 、
、 等可溶性杂质。
等可溶性杂质。 、
、 、
、 为
为 、
、 、
、 ,下列试剂的添加顺序不合理的是
,下列试剂的添加顺序不合理的是
|
|
| |
A |
|
|
|
B |
|
|
|
C |
|
|
|
D |
|
|
|
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
8 . 回答下列问题:
(1)从海水中得到的粗盐中常含 、
、 、
、 等杂质离子,可依次加入
等杂质离子,可依次加入_______ 、_______ 、_______ 、稀盐酸来进行提纯。加入适量盐酸的目的是_______ 。
(2)用上述方法得到氯化钠,配制氯化钠饱和溶液进行如下图所示电解实验。
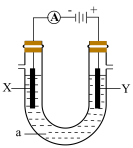
①写出该电解反应的化学方程式_______ 。
②简述检测Y极附近产生的气体的实验方案:_______
(3)下列方法可用于海水淡化的是_______ (填字母)。
A.蒸馏法 B.萃取法 C.过滤法
(4)①“84”消毒液是生活中常见的消毒剂, 与
与 溶液反应制取“84”消毒液的化学方程式为
溶液反应制取“84”消毒液的化学方程式为_______ 。
②“84”消毒液的稀溶液在浸泡餐具过程中,因吸收空气中 使消毒杀菌能力增强,产物中有小苏打,请用化学方程式说明原因:
使消毒杀菌能力增强,产物中有小苏打,请用化学方程式说明原因:_______ 。
(5)目前很多自来水厂使用 来消毒、杀菌。工业制取
来消毒、杀菌。工业制取 的反应:
的反应: ,请用双线桥表示反应中电子转移情况
,请用双线桥表示反应中电子转移情况_______ 。
(6)物质的制备是化学学科的基本研究方向。
①室温下,将氨水和 溶液混合,可制得
溶液混合,可制得 溶液。离子方程式为
溶液。离子方程式为_______ 。
②软锰矿(主要成分 )的水悬浊液可吸收烟气中的
)的水悬浊液可吸收烟气中的 并同时制备
并同时制备 。制备
。制备 反应的化学方程式为
反应的化学方程式为_______ 。
(1)从海水中得到的粗盐中常含
 、
、 、
、 等杂质离子,可依次加入
等杂质离子,可依次加入(2)用上述方法得到氯化钠,配制氯化钠饱和溶液进行如下图所示电解实验。

①写出该电解反应的化学方程式
②简述检测Y极附近产生的气体的实验方案:
(3)下列方法可用于海水淡化的是
A.蒸馏法 B.萃取法 C.过滤法
(4)①“84”消毒液是生活中常见的消毒剂,
 与
与 溶液反应制取“84”消毒液的化学方程式为
溶液反应制取“84”消毒液的化学方程式为②“84”消毒液的稀溶液在浸泡餐具过程中,因吸收空气中
 使消毒杀菌能力增强,产物中有小苏打,请用化学方程式说明原因:
使消毒杀菌能力增强,产物中有小苏打,请用化学方程式说明原因:(5)目前很多自来水厂使用
 来消毒、杀菌。工业制取
来消毒、杀菌。工业制取 的反应:
的反应: ,请用双线桥表示反应中电子转移情况
,请用双线桥表示反应中电子转移情况(6)物质的制备是化学学科的基本研究方向。
①室温下,将氨水和
 溶液混合,可制得
溶液混合,可制得 溶液。离子方程式为
溶液。离子方程式为②软锰矿(主要成分
 )的水悬浊液可吸收烟气中的
)的水悬浊液可吸收烟气中的 并同时制备
并同时制备 。制备
。制备 反应的化学方程式为
反应的化学方程式为
您最近一年使用:0次
名校
9 . 铝元素是地壳中含量最多的金属元素(约占地壳总量的7.73%),主要以铝土矿形式存在(主要成分是 )。要从铝土矿中提取铝,首先要获得纯度较高的氧化铝(熔点:2054℃),主要的工艺流程如图所示:
)。要从铝土矿中提取铝,首先要获得纯度较高的氧化铝(熔点:2054℃),主要的工艺流程如图所示:
 )。要从铝土矿中提取铝,首先要获得纯度较高的氧化铝(熔点:2054℃),主要的工艺流程如图所示:
)。要从铝土矿中提取铝,首先要获得纯度较高的氧化铝(熔点:2054℃),主要的工艺流程如图所示:
A.碱溶①后,溶液中主要含有的阳离子为 和 和 |
B.步骤②通入足量 反应的离子方程式为 反应的离子方程式为 |
| C.灼烧③一般在蒸发皿中进行 |
D.电解④添加冰晶石 (Na3AlF6)的主要作用是降低 的熔融温度 的熔融温度 |
您最近一年使用:0次
2024-01-14更新
|
306次组卷
|
3卷引用:热点11 自然资源的开发利用
10 . 粗盐提纯实验的科学探究。
I.粗盐中含有较多的杂质,化学兴趣小组同学按照课本“活动与探究”的要求做粗盐提纯实验。
(1)“活动与探究”中,操作步骤有:①计算产率、②过滤、③溶解、④蒸发,正确的操作顺序为___________ (填序号)。
(2)仪器B的名称是___________ ,在实验中三个步骤中都须使用的一种仪器是___________ (填序号)。

Ⅱ.化学兴趣小组同学欲除去固体氯化钠中混有的氯化钙。设计实验方案如下,请参与实验并回答问题。
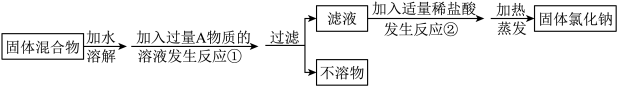
(3)写出A物质的化学式:___________ 。
(4)写出反应②的化学方程式:___________ 。
(5)反应①中加入过量A物质的目的是___________ ;反应②中如果加入盐酸也过量,则对所得到的氯化钠纯度___________ (填“有”或“没有”)影响。
(6)分离后所得氯化钠的质量与分离前原混合物中氯化钠的质量相比较,结果___________ (填增大、不变或减少)。
I.粗盐中含有较多的杂质,化学兴趣小组同学按照课本“活动与探究”的要求做粗盐提纯实验。
(1)“活动与探究”中,操作步骤有:①计算产率、②过滤、③溶解、④蒸发,正确的操作顺序为
(2)仪器B的名称是

Ⅱ.化学兴趣小组同学欲除去固体氯化钠中混有的氯化钙。设计实验方案如下,请参与实验并回答问题。

(3)写出A物质的化学式:
(4)写出反应②的化学方程式:
(5)反应①中加入过量A物质的目的是
(6)分离后所得氯化钠的质量与分离前原混合物中氯化钠的质量相比较,结果
您最近一年使用:0次



