名校
1 .  是一种常见的氧化剂,工业上利用软锰矿
是一种常见的氧化剂,工业上利用软锰矿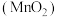 制备高锰酸钾的流程如下,在实验室中模拟该流程制备
制备高锰酸钾的流程如下,在实验室中模拟该流程制备 ,并对产物纯度进行测定。
,并对产物纯度进行测定。
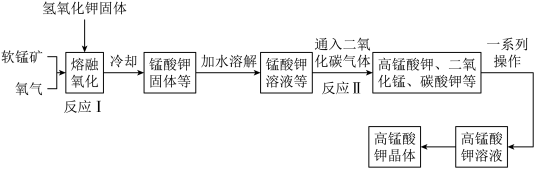
回答下列问题:
(1)反应Ⅰ需要的温度约为400℃,应选择的加热仪器为_______ 。
A酒精灯 B.电磁炉 C.电吹风
(2)加水溶解步骤必须要用到的玻璃仪器有_______。
(3)若要除去 、
、 溶液中的
溶液中的 ,应进行操作
,应进行操作_______ (填操作名称)。
(4)由 溶液获的
溶液获的 晶体的一系列操作为:蒸发浓缩至饱和、
晶体的一系列操作为:蒸发浓缩至饱和、_______ 、过滤、洗涤、干燥(填操作名称)。
(5)研究表明,反应Ⅰ分两步进行:
第一步反应生成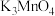 ,反应方程式为
,反应方程式为_______ 。
第二步反应方程式为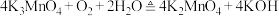
(6)写出反应Ⅱ的离子方程式_______ 。
(7)所得产品中只含有杂质 ,通过元素分析仪测定出产品中所有氧原子的质量分数为40.48%,产品的纯度为
,通过元素分析仪测定出产品中所有氧原子的质量分数为40.48%,产品的纯度为_______ %(保留两位小数)。
 是一种常见的氧化剂,工业上利用软锰矿
是一种常见的氧化剂,工业上利用软锰矿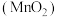 制备高锰酸钾的流程如下,在实验室中模拟该流程制备
制备高锰酸钾的流程如下,在实验室中模拟该流程制备 ,并对产物纯度进行测定。
,并对产物纯度进行测定。
回答下列问题:
(1)反应Ⅰ需要的温度约为400℃,应选择的加热仪器为
A酒精灯 B.电磁炉 C.电吹风
(2)加水溶解步骤必须要用到的玻璃仪器有_______。
| A.烧杯 | B.玻璃棒 | C.量筒 | D.酒精灯 |
 、
、 溶液中的
溶液中的 ,应进行操作
,应进行操作(4)由
 溶液获的
溶液获的 晶体的一系列操作为:蒸发浓缩至饱和、
晶体的一系列操作为:蒸发浓缩至饱和、(5)研究表明,反应Ⅰ分两步进行:
第一步反应生成
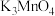 ,反应方程式为
,反应方程式为第二步反应方程式为
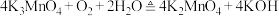
(6)写出反应Ⅱ的离子方程式
(7)所得产品中只含有杂质
 ,通过元素分析仪测定出产品中所有氧原子的质量分数为40.48%,产品的纯度为
,通过元素分析仪测定出产品中所有氧原子的质量分数为40.48%,产品的纯度为
您最近一年使用:0次
名校
2 . 某固体混合物,可能含有CaO、 、
、 、
、 、NaCl中的几种,为检验其成分,做了如下实验:
、NaCl中的几种,为检验其成分,做了如下实验:
①取一定量固体溶于足量水,搅拌后得到无色透明溶液和白色沉淀,过滤得到滤液Ⅰ和沉淀Ⅰ,沉淀质量为10.00g。
②向滤液Ⅰ中加入过量的 溶液,产生白色沉淀,过滤得到滤液Ⅱ和沉淀Ⅱ,沉淀质量为43.00g。
溶液,产生白色沉淀,过滤得到滤液Ⅱ和沉淀Ⅱ,沉淀质量为43.00g。
③向沉淀Ⅱ中加入过量的盐酸,仍有固体未溶解,过滤得到沉淀Ⅲ,沉淀质量为23.30g。
④向滤液Ⅱ中加入硝酸酸化后,再加入过量的 溶液,得到大量白色沉淀,过滤得到沉淀Ⅳ,沉淀质量为71.75g。
溶液,得到大量白色沉淀,过滤得到沉淀Ⅳ,沉淀质量为71.75g。
已知:溶液中有 、
、 时,
时, 更容易和
更容易和 形成沉淀。
形成沉淀。
回答下列问题:
(1)通过实验①可知,一定不存在的是_______ (填化学式,下同)。
(2)沉淀Ⅰ、沉淀Ⅱ分别是_______ 、_______ 。
(3)本实验需要多次过滤,过滤需要用到得玻璃仪器有_______。
(4)写出实验④反应的离子方程式_______ 。
(5)该固体中一定含有_______ (填化学式),质量之比为_______ 。
 、
、 、
、 、NaCl中的几种,为检验其成分,做了如下实验:
、NaCl中的几种,为检验其成分,做了如下实验:①取一定量固体溶于足量水,搅拌后得到无色透明溶液和白色沉淀,过滤得到滤液Ⅰ和沉淀Ⅰ,沉淀质量为10.00g。
②向滤液Ⅰ中加入过量的
 溶液,产生白色沉淀,过滤得到滤液Ⅱ和沉淀Ⅱ,沉淀质量为43.00g。
溶液,产生白色沉淀,过滤得到滤液Ⅱ和沉淀Ⅱ,沉淀质量为43.00g。③向沉淀Ⅱ中加入过量的盐酸,仍有固体未溶解,过滤得到沉淀Ⅲ,沉淀质量为23.30g。
④向滤液Ⅱ中加入硝酸酸化后,再加入过量的
 溶液,得到大量白色沉淀,过滤得到沉淀Ⅳ,沉淀质量为71.75g。
溶液,得到大量白色沉淀,过滤得到沉淀Ⅳ,沉淀质量为71.75g。已知:溶液中有
 、
、 时,
时, 更容易和
更容易和 形成沉淀。
形成沉淀。回答下列问题:
(1)通过实验①可知,一定不存在的是
(2)沉淀Ⅰ、沉淀Ⅱ分别是
(3)本实验需要多次过滤,过滤需要用到得玻璃仪器有_______。
| A.烧杯 | B.玻璃棒 | C.漏斗 | D.酒精灯 |
(5)该固体中一定含有
您最近一年使用:0次
解题方法
3 . 下列基本实验操作正确的是
| A | B | C | D |
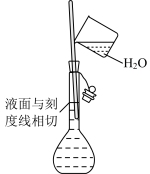 | 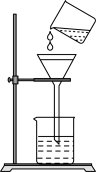 | 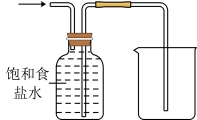 | 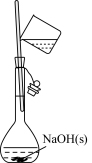 |
| 配制溶液 | 过滤 | 收集氯气 | 配制 的 的 溶液 溶液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-09-13更新
|
224次组卷
|
9卷引用:重庆市三峡名校联盟2022-2023学年高一上学期联考化学试题
重庆市三峡名校联盟2022-2023学年高一上学期联考化学试题山西省吕梁市2021-2022学年高一上学期期末考试化学试题广东省名校联盟2021-2022学年高一上学期期末考试化学试题河北省秦皇岛市2021-2022学年高一上学期期末统一考试化学试题(已下线)2.3.4 配制一定物质的量浓度的溶液-2022-2023学年高一化学上学期课后培优分级练(人教版2019必修第一册)湖南省衡阳市祁东县2021-2022学年高一上学期期末考试化学试题云南省楚雄州2021-2022学年高一上学期期末教育学业质量监测化学试题河北省廊坊市2021-2022学年高一上学期期末统一考试化学试题河北省秦皇岛市青龙满族自治县实验中学2022-2023学年高一上学期期末考试化学试题
名校
解题方法
4 . 要除去下列物质中的少量杂质(括号内为杂质),下列实验方案设计中,不合理的是
| A.CO(CO2):将气体先通入氢氧化钠溶液,再通过浓硫酸 |
| B.NaCl溶液(NaOH):加入过量的H2SO4溶液 |
| C.CaCO3(CaCl2):加水溶解→过滤→洗涤→干燥 |
| D.KCl溶液(K2CO3):加入适量的稀盐酸 |
您最近一年使用:0次
2022-06-17更新
|
146次组卷
|
4卷引用:重庆市第十八中学2022-2023学年高一上学期10月月考化学试题
重庆市第十八中学2022-2023学年高一上学期10月月考化学试题(已下线)第04讲 初中化学实验-【暑假自学课】2022年新高一化学暑假精品课(沪科版2020必修第一册)重庆西南大学附属中学校2023-2024学年高一上学期定时检测(一)化学试题重庆市第十八中学2023-2024学年高一上学期11月期中化学试题
5 . 下列各组实验装置、所用试剂、实验现象及结论都正确的是
| A | B | C | D |
 | 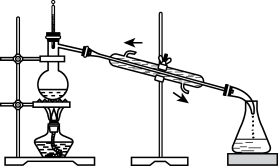 | 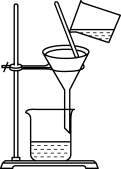 |  |
| 分离苯萃取碘水后已分层的有机层和水层 | 从三氯甲烷和四氯甲烷混合物中蒸馏出三氯甲烷 | 趁热过滤提纯苯甲酸 | 萃取时,将所需试剂加入分液漏斗,塞上玻璃塞,按如图所示方式用力振荡 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-04-21更新
|
143次组卷
|
2卷引用:重庆市名校联盟2021-2022学年高二下学期第一次联合考试化学试题
名校
6 . 某工业废水中存在大盘的Na+、 、Cu2+、
、Cu2+、 ,欲除去其中的Cu2+、
,欲除去其中的Cu2+、 ,设计的工艺流程如图所示:
,设计的工艺流程如图所示:

(1)加入NaOH溶液时反应的离子方程式:_______ 。
(2)试剂a为_______ ,试剂b为_______ 。
(3)流程图中操作X为_______ 。
(4)检验废水中的 已沉淀完全的方法为
已沉淀完全的方法为_______ 。
 、Cu2+、
、Cu2+、 ,欲除去其中的Cu2+、
,欲除去其中的Cu2+、 ,设计的工艺流程如图所示:
,设计的工艺流程如图所示:
(1)加入NaOH溶液时反应的离子方程式:
(2)试剂a为
(3)流程图中操作X为
(4)检验废水中的
 已沉淀完全的方法为
已沉淀完全的方法为
您最近一年使用:0次
7 . 中国女药学家屠呦呦因发现青蒿素对疟疾的治疗作用而成为2015年诺贝尔生理学或医学奖获得者之一、青蒿素为无色针状晶体,易溶于丙酮、氯仿和苯中,在甲醇、乙醇、乙醚、石油醚中可溶解,在水中几乎不溶,熔点为 ℃,热稳定性差。已知:乙醚沸点为35℃。提取青蒿素的主要工艺为
℃,热稳定性差。已知:乙醚沸点为35℃。提取青蒿素的主要工艺为
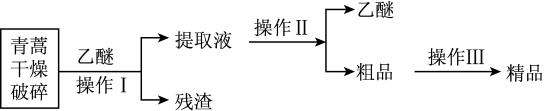
下列有关此工艺操作不正确的是
 ℃,热稳定性差。已知:乙醚沸点为35℃。提取青蒿素的主要工艺为
℃,热稳定性差。已知:乙醚沸点为35℃。提取青蒿素的主要工艺为
下列有关此工艺操作不正确的是
| A.破碎的目的是提高青蒿素的浸取率 | B.操作I是萃取 |
| C.操作II是蒸馏 | D.操作III是重结晶 |
您最近一年使用:0次
2022-03-21更新
|
225次组卷
|
3卷引用:重庆市缙云教育联盟2021-2022学年高二5月质量检测化学试题
8 . 实验室模拟“侯氏制碱法”原理制备少量纯碱: 。其实验过程包括:制取氨气和
。其实验过程包括:制取氨气和 制取
制取 分离
分离 分解
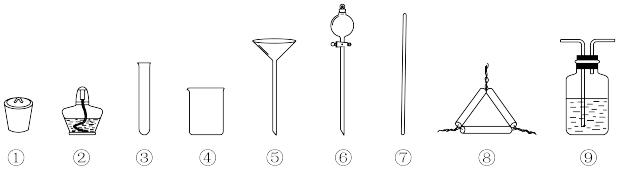
分解 四个步骤。下列实验必须选用的主要仪器(如图所示,夹持仪器和滤纸省略)错误的是
四个步骤。下列实验必须选用的主要仪器(如图所示,夹持仪器和滤纸省略)错误的是
 。其实验过程包括:制取氨气和
。其实验过程包括:制取氨气和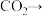 制取
制取 分离
分离 分解
分解 四个步骤。下列实验必须选用的主要仪器(如图所示,夹持仪器和滤纸省略)错误的是
四个步骤。下列实验必须选用的主要仪器(如图所示,夹持仪器和滤纸省略)错误的是
| A.实验室制取氨气,可选用②③ |
B.制取 ,可选用④⑦ ,可选用④⑦ |
C.分离 ,可选用④⑤⑦ ,可选用④⑤⑦ |
D.分解 ,可选用①②⑦⑧ ,可选用①②⑦⑧ |
您最近一年使用:0次
解题方法
9 . 某工厂的废水中含有较多的 和
和 。为了减少污染并变废为宝, 用如图所示的工艺流程从废水中回收
。为了减少污染并变废为宝, 用如图所示的工艺流程从废水中回收 和金属铜。
和金属铜。
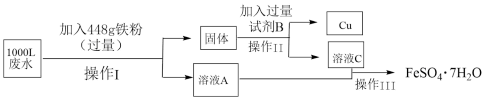
请回答下列问题:
(1)向废水中加入铁粉,所发生的主要反应的离子方程式为___________ 。
(2)操作Ⅰ和操作Ⅱ的名称是___________ ,所用到的玻璃仪器有___________ 。
(3)流程中“固体”的主要成分是___________ (填化学式);加入试剂B所发生反应的化学方程式为___________ 。
(4)操作Ⅲ包括蒸发浓缩、___________ 、过滤、___________ 、干燥。
(5)设计实验方案检验废水中是否含有 :
:___________ 。
(6)若废水中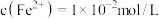 ,
,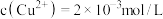 ,上述1000L废水经处理后,理论上可获得
,上述1000L废水经处理后,理论上可获得 的质量是
的质量是___________ g。
 和
和 。为了减少污染并变废为宝, 用如图所示的工艺流程从废水中回收
。为了减少污染并变废为宝, 用如图所示的工艺流程从废水中回收 和金属铜。
和金属铜。
请回答下列问题:
(1)向废水中加入铁粉,所发生的主要反应的离子方程式为
(2)操作Ⅰ和操作Ⅱ的名称是
(3)流程中“固体”的主要成分是
(4)操作Ⅲ包括蒸发浓缩、
(5)设计实验方案检验废水中是否含有
 :
:(6)若废水中
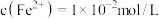 ,
,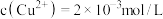 ,上述1000L废水经处理后,理论上可获得
,上述1000L废水经处理后,理论上可获得 的质量是
的质量是
您最近一年使用:0次



