名校
解题方法
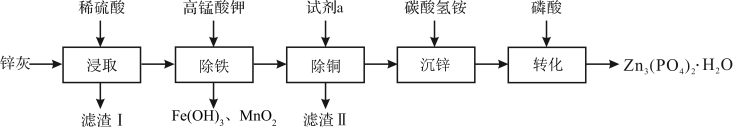
1 . 四水合磷酸锌 [Zn3(PO4)2·4H2O,摩尔质量为457 g·mol-1,难溶于水] 是一种性能优良的绿色环保防锈颜料。实验室以锌灰(含ZnO、PbO、CuO、FeO、Fe2O3、SiO2等)为原料制备Zn3(PO4)2·4H2O的流程如图,回答下列问题:
已知:①6NH4HCO3 + 3ZnSO4 ZnCO3·2Zn(OH)2·H2O↓ + 3(NH4)2SO4 + 5CO2↑
ZnCO3·2Zn(OH)2·H2O↓ + 3(NH4)2SO4 + 5CO2↑
②ZnCO3·2Zn(OH)2·H2O + 2H3PO4 Zn3(PO4)2·4H2O + 2H2O + CO2↑
Zn3(PO4)2·4H2O + 2H2O + CO2↑
③常温下,Fe3+、Fe2+、Cu2+、Zn2+生成氢氧化物沉淀时的pH:
(1)滤渣Ⅰ的主要成分为_______ ;试剂a为_______ ;
(2)“除铁”操作时,需先将溶液调至接近中性,然后再滴加KMnO4溶液,使溶液中的铁元素转化为Fe(OH)3,该反应的离子方程式为_______ ;
(3)“转化”结束后,从混合液中分离得到Zn3(PO4)2·4H2O的操作包括_______ 和干燥。
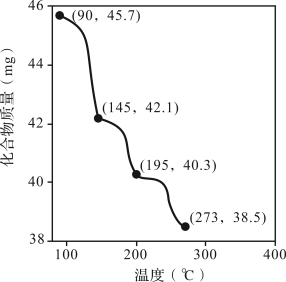
(4)称取45.7 mg Zn3(PO4)2·4H2O进行热重分析,化合物质量随温度的变化关系如图所示,为获得Zn3(PO4)2·2H2O和Zn3(PO4)2·H2O的混合产品,烘干时的温度范围为_______。
(5)为测定产品中Zn3(PO4)2·4H2O的含量,进行如下实验:(已知:Zn2+与H2Y2−按1:1反应;杂质不反应。)
步骤Ⅰ:准确称取0.4570g产品于烧杯中,加入适量盐酸使其溶解,将溶液转移至100 mL容量瓶,定容。
步骤Ⅱ:移取20.00 mL上述溶液于锥形瓶中,加入指示剂,在pH = 5~6的缓冲溶液中用0.02000mol·L-1 Na2H2Y标准溶液滴定至终点,测得Na2H2Y标准溶液的用量为27.60 mL。
步骤Ⅱ中移取溶液时所使用的玻璃仪器为_______ ;产品中Zn3(PO4)2·4H2O的质量分数为_______ 。下列操作中,导致产品中Zn3(PO4)2·4H2O含量测定值偏低的是_______ 。
a.步骤I中定容时俯视刻度线
b.步骤I中转移溶液时未洗涤烧杯
c.步骤II中滴定管未用Na2H2Y标准溶液润洗
d.步骤II中滴定前滴定管内无气泡,滴定结束后有气泡

已知:①6NH4HCO3 + 3ZnSO4
 ZnCO3·2Zn(OH)2·H2O↓ + 3(NH4)2SO4 + 5CO2↑
ZnCO3·2Zn(OH)2·H2O↓ + 3(NH4)2SO4 + 5CO2↑②ZnCO3·2Zn(OH)2·H2O + 2H3PO4
 Zn3(PO4)2·4H2O + 2H2O + CO2↑
Zn3(PO4)2·4H2O + 2H2O + CO2↑③常温下,Fe3+、Fe2+、Cu2+、Zn2+生成氢氧化物沉淀时的pH:
| Fe3+ | Fe2+ | Cu2+ | Zn2+ | |
| 开始沉淀时的pH | 1.9 | 7.0 | 4.7 | 5.7 |
| 完全沉淀时的pH | 3.7 | 9.0 | 6.7 | 8.1 |
(2)“除铁”操作时,需先将溶液调至接近中性,然后再滴加KMnO4溶液,使溶液中的铁元素转化为Fe(OH)3,该反应的离子方程式为
(3)“转化”结束后,从混合液中分离得到Zn3(PO4)2·4H2O的操作包括
(4)称取45.7 mg Zn3(PO4)2·4H2O进行热重分析,化合物质量随温度的变化关系如图所示,为获得Zn3(PO4)2·2H2O和Zn3(PO4)2·H2O的混合产品,烘干时的温度范围为_______。

| A.90~145℃ | B.145~195℃ | C.195~273℃ | D.>273℃ |
步骤Ⅰ:准确称取0.4570g产品于烧杯中,加入适量盐酸使其溶解,将溶液转移至100 mL容量瓶,定容。
步骤Ⅱ:移取20.00 mL上述溶液于锥形瓶中,加入指示剂,在pH = 5~6的缓冲溶液中用0.02000mol·L-1 Na2H2Y标准溶液滴定至终点,测得Na2H2Y标准溶液的用量为27.60 mL。
步骤Ⅱ中移取溶液时所使用的玻璃仪器为
a.步骤I中定容时俯视刻度线
b.步骤I中转移溶液时未洗涤烧杯
c.步骤II中滴定管未用Na2H2Y标准溶液润洗
d.步骤II中滴定前滴定管内无气泡,滴定结束后有气泡
您最近一年使用:0次
2021-09-16更新
|
666次组卷
|
3卷引用:2020年全国卷Ⅰ理综化学高考真题变式题
解题方法
2 . 碱式碳酸镁 是重要的无机化工产品。一种由白云石
是重要的无机化工产品。一种由白云石 主要成分为
主要成分为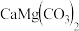 ,还含少量
,还含少量 、
、 等
等 为原料制备碱式碳酸镁
为原料制备碱式碳酸镁 国家标准中CaO 的质量分数
国家标准中CaO 的质量分数
 的实验流程如下:
的实验流程如下:
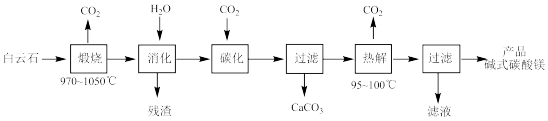
 “煅烧”时发生主要反应的化学方程式为
“煅烧”时发生主要反应的化学方程式为________________ 。
 常温常压下“碳化”可使镁元素转化为
常温常压下“碳化”可使镁元素转化为 ,“碳化”时终点pH对最终产品中CaO含量及碱式碳酸镁产率的影响如图1和图2所示。
,“碳化”时终点pH对最终产品中CaO含量及碱式碳酸镁产率的影响如图1和图2所示。
图1 CaO含量与碳化终点pH的关系
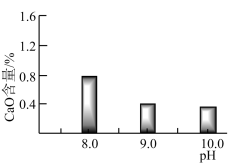
图2碱式碳酸镁产率与碳化终点pH的关系

 应控制“碳化”终点PH 约为
应控制“碳化”终点PH 约为__________ 。
 图
图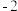 中,当
中,当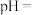
 时,镁元素的主要存在形式是
时,镁元素的主要存在形式是__________________  写化学式
写化学式 。
。
 “过滤”时须用到的玻璃仪器有:烧杯、玻璃棒、
“过滤”时须用到的玻璃仪器有:烧杯、玻璃棒、__________________ 。
 一种测定碱式碳酸镁
一种测定碱式碳酸镁 组成的方法如下:
组成的方法如下:
 称取一定量的碱式碳酸镁晶体溶于足量的盐酸,收集到气体
称取一定量的碱式碳酸镁晶体溶于足量的盐酸,收集到气体 标准状况
标准状况 ;往所得溶液中加入足量的NaOH溶液,过滤,将所得沉淀洗涤、干燥,称量得固体
;往所得溶液中加入足量的NaOH溶液,过滤,将所得沉淀洗涤、干燥,称量得固体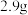 。
。
 另取一定量的碱式碳酸镁晶体在空气中加热,固体残留率
另取一定量的碱式碳酸镁晶体在空气中加热,固体残留率 固体样品的剩余质量
固体样品的剩余质量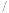 固体样品的起始质量
固体样品的起始质量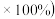 随温度的变化如下图所示
随温度的变化如下图所示 样品在
样品在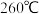 时完全失去结晶水
时完全失去结晶水 。
。
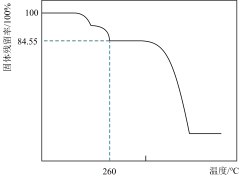
根据以上实验数据计算确定碱式碳酸镁晶体的化学式 写出计算过程
写出计算过程
_________ 。
 是重要的无机化工产品。一种由白云石
是重要的无机化工产品。一种由白云石 主要成分为
主要成分为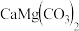 ,还含少量
,还含少量 、
、 等
等 为原料制备碱式碳酸镁
为原料制备碱式碳酸镁 国家标准中CaO 的质量分数
国家标准中CaO 的质量分数
 的实验流程如下:
的实验流程如下: 
 “煅烧”时发生主要反应的化学方程式为
“煅烧”时发生主要反应的化学方程式为 常温常压下“碳化”可使镁元素转化为
常温常压下“碳化”可使镁元素转化为 ,“碳化”时终点pH对最终产品中CaO含量及碱式碳酸镁产率的影响如图1和图2所示。
,“碳化”时终点pH对最终产品中CaO含量及碱式碳酸镁产率的影响如图1和图2所示。图1 CaO含量与碳化终点pH的关系

图2碱式碳酸镁产率与碳化终点pH的关系

 应控制“碳化”终点PH 约为
应控制“碳化”终点PH 约为 图
图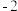 中,当
中,当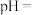
 时,镁元素的主要存在形式是
时,镁元素的主要存在形式是 写化学式
写化学式 。
。 “过滤”时须用到的玻璃仪器有:烧杯、玻璃棒、
“过滤”时须用到的玻璃仪器有:烧杯、玻璃棒、 一种测定碱式碳酸镁
一种测定碱式碳酸镁 组成的方法如下:
组成的方法如下: 称取一定量的碱式碳酸镁晶体溶于足量的盐酸,收集到气体
称取一定量的碱式碳酸镁晶体溶于足量的盐酸,收集到气体 标准状况
标准状况 ;往所得溶液中加入足量的NaOH溶液,过滤,将所得沉淀洗涤、干燥,称量得固体
;往所得溶液中加入足量的NaOH溶液,过滤,将所得沉淀洗涤、干燥,称量得固体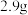 。
。 另取一定量的碱式碳酸镁晶体在空气中加热,固体残留率
另取一定量的碱式碳酸镁晶体在空气中加热,固体残留率 固体样品的剩余质量
固体样品的剩余质量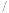 固体样品的起始质量
固体样品的起始质量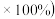 随温度的变化如下图所示
随温度的变化如下图所示 样品在
样品在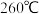 时完全失去结晶水
时完全失去结晶水 。
。
根据以上实验数据计算确定碱式碳酸镁晶体的化学式
 写出计算过程
写出计算过程
您最近一年使用:0次
2020·贵州铜仁·一模
解题方法
3 . 过碳酸钠(2Na2CO3・3H2O2)又名过氧碳酸钠,白色颗粒状粉末,其水溶液呈碱性,50℃可分解为碳酸钠和过氧化氢,具有Na2CO3和H2O2的双重性质,是很好的消毒剂、漂白剂、供氧剂。以工业碳酸钠和H2O2为原料制备过碳酸钠的实验装置及步骤:
I.称取10.0g碳酸钠,溶于40mL蒸馏水中,冷却至273K待用。
II.量取15mL30%的H2O2溶液加入到三颈烧瓶中,冷却至273K后,加入复合稳定剂,搅拌均匀。
III.在控温及搅拌条件下,将碳酸钠溶液滴入到步骤II的混合液中,待反应液冷却至268K左右,边搅拌边加入4.0gNaCl,静置结晶。
IV.过滤,用无水乙醇洗涤后,真空干燥。
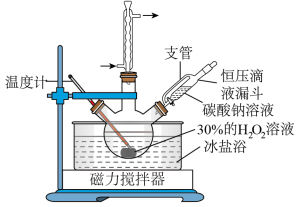
请回答以下问题:
(1)球形冷凝管中回流的主要物质除H2O外还有__________________ (填化学式)。
(2)制备过程中涉及的反应及干燥等操作均需在较低温度下进行,原因是________________ 。
(3)步骤II中加入复合稳定剂的目的之一是与工业碳酸钠中含有的Fe3+生成稳定的配合物,以防Fe3+对制备反应产生不良影响。该不良影响是指__________________________ 。
(4)步骤IV中完成"过滤”操作所需玻璃仪器有烧杯、____________ 和____________ .
(5)产品中H2O2含量的测定
准确称取产品0.1000g于碘量瓶中,加入50mL蒸馏水,并立即加入6mL2mol·L-1H3PO4溶液,再加入lgKI固体(过量),摇匀后于暗处放置10min,加入适量指示剂,用0.1000rnol·L-1Na2S2O3标准液滴定至终点,消耗Na2S2O3标准溶液17.00mL。(已知:2Na2S2O3+I2=Na2S4O6+2NaI)
①所加指示剂的名称是____________ ;确定达到滴定终点的依据是_____________
②若加入KI固体摇匀后未将碘量瓶“在暗处放置10min”,就立即进行滴定操作,测定的结果将会____________ (选填“偏大"、“偏小”或“无影响”)。
③根据实验数据计算产品中H2O2的质量分数为____________ %。
I.称取10.0g碳酸钠,溶于40mL蒸馏水中,冷却至273K待用。
II.量取15mL30%的H2O2溶液加入到三颈烧瓶中,冷却至273K后,加入复合稳定剂,搅拌均匀。
III.在控温及搅拌条件下,将碳酸钠溶液滴入到步骤II的混合液中,待反应液冷却至268K左右,边搅拌边加入4.0gNaCl,静置结晶。
IV.过滤,用无水乙醇洗涤后,真空干燥。

请回答以下问题:
(1)球形冷凝管中回流的主要物质除H2O外还有
(2)制备过程中涉及的反应及干燥等操作均需在较低温度下进行,原因是
(3)步骤II中加入复合稳定剂的目的之一是与工业碳酸钠中含有的Fe3+生成稳定的配合物,以防Fe3+对制备反应产生不良影响。该不良影响是指
(4)步骤IV中完成"过滤”操作所需玻璃仪器有烧杯、
(5)产品中H2O2含量的测定
准确称取产品0.1000g于碘量瓶中,加入50mL蒸馏水,并立即加入6mL2mol·L-1H3PO4溶液,再加入lgKI固体(过量),摇匀后于暗处放置10min,加入适量指示剂,用0.1000rnol·L-1Na2S2O3标准液滴定至终点,消耗Na2S2O3标准溶液17.00mL。(已知:2Na2S2O3+I2=Na2S4O6+2NaI)
①所加指示剂的名称是
②若加入KI固体摇匀后未将碘量瓶“在暗处放置10min”,就立即进行滴定操作,测定的结果将会
③根据实验数据计算产品中H2O2的质量分数为
您最近一年使用:0次
名校
4 . 某同学设计如下实验方案,以分离KCl和BaCl2两种固体混合物,试回答下列问题:

供选试剂:Na2SO4溶液、K2CO3溶液、K2SO4溶液、盐酸
(1)操作①的名称是______ ,操作②的名称是_________ 。
(2)试剂a是________ (填化学式,下同),试剂b是_______ ,固体B是________ 。
(3)加入试剂a所发生反应的化学方程式为_______ 。加入试剂b所发生反应的离子方程式为______ 。
(4)该方案能否达到实验目的:_____ (填“能”或“不能”)。若不能,应如何改进?(若能,此问不用回答)___ 。
(5)若要测定原混合物中BaCl2的质量分数,除了要准确称量混合物的质量外,至少还要获得的数据是____ 的质量。

供选试剂:Na2SO4溶液、K2CO3溶液、K2SO4溶液、盐酸
(1)操作①的名称是
(2)试剂a是
(3)加入试剂a所发生反应的化学方程式为
(4)该方案能否达到实验目的:
(5)若要测定原混合物中BaCl2的质量分数,除了要准确称量混合物的质量外,至少还要获得的数据是
您最近一年使用:0次
2020-06-10更新
|
668次组卷
|
24卷引用:湖南省长沙市第一中学2017-2018学年高一上学期期中考试化学试题
湖南省长沙市第一中学2017-2018学年高一上学期期中考试化学试题2018-2019学年高一人教版化学必修1:第一章从实验学化学练习题湖北省武汉市钢城四中2018-2019学年高一上学期10月月考化学试题(已下线)【走进新高考】(人教版必修一)第一章 从实验学化学 单元练习02云南省楚雄州南华县第一中学2018-2019学年高一上学期期中考试化学试题【校级联考】安徽省滁州市定远县西片区2018-2019学年高一上学期期中考试化学试题安徽省阜阳市第三中学2019-2020学年高一上学期第一次调研考试化学试题贵州省贵阳一中2019—2020学年度高一上学期第一次月考化学试题内蒙古第一机械制造(集团)有限公司第一中学2019-2020学年高一10月月考化学试题人教版高中化学必修1第一章《从实验学化学》测试卷5人教版高中化学必修1第一章《从实验学化学》测试卷6广西贺州市富川县民族中学2019-2020学年高一上学期期末考试化学试题四川省攀枝花市第十五中学2019-2020学年高一上学期期中考试化学试题(已下线)第一章 从实验学化学(能力提升)-2020-2021学年高一化学单元测试定心卷(人教版必修1)河南省南阳市第一中学2020-2021学年高一上学期第一次月考化学试题2015-2016学年广西柳州铁路第一中学高一上段考化学试卷云南省昭通市盐津县水田新区中学2018-2019学年高一上学期11月份考试化学试题贵州省黄平县且兰高级中学2018-2019学年高一上学期12月份考试化学试题云南省昭通市巧家县二中2019-2020学年高一10月月考化学试题云南省保山市昌宁县二中2019-2020学年高一10月月考化学试题云南省施甸县第一中学2019-2020学年高一12月月考化学试题云南省永善县第二中学2019—2020学年高一上学期期末考试化学试题四川省冕宁中学2020-2021学年高一上学期期中考试化学试题河北省承德第一中学2020-2021学年高一下学期第二次月考化学试题
5 . 实验小组的同学欲对一粗盐样品进行初步提纯。所用实验仪器或用品如下:
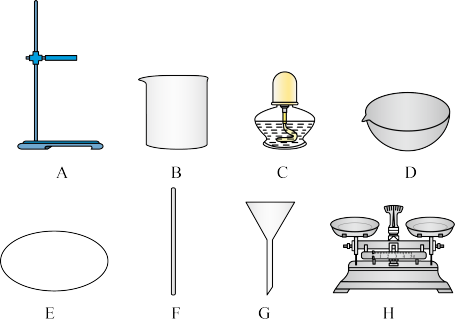
(1)D的名称是____ 。
(2)提纯的步骤是溶解、过滤、____ 。
(3)“过滤”操作的要点可概括为“一贴、二低、三靠”,其中“二低”的含义是____ 。
(4)实验小组通过正确的计算发现,所得实验结果与该粗盐的实际含量对比,实验测得的结果比实际偏低,请分析可能的原因:___ 。

(1)D的名称是
(2)提纯的步骤是溶解、过滤、
(3)“过滤”操作的要点可概括为“一贴、二低、三靠”,其中“二低”的含义是
(4)实验小组通过正确的计算发现,所得实验结果与该粗盐的实际含量对比,实验测得的结果比实际偏低,请分析可能的原因:
您最近一年使用:0次
名校
6 . 下列关于硫的叙述中不正确的是( )
| A.试管内壁附着的硫可用二硫化碳溶解除去 |
| B.硫在自然界中只能以硫化物和硫酸盐的形态存在 |
| C.化石燃料的大量燃烧是空气中二氧化硫含量升高的原因 |
| D.分离黑火药中的硝酸钾、木炭、硫要用到二硫化碳、水及过滤操作 |
您最近一年使用:0次
2020-01-05更新
|
525次组卷
|
10卷引用:苏教版(2020)高一必修第一册专题4第一单元课时1 硫、二氧化硫和三氧化硫
苏教版(2020)高一必修第一册专题4第一单元课时1 硫、二氧化硫和三氧化硫鲁科版(2019)高一必修第一册第3章 物质的性质与转化 第2节 硫的转化 课时1 硫、二氧化硫和三氧化硫云南省禄丰县民族中学2019-2020学年高一12月月考化学试题云南省屏边县第一中学2019-2020学年高一上学期12月月考化学试题山东省济宁市微山县第一中学2019-2020学年高一下学期网络课堂第一阶段网络测试化学试题云南省元江县一中2020-2021学年高一上学期期中考试化学试题(已下线)5.1.1硫和二氧化硫-随堂练习山东省嘉祥县第一中学2020-2021学年高一下学期第一次月考化学试题山东济宁泗水县泗水镇第三中学2020-2021学年高一下学期4月月考化学试题安徽省淮北师范大学附属实验中学2022-2023学年高一下学期第一次月考化学试题
7 . 实验小组的同学欲对一粗盐样品进行初步提纯。所用实验仪器或用品如下:
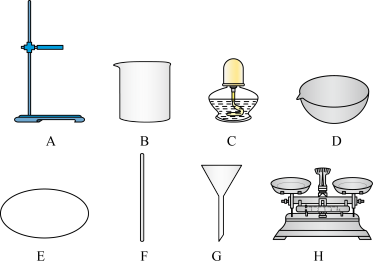
(1)D的名称是________ 。
(2)提纯的步骤是:溶解、过滤、________ 、计算产率。
(3)“过滤”操作的要点可概括为“一贴、二低、三靠”,其中“二低”的含义是________________________ 。
(4)实验小组通过正确的计算发现,所得实验结果与该粗盐的实际含量对比,实验测得的结果比实际偏低,请分析可能的原因:________________________________________________ 。

(1)D的名称是
(2)提纯的步骤是:溶解、过滤、
(3)“过滤”操作的要点可概括为“一贴、二低、三靠”,其中“二低”的含义是
(4)实验小组通过正确的计算发现,所得实验结果与该粗盐的实际含量对比,实验测得的结果比实际偏低,请分析可能的原因:
您最近一年使用:0次
11-12高三上·江苏常州·期中
名校
8 . 某同学设计如下实验测量m g铜银合金样品中铜的质量分数:
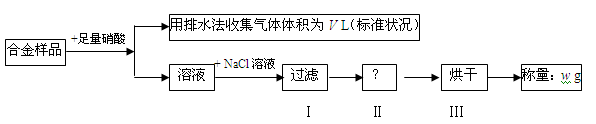
下列说法中不正确的是

下列说法中不正确的是
| A.收集到的V L气体全为 NO |
| B.过滤用到的玻璃仪器是:烧杯、漏斗、玻璃棒 |
| C.操作Ⅱ应是洗涤 |
D.铜的质量分数为: ×100% ×100% |
您最近一年使用:0次
2016-12-09更新
|
150次组卷
|
8卷引用:2012届四川省成都树德中学高考适应考试(一)理科综合化学试卷
(已下线)2012届四川省成都树德中学高考适应考试(一)理科综合化学试卷(已下线)2012届四川省成都树德中学高考适应考试(一)理科化学试卷 高一必修第一册(鲁科2019)第3章 第3节 氮的循环(已下线)2011届江苏省常州市横山桥高级中学高三上学期期中考试化学(已下线)2011届浙江省学军中学高三上学期期中考试化学试题(已下线)2012届浙江省海盐元济高级中学高三上学期10月份月考化学试卷(已下线)2015届福建省八县一中高三上学期半期联考化学试卷陕西省西安市第一中学2022-2023学年高一下学期5月月考化学试题
12-13高一·全国·课时练习
名校
9 . 已知化合物甲和乙都不溶于水,甲可溶于质量分数大于或等于98%的硫酸,而乙不溶。现有一份甲和乙的混合物样品,通过实验进行分离,可得到固体甲。(实验中使用的过滤器是用于过滤强酸性液体的耐酸过滤器。)
请填写表中空格,完成由上述混合物得到固体甲的实验设计。
请填写表中空格,完成由上述混合物得到固体甲的实验设计。
| 序号 | 实验步骤 | 简述实验操作(不必叙述如何组装实验装置) |
| ① | 溶解 | 将混合物放入烧杯中,加入98% H2SO4,充分搅拌直到固体不再溶解。 |
| ② | ||
| ③ | ||
| ④ | ||
| ⑤ | 洗涤沉淀 | |
| ⑥ | 检验沉淀 是否洗净 |
您最近一年使用:0次
2016-12-09更新
|
352次组卷
|
7卷引用:2012年沪科版高中化学10.2结晶水合物中结晶水含量的测练习卷
(已下线)2012年沪科版高中化学10.2结晶水合物中结晶水含量的测练习卷(已下线)2012年苏教版高中化学选修6 1.1海带中碘元素的分离及检验练习卷(已下线)2012-2013学年江苏省江都市甘棠中学高二下学期期末考试化学试卷黑龙江省哈尔滨市第三中学2017-2018学年高一上学期第一次验收考试化学试题化学沪科版化学高二上:10.2《结晶水合物中结晶水含量的测定》测试(已下线)2012-2013学年江苏省郑梁梅中学高二下学期期末考试化学试卷(已下线)1.3.2 过滤、结晶、蒸馏-【帮课堂】2022-2023学年高一化学同步精品讲义(沪科版2020必修第一册)



