8. 过碳酸钠(2Na
2CO
3・3H
2O
2)又名过氧碳酸钠,白色颗粒状粉末,其水溶液呈碱性,50℃可分解为碳酸钠和过氧化氢,具有Na
2CO
3和H
2O
2的双重性质,是很好的消毒剂、漂白剂、供氧剂。以工业碳酸钠和H
2O
2为原料制备过碳酸钠的实验装置及步骤:
I.称取10.0g碳酸钠,溶于40mL蒸馏水中,冷却至273K待用。
II.量取15mL30%的H
2O
2溶液加入到三颈烧瓶中,冷却至273K后,加入复合稳定剂,搅拌均匀。
III.在控温及搅拌条件下,将碳酸钠溶液滴入到步骤II的混合液中,待反应液冷却至268K左右,边搅拌边加入4.0gNaCl,静置结晶。
IV.过滤,用无水乙醇洗涤后,真空干燥。
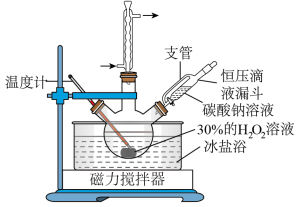
请回答以下问题:
(1)球形冷凝管中回流的主要物质除H
2O外还有
__________________(填化学式)。
(2)制备过程中涉及的反应及干燥等操作均需在较低温度下进行,原因是
________________。
(3)步骤II中加入复合稳定剂的目的之一是与工业碳酸钠中含有的Fe
3+生成稳定的配合物,以防Fe
3+对制备反应产生不良影响。该不良影响是指
__________________________。
(4)步骤IV中完成"过滤”操作所需玻璃仪器有烧杯、
____________和
____________.
(5)产品中H
2O
2含量的测定
准确称取产品0.1000g于碘量瓶中,加入50mL蒸馏水,并立即加入6mL2mol·L
-1H
3PO
4溶液,再加入lgKI固体(过量),摇匀后于暗处放置10min,加入适量指示剂,用0.1000rnol·L
-1Na
2S
2O
3标准液滴定至终点,消耗Na
2S
2O
3标准溶液17.00mL。(已知:2Na
2S
2O
3+I
2=Na
2S
4O
6+2NaI)
①所加指示剂的名称是
____________;确定达到滴定终点的依据是
_____________②若加入KI固体摇匀后未将碘量瓶“在暗处放置10min”,就立即进行滴定操作,测定的结果将会
____________(选填“偏大"、“偏小”或“无影响”)。
③根据实验数据计算产品中H
2O
2的质量分数为
____________%。