名校
解题方法
1 . 有一混合物水溶液含有以下离子中的若干种: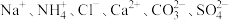 ,现取两份100 mL的该溶液分别进行如下实验(已知:
,现取两份100 mL的该溶液分别进行如下实验(已知: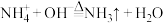 ):
):
(1)第一份加足量NaOH溶液,加热,收集到标准状况下的气体448 mL。
(2)第二份加足量BaCl2溶液,得沉淀4.30 g,再用足量盐酸洗涤、干燥后,沉淀质量为2.33 g。
根据上述实验,下列推测正确的是
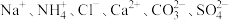 ,现取两份100 mL的该溶液分别进行如下实验(已知:
,现取两份100 mL的该溶液分别进行如下实验(已知: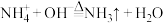 ):
):(1)第一份加足量NaOH溶液,加热,收集到标准状况下的气体448 mL。
(2)第二份加足量BaCl2溶液,得沉淀4.30 g,再用足量盐酸洗涤、干燥后,沉淀质量为2.33 g。
根据上述实验,下列推测正确的是
A.原溶液中一定存在的离子为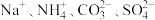 |
| B.原溶液中Na+的物质的量浓度至少为0.1 mol/L |
| C.原溶液中Cl-一定不存在 |
D.原溶液中 的物质的量浓度为0.01 mol/L 的物质的量浓度为0.01 mol/L |
您最近一年使用:0次
2024-02-29更新
|
177次组卷
|
4卷引用:安徽省合肥市第一中学2023-2024学年高一下学期月考化学试题(一)
名校
2 . 胆矾(CuSO4·5H2O)又名蓝矾,是化学工业、医药领域中的常见物质。某实验小组利用有色金属加工企业的废材制得粗胆矾晶体。
(1)制得的粗晶体中可能含有Fe2(SO4)3、FeCl3 杂质,选用下列试剂,确定所含杂质。可选试剂有:蒸馏水、稀硫酸、氨水、Ba(NO3)2 溶液、BaCl2 溶液、AgNO3 溶液。请补充以下实验步骤:
①取一定量样品,加入蒸馏水、稀硫酸,固体溶解,得到蓝色透明溶液;
②取少量①所得溶液,滴加_______ 至过量,先析出沉淀,后沉淀部分溶解,过滤得深蓝色溶液,滤渣为红褐色;
③另取少量①所得溶液,加入足量的_______ 溶液,出现白色沉淀;
④取③中所得上层清液,加入_______ 溶液,无明显现象。
实验结论:粗胆矾晶体中含有Fe2(SO4)3,不含FeCl3。
(2)CuSO4·5H2O的含量测定:
①称取1.250g产品配成100 mL溶液,取25.00 mL溶液于锥形瓶中,加入足量NaF溶液后,再滴加KI溶液至不再产生CuI沉淀;
②以淀粉溶液作为指示剂,用0.1000 mol·L-1 Na2S2O3标准溶液进行滴定,平行滴定3次。已知:Fe3++6F-=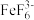 ;I2+2Na2S2O3=2NaI+Na2S4O6
;I2+2Na2S2O3=2NaI+Na2S4O6
请回答:步骤①中,加入足量NaF溶液的可能原因是_______ ,若不加NaF溶液,可导致最终的测量值_______ (填 “偏大”“偏小”或“无影响”)。滴加KI溶液生成沉淀的离子方程式为_______ ; 若Na2S2O3标准溶液的平均用量为10.00 mL,则产品中胆矾的质量分数为_______ 。
(1)制得的粗晶体中可能含有Fe2(SO4)3、FeCl3 杂质,选用下列试剂,确定所含杂质。可选试剂有:蒸馏水、稀硫酸、氨水、Ba(NO3)2 溶液、BaCl2 溶液、AgNO3 溶液。请补充以下实验步骤:
①取一定量样品,加入蒸馏水、稀硫酸,固体溶解,得到蓝色透明溶液;
②取少量①所得溶液,滴加
③另取少量①所得溶液,加入足量的
④取③中所得上层清液,加入
实验结论:粗胆矾晶体中含有Fe2(SO4)3,不含FeCl3。
(2)CuSO4·5H2O的含量测定:
①称取1.250g产品配成100 mL溶液,取25.00 mL溶液于锥形瓶中,加入足量NaF溶液后,再滴加KI溶液至不再产生CuI沉淀;
②以淀粉溶液作为指示剂,用0.1000 mol·L-1 Na2S2O3标准溶液进行滴定,平行滴定3次。已知:Fe3++6F-=
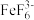 ;I2+2Na2S2O3=2NaI+Na2S4O6
;I2+2Na2S2O3=2NaI+Na2S4O6请回答:步骤①中,加入足量NaF溶液的可能原因是
您最近一年使用:0次
名校
解题方法
3 . 某溶液仅由 、Cl-、
、Cl-、  、
、 、
、 、Fe3+、Al3+和K+中的若干种离子组成,且各离子浓度相等,取适量溶液进行如下实验:
、Fe3+、Al3+和K+中的若干种离子组成,且各离子浓度相等,取适量溶液进行如下实验:
①取该溶液加入过量NaOH溶液,加热,产生无色气体;
②将①过滤、洗涤、灼烧,得到固体a;
③向上述滤液中加足量BaCl2 溶液,产生白色沉淀:
根据以上实验,下列推断错误的是
 、Cl-、
、Cl-、  、
、 、
、 、Fe3+、Al3+和K+中的若干种离子组成,且各离子浓度相等,取适量溶液进行如下实验:
、Fe3+、Al3+和K+中的若干种离子组成,且各离子浓度相等,取适量溶液进行如下实验:①取该溶液加入过量NaOH溶液,加热,产生无色气体;
②将①过滤、洗涤、灼烧,得到固体a;
③向上述滤液中加足量BaCl2 溶液,产生白色沉淀:
根据以上实验,下列推断错误的是
A.根据操作①,推断一定存在 |
| B.②中固体a为氧化铁 |
C.原溶液中一定不存在  、Al3+,可能含有K+ 、Al3+,可能含有K+ |
D.说明原溶液中一定存在 、Cl-、 、Cl-、 、 、 、Fe3+、 、Fe3+、 |
您最近一年使用:0次
2023-04-26更新
|
2133次组卷
|
11卷引用:安徽省马鞍山市2023届高三第一次教学质量监测(一模)理综化学试题
安徽省马鞍山市2023届高三第一次教学质量监测(一模)理综化学试题宁夏回族自治区石嘴山市第三中学2022-2023学年高三下学期第四次模拟考试理综化学试题(已下线)考点巩固卷02 化学物质及其变化(3大考点44题)?-2024年高考化学一轮复习考点通关卷(新高考通用)(已下线)开学摸底考试卷-2024年高考化学一轮复习考点通关卷(新高考通用)(已下线)专题12 水溶液中的离子反应与平衡-2023年高考化学真题题源解密(全国通用)河北省泊头市第一中学2023-2024学年高三上学期开学考试化学试题河南省商丘市第一高级中学2023-2024学年高三上学期10月份月考化学试题辽宁省锦州市渤海大学附属高级中学2023-2024学年高三上学期第二次考试化学试题江西省名校协作体2023-2024学年高三上学期11月期中化学试题2023届宁夏石嘴山第三中学高三下学期第四次模拟理科综合试题(已下线)题型4 离子反应 氧化还原反应(25题)-2024年高考化学常考点必杀300题(新高考通用)
名校
4 . 下列实验“操作和现象”与“结论”对应关系正确的是
| 选项 | 实验操作及现象 | 实验结论 |
| A | 向某溶液中加BaCl2溶液,有白色沉淀生成,加盐酸酸化,沉淀不溶解 | 该溶液中一定含有 |
| B | 向某溶液中同时加入几滴KSCN溶液和少量新制的氯水,溶液变为红色 | 该溶液中一定含有Fe2+ |
| C | 向某溶液中加入稀盐酸,产生能使澄清石灰水变浑浊的无色气体 | 该溶液中不一定含有 |
| D | 向某溶液加硝酸银溶液,产生白色沉淀 | 该溶液中一定含有Cl- |
A.A  | B.B  | C.C  | D.D |
您最近一年使用:0次
2022-12-11更新
|
425次组卷
|
7卷引用:安徽省淮北市第一中学2022-2023学年高一上学期期末考试化学试题
名校
解题方法
5 . 某无色待测液中可能含有 、
、 、
、 、
、 、
、 等阳离子。某同学进行如下实验:
等阳离子。某同学进行如下实验:
I.加入过量的稀盐酸,有白色沉淀生成。
II.过滤,取少许滤液,向其中加入过量的稀硫酸,又有白色沉淀生成。
III.另取少量步骤II中的滤液,加入 溶液至溶液呈碱性,加热,可产生使湿润的红色石蕊试纸变蓝色的气体。
溶液至溶液呈碱性,加热,可产生使湿润的红色石蕊试纸变蓝色的气体。
请回答下列问题:
(1)待测液中一定含有的离子是_______ ,一定不含有的离子是_______ 。
(2)还有一种离子不能确定是否存在,检验这种离子的实验时观察到的现象是_______ 。
(3)请你写出“步骤III”中产生气体的离子方程式_______ 。
 、
、 、
、 、
、 、
、 等阳离子。某同学进行如下实验:
等阳离子。某同学进行如下实验:I.加入过量的稀盐酸,有白色沉淀生成。
II.过滤,取少许滤液,向其中加入过量的稀硫酸,又有白色沉淀生成。
III.另取少量步骤II中的滤液,加入
 溶液至溶液呈碱性,加热,可产生使湿润的红色石蕊试纸变蓝色的气体。
溶液至溶液呈碱性,加热,可产生使湿润的红色石蕊试纸变蓝色的气体。请回答下列问题:
(1)待测液中一定含有的离子是
(2)还有一种离子不能确定是否存在,检验这种离子的实验时观察到的现象是
(3)请你写出“步骤III”中产生气体的离子方程式
您最近一年使用:0次
名校
解题方法
6 . 某无色透明溶液中加入 后,有无色无味气体产生,同时产生沉淀。则原溶液中可能含有的离子是
后,有无色无味气体产生,同时产生沉淀。则原溶液中可能含有的离子是
 后,有无色无味气体产生,同时产生沉淀。则原溶液中可能含有的离子是
后,有无色无味气体产生,同时产生沉淀。则原溶液中可能含有的离子是A. | B. | C. | D. |
您最近一年使用:0次
2022-07-07更新
|
1140次组卷
|
12卷引用:安徽省芜湖市无为市华星学校2020-2021学年高一上学期第二次月考化学试题
安徽省芜湖市无为市华星学校2020-2021学年高一上学期第二次月考化学试题人教版(2019)高一必修第一册第二章 海水中的重要元素 第一节 钠及其化合物 课时2 钠的几种化合物 焰色试验湖南省长沙市周南中学2020-2021学年高一上学期第一次月考化学试题湖南省湘潭电机子弟中学2020-2021学年高一上学期段考化学试题陕西省咸阳市2021-2022学年高一下学期期末考试化学试题(已下线)第07讲 钠及其氧化物-【帮课堂】2022-2023学年高一化学同步精品讲义(人教2019必修第一册 )云南省玉溪市通海县第一中学2021—2022学年高一上学期期末考试化学试题广东省佛山市禅城区2022-2023学年高三统一调研测试(一) 化学试题广东省珠海市教研联盟(两校)2022-2023学年高三上学期十月联考化学试题广东省佛山市禅城区2022-2023学年高三上学期统一调研测试(一)化学试题福建省福州市三校2022-2023学年高三上学期期中联考化学试题广东省陆丰市甲子中学2022-2023学年高三上学期第三次月考化学试题
7 . 磷酸亚铁锂(LiFePO4)是生产锂电池的重要材料。实验室中用下图装置制备LiFePO4:在仪器A中加入40mL蒸馏水、少量抗坏血酸,再加入0.01molH3PO4和0.01molFeSO4·7H2O,用搅拌器搅拌溶解后,缓慢加入0.03molLiOH·H2O,继续搅拌5min。快速将反应液装入反应釜中,保持170℃恒温5h。
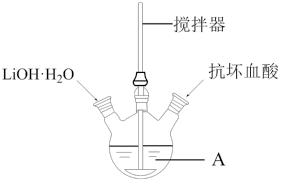
(1)仪器A的名称是_______ ;实验所用蒸馏水若未经煮沸直接使用,则可能发生反应的离子方程式为_______ 。
(2)实验中可用Na2SO3代替抗坏血酸,其原理是_______ (用离子方程式表示);不能用铁粉代替抗坏血酸的原因是_______ 。
(3)反应釜中反应充分后,要得到LiFePO4固体产品的实验操作是将反应液冷却至室温,_______ 、用蒸馏水洗涤沉淀、_______ 。
(4)检验产品中是否混有Fe(OH)3或FePO4杂质的方法是_______ 。
(5)若实验得到无杂质产品1.28g,则LiFePO4的产率为_______ %(保留小数点后1位)。

(1)仪器A的名称是
(2)实验中可用Na2SO3代替抗坏血酸,其原理是
(3)反应釜中反应充分后,要得到LiFePO4固体产品的实验操作是将反应液冷却至室温,
(4)检验产品中是否混有Fe(OH)3或FePO4杂质的方法是
(5)若实验得到无杂质产品1.28g,则LiFePO4的产率为
您最近一年使用:0次
名校
8 . 硫及其化合物在生产中应用广泛。
(1)古文献《新修本草》关于绿矾 的记载:“本来绿色,新出窟未见风者,正如琉璃,烧之赤色”。《物理小识》中记录:“青矾厂气熏人,衣服当之易烂。栽木不茂”。
的记载:“本来绿色,新出窟未见风者,正如琉璃,烧之赤色”。《物理小识》中记录:“青矾厂气熏人,衣服当之易烂。栽木不茂”。
①实验室检验绿矾变质的试剂是___________ (填化学式,下同)溶液。
②“青矾厂气”中一定含有___________ ,赤色固体可能是___________ 。
(2)“价类二维”和“性质决定用途”是化学学科的两种重要思维方式。部分含硫物质的分类与相应硫元素的化合价关系如图所示。
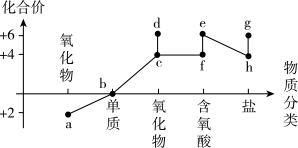
①下列物质能与d反应,但不属于氧化还原反应的是___________ (填序号)。
A. 溶液 B.
溶液 B. 溶液 C.
溶液 C. D.
D. 溶液
溶液
②f的钠盐长期放置容易变质,原因为___________ (用化学方程式表示)。
③为确认工业废气中含有c和d,将其通入依次以下装置。
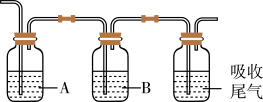
A、B中供选择的试剂有:a.品红 b. c.
c. d.
d. e.浓硫酸
e.浓硫酸
B中溶液为___________ (填标号),可观察到A中的现象为___________ 。
(3)硫酸的产量是衡量一个国家无机化工发展水平的标志。甲、乙两位同学用铜和硫酸作原料,设计了两种制取硫酸铜的方案。
方案甲:铜与浓硫酸加热直接反应,即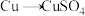 。
。
方案乙: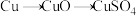 。
。
①方案甲中,铜和浓硫酸发生反应的化学方程式是___________ 。该反应体现了浓硫酸的___________ 。
②这两种方案,你认为哪一种方案更合理?___________ 。理由是___________ 。
(1)古文献《新修本草》关于绿矾
 的记载:“本来绿色,新出窟未见风者,正如琉璃,烧之赤色”。《物理小识》中记录:“青矾厂气熏人,衣服当之易烂。栽木不茂”。
的记载:“本来绿色,新出窟未见风者,正如琉璃,烧之赤色”。《物理小识》中记录:“青矾厂气熏人,衣服当之易烂。栽木不茂”。①实验室检验绿矾变质的试剂是
②“青矾厂气”中一定含有
(2)“价类二维”和“性质决定用途”是化学学科的两种重要思维方式。部分含硫物质的分类与相应硫元素的化合价关系如图所示。

①下列物质能与d反应,但不属于氧化还原反应的是
A.
 溶液 B.
溶液 B. 溶液 C.
溶液 C. D.
D. 溶液
溶液②f的钠盐长期放置容易变质,原因为
③为确认工业废气中含有c和d,将其通入依次以下装置。

A、B中供选择的试剂有:a.品红 b.
 c.
c. d.
d. e.浓硫酸
e.浓硫酸B中溶液为
(3)硫酸的产量是衡量一个国家无机化工发展水平的标志。甲、乙两位同学用铜和硫酸作原料,设计了两种制取硫酸铜的方案。
方案甲:铜与浓硫酸加热直接反应,即
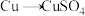 。
。方案乙:
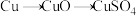 。
。①方案甲中,铜和浓硫酸发生反应的化学方程式是
②这两种方案,你认为哪一种方案更合理?
您最近一年使用:0次
9 . 下列有关实验操作、现象和结论均正确的是
| 选项 | 实验操作 | 现象 | 结论 |
| A | 向某白色晶体中滴加几滴浓硫酸,将湿润的品红试纸靠近试管口 | 产生的无色气体使试纸变白 | 该晶体中一定含有SO |
| B | 向5mL0.1mol·L-1KI溶液中加入10mL0.1mol·L-1FeCl3溶液,充分反应后滴加KSCN溶液 | 溶液变红 | I-与Fe3+的反应是可逆反应 |
| C | 常温下,用pH计测量0.1mol·L-1NH4CN溶液的pH | pH=8.6 | 电离平衡常数:Kb(NH3·H2O)>Ka(HCN) |
| D | 取一支试管装入2mL2mol·L-1NaOH溶液,先滴入1mL1mol·L-1MgCl2溶液,再滴入几滴1mol·L-1CuCl2溶液 | 先生成白色沉淀,后沉淀变为蓝色 | Ksp[Cu(OH)2]>Ksp(Mg(OH)2) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
10 . 下列检验或鉴别的说法中,不正确的是
| A.用相互滴加的方法可以鉴别盐酸和Na2CO3溶液 |
| B.某气体可使淀粉—KI溶液变蓝,该气体一定是Cl2 |
| C.某溶液的焰色试验呈黄色,该溶液中可能含有钾元素 |
| D.某溶液滴入KSCN溶液不变红,再滴入氯水后溶液变红,则原溶液中一定含有Fe2+ |
您最近一年使用:0次
2022-04-04更新
|
177次组卷
|
2卷引用:安徽省六安第一中学2021-2022学年高一上学期期末考试化学试题



