名校
1 . 研究含氮元素物质的反应对生产、生活、科研等方面具有重要的意义。请回答下列问题: 不稳定,在水溶液中就会发生歧化反应,其中一种产物为
不稳定,在水溶液中就会发生歧化反应,其中一种产物为 。
。
请回答:
(1)写出肼的电子式______ 。
(2)写出反应I的化学方程式______ 。
(3)下列说法正确的是______。
(4)已知: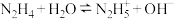 ,
, 与
与 溶液作用,产生常见气体M,并生成一种溶于稀硝酸的白色沉淀N。
溶液作用,产生常见气体M,并生成一种溶于稀硝酸的白色沉淀N。
①生成的气体M和白色沉淀N的成分分别是______ 、______ (填化学式)。
②请设计实验验证白色沉淀N的组成元素______ 。

已知:①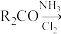
 (异肼)
(异肼)
 不稳定,在水溶液中就会发生歧化反应,其中一种产物为
不稳定,在水溶液中就会发生歧化反应,其中一种产物为 。
。请回答:
(1)写出肼的电子式
(2)写出反应I的化学方程式
(3)下列说法正确的是______。
A.碱性: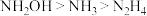 |
| B.肼可以用做还原剂,也可用做配合物的配体 |
| C.肼在水中的溶解度小于在苯中的溶解度 |
| D.反应Ⅱ中的产物之一可以循环利用 |
(4)已知:
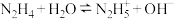 ,
, 与
与 溶液作用,产生常见气体M,并生成一种溶于稀硝酸的白色沉淀N。
溶液作用,产生常见气体M,并生成一种溶于稀硝酸的白色沉淀N。①生成的气体M和白色沉淀N的成分分别是
②请设计实验验证白色沉淀N的组成元素
您最近一年使用:0次
名校
2 . 胆矾(CuSO4·5H2O)又名蓝矾,是化学工业、医药领域中的常见物质。某实验小组利用有色金属加工企业的废材制得粗胆矾晶体。
(1)制得的粗晶体中可能含有Fe2(SO4)3、FeCl3 杂质,选用下列试剂,确定所含杂质。可选试剂有:蒸馏水、稀硫酸、氨水、Ba(NO3)2 溶液、BaCl2 溶液、AgNO3 溶液。请补充以下实验步骤:
①取一定量样品,加入蒸馏水、稀硫酸,固体溶解,得到蓝色透明溶液;
②取少量①所得溶液,滴加_______ 至过量,先析出沉淀,后沉淀部分溶解,过滤得深蓝色溶液,滤渣为红褐色;
③另取少量①所得溶液,加入足量的_______ 溶液,出现白色沉淀;
④取③中所得上层清液,加入_______ 溶液,无明显现象。
实验结论:粗胆矾晶体中含有Fe2(SO4)3,不含FeCl3。
(2)CuSO4·5H2O的含量测定:
①称取1.250g产品配成100 mL溶液,取25.00 mL溶液于锥形瓶中,加入足量NaF溶液后,再滴加KI溶液至不再产生CuI沉淀;
②以淀粉溶液作为指示剂,用0.1000 mol·L-1 Na2S2O3标准溶液进行滴定,平行滴定3次。已知:Fe3++6F-=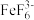 ;I2+2Na2S2O3=2NaI+Na2S4O6
;I2+2Na2S2O3=2NaI+Na2S4O6
请回答:步骤①中,加入足量NaF溶液的可能原因是_______ ,若不加NaF溶液,可导致最终的测量值_______ (填 “偏大”“偏小”或“无影响”)。滴加KI溶液生成沉淀的离子方程式为_______ ; 若Na2S2O3标准溶液的平均用量为10.00 mL,则产品中胆矾的质量分数为_______ 。
(1)制得的粗晶体中可能含有Fe2(SO4)3、FeCl3 杂质,选用下列试剂,确定所含杂质。可选试剂有:蒸馏水、稀硫酸、氨水、Ba(NO3)2 溶液、BaCl2 溶液、AgNO3 溶液。请补充以下实验步骤:
①取一定量样品,加入蒸馏水、稀硫酸,固体溶解,得到蓝色透明溶液;
②取少量①所得溶液,滴加
③另取少量①所得溶液,加入足量的
④取③中所得上层清液,加入
实验结论:粗胆矾晶体中含有Fe2(SO4)3,不含FeCl3。
(2)CuSO4·5H2O的含量测定:
①称取1.250g产品配成100 mL溶液,取25.00 mL溶液于锥形瓶中,加入足量NaF溶液后,再滴加KI溶液至不再产生CuI沉淀;
②以淀粉溶液作为指示剂,用0.1000 mol·L-1 Na2S2O3标准溶液进行滴定,平行滴定3次。已知:Fe3++6F-=
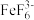 ;I2+2Na2S2O3=2NaI+Na2S4O6
;I2+2Na2S2O3=2NaI+Na2S4O6请回答:步骤①中,加入足量NaF溶液的可能原因是
您最近一年使用:0次
3 . 检验某溶液中是否含有 的操作方法
的操作方法___________
 的操作方法
的操作方法
您最近一年使用:0次
21-22高一下·上海浦东新·期中
名校
解题方法
4 . 铁元素在化合物中有多种化合价,常见的有+2,+3价。
Ⅰ.某溶液中有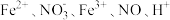 和
和 六种粒子,分别属于同一氧化还原反应中的反应物和生成物。
六种粒子,分别属于同一氧化还原反应中的反应物和生成物。
(1)请写出该反应的离子方程式___________ 。
(2)该反应中氧化剂与还原剂的物质的量之比为___________ ;产生2mol还原产物时转移电子的总数为___________ 。
Ⅱ.磁铁矿的主要成分是 。某同学设计实验证明磁铁矿石中存在+2、+3价的铁元素。步骤如下:
。某同学设计实验证明磁铁矿石中存在+2、+3价的铁元素。步骤如下:
①取少量磁铁矿石样品,加入过量的试剂A溶解。
②验证:
取溶解后的液体少许,加入少量试剂B,观察现象。
③验证:
取溶解后的液体少许,加入少量试剂C,观察现象。
(3)试剂A为___________ ,发生反应的离子方程式为___________ 。
(4)试剂B为___________ ,观察到___________ ,则证明有 。
。
(5)试剂C为___________ ,观察到___________ ,则证明有 。
。
Ⅰ.某溶液中有
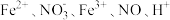 和
和 六种粒子,分别属于同一氧化还原反应中的反应物和生成物。
六种粒子,分别属于同一氧化还原反应中的反应物和生成物。(1)请写出该反应的离子方程式
(2)该反应中氧化剂与还原剂的物质的量之比为
Ⅱ.磁铁矿的主要成分是
 。某同学设计实验证明磁铁矿石中存在+2、+3价的铁元素。步骤如下:
。某同学设计实验证明磁铁矿石中存在+2、+3价的铁元素。步骤如下:①取少量磁铁矿石样品,加入过量的试剂A溶解。
②验证:

取溶解后的液体少许,加入少量试剂B,观察现象。
③验证:

取溶解后的液体少许,加入少量试剂C,观察现象。
(3)试剂A为
(4)试剂B为
 。
。(5)试剂C为
 。
。
您最近一年使用:0次
名校
解题方法
5 . 某无色待测液中可能含有 、
、 、
、 、
、 、
、 等阳离子。某同学进行如下实验:
等阳离子。某同学进行如下实验:
I.加入过量的稀盐酸,有白色沉淀生成。
II.过滤,取少许滤液,向其中加入过量的稀硫酸,又有白色沉淀生成。
III.另取少量步骤II中的滤液,加入 溶液至溶液呈碱性,加热,可产生使湿润的红色石蕊试纸变蓝色的气体。
溶液至溶液呈碱性,加热,可产生使湿润的红色石蕊试纸变蓝色的气体。
请回答下列问题:
(1)待测液中一定含有的离子是_______ ,一定不含有的离子是_______ 。
(2)还有一种离子不能确定是否存在,检验这种离子的实验时观察到的现象是_______ 。
(3)请你写出“步骤III”中产生气体的离子方程式_______ 。
 、
、 、
、 、
、 、
、 等阳离子。某同学进行如下实验:
等阳离子。某同学进行如下实验:I.加入过量的稀盐酸,有白色沉淀生成。
II.过滤,取少许滤液,向其中加入过量的稀硫酸,又有白色沉淀生成。
III.另取少量步骤II中的滤液,加入
 溶液至溶液呈碱性,加热,可产生使湿润的红色石蕊试纸变蓝色的气体。
溶液至溶液呈碱性,加热,可产生使湿润的红色石蕊试纸变蓝色的气体。请回答下列问题:
(1)待测液中一定含有的离子是
(2)还有一种离子不能确定是否存在,检验这种离子的实验时观察到的现象是
(3)请你写出“步骤III”中产生气体的离子方程式
您最近一年使用:0次
名校
6 . 硫及其化合物在生产中应用广泛。
(1)古文献《新修本草》关于绿矾 的记载:“本来绿色,新出窟未见风者,正如琉璃,烧之赤色”。《物理小识》中记录:“青矾厂气熏人,衣服当之易烂。栽木不茂”。
的记载:“本来绿色,新出窟未见风者,正如琉璃,烧之赤色”。《物理小识》中记录:“青矾厂气熏人,衣服当之易烂。栽木不茂”。
①实验室检验绿矾变质的试剂是___________ (填化学式,下同)溶液。
②“青矾厂气”中一定含有___________ ,赤色固体可能是___________ 。
(2)“价类二维”和“性质决定用途”是化学学科的两种重要思维方式。部分含硫物质的分类与相应硫元素的化合价关系如图所示。
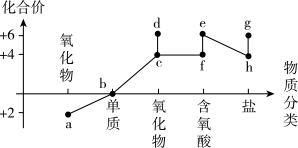
①下列物质能与d反应,但不属于氧化还原反应的是___________ (填序号)。
A. 溶液 B.
溶液 B. 溶液 C.
溶液 C. D.
D. 溶液
溶液
②f的钠盐长期放置容易变质,原因为___________ (用化学方程式表示)。
③为确认工业废气中含有c和d,将其通入依次以下装置。
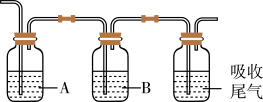
A、B中供选择的试剂有:a.品红 b. c.
c. d.
d. e.浓硫酸
e.浓硫酸
B中溶液为___________ (填标号),可观察到A中的现象为___________ 。
(3)硫酸的产量是衡量一个国家无机化工发展水平的标志。甲、乙两位同学用铜和硫酸作原料,设计了两种制取硫酸铜的方案。
方案甲:铜与浓硫酸加热直接反应,即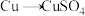 。
。
方案乙: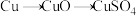 。
。
①方案甲中,铜和浓硫酸发生反应的化学方程式是___________ 。该反应体现了浓硫酸的___________ 。
②这两种方案,你认为哪一种方案更合理?___________ 。理由是___________ 。
(1)古文献《新修本草》关于绿矾
 的记载:“本来绿色,新出窟未见风者,正如琉璃,烧之赤色”。《物理小识》中记录:“青矾厂气熏人,衣服当之易烂。栽木不茂”。
的记载:“本来绿色,新出窟未见风者,正如琉璃,烧之赤色”。《物理小识》中记录:“青矾厂气熏人,衣服当之易烂。栽木不茂”。①实验室检验绿矾变质的试剂是
②“青矾厂气”中一定含有
(2)“价类二维”和“性质决定用途”是化学学科的两种重要思维方式。部分含硫物质的分类与相应硫元素的化合价关系如图所示。

①下列物质能与d反应,但不属于氧化还原反应的是
A.
 溶液 B.
溶液 B. 溶液 C.
溶液 C. D.
D. 溶液
溶液②f的钠盐长期放置容易变质,原因为
③为确认工业废气中含有c和d,将其通入依次以下装置。

A、B中供选择的试剂有:a.品红 b.
 c.
c. d.
d. e.浓硫酸
e.浓硫酸B中溶液为
(3)硫酸的产量是衡量一个国家无机化工发展水平的标志。甲、乙两位同学用铜和硫酸作原料,设计了两种制取硫酸铜的方案。
方案甲:铜与浓硫酸加热直接反应,即
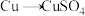 。
。方案乙:
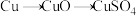 。
。①方案甲中,铜和浓硫酸发生反应的化学方程式是
②这两种方案,你认为哪一种方案更合理?
您最近一年使用:0次
7 . 为检验某种阳离子为Na+的溶液中含有的阴离子是SO 、CO
、CO 还是OH-、Cl-,下列设计的方案中合理的是
还是OH-、Cl-,下列设计的方案中合理的是____ 。
方案一:检验CO :向待测液中加入足量的盐酸产生气泡,将气体通入澄清石灰水中有白色沉淀生成
:向待测液中加入足量的盐酸产生气泡,将气体通入澄清石灰水中有白色沉淀生成
方案二:检验SO :先向待测液中加入盐酸至溶液呈酸性,未见沉淀或气体生成,再加入BaCl2溶液出现白色沉淀
:先向待测液中加入盐酸至溶液呈酸性,未见沉淀或气体生成,再加入BaCl2溶液出现白色沉淀
方案三:检验OH-:向待测液中加入石蕊溶液,溶液变蓝色
方案四:检验Cl-:向待测溶液中依次加入稀盐酸和AgNO3溶液,有白色沉淀生成
 、CO
、CO 还是OH-、Cl-,下列设计的方案中合理的是
还是OH-、Cl-,下列设计的方案中合理的是方案一:检验CO
 :向待测液中加入足量的盐酸产生气泡,将气体通入澄清石灰水中有白色沉淀生成
:向待测液中加入足量的盐酸产生气泡,将气体通入澄清石灰水中有白色沉淀生成方案二:检验SO
 :先向待测液中加入盐酸至溶液呈酸性,未见沉淀或气体生成,再加入BaCl2溶液出现白色沉淀
:先向待测液中加入盐酸至溶液呈酸性,未见沉淀或气体生成,再加入BaCl2溶液出现白色沉淀方案三:检验OH-:向待测液中加入石蕊溶液,溶液变蓝色
方案四:检验Cl-:向待测溶液中依次加入稀盐酸和AgNO3溶液,有白色沉淀生成
您最近一年使用:0次
名校
解题方法
8 . (1)向NaHSO4溶液中滴加Ba(OH)2溶液至中性,发生反应的离子方程式为___ ,若继续滴加Ba(OH)2溶液,又发生反应的离子方程式为_______ 。
(2)+6价铬的化合物毒性较大,常用NaHSO3将废液中的Cr2O 还原成Cr3+,该反应的离子方程式为
还原成Cr3+,该反应的离子方程式为______ 。
(3)向偏铝酸钠溶液中通入足量CO2的离子方程式为_____
(4)用电石制得的乙炔中常含有PH3和H2S杂质而带有臭味,可通过CuSO4溶液洗气除去。
①___ ____CuSO4+_______PH3+_______H2O=_____Cu3P↓+______H3PO4+____H2SO4,此反应中:氧化剂和还原剂物质的量之比为_______ ,若生成1mol Cu3P,转移电子数为______ 。
②H2S气体和CuSO4溶液反应有黑色沉淀产生,离子方程式为______
(5)检验某溶液中只有Fe2+而不含有Fe3+,方法是______
(2)+6价铬的化合物毒性较大,常用NaHSO3将废液中的Cr2O
 还原成Cr3+,该反应的离子方程式为
还原成Cr3+,该反应的离子方程式为(3)向偏铝酸钠溶液中通入足量CO2的离子方程式为
(4)用电石制得的乙炔中常含有PH3和H2S杂质而带有臭味,可通过CuSO4溶液洗气除去。
①
②H2S气体和CuSO4溶液反应有黑色沉淀产生,离子方程式为
(5)检验某溶液中只有Fe2+而不含有Fe3+,方法是
您最近一年使用:0次
20-21高二下·浙江·阶段练习
9 . 牙膏是生活必需品。下面是牙膏中某些主要成分的检验流程图:
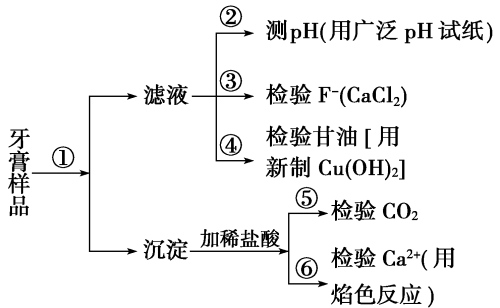
请回答下列问题:
(1)在①中加水、搅拌、静置后,接下来的实验操作名称是_______ ,所需要的主要玻璃仪器有_______ 。
(2)在②中用pH试纸测溶液的pH的操作方法是_______ 。
(3)写出④中发生反应的化学方程式_______ 。
(4)在⑥中检验Ca2+的存在,除可用焰色反应外,还可利用Ca2+和_______ 溶液的反应来进行。

请回答下列问题:
(1)在①中加水、搅拌、静置后,接下来的实验操作名称是
(2)在②中用pH试纸测溶液的pH的操作方法是
(3)写出④中发生反应的化学方程式
(4)在⑥中检验Ca2+的存在,除可用焰色反应外,还可利用Ca2+和
您最近一年使用:0次
名校
解题方法
10 . 某无色溶液只可能含有下列离子Na+、Ba2+、Cu2+、CO 、Cl﹣、Mg2+中的某些离子。①向此溶液中滴加稀盐酸无明显现象。②取少量①的溶液并加入少量的Na2SO4溶液,有白色沉淀产生。③取②的上层清液并加入过量的NaOH溶液,无明显现象。
、Cl﹣、Mg2+中的某些离子。①向此溶液中滴加稀盐酸无明显现象。②取少量①的溶液并加入少量的Na2SO4溶液,有白色沉淀产生。③取②的上层清液并加入过量的NaOH溶液,无明显现象。
(1)应最先判断出溶液中一定不含有哪种离子______ ,说明判断的理由____________ 。由步骤①可判断原溶液中一定不含有的离子是______ ,说明判断的理由____________ 。
(2)②中反应的离子方程式为________ 。不能确定是否含有的离子是______ 。
 、Cl﹣、Mg2+中的某些离子。①向此溶液中滴加稀盐酸无明显现象。②取少量①的溶液并加入少量的Na2SO4溶液,有白色沉淀产生。③取②的上层清液并加入过量的NaOH溶液,无明显现象。
、Cl﹣、Mg2+中的某些离子。①向此溶液中滴加稀盐酸无明显现象。②取少量①的溶液并加入少量的Na2SO4溶液,有白色沉淀产生。③取②的上层清液并加入过量的NaOH溶液,无明显现象。(1)应最先判断出溶液中一定不含有哪种离子
(2)②中反应的离子方程式为
您最近一年使用:0次
2020-12-03更新
|
101次组卷
|
2卷引用:青海省西宁市海湖中学2020-2021学年高一上学期第二次阶段考试化学试题



