| 选项 | 试剂 | 试纸或试液 | 现象 | 结论 |
| A | 浓氨水、生石灰 | 红色石蕊试纸 | 变蓝 | NH3为碱性气体 |
| B | 浓盐酸、浓硫酸 | pH试纸 | 变红 | HCl为酸性气体 |
| C | 浓盐酸、二氧化锰 | 淀粉碘化钾试液 | 变蓝 | Cl2具有氧化性 |
| D | 亚硫酸钠、硫酸 | 品红试液 | 褪色 | SO2具有还原性 |
| A.A | B.B | C.C | D.D |
 Fe2O3+SO2↑+SO3↑。下列有关操作、装置、原理及对现象的表述正确的是
Fe2O3+SO2↑+SO3↑。下列有关操作、装置、原理及对现象的表述正确的是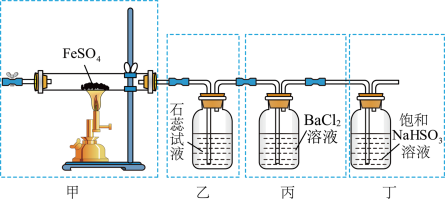
| A.用装置甲高温分解FeSO4,点燃酒精喷灯前应先向装置内通一段时间N2 |
| B.用装置乙可检验分解产生的SO2,现象是石蕊试液先变红后褪色 |
| C.用装置丙可检验分解产生的SO3,现象是产生白色沉淀 |
| D.用装置丁可吸收尾气,避免污染环境 |
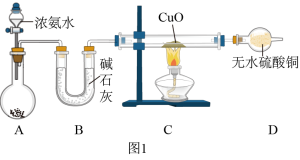
(1)如图装置制备NH3,反应方程式为
(2)装置A中烧瓶内试剂可选用
a.烧碱溶液 b.生石灰 c.浓硫酸
(3)连接好装置并检验装置的气密性后,装入试剂,然后应先
Ⅰ.打开旋塞逐滴向圆底烧瓶中加入氨水 Ⅱ.加热装置C
(4)实验中观察到C中CuO粉末变红,D中无水硫酸铜变蓝,并收集到一种单质气体,则该反应相关化学方程式为
(5)图1的实验装置图存在的明显不足是
(6)向浓CaCl2溶液中通入CO2气体没现象, 但若先通入NH3,再通入CO2则可制备纳米级碳酸钙,反应方程式:
(1)实验室中利用反应2H2O2
 2H2O+O2↑制取O2,可选用的发生装置是
2H2O+O2↑制取O2,可选用的发生装置是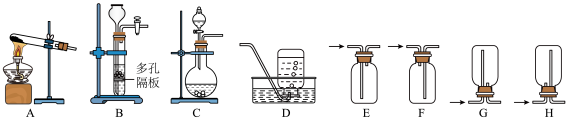
(3)过氧化氢是一种二元弱酸,写出H2O2的第一步电离方程式:
(4)某课外兴趣小组欲探究温度对H2O2电离平衡的影响,进行如下实验:
①实验任务:利用灵敏pH计测量溶液的pH,并探究电离过程是否吸热。
②查阅资料:20℃时,Ka1(H2O2)=2.4×10-12,lg6≈0.778。
③提出猜想:反应物浓度相同时;温度越高,酸性越强,pH越小。
④设计实验、验证猜想。取试样进行表正实验1~3,记录数据。
| 试祥 | 温度/℃ | pH | |
| 1 | 10mL1.5mol/L的双氧水 | 20 | X1 |
| 2 | 10mL1.5mol/L的双氧水 | 30 | X2 |
| 3 | 10mL1.5mol/L的双氧水 | 50 | X3 |
实验结果:X2<X1<X3且X1=
⑥优化实验。在20℃下进行下列实验:
| 试样 | 反应前后温度变化/℃ | |
| 4 | 10mL1.5mol/L的双氧水、10mL1.5mol/L的NaOH溶液 | △T1 |
| 5 | 10mL1.5mol/L的H2SO4溶液10mL1.5mol/L的NaOH溶液 | △T2 |
 虽是大气污染物之一,但也是重要的工业原料,某同学在实验室设计如下实验,对
虽是大气污染物之一,但也是重要的工业原料,某同学在实验室设计如下实验,对 的部分性质进行了探究。
的部分性质进行了探究。(1)二氧化硫的水溶液
 易溶于水,常温常压下溶解度为
易溶于水,常温常压下溶解度为 ,溶于水生成
,溶于水生成 。已知
。已知 ,欲验证酸性:
,欲验证酸性: ,设计以下实验达到目的(部分夹持装置已省略)。装置图中
,设计以下实验达到目的(部分夹持装置已省略)。装置图中 处发生的反应的方程式为
处发生的反应的方程式为 的作用是
的作用是 的酸性强于
的酸性强于 的实验现象为
的实验现象为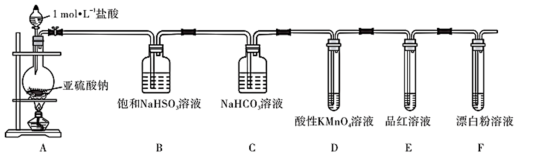
(2)①请设计简单实验方案比较室温下
 溶液中
溶液中 的电离平衡常数
的电离平衡常数 与水解平衡常数
与水解平衡常数 的相对大小:
的相对大小:②
 时,
时,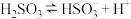 的电离常数
的电离常数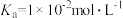 ,则该温度下
,则该温度下 、
、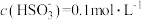 的
的 溶液中
溶液中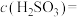
(3)亚硫酰氯(俗称氯化亚砜,
 )是一种液态化合物,沸点
)是一种液态化合物,沸点 ,在农药、制药行业、有机合成等领域用途广泛。
,在农药、制药行业、有机合成等领域用途广泛。 遇水剧烈反应,液面上产生白雾,并伴有刺激性气味的气体产生。蒸干
遇水剧烈反应,液面上产生白雾,并伴有刺激性气味的气体产生。蒸干 溶液不能得到无水
溶液不能得到无水 ,使
,使 与
与 混合加热可得到无水
混合加热可得到无水 ,试解释原因:
,试解释原因:
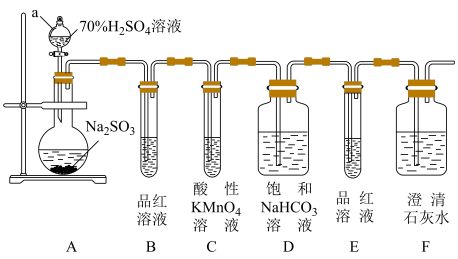
(1)仪器a的名称为
(2)①C中生成一种单质气体和红色物质,C中发生反应的化学方程式为
②实验测得反应后装置D增重mg,F中生成气体的体积折合成标准状况下为VL,则氨气中N和H的个数比为
(3)装置E中浓硫酸的作用:
(4)氨气还可以用来检测氯气管道是否泄漏,若氯气管道泄漏会有白烟和一种单质气体生成,写出反应的化学方程式:
(2)B中品红溶液褪色,是因为SO2具有
(3)证明亚硫酸酸性比碳酸酸性强的实验现象是
(4)若将SO2气体直接通入澄清石灰水中,溶液变浑浊,则该反应的离子方程式为
8 . 某班同学用如下实验探究过氧化氢的性质。回答下列问题:
(1)甲组同学拟配制5%的H2O2溶液,他们先从文献查得H2O2的稳定性与pH的关系如图所示。则配制H2O2溶液时应滴入几滴

(2)乙组同学向一支试管中加入2mLFeCl2溶液,再滴入几滴甲组同学配制的H2O2溶液,最后滴入KSCN溶液,溶液变红,H2O2与Fe2+发生反应的离子方程式为
(3)丙组同学取2mLKMnO4溶液于试管中,向其中滴几滴5%的H2O2溶液,发现溶液逐渐褪色,该反应中的还原剂是
(4)丁组同学向一支试管中加入2mL5%的H2O2溶液、0.5mL乙醚、1mLlmol/LH2SO4溶液和3~4滴0.5mol/LK2Cr2O7溶液,发现上层乙醚层为蓝色(CrO5的乙醚溶液),一段时间后上层蓝色消失。

①乙醚的主要作用是
②开始时,H2O2溶液与K2Cr2O7酸性溶液反应生成CrO5,该反应属于
③一段时间后,乙醚层中的CrO5与水相中的H+作用生成Cr3+并产生无色气泡,从而使蓝色逐渐消失,该反应的离子方程式为
 与Mg的反应,实验时首先关闭K,使①中的反应进行,然后加热玻璃管③。下列说法正确的是
与Mg的反应,实验时首先关闭K,使①中的反应进行,然后加热玻璃管③。下列说法正确的是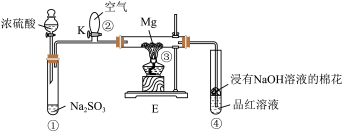
| A.②中只生成2种产物 |
| B.停止实验时,先打开K可防倒吸 |
| C.实验结束后加热④中溶液,没有明显现象 |
D.浓硫酸浓度越大生成 的速率越快 的速率越快 |
(1)甲组同学分别利用如图所示装置制取SO2 和CH4。
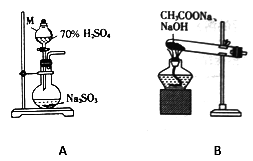
①仪器M的名称为
②用A装置制备SO2,不宜使用稀硫酸,其原因是
③用B装置制取甲烷的化学方程式为CH3COONa+NaOH
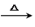 CH4↑+Na2CO3,实际实验中常用碱石灰(NaOH 和CaO的混合物)来代替NaOH,原因是
CH4↑+Na2CO3,实际实验中常用碱石灰(NaOH 和CaO的混合物)来代替NaOH,原因是(2)乙组同学利用甲组制得的CH4和SO2进行实验,并验证产物中除单质硫外还含有CO2。为进行验证,选用甲组实验中的装置A、B和下图所示的装置进行实验,发现G中有淡黄色固体生成,C中澄清石灰水变浑浊。
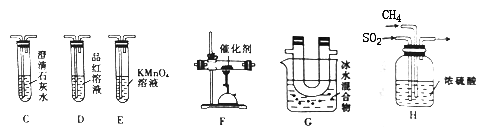
①乙组同学的实验装置中,依次连接的合理顺序为A、B→H→
②E装置的作用是
③F装置中发生反应的化学方程式为



