1 . 某同学按如图所示实验装置探究铜与浓硫酸的反应,记录如表。不正确的
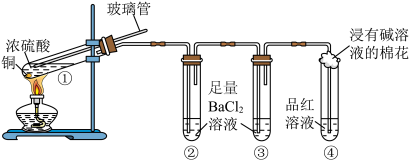

| 试管 | ① | ② | ③ | ④ |
| 实验现象 | 溶液仍为无色,有白雾、白色固体产生 | 有大量白色沉淀产生 | 有少量白色沉淀产生 | 品红溶液褪色 |
| A.①中可能有部分浓硫酸挥发了 |
B.实验时若先往装置内通入足量 ,再加热试管①,实验现象会有所不同 ,再加热试管①,实验现象会有所不同 |
C.②中白色沉淀是 |
| D.为了确定①中白色固体是否为硫酸铜,可向冷却后的试管中注入水,振荡 |
您最近一年使用:0次
名校
解题方法
2 . 骉同学制备氯气并对产生氯气的条件进行探究。
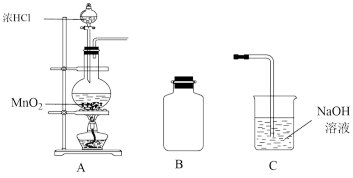
(1)装置A中用MnO2与浓盐酸反应制取Cl2,要获得纯净的Cl2,还需要将生成的气体依次通过饱和食盐水和浓硫酸,其中饱和食盐水的作用是___________ 。
(2)B用于收集Cl2,请完善装置B并用箭头标明进出气体方向___________ 。
(3)C用于吸收多余的Cl2,C中发生反应的化学方程式是___________ 。
(4)骉同学和騳同学欲研究盐酸的浓度对制Cl2的影响,设计实验进行如下探究。
根据实验现象和信息,推测完成以下问题:
①已知MnO2呈弱碱性。I中溶液呈浅棕色是由于MnO2与浓盐酸发生了复分解反应,反应的化学方程式是___________ 。
②II中发生了分解反应,反应的化学方程式是___________ 。
③騳同学猜测III中无明显现象的原因,可能是 或
或 较低,设计实验IV进行探究:
较低,设计实验IV进行探究:
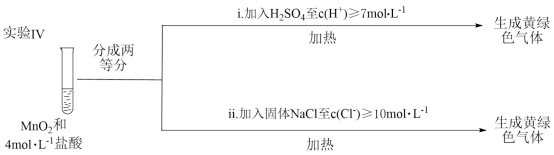
将实验III、IV进行对比,得出的结论_______ ;将i、ii进行对比,得出的结论是_______ 。

(1)装置A中用MnO2与浓盐酸反应制取Cl2,要获得纯净的Cl2,还需要将生成的气体依次通过饱和食盐水和浓硫酸,其中饱和食盐水的作用是
(2)B用于收集Cl2,请完善装置B并用箭头标明进出气体方向
(3)C用于吸收多余的Cl2,C中发生反应的化学方程式是
(4)骉同学和騳同学欲研究盐酸的浓度对制Cl2的影响,设计实验进行如下探究。
| 实验 | 操作 | 现象 |
| I | 常温下将MnO2和 浓盐酸混合 浓盐酸混合 | 溶液呈浅棕色,有刺激性气味 |
| II | 将Ⅰ中混合物过滤,加热滤液 | 生成大量黄绿色气体 |
| III | 加热MnO2和 稀盐酸混合物 稀盐酸混合物 | 无明显现象 |
①已知MnO2呈弱碱性。I中溶液呈浅棕色是由于MnO2与浓盐酸发生了复分解反应,反应的化学方程式是
②II中发生了分解反应,反应的化学方程式是
③騳同学猜测III中无明显现象的原因,可能是
 或
或 较低,设计实验IV进行探究:
较低,设计实验IV进行探究:
将实验III、IV进行对比,得出的结论
您最近一年使用:0次
名校
解题方法
3 . 为探究过氧化钠与 和
和 的反应产物成分,设计了如图实验:
的反应产物成分,设计了如图实验:

(1)写出过氧化钠与 反应的化学方程式
反应的化学方程式_______ 。
(2)实验装置中D的作用是_______ 。
(3)请解释C装置中饱和澄清石灰水变浑浊的原因:_______ 。
(4)某兴趣小组探究反应后 中
中 型管中固体成分
型管中固体成分
①推测反应后 中
中 型管中固体成分可能为:a.
型管中固体成分可能为:a.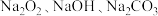 ;b.
;b.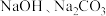 ;c.
;c._______ 。
②为了验证 与
与 和
和 的反应产物成分,他们将反应后的固体溶于水并进行如下具体操作:
的反应产物成分,他们将反应后的固体溶于水并进行如下具体操作:
③由②中实验步骤Ⅰ和Ⅱ该兴趣小组得出结论:过氧化钠与二氧化碳、水蒸气反应固体产物 和
和 ,请问该兴趣小组的结论
,请问该兴趣小组的结论_______ (填“是”或“否”)正确,判断的理由是(结合化学方程式阐述):_______ 。
 和
和 的反应产物成分,设计了如图实验:
的反应产物成分,设计了如图实验:
(1)写出过氧化钠与
 反应的化学方程式
反应的化学方程式(2)实验装置中D的作用是
(3)请解释C装置中饱和澄清石灰水变浑浊的原因:
(4)某兴趣小组探究反应后
 中
中 型管中固体成分
型管中固体成分①推测反应后
 中
中 型管中固体成分可能为:a.
型管中固体成分可能为:a.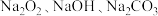 ;b.
;b.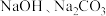 ;c.
;c.②为了验证
 与
与 和
和 的反应产物成分,他们将反应后的固体溶于水并进行如下具体操作:
的反应产物成分,他们将反应后的固体溶于水并进行如下具体操作:| 实验步骤 | 实验现象 | 实验结论 |
| Ⅰ.取少量溶液于试管中,向其中加入足量的氯化钡溶液,静置 | 产生 | 固体成分含有碳酸钠 |
| Ⅱ.取适量Ⅰ的上层清液于试管中,向其中滴加少量氯化铜溶液 | 产生蓝色沉淀 | 溶液中含 |
 和
和 ,请问该兴趣小组的结论
,请问该兴趣小组的结论
您最近一年使用:0次
2023-09-17更新
|
178次组卷
|
2卷引用:山东省菏泽市2022-2023学年高一上学期11月期中考试化学(A)试题
4 . 物质的类别和核心元素的化合价是研究物质性质的两个重要角度。“价类二维图”是研究物质性质的重要手段。下图所示是氮及其部分化合物的“价类二维图”,根据图示回答下列问题。
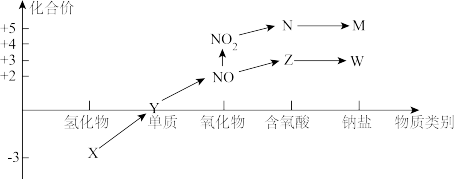
某化学兴趣小组利用如图装置制备X并探究其相关性质。

(1)从物质的性质分析,B中盛放的试剂名称为:_______ 。
(2)将D与a相连,在E中产生白色沉淀,其沉淀的化学式为:_______ ,若向a处分别通入_______ (填标号),在E中也会产生白色沉淀。
A. B.
B. C.
C. D.
D.
(3)实验发现C中粉末完全变红,D中无水硫酘铜变蓝,还产生单质Y。若C中红色固体为单质,实验后将C中固体与稀硝酸混合,充分反应后红色固体有剩余,再加入下列的_______(填标号)试剂,固体又可以继续溶解。
(4)人体正常的血红蛋白含有 ,但若误食W,会导致血红蛋白含有的
,但若误食W,会导致血红蛋白含有的 转化为
转化为 而中毒,服用维生素C可解毒。解毒时维生素C的作用是
而中毒,服用维生素C可解毒。解毒时维生素C的作用是_______ (填“还原性”或“氧化性”)。

某化学兴趣小组利用如图装置制备X并探究其相关性质。

(1)从物质的性质分析,B中盛放的试剂名称为:
(2)将D与a相连,在E中产生白色沉淀,其沉淀的化学式为:
A.
 B.
B. C.
C. D.
D.
(3)实验发现C中粉末完全变红,D中无水硫酘铜变蓝,还产生单质Y。若C中红色固体为单质,实验后将C中固体与稀硝酸混合,充分反应后红色固体有剩余,再加入下列的_______(填标号)试剂,固体又可以继续溶解。
A. 溶液 溶液 | B. 溶液 溶液 | C.稀 | D. 溶液 溶液 |
(4)人体正常的血红蛋白含有
 ,但若误食W,会导致血红蛋白含有的
,但若误食W,会导致血红蛋白含有的 转化为
转化为 而中毒,服用维生素C可解毒。解毒时维生素C的作用是
而中毒,服用维生素C可解毒。解毒时维生素C的作用是
您最近一年使用:0次
2021·广东·模拟预测
名校
5 . 铜与浓硝酸反应生成NO2,浓硝酸变稀后生成NO(沸点为−151℃),某探究小组由这一实验事实出发,猜测碳与浓硝酸反应生成NO2,浓硝酸变稀后生成NO,并设计如图所示装置进行验证(加热和尾气处理装置、夹持仪器均已略去)。回答下列问题:

(1)仪器a的名称为_______ ;N2的作用除将装置内空气排尽外,还有_______ 。
(2)打开弹簧夹1、2,在持续通入N2的条件下,先把碳加热至红热后停止加热,再缓慢滴入浓硝酸的原因为_______ ;反应产生的气体干燥后进入装置C的冷却瓶,气体颜色变浅接近于无色,其原因为_______ ;一段时间后,打开弹簧夹3,通入O2,冷却瓶中气体进入装置D后气体颜色仍无明显变化,说明该小组的猜测_______ (填“正确”或“错误”)。
(3)该小组对上面装置进行改进,验证碳被浓硝酸氧化的产物为CO2(加热装置和夹持仪器已略去)。

已知:NO2能与NaOH溶液反应,NO不能与NaOH溶液反应。
①装置F、G中的试剂可以分别选用_______ 、_______ (填标号)。
a.蒸馏水 b.NaOH溶液 c.Na2CO3溶液 d.澄清石灰水
②装置H中盛有NaOH溶液,向其中通入足量氧气进行尾气处理,生成NaNO3,该反应的离子方程式为_______ 。

(1)仪器a的名称为
(2)打开弹簧夹1、2,在持续通入N2的条件下,先把碳加热至红热后停止加热,再缓慢滴入浓硝酸的原因为
(3)该小组对上面装置进行改进,验证碳被浓硝酸氧化的产物为CO2(加热装置和夹持仪器已略去)。

已知:NO2能与NaOH溶液反应,NO不能与NaOH溶液反应。
①装置F、G中的试剂可以分别选用
a.蒸馏水 b.NaOH溶液 c.Na2CO3溶液 d.澄清石灰水
②装置H中盛有NaOH溶液,向其中通入足量氧气进行尾气处理,生成NaNO3,该反应的离子方程式为
您最近一年使用:0次
6 . “84”消毒液是一种常见的含氯消毒剂,化学实验小组同学对“84”消毒液的制备、保存及性质等进行如下探究,请回答下列问题:
(1)实验小组欲利用 与NaOH溶液反应制备“84”消毒液,选择实验装置如下:
与NaOH溶液反应制备“84”消毒液,选择实验装置如下:

①A中发生反应的离子方程式为___________ 。
②C中盛装试剂为___________ 。
③仪器的连接顺序为a→___________ (按气流方向,用小写字母表示)。
(2)D装置的作用是___________ ,若用如图E装置代替D装置,则E中溶液可选下列试剂中的___________ 。
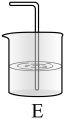
A.NaOH溶液 B.饱和NaCl溶液 C. 溶液 D.KI溶液
溶液 D.KI溶液
(3)“84”消毒液需要避光密封保存,否则容易变质而失效,用化学方程式解释其原因:
①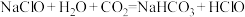 ;
;
②___________ 。
(4)将 通入到热的KOH溶液中可制得
通入到热的KOH溶液中可制得 ,该反应的离子方程式为
,该反应的离子方程式为___________ 。
(1)实验小组欲利用
 与NaOH溶液反应制备“84”消毒液,选择实验装置如下:
与NaOH溶液反应制备“84”消毒液,选择实验装置如下:
①A中发生反应的离子方程式为
②C中盛装试剂为
③仪器的连接顺序为a→
(2)D装置的作用是

A.NaOH溶液 B.饱和NaCl溶液 C.
 溶液 D.KI溶液
溶液 D.KI溶液(3)“84”消毒液需要避光密封保存,否则容易变质而失效,用化学方程式解释其原因:
①
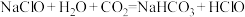 ;
;②
(4)将
 通入到热的KOH溶液中可制得
通入到热的KOH溶液中可制得 ,该反应的离子方程式为
,该反应的离子方程式为
您最近一年使用:0次
解题方法
7 . 钠及其化合物在人类生产生活中有着重大的作用。
(1)金属钠要隔绝空气密封保存,请用化学方程式表示原因(Na参与的反应)_______ 。
(2)加热条件下,钠可以在氧气中燃烧,现象是_______ 。
过氧化钠可用于呼吸面具中的氧气供给,某课外活动小组设计如图装置,证明二氧化碳跟过氧化钠反应时需要与水接触。

(3)装置①中反应的离子方程式是_______ 。
(4)装置②中的试剂的作用是_______ 。
(5)装置③中的试剂是_______ 。
(6)进行实验。步骤1:打开弹簧夹 ,关闭
,关闭 ,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处。步骤2:打开弹簧夹
,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处。步骤2:打开弹簧夹 ,关闭
,关闭 ,打开分液漏斗活塞加入盐酸,将带火量的木条放在a处。a处带火星的木条复燃的是步骤
,打开分液漏斗活塞加入盐酸,将带火量的木条放在a处。a处带火星的木条复燃的是步骤_______ (填“1”或“2”)。
(7)用单线桥表示过氧化钠跟二氧化碳反应的电子转移情况_______ 。
(1)金属钠要隔绝空气密封保存,请用化学方程式表示原因(Na参与的反应)
(2)加热条件下,钠可以在氧气中燃烧,现象是
过氧化钠可用于呼吸面具中的氧气供给,某课外活动小组设计如图装置,证明二氧化碳跟过氧化钠反应时需要与水接触。

(3)装置①中反应的离子方程式是
(4)装置②中的试剂的作用是
(5)装置③中的试剂是
(6)进行实验。步骤1:打开弹簧夹
 ,关闭
,关闭 ,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处。步骤2:打开弹簧夹
,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处。步骤2:打开弹簧夹 ,关闭
,关闭 ,打开分液漏斗活塞加入盐酸,将带火量的木条放在a处。a处带火星的木条复燃的是步骤
,打开分液漏斗活塞加入盐酸,将带火量的木条放在a处。a处带火星的木条复燃的是步骤(7)用单线桥表示过氧化钠跟二氧化碳反应的电子转移情况
您最近一年使用:0次
名校
解题方法
8 . 某化学兴趣小组对 的性质展开探究,设计了如图实验。已知
的性质展开探究,设计了如图实验。已知 为拟卤素,它的化学性质与卤素单质相似。下列说法正确的是
为拟卤素,它的化学性质与卤素单质相似。下列说法正确的是
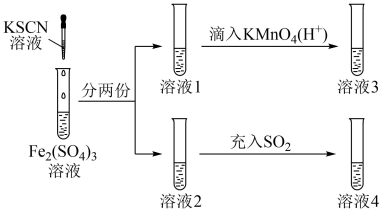
 的性质展开探究,设计了如图实验。已知
的性质展开探究,设计了如图实验。已知 为拟卤素,它的化学性质与卤素单质相似。下列说法正确的是
为拟卤素,它的化学性质与卤素单质相似。下列说法正确的是
A.向 溶液中滴加 溶液中滴加 溶液,生成血红色沉淀 溶液,生成血红色沉淀 |
B.溶液3红色褪去,氧化性: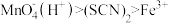 |
C.溶液3中 元素的主要存在形式为 元素的主要存在形式为 |
D.溶液4红色褪去, 表现出漂白性 表现出漂白性 |
您最近一年使用:0次
2021-11-19更新
|
458次组卷
|
4卷引用:广东省茂名市化州市2021-2022学年高三上学期11月份调研考化学试题
广东省茂名市化州市2021-2022学年高三上学期11月份调研考化学试题(已下线)专题36 物质的制备及实验方案的设计与评价(限时精炼)-2022年高三毕业班化学常考点归纳与变式演练河南省信阳高级中学2021-2022学年高一下学期3月考试化学试题(已下线)第3讲 氧化还原反应
名校
解题方法
9 . 无水  是常用的芳香烃取代反应催化剂,它具有易水解、易升华的性质。铁粉与氯气反应制备无水
是常用的芳香烃取代反应催化剂,它具有易水解、易升华的性质。铁粉与氯气反应制备无水  的实验装置如图所示:
的实验装置如图所示:

E和G用来收集产物。回答下列问题:
(1)在E、G处收集产物是利用了
___________ 的性质。
(2)实验过程中若F处出现堵塞,则在B处可观察到的现象是___________ 。可通过___________ (填简单操作),使实验能继续
(3)Ⅰ中反应的离子方程式为___________ 。
(4)实验室中还常用 与
与 晶体共热制备无水
晶体共热制备无水 ,其化学反应方程式为
,其化学反应方程式为___________ 。检验水合三氯化铁原料中是否存在 的试剂是
的试剂是___________ 。
 是常用的芳香烃取代反应催化剂,它具有易水解、易升华的性质。铁粉与氯气反应制备无水
是常用的芳香烃取代反应催化剂,它具有易水解、易升华的性质。铁粉与氯气反应制备无水  的实验装置如图所示:
的实验装置如图所示:
E和G用来收集产物。回答下列问题:
(1)在E、G处收集产物是利用了

(2)实验过程中若F处出现堵塞,则在B处可观察到的现象是
(3)Ⅰ中反应的离子方程式为
(4)实验室中还常用
 与
与 晶体共热制备无水
晶体共热制备无水 ,其化学反应方程式为
,其化学反应方程式为 的试剂是
的试剂是
您最近一年使用:0次
10 . 某同学通过系列实验探究Mg及其化合物的性质,操作正确且能达到目的的是
| A.将水加入浓硫酸中得到稀硫酸,置镁片于其中探究讨Mg的活泼性 |
| B.将NaOH溶液缓慢滴入MgSO4溶液中,观察Mg(OH)2沉淀的生成 |
| C.将Mg(OH)2浊液直接倒入已装好滤纸的漏斗中过滤,洗涤并收集沉淀 |
| D.将Mg(OH)2沉淀转入蒸发皿中,加足量稀盐酸,加热蒸干得无水MgCl2固体 |
您最近一年使用:0次
2019-01-30更新
|
1736次组卷
|
20卷引用:2011年普通高等学校招生全国统一考试化学卷(广东)
2011年普通高等学校招生全国统一考试化学卷(广东)(已下线)2011-2012学年福建省师大附中高三上学期期中考试化学试卷(已下线)2012届福建省厦门双十中学高三第二次月考化学试卷(已下线)2011-2012学年浙江省杭州十四中高一上学期期末化学试卷(已下线)2011-2012学年度江西省临川十中上学期高三期末考试化学试卷(已下线)2014届广东省揭阳一中高三上学期期中考试化学试卷2015届甘肃省武威第五中学高三11月月考化学试卷2015届河北省保定市重点高中高三12月联考化学试卷2015届山东省菏泽市曹县三桐中学高三1月月考化学试卷2016届山西省山大附中高三上学期10月月考化学试卷2017届江苏省运河中学高三暑假开学调研化学试卷江西省余江县第一中学2016-2017学年高一上学期选拔考试化学试题山西省太原市第五中学校2020届高三上学期9月阶段性检测化学试题江西省宜春市奉新县第一中学2020届高三上学期第二次月考化学试题江西省上饶中学2019-2020学年高三上学期第一次月考化学试题新疆昌吉州行知学校2020届高三上学期第二次月考化学试题甘肃省武威市第六中学2020届高三上学期第四次阶段性复习过关考试化学试题(已下线)上海建平中学2013年2月高三开学模拟考试化学试题(已下线)上海市奉贤区2012届高三上学期期末调研测试化学试题广东省梅州市大埔县虎山中学2022届高三第一次段考(8月月考)化学试题



