名校
解题方法
1 . 含硫的物质与人们的生活密切相关。已知硫元素常见的化合价有-2、0、+4、+6四种,其不同价态的物质间可相互转化。完成下列填空:
(1)请写出硫在元素周期表的位置:___________ 。
(2)硫与硅为同一周期元素,通过下列事实能比较两者非金属性强弱的是___________。
(3)二氧化硫是形成酸雨的“元凶”之一,由二氧化硫形成的酸雨的主要成分是硫酸。以下是二氧化硫形成酸雨的两种途径: 转化成
转化成 的化学方程式:
的化学方程式:___________ 。
你认为减少酸雨产生的无效措施是___________ (填字母序号)
A.少用煤作燃料 B.把工厂烟囱造高 C.燃料脱硫 D.开发新能源
某同学利用如图所示装置探究二氧化硫气体的性质,回答下列问题:___________ 。
(5)当观察到②中溶液颜色变浅时,①中的现象是___________ 。
(6)装置③的作用是___________ 。
(7)②中的现象说明二氧化硫具有的性质是___________ 。
(8)从氧化还原角度制备硫代硫酸钠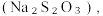 下列方案合理的是(填编号)___________。
下列方案合理的是(填编号)___________。
(9)为进一步减少 的污染并变废为宝,我国正在探索在一定条件下,用CO还原
的污染并变废为宝,我国正在探索在一定条件下,用CO还原 得到单质硫的方法来除去
得到单质硫的方法来除去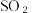 写出该反应的化学方程式:
写出该反应的化学方程式:___________ 。
(1)请写出硫在元素周期表的位置:
(2)硫与硅为同一周期元素,通过下列事实能比较两者非金属性强弱的是___________。
A.热稳定性: | B.溶解度: 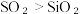 |
C.单质的熔点: | D.酸性:  |
(3)二氧化硫是形成酸雨的“元凶”之一,由二氧化硫形成的酸雨的主要成分是硫酸。以下是二氧化硫形成酸雨的两种途径:

 转化成
转化成 的化学方程式:
的化学方程式:你认为减少酸雨产生的无效措施是
A.少用煤作燃料 B.把工厂烟囱造高 C.燃料脱硫 D.开发新能源
某同学利用如图所示装置探究二氧化硫气体的性质,回答下列问题:
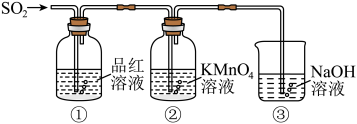
(5)当观察到②中溶液颜色变浅时,①中的现象是
(6)装置③的作用是
(7)②中的现象说明二氧化硫具有的性质是
(8)从氧化还原角度制备硫代硫酸钠
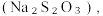 下列方案合理的是(填编号)___________。
下列方案合理的是(填编号)___________。A.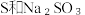 | B. 和浓 和浓 | C.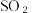 和 和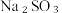 | D.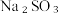 和 和 |
(9)为进一步减少
 的污染并变废为宝,我国正在探索在一定条件下,用CO还原
的污染并变废为宝,我国正在探索在一定条件下,用CO还原 得到单质硫的方法来除去
得到单质硫的方法来除去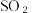 写出该反应的化学方程式:
写出该反应的化学方程式:
您最近一年使用:0次
解题方法
2 . 某小组同学探究卤族元素性质递变规律,设计如下实验:
(1)实验①的离子方程式为_______ 。实验②的现象是_______ 。
(2)综合实验①②③,Cl2、Br2、I2单质的氧化性由强到弱的顺序是_______ (用化学式表示);从原子结构的角度解释上述递变规律。_______
(3)实验中加入CCl4萃取的目的是_______ ;CCl4可以作为萃取剂的原因是_______ 。
| 序号 | 过程 | 现象 | 结论 |
| ① | 向NaBr溶液中加入少量氯水,再加入CCl4,振荡后静置 | 液体分层,下层呈红棕色 | 氧化性:Cl2>Br2 |
| ② | 向KI溶液中加入少量氯水,再加入CCl4,振荡后静置 | 氧化性:Cl2>I2 | |
| ③ | 向KI溶液中加入少量溴水,再加入CCl4,振荡后静置 |
(2)综合实验①②③,Cl2、Br2、I2单质的氧化性由强到弱的顺序是
(3)实验中加入CCl4萃取的目的是
您最近一年使用:0次
名校
解题方法
3 . 某实验小组欲探究 和
和 能否发生反应,设计如下图所示的实验装置进行实验。注:已检验装置气密性,且实验前已经用氮气排净装置内的空气。
能否发生反应,设计如下图所示的实验装置进行实验。注:已检验装置气密性,且实验前已经用氮气排净装置内的空气。
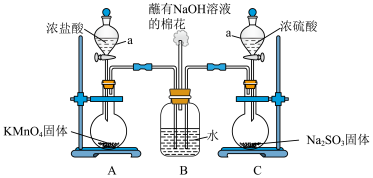
(1)装置C中反应的化学方程式_______ 。
(2)装置A中的反应为_______ _______
_______ (浓)=_______
(浓)=_______ _______
_______ _______
_______ _______
_______ 。
。
①配平该反应并用单线桥表示电子转移_______ 。
②反应中的氧化剂和还原剂的物质的量之比是_______ ,生成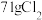 转移的电子是
转移的电子是_______  。
。
(3)打开装置A、C中仪器a的活塞,一段时间后关闭活塞。待反应完全后,又继续如下实验甲同学取适量B中溶液于试管中,向其中滴加一滴 
稀溶液 ,即有白色沉淀生成。
①甲同学由此认为 和
和 发生了反应,理由是该反应中生成了
发生了反应,理由是该反应中生成了_______ 离子(写离子符号)。
②乙认为甲的结论不合理,认为A中生成的 中混有杂质,乙认为混有的杂质是
中混有杂质,乙认为混有的杂质是_______ ;
③丙认为白色沉淀不能证明 和
和 发生反应,因氯气的水溶液加
发生反应,因氯气的水溶液加 溶液也有白色沉淀产生,可改为取B中溶液于试管中滴加X,有白色沉淀生成即可证明,X是
溶液也有白色沉淀产生,可改为取B中溶液于试管中滴加X,有白色沉淀生成即可证明,X是_______ (填编号)
a. 溶液 b.
溶液 b. 溶液 c.
溶液 c. 溶液 d.品红溶液
溶液 d.品红溶液
(4) 与
与 同时通入水中反应的离子方程式
同时通入水中反应的离子方程式_______ 。
 和
和 能否发生反应,设计如下图所示的实验装置进行实验。注:已检验装置气密性,且实验前已经用氮气排净装置内的空气。
能否发生反应,设计如下图所示的实验装置进行实验。注:已检验装置气密性,且实验前已经用氮气排净装置内的空气。
(1)装置C中反应的化学方程式
(2)装置A中的反应为_______
 _______
_______ (浓)=_______
(浓)=_______ _______
_______ _______
_______ _______
_______ 。
。①配平该反应并用单线桥表示电子转移
②反应中的氧化剂和还原剂的物质的量之比是
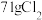 转移的电子是
转移的电子是 。
。(3)打开装置A、C中仪器a的活塞,一段时间后关闭活塞。待反应完全后,又继续如下实验甲同学取适量B中溶液于试管中,向其中滴加

①甲同学由此认为
 和
和 发生了反应,理由是该反应中生成了
发生了反应,理由是该反应中生成了②乙认为甲的结论不合理,认为A中生成的
 中混有杂质,乙认为混有的杂质是
中混有杂质,乙认为混有的杂质是③丙认为白色沉淀不能证明
 和
和 发生反应,因氯气的水溶液加
发生反应,因氯气的水溶液加 溶液也有白色沉淀产生,可改为取B中溶液于试管中滴加X,有白色沉淀生成即可证明,X是
溶液也有白色沉淀产生,可改为取B中溶液于试管中滴加X,有白色沉淀生成即可证明,X是a.
 溶液 b.
溶液 b. 溶液 c.
溶液 c. 溶液 d.品红溶液
溶液 d.品红溶液(4)
 与
与 同时通入水中反应的离子方程式
同时通入水中反应的离子方程式
您最近一年使用:0次
2024-01-15更新
|
266次组卷
|
2卷引用:上海市上海中学2023-2024学年高一上学期期末考试化学试卷
4 . 在实验室里制取乙烯,常因温度过高而使乙醇和浓硫酸反应生成少量的二氧化硫,有人设计下列实验图以确认上述混合气体中有C2H4和SO2。回答下列问题:

(1)I、II、III、IV装置可盛放的试剂是:I___________ ;II___________ ;III___________ ;IV___________ (将下列有关试剂的序号填入空格内)。
A.品红溶液 B.NaOH溶液 C.浓硫酸 D.酸性KMnO4溶液
(2)能说明SO2气体存在的现象是___________ 。
(3)使用装置II的目的是___________ 。
(4)使用装置III的目的是___________ 。
(5)确定含有乙烯的现象是___________ 。

(1)I、II、III、IV装置可盛放的试剂是:I
A.品红溶液 B.NaOH溶液 C.浓硫酸 D.酸性KMnO4溶液
(2)能说明SO2气体存在的现象是
(3)使用装置II的目的是
(4)使用装置III的目的是
(5)确定含有乙烯的现象是
您最近一年使用:0次
2023-06-29更新
|
69次组卷
|
18卷引用:上海市奉城高级中学2018-2019学年高二上学期期末考试化学试题
上海市奉城高级中学2018-2019学年高二上学期期末考试化学试题云南省绥江县一中2018-2019学年高一下学期期末考试化学试题陕西省西安市蓝田县大学区联考2022-2023学年高二下学期6月期末考试化学试题(已下线)2012年人教版高中化学选修5 2.1脂肪烃练习卷(已下线)2014年高一化学人教版必修2 3.2.1乙烯练习卷内蒙古北京八中乌兰察布分校2016-2017学年高一下学期第二次调考化学试题高二人教版选修5 第三章 烃的含氧衍生物 第一节 醇酚吉林省公主岭市范家屯镇第一中学2019-2020学年高二上学期第二次月考化学试题黑龙江省大兴安岭地区漠河县第一中学2018-2019学年高二上学期第一次月考化学试题课时1 石油的炼制 乙烯——A学习区 夯实基础(鲁科版必修2)课时1 甲烷 石油的炼制与乙烯——A学习区 夯实基础(鲁科版(2019)第二册)山东省德州市齐河县实验中学2019-2020学年高一下学期期中考试化学试题福建省莆田第七中学2020-2021学年高二上学期第一次月考化学试题安徽省安庆桐城市第八中学2020-2021学年高二上学期第一次段考化学试题黑龙江省双鸭山市第一中学2020-2021学年高二下学期4月月考化学试题云南省元阳县一中2020-2021学年高一下学期6月份考试化学试题2.1.1有机化学反应的主要类型(课前)-鲁科版选择性必修3陕西省西安市蓝田县大学区联考2022-2023学年高二下学期4月期中考试化学试题
名校
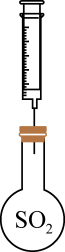
5 . 用如图装置探究 的性质。限选试剂:
的性质。限选试剂: 溶液、稀
溶液、稀 、
、 溶液、
溶液、 溶液、淀粉、
溶液、淀粉、 溶液、新制
溶液、新制 溶液。
溶液。
 的性质。限选试剂:
的性质。限选试剂: 溶液、稀
溶液、稀 、
、 溶液、
溶液、 溶液、淀粉、
溶液、淀粉、 溶液、新制
溶液、新制 溶液。
溶液。
| 操作步骤 | 预期现象 | 解释原因 |
用注射器将新制 溶液注入充满 溶液注入充满 的烧瓶 的烧瓶 | 产生乳白色浑浊 | +4价S具有 |
用注射器将 的烧瓶中 的烧瓶中 | +4价S具有还原性 |
您最近一年使用:0次
名校
解题方法
6 . 下图中甲是演示金属钠与水反应的实验装置,为收集并检验气体产物,某兴趣小组将甲装置改进成如图中乙或丙所示的装置,请根据要求回答下列问题。
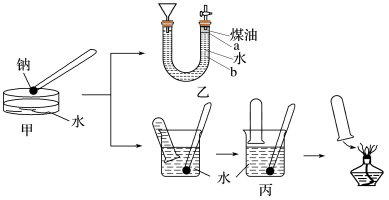
(1)写出钠与水反应的离子方程式:___________ 。和铝相比,钠与水反应更剧烈的原因是___________ (从原子结构的角度进行解释说明)。
(2)若按乙装置实验,液体添加完毕后,关闭活塞,打开右边胶塞,向煤油中加入一小块钠,立即塞好胶塞,可观察到的现象是________。
(3)用乙装置实验,点燃气体产物时,是否需要检验纯度?___ (填“是“或“否”)。
(4)按图丙所示方法来收集产生的气体,需将钠用某种金属包好,再放入水中。取相同质量的钠按下列两种情况收集产生的气体:①用扎有多个小孔的铝箔包住钠②用扎有多个小孔的铜箔包住钠,在相同条件下的体积关系是________ 。
A.二者收集气体一样多 B.①收集气体体积较大 C.②收集气体体积较大

(1)写出钠与水反应的离子方程式:
(2)若按乙装置实验,液体添加完毕后,关闭活塞,打开右边胶塞,向煤油中加入一小块钠,立即塞好胶塞,可观察到的现象是________。
| A.钠块始终保持在煤油中的a处,直至完全消失 |
| B.钠处于煤油和水的交界处上下浮动 |
| C.随反应的进行煤油与胶塞处液面下降,漏斗中液面上升 |
| D.最终钠块在煤油中燃烧起来 |
(4)按图丙所示方法来收集产生的气体,需将钠用某种金属包好,再放入水中。取相同质量的钠按下列两种情况收集产生的气体:①用扎有多个小孔的铝箔包住钠②用扎有多个小孔的铜箔包住钠,在相同条件下的体积关系是
A.二者收集气体一样多 B.①收集气体体积较大 C.②收集气体体积较大
您最近一年使用:0次
名校
解题方法
7 . 某同学为了验证Fe2+是否能将H2SO3氧化成 ,用50mL,0.1mol/LFeCl3溶液吸收一定量的
,用50mL,0.1mol/LFeCl3溶液吸收一定量的 气体后,进行以下实验:
气体后,进行以下实验:
(1)检验吸收液中是否含有 的操作为
的操作为_____________ 。
(2)请写出FeCl3吸收SO2的离子方程式:___________ ,反应中的氧化产物是__________ 。
(3)吸收液中除了含有H+、Cl-、 以外,该同学对其他成分(Fe3+、Fe2+、H2SO3)的可能组合进行了猜想和探究:
以外,该同学对其他成分(Fe3+、Fe2+、H2SO3)的可能组合进行了猜想和探究:
①提出假设。
假设1:溶液中存在Fe2+
假设2:溶液中存在Fe3+、Fe2+
假设3:溶液中存在__________ 。
②设计方案,进行实验,验证假设。
请写出实验步骤以及预期现象和结论(可不填满)。限选实验试剂和仪器:试管、滴管、0.1mol/LKMnO4溶液、0.1mol/LKSCN溶液、品红溶液。
 ,用50mL,0.1mol/LFeCl3溶液吸收一定量的
,用50mL,0.1mol/LFeCl3溶液吸收一定量的 气体后,进行以下实验:
气体后,进行以下实验:(1)检验吸收液中是否含有
 的操作为
的操作为(2)请写出FeCl3吸收SO2的离子方程式:
(3)吸收液中除了含有H+、Cl-、
 以外,该同学对其他成分(Fe3+、Fe2+、H2SO3)的可能组合进行了猜想和探究:
以外,该同学对其他成分(Fe3+、Fe2+、H2SO3)的可能组合进行了猜想和探究:①提出假设。
假设1:溶液中存在Fe2+
假设2:溶液中存在Fe3+、Fe2+
假设3:溶液中存在
②设计方案,进行实验,验证假设。
请写出实验步骤以及预期现象和结论(可不填满)。限选实验试剂和仪器:试管、滴管、0.1mol/LKMnO4溶液、0.1mol/LKSCN溶液、品红溶液。
| 实验步骤 | 预期现象和结论 |
| 步骤1:用试管取样品溶液2~3mL,滴入 | 若 |
| 步骤2: | 若 |
| 步骤3(可补充): |
您最近一年使用:0次
名校
解题方法
8 . 人类的生产和生活都离不开金属。金属材料的使用作为一个时代的标志,见证了人类文明发展的过程,历史上人类冶炼不同金属的大致年代如图所示:
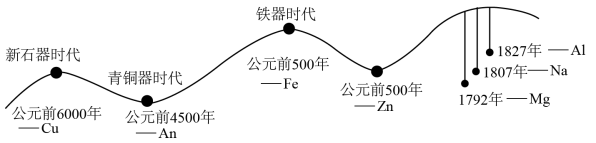
(1)由图可知:人类最早使用的合金是________ ,通过敲打可将金属材料打制成不同的形状,是利用了金属的________ 性。含碳量在0.03%~2%之间某合金,是目前使用量最大的合金,这种合金是________ (填字母)。
A.铝合金 B.镁合金 C.生铁 D,钢
(2)北宋沈插在《梦溪笔谈》中记载:“信州铅山有苦泉,流以为涧,挹其水熬之则成胆矾,熬胆矾铁釜,久之亦化为铜”。下列叙述正确的是________ (填字母)。
A.“苦泉”的溶质之一: ;
;
B.“挹其水熬之”:蒸发溶剂;
C.“熬胆矾铁釜,久之亦化为铜”:发生分解反应。
(3)铝的使用距今仅200年左右,现如今铝的年产量得到大幅度的提高。铝虽然较活泼,但抗腐蚀性能好,原因是________ (用化学方程式表示)。
(4)某溶液中含有 、
、 、
、 、
、 等离子,向其中加入过量
等离子,向其中加入过量 后,过滤,将滤渣投入足量盐酸中,所得溶液与原溶液相比,溶液中大量减少的正离子是
后,过滤,将滤渣投入足量盐酸中,所得溶液与原溶液相比,溶液中大量减少的正离子是________ (填字母),大量增加的离子有________ (填化学式)。
A. B.
B. C.
C. D.
D.
工业上用废铁皮制取铁红 的部分流程示意图如下:
的部分流程示意图如下:
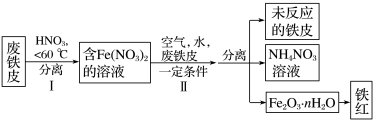
(5)步骤II中发生反应: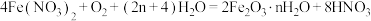 ,反应产生的
,反应产生的 又可将废铁皮中的铁转化为
又可将废铁皮中的铁转化为 ,该反应的化学方程式为:
,该反应的化学方程式为:________ 。
 可制取新型、高效水处理剂——高铁酸钾
可制取新型、高效水处理剂——高铁酸钾 。
。
________ ________
________ ________
________ ________
________ (高铁酸钾)+________
(高铁酸钾)+________ ________
________
(6)配平上述反应,并用单线桥法表示反应过程中的电子转移方向和数目________ 。
(7)此过程中氧化剂是________ (填化学式)。
(8)高铁酸钾 是一种新型、高效的绿色水处理剂,在水中反应生成氢氧化铁胶体。高铁酸钾作为水处理剂的作用有
是一种新型、高效的绿色水处理剂,在水中反应生成氢氧化铁胶体。高铁酸钾作为水处理剂的作用有________ 、________
工业上常用铝质容器盛装冷浓酸,为研究铝质材料与热浓硫酸的反应,某学习小组进行了以下探究活动:
(9)将铝片放入氢氧化钠溶液中可去除表面氧化膜,反应的离子方程式为:________ 。
(10)将已除去表面氧化膜的铝片继续置于氢氧化钠溶液中,迅速产生大量气泡,反应的化学方程式为:________ 。反应过程中氧化剂与还原剂的物质的量之比为________ 。
(11)另取一同样已除去表面氧化膜的铝片放入冷浓硫酸中,10分钟后,移入硫酸铜溶液中,片刻后取出观察,铝片表面无明显变化,其原因是________ 。
(12)另称取铝片6.0g放入15.0mL浓硫酸中,加热,充分应后收集到气体X;甲同学取448mL(标准状况)气体X通入足量过氧化氢溶液中,然后再加入足量 溶液,经适当操作后得干燥固体2.33g,由于此推知气体X中
溶液,经适当操作后得干燥固体2.33g,由于此推知气体X中 的体积分数为
的体积分数为________ 。
分析上述实验中 体积分数的结果,丙同学认为气体X中还可能含量有
体积分数的结果,丙同学认为气体X中还可能含量有 ;为此设计了下列探究实验装置(图中央持仪器省略)。
;为此设计了下列探究实验装置(图中央持仪器省略)。
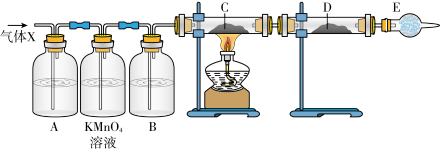
(13)丙同学认为还可能产生氢气的理由是________ 。
(14)A中试剂可选用________。
(15)B中加入的试剂是________ ,E的作用是________ 。
(16)可以证明气体X中含有氢气的实验现象是:________ 。

(1)由图可知:人类最早使用的合金是
A.铝合金 B.镁合金 C.生铁 D,钢
(2)北宋沈插在《梦溪笔谈》中记载:“信州铅山有苦泉,流以为涧,挹其水熬之则成胆矾,熬胆矾铁釜,久之亦化为铜”。下列叙述正确的是
A.“苦泉”的溶质之一:
 ;
;B.“挹其水熬之”:蒸发溶剂;
C.“熬胆矾铁釜,久之亦化为铜”:发生分解反应。
(3)铝的使用距今仅200年左右,现如今铝的年产量得到大幅度的提高。铝虽然较活泼,但抗腐蚀性能好,原因是
(4)某溶液中含有
 、
、 、
、 、
、 等离子,向其中加入过量
等离子,向其中加入过量 后,过滤,将滤渣投入足量盐酸中,所得溶液与原溶液相比,溶液中大量减少的正离子是
后,过滤,将滤渣投入足量盐酸中,所得溶液与原溶液相比,溶液中大量减少的正离子是A.
 B.
B. C.
C. D.
D.
工业上用废铁皮制取铁红
 的部分流程示意图如下:
的部分流程示意图如下:
(5)步骤II中发生反应:
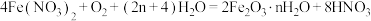 ,反应产生的
,反应产生的 又可将废铁皮中的铁转化为
又可将废铁皮中的铁转化为 ,该反应的化学方程式为:
,该反应的化学方程式为: 可制取新型、高效水处理剂——高铁酸钾
可制取新型、高效水处理剂——高铁酸钾 。
。________
 ________
________ ________
________ ________
________ (高铁酸钾)+________
(高铁酸钾)+________ ________
________
(6)配平上述反应,并用单线桥法表示反应过程中的电子转移方向和数目
(7)此过程中氧化剂是
(8)高铁酸钾
 是一种新型、高效的绿色水处理剂,在水中反应生成氢氧化铁胶体。高铁酸钾作为水处理剂的作用有
是一种新型、高效的绿色水处理剂,在水中反应生成氢氧化铁胶体。高铁酸钾作为水处理剂的作用有工业上常用铝质容器盛装冷浓酸,为研究铝质材料与热浓硫酸的反应,某学习小组进行了以下探究活动:
(9)将铝片放入氢氧化钠溶液中可去除表面氧化膜,反应的离子方程式为:
(10)将已除去表面氧化膜的铝片继续置于氢氧化钠溶液中,迅速产生大量气泡,反应的化学方程式为:
(11)另取一同样已除去表面氧化膜的铝片放入冷浓硫酸中,10分钟后,移入硫酸铜溶液中,片刻后取出观察,铝片表面无明显变化,其原因是
(12)另称取铝片6.0g放入15.0mL浓硫酸中,加热,充分应后收集到气体X;甲同学取448mL(标准状况)气体X通入足量过氧化氢溶液中,然后再加入足量
 溶液,经适当操作后得干燥固体2.33g,由于此推知气体X中
溶液,经适当操作后得干燥固体2.33g,由于此推知气体X中 的体积分数为
的体积分数为分析上述实验中
 体积分数的结果,丙同学认为气体X中还可能含量有
体积分数的结果,丙同学认为气体X中还可能含量有 ;为此设计了下列探究实验装置(图中央持仪器省略)。
;为此设计了下列探究实验装置(图中央持仪器省略)。
(13)丙同学认为还可能产生氢气的理由是
(14)A中试剂可选用________。
| A.溴水 | B.品红溶液 | C.氢氧化钠溶液 | D.饱和食盐水 |
(16)可以证明气体X中含有氢气的实验现象是:
您最近一年使用:0次
解题方法
9 . 为了探究化学能与热能的转化,某实验小组设计了如下三套实验装置:

(1)上述 3 个装置中,不能证明“铜与浓硝酸反应是吸热反应还是放热反应”的是______ ;
(2)某同学选用装置I 进行实验(实验前U 型管里液面左右相平),在甲试管里加入适量氢氧化钡溶液与稀硫酸,U 型管中可观察到的现象是___________ ,说明该反应属于___________ (选填“吸热” 或“放热”)反应。
(3)为探究固体M 溶于水的热效应,选择装置 II 进行实验(反应在甲中进行)。
①若 M 为Na,则实验过程中烧杯中可观察到的现象是___________
②若观察到烧杯里产生气泡,则说明 M 溶于水___________ (选填“一定是放热反应”、“一定是吸热反应” 或“可能是放热反应”),理由是___________ 。
③若观察到烧杯里玻璃管内形成一段水柱,则 M 溶于水是___________ (选填“放热”或“吸热”)过程。
(4)C(石墨)与适量 H2O(g)反应生成标准状况下 CO 和H2各 2.24L 时,吸收 3.13kJ 热量,该反应的热化学方程式为___________ 。

(1)上述 3 个装置中,不能证明“铜与浓硝酸反应是吸热反应还是放热反应”的是
(2)某同学选用装置I 进行实验(实验前U 型管里液面左右相平),在甲试管里加入适量氢氧化钡溶液与稀硫酸,U 型管中可观察到的现象是
(3)为探究固体M 溶于水的热效应,选择装置 II 进行实验(反应在甲中进行)。
①若 M 为Na,则实验过程中烧杯中可观察到的现象是
②若观察到烧杯里产生气泡,则说明 M 溶于水
③若观察到烧杯里玻璃管内形成一段水柱,则 M 溶于水是
(4)C(石墨)与适量 H2O(g)反应生成标准状况下 CO 和H2各 2.24L 时,吸收 3.13kJ 热量,该反应的热化学方程式为
您最近一年使用:0次
名校
解题方法
10 . 常温下浓硫酸和铁钉会发生钝化,从而可以用铁制容器储存运输浓硫酸。但在加热条件下,这种钝化会被破坏,过量的浓硫酸和铁会反应生成硫酸铁、二氧化硫和水。回答以下问题:
(1)写出以上反应的化学方程式并用单线桥标出电子转移的方向和数目:___________
(2)该反应中氧化产物是___________ (填化学式),浓硫酸起到作用___________ (填序号)。
①吸水性 ②脱水性 ③强氧化性 ④难挥发性⑤酸性
(3)若转移的电子数为 ,则生成标准状况下的
,则生成标准状况下的 气体
气体___________ L。
(4)检验反应后溶液中 的方法是:
的方法是:___________ 。
(5)我国农业因遭受酸雨而造成每年损失高达15亿多元。为了有效控制酸雨,目前国务院已批准了《酸雨控制区和二氧化硫污染控制区划分方案》等法规。现有雨水样品1份,每隔一段时间测定该雨水样品的pH,所得数据如下表:
分析数据,回答下列问题:
①雨水样品pH变化的原因是(用化学反应方程式表示)___________ 。
②如果将刚取样的上述雨水和自来水(含有余氯)相混合,酸性将变___________ (填“强”或“弱”)。
(6)浓硫酸与木炭粉在加热条件下的化学方程式为___________ 。
(7)已知酸性KMnO4溶液可以吸收SO2,试用下图所示各装置设计一个实验,验证上述反应所产生的各种产物。
这些装置的连接顺序(按产物气流从左到右的方向)是(填装置的编号):___________
___________→___________→___________→___________。
(8)实验时可观察到装置①中A瓶的溶液褪色,C瓶的溶液不褪色。A瓶溶液的作用是___________ ,B瓶溶液的作用是___________ ,C瓶溶液的作用是___________ 。
(9)装置②中所加的固体药品是___________ ,可确证的产物是___________ ,确定装置②在整套装置中位置的理由是___________ 。
(10)装置③中所盛溶液是___________ ,可验证的产物是___________ 。
(1)写出以上反应的化学方程式并用单线桥标出电子转移的方向和数目:
(2)该反应中氧化产物是
①吸水性 ②脱水性 ③强氧化性 ④难挥发性⑤酸性
(3)若转移的电子数为
 ,则生成标准状况下的
,则生成标准状况下的 气体
气体(4)检验反应后溶液中
 的方法是:
的方法是:(5)我国农业因遭受酸雨而造成每年损失高达15亿多元。为了有效控制酸雨,目前国务院已批准了《酸雨控制区和二氧化硫污染控制区划分方案》等法规。现有雨水样品1份,每隔一段时间测定该雨水样品的pH,所得数据如下表:
| 测试时间/h | 0 | 1 | 2 | 3 | 4 |
| 雨水的pH | 4.73 | 4.62 | 4.56 | 4.55 | 4.55 |
①雨水样品pH变化的原因是(用化学反应方程式表示)
②如果将刚取样的上述雨水和自来水(含有余氯)相混合,酸性将变
(6)浓硫酸与木炭粉在加热条件下的化学方程式为
(7)已知酸性KMnO4溶液可以吸收SO2,试用下图所示各装置设计一个实验,验证上述反应所产生的各种产物。
| 编号 | ① | ② | ③ | ④ |
| 装置 | 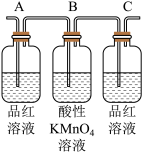 | 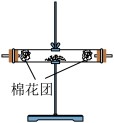 | 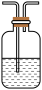 |  |
___________→___________→___________→___________。
(8)实验时可观察到装置①中A瓶的溶液褪色,C瓶的溶液不褪色。A瓶溶液的作用是
(9)装置②中所加的固体药品是
(10)装置③中所盛溶液是
您最近一年使用:0次



