1 . 从海带中提取碘,设计如下实验方案,下列说法不正确 的是
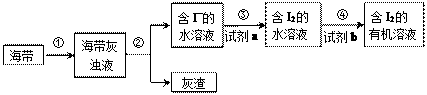

| A.步骤①的操作方法:灼烧和溶解 |
| B.步骤①需用的主要仪器:坩埚和烧杯 |
| C.步骤③的试剂a必须是氧化剂 |
| D.步骤④的试剂b可选用酒精 |
您最近一年使用:0次
解题方法
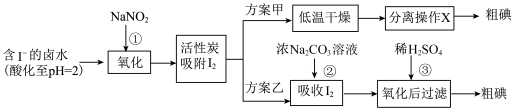
2 . 从海水中可以提取很多有用的物质,例如从海水制盐所得到的卤水中可以提取碘。活性炭吸附法是工业提碘的方法之一,其流程如下:
资料显示:Ⅰ. pH=2时,NaNO2溶液只能将 I-氧化为I2,同时生成NO
Ⅱ. I2+5Cl2+6H2O === 2HIO3+10HCl
Ⅲ. 5 +2
+2 +2H+ = I2+5
+2H+ = I2+5 +H2O
+H2O
(1)反应①的离子方程式____________________ 。
(2)方案甲中,根据I2的特性,分离操作X的方法是____________ 。
(3)已知:反应②中每吸收3mol I2转移5mol电子,离子方程式是__________ 。
(4)Cl2、酸性KMnO4等都是常用的强氧化剂,但该工艺中氧化卤水中的I-却选择了价格较高的NaNO2,原因是_______________________ 。
(5)方案乙中,已知反应③过滤后,滤液中仍存在少量的I2、I-、 。请
。请分别 检验滤液中的I-、 ,将实验方案补充完整。实验中可供选择的试剂:稀H2SO4、淀粉溶液、Fe2(SO4)3溶液、Na2SO3溶液
,将实验方案补充完整。实验中可供选择的试剂:稀H2SO4、淀粉溶液、Fe2(SO4)3溶液、Na2SO3溶液
a.滤液用CCl4多次萃取、分液,直到水层用淀粉溶液检验不出碘单质存在。
b._____________________ 。
资料显示:Ⅰ. pH=2时,NaNO2溶液只能将 I-氧化为I2,同时生成NO
Ⅱ. I2+5Cl2+6H2O === 2HIO3+10HCl
Ⅲ. 5
 +2
+2 +2H+ = I2+5
+2H+ = I2+5 +H2O
+H2O (1)反应①的离子方程式
(2)方案甲中,根据I2的特性,分离操作X的方法是
(3)已知:反应②中每吸收3mol I2转移5mol电子,离子方程式是
(4)Cl2、酸性KMnO4等都是常用的强氧化剂,但该工艺中氧化卤水中的I-却选择了价格较高的NaNO2,原因是
(5)方案乙中,已知反应③过滤后,滤液中仍存在少量的I2、I-、
 。请
。请 ,将实验方案补充完整。实验中可供选择的试剂:稀H2SO4、淀粉溶液、Fe2(SO4)3溶液、Na2SO3溶液
,将实验方案补充完整。实验中可供选择的试剂:稀H2SO4、淀粉溶液、Fe2(SO4)3溶液、Na2SO3溶液a.滤液用CCl4多次萃取、分液,直到水层用淀粉溶液检验不出碘单质存在。
b.
您最近一年使用:0次



