1 . 化学实验源于生活。下列实验方案设计、现象与结论均正确的是
| 选项 | 目的 | 方案设计 | 现象结论 |
| A | 检验鸡皮中是否含有脂肪 | 取一小块鸡皮于表面皿上,将几滴浓硝酸滴到鸡皮上 | 一段时间后鸡皮变黄,说明鸡皮中含有脂肪 |
| B | 检验火柴头中是否含有氯元素 | 将几根未燃过的火柴头浸入水中,稍后取少量溶液于试管中,加入稀 、 、 溶液 溶液 | 若有白色沉淀产生,说明火柴头中含有氯元素 |
| C | 检验海带中的碘元素 | 向海带灰的浸取液中通入适量氯气,再加入 萃取 萃取 | 若下层出现紫红色,则海带中含有碘元素 |
| D | 检验黑木耳中的铁元素 | 取少量黑木耳剪碎研磨后加水搅拌,取上层清液于试管中,加入稀硫酸后再加入KSCN溶液 | 若溶液未变红,说明黑木耳中不含三价铁元素 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2 . 从海产品(如海带)中提取碘是工业获取碘的重要途径。其流程如下:
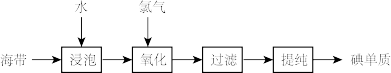
下列说法中不正确的是

下列说法中不正确的是
| A.碘元素在海带中以游离态存在 |
| B.使海带中的碘进入水中也可将海带灼烧成灰再加水浸取 |
C.用 代替 代替 不会产生额外污染 不会产生额外污染 |
| D.碘单质容易升华,可以利用升华法提纯含有氯化钠杂质的碘单质 |
您最近半年使用:0次
名校
3 . 海洋化学资源的综合利用对人类的发展意义重大。
Ⅰ.以海水为原料获得的粗盐中含有 、
、 、
、 和难溶性杂质。
和难溶性杂质。
(1)除去粗盐中可溶性杂质,加入试剂的顺序是_______ (填标号),过滤,滴加稀盐酸调节溶液呈中性。
A.


B.


C.


Ⅱ.从海藻中提取碘:
步骤一:制备含碘离子的溶液

(2)实验室焙烧海藻的装置如图,仪器A的名称是_______ 。

步骤二:活性炭吸附法提取碘,其流程如下:
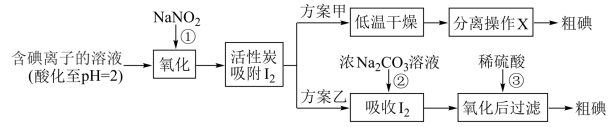
资料显示: 时,
时, 溶液只能将
溶液只能将 氧化为
氧化为 ,同时生成NO。
,同时生成NO。
(3)写出反应①的离子方程式:_______ 。
(4)方案甲中,根据 的特性,分离操作X应为
的特性,分离操作X应为_______ 、_______ 。
(5)方案乙中, 浓溶液吸收
浓溶液吸收 有
有 生成,写出反应②的离子方程式:
生成,写出反应②的离子方程式:_______ 。
(6)方案乙中,已知:反应③充分进行后,过滤,滤液中仍存在少量的 、
、 。为检验滤液中的
。为检验滤液中的 ,请将下列实验方案补充完整。实验中可供选择的试剂:稀
,请将下列实验方案补充完整。实验中可供选择的试剂:稀 、淀粉溶液、
、淀粉溶液、 溶液、
溶液、 。
。
A.将滤液_______ ,直到水层用淀粉溶液检验不出碘单质存在。
B.从水层取少量溶液于试管中,_______ 。
Ⅰ.以海水为原料获得的粗盐中含有
 、
、 、
、 和难溶性杂质。
和难溶性杂质。(1)除去粗盐中可溶性杂质,加入试剂的顺序是
A.



B.



C.



Ⅱ.从海藻中提取碘:
步骤一:制备含碘离子的溶液

(2)实验室焙烧海藻的装置如图,仪器A的名称是

步骤二:活性炭吸附法提取碘,其流程如下:

资料显示:
 时,
时, 溶液只能将
溶液只能将 氧化为
氧化为 ,同时生成NO。
,同时生成NO。(3)写出反应①的离子方程式:
(4)方案甲中,根据
 的特性,分离操作X应为
的特性,分离操作X应为(5)方案乙中,
 浓溶液吸收
浓溶液吸收 有
有 生成,写出反应②的离子方程式:
生成,写出反应②的离子方程式:(6)方案乙中,已知:反应③充分进行后,过滤,滤液中仍存在少量的
 、
、 。为检验滤液中的
。为检验滤液中的 ,请将下列实验方案补充完整。实验中可供选择的试剂:稀
,请将下列实验方案补充完整。实验中可供选择的试剂:稀 、淀粉溶液、
、淀粉溶液、 溶液、
溶液、 。
。A.将滤液
B.从水层取少量溶液于试管中,
您最近半年使用:0次
2023-11-01更新
|
113次组卷
|
2卷引用:江西省上饶广丰中学2023-2024学年高一上学期10月月考化学试题
名校
4 . 工业上制备相关物质,涉及的反应原理及部分流程较为合理的是
A.制取镁:海水 Mg(OH)2 Mg(OH)2 MgO MgO Mg Mg |
B.冶炼铝:铝土矿 NaAlO2 NaAlO2 无水AlCl3 无水AlCl3 Al Al |
C.制纯碱:饱和NaCl(aq)  NaHCO3(s) NaHCO3(s)  Na2CO3(s) Na2CO3(s) |
D.制碘:海带 海带灰 海带灰  I2(aq) I2(aq) I2 I2 |
您最近半年使用:0次
2023-09-11更新
|
197次组卷
|
2卷引用:江西省宜春市宜丰中学2023-2024学年高二上学期开学考试化学试题
名校
5 . 海带提碘过程中以 为溶剂将
为溶剂将 从碘水溶液中提取出来,通过下列实验可从
从碘水溶液中提取出来,通过下列实验可从 的
的 溶液中回收
溶液中回收 。
。

下列说法错误的是
 为溶剂将
为溶剂将 从碘水溶液中提取出来,通过下列实验可从
从碘水溶液中提取出来,通过下列实验可从 的
的 溶液中回收
溶液中回收 。
。
下列说法错误的是
| A.反应1的目的为将富集在四氯化碳中的碘单质利用化学转化法重新富集在水中 |
| B.操作1需要用到的玻璃仪器有普通漏斗、烧杯和玻璃棒 |
C.反应2的离子方程式为 |
| D.操作2的名称为过滤 |
您最近半年使用:0次
2023-08-21更新
|
209次组卷
|
2卷引用:江西省宜春市丰城拖船中学2023-2024学年高二上学期开学化学试题
名校
解题方法
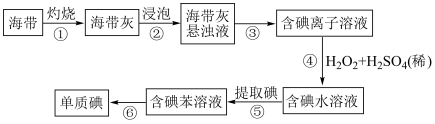
6 . (一)海带中含有丰富的碘.为从海带中提取碘,某研究性学习小组设计并进行以下实验:
提示:苯是有机萃取剂,其密度小于水。
(1)步骤③⑤和的实验操作名称分别是______ ,______ 。
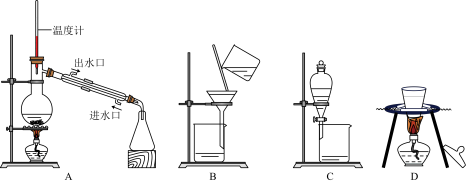
(2)①需用到以下装置是______ 。
(3)步骤④中反应的离子方程式是______ 。
(4)步骤⑤中,______ (填“能”或“不能”)用酒精来萃取碘的理由______ 。
(二)海水提碘实验中,得到碘的苯溶液后也可用“反萃取法”萃取、富集碘单质,实验步骤如下:
(5)上述过程②中,发生的离子方程式______ 。
(6)请设计一种检验过程③提取碘后的水溶液中是否还含有单质碘的简单方法:______ 。
提示:苯是有机萃取剂,其密度小于水。
(1)步骤③⑤和的实验操作名称分别是
(2)①需用到以下装置是
(3)步骤④中反应的离子方程式是
(4)步骤⑤中,
(二)海水提碘实验中,得到碘的苯溶液后也可用“反萃取法”萃取、富集碘单质,实验步骤如下:

(5)上述过程②中,发生的离子方程式
(6)请设计一种检验过程③提取碘后的水溶液中是否还含有单质碘的简单方法:
您最近半年使用:0次
2023-08-14更新
|
205次组卷
|
4卷引用:江西省宜春市丰城拖船中学2023-2024学年高二上学期开学化学试题
名校
7 . 实验室模拟工业海带提砷的流程如图。下列说法错误的是
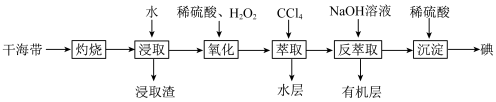
| A.“灼烧”用到的硅酸盐仪器有坩埚、泥三角、玻璃棒、酒精灯 |
B.“氧化”时发生反应的离子方程式为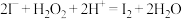 |
| C.“反萃取”所得有机层经处理后可循环再利用 |
D.“沉淀”时每生成 碘,理论上转移 碘,理论上转移 电子 电子 |
您最近半年使用:0次
2023-08-03更新
|
261次组卷
|
3卷引用:江西省抚州市黎川县第二中学2023-2024学年高二上学期开学考试化学试题
名校
解题方法
8 . 海藻中食含碘元素。某小组同学在实验室里用灼烧海藻的灰分提取碘,流程如下图所示:
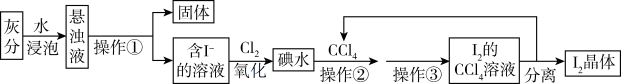
(1)操作①的名称_____ ,操作③的名称_____ 。实验室进行操作①使用的仪器有铁架台(带铁圈)、漏斗和_____ 。
(2)操作②选用CCl4的理由是_____(填写序号)。
(3)用NaOH溶液反萃取后再加稀硫酸,可以分离I2和CCl4。有关化学方程式为:
碱性条件: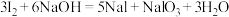 ;
;
酸性条件: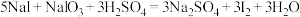 。
。
以下是反萃取过程的操作,请填写相关空格:
①向装有I2的CCl4溶液的_____ (填仪器名称)中加入少量1mol/LNaOH溶液;
②振荡至溶液的_____ 色消失,静置,分层,则_____ (填“上”。“下”)层为CCl4;
③将含碘的碱溶液从仪器的_____ (填“上”、“下”)口倒入烧杯中;
④边搅拌边加入几滴1mol⋅L-1H2SO4溶液,溶液立即转为棕黄色,并析出碘晶体。
(4)本实验中可以循环利用的物质是_____ 。

(1)操作①的名称
(2)操作②选用CCl4的理由是_____(填写序号)。
| A.CCl4不溶于水 | B.CCl4的密度比水大 |
| C.碘在CCl4中比在水中溶解度更大 | D.CCl4与碘水不反应 |
碱性条件:
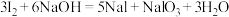 ;
;酸性条件:
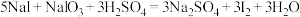 。
。以下是反萃取过程的操作,请填写相关空格:
①向装有I2的CCl4溶液的
②振荡至溶液的
③将含碘的碱溶液从仪器的
④边搅拌边加入几滴1mol⋅L-1H2SO4溶液,溶液立即转为棕黄色,并析出碘晶体。
(4)本实验中可以循环利用的物质是
您最近半年使用:0次
2023-07-19更新
|
94次组卷
|
2卷引用:江西省抚州市黎川县第二中学2023-2024学年高二上学期开学考试化学试题
名校
解题方法
9 . 某学习小组按如下实验流程从海带浸取液中提取碘。

| A.NaOH的作用是将I2转化成离子进入水层,应控制NaOH溶液的浓度和体积 |
| B.加NaOH溶液后分液时,先将下层液体放出后,再从下口将上层液体放出 |
C.加入H2SO4溶液,反应的离子方程式为 |
| D.坩埚中灼烧干海带可制得海带灰 |
您最近半年使用:0次
2023-07-08更新
|
298次组卷
|
3卷引用:江西省井冈山大学附属中学2022-2023学年高一下学期期末考试化学试题
解题方法
10 . 海带是一种含碘量很高的海藻,从中提取的碘广泛应用于医药、食品和化工。实验室里从海带中提取碘的流程如图,下列有关说法正确的是
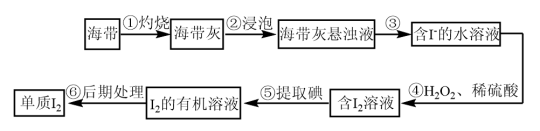

| A.实验室在蒸发皿中灼烧干海带,并用玻璃棒搅拌 |
| B.海带灰的悬浊液中加入几滴淀粉溶液,溶液变蓝色 |
| C.操作③与操作⑤方法相同 |
| D.操作④发生的离子反应:2I-+2H++H2O2=I2+2H2O |
您最近半年使用:0次



