名校
解题方法
1 . 以海带为原料提取碘单质的流程如下:
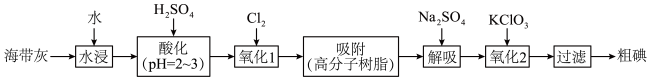
回答下列问题:
(1)为提高“水浸”速率,宜采取的措施有:
 ,不宜过量的原因是
,不宜过量的原因是(2)“过滤”操作需要的玻璃仪器有
(3)“吸附”的目的是
(4)“解吸”中氧化剂、还原剂的物质的量之比为
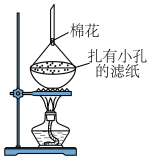
(5)“氧化2”中
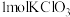 完全反应转移
完全反应转移 电子。与出该反应的离子方程式:
电子。与出该反应的离子方程式:(6)利用如图装置提纯碘。
提纯 的原理是
的原理是
您最近半年使用:0次
2024-01-24更新
|
62次组卷
|
2卷引用:吉林省白城市通榆县第一中学校2023-2024学年高三上学期第四次质量检测 化学试题
名校
解题方法
2 . 海水是一个巨大的化学资源宝库。请回答下列问题:
Ⅰ.从海带中提取碘单质
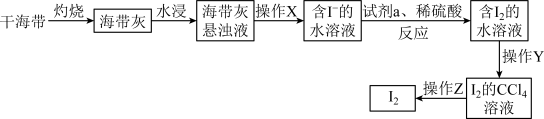
(1)“灼烧”过程需要用到的仪器为酒精灯、三脚架、泥三角、_____ ,“操作X”的名称为_____ 。
(2)若试剂 选择
选择 ,试剂
,试剂 参与反应的离子方程式为
参与反应的离子方程式为_____ ,氧化性:
_____ (填“>”或“<”) 。
。
(3)“操作Y”为萃取分液,萃取后分液时,转移 的
的 溶液至烧杯中的操作是
溶液至烧杯中的操作是_____ 。
Ⅱ.海水提溴:海水→海水淡化→ 氧化→空气吹出→吸收→……→液溴
氧化→空气吹出→吸收→……→液溴
(4)“空气吹出”体现了溴的_____ 性,该步骤的目的是_____ 。
(5)若“吸收”步骤使用浓的 溶液,则反应后产物有
溶液,则反应后产物有 、
、 ,该过程发生反应的离子方程式为
,该过程发生反应的离子方程式为_____ 。若反应后得到 、
、 、
、 的混合溶液,经测定,
的混合溶液,经测定,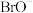 与
与 的物质的量之比为
的物质的量之比为 ,则
,则 与
与 反应时,被还原的溴元素和被氧化的溴元素的物质的量之比
反应时,被还原的溴元素和被氧化的溴元素的物质的量之比_____ 。
Ⅰ.从海带中提取碘单质

(1)“灼烧”过程需要用到的仪器为酒精灯、三脚架、泥三角、
(2)若试剂
 选择
选择 ,试剂
,试剂 参与反应的离子方程式为
参与反应的离子方程式为
 。
。(3)“操作Y”为萃取分液,萃取后分液时,转移
 的
的 溶液至烧杯中的操作是
溶液至烧杯中的操作是Ⅱ.海水提溴:海水→海水淡化→
 氧化→空气吹出→吸收→……→液溴
氧化→空气吹出→吸收→……→液溴(4)“空气吹出”体现了溴的
(5)若“吸收”步骤使用浓的
 溶液,则反应后产物有
溶液,则反应后产物有 、
、 ,该过程发生反应的离子方程式为
,该过程发生反应的离子方程式为 、
、 、
、 的混合溶液,经测定,
的混合溶液,经测定,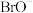 与
与 的物质的量之比为
的物质的量之比为 ,则
,则 与
与 反应时,被还原的溴元素和被氧化的溴元素的物质的量之比
反应时,被还原的溴元素和被氧化的溴元素的物质的量之比
您最近半年使用:0次
3 . 海洋资源的利用具有非常广阔的前景。回答下列问题:
Ⅰ.海水提溴
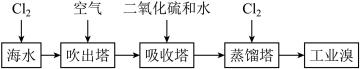
(1)溴元素在元素周期表中的位置为_______
(2)吸收塔用二氧化硫和水吸收 的离子方程式为:
的离子方程式为:_______
(3)蒸馏塔的蒸馏温度应控制在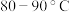 最有利于生产,原因可能为:温度过高,
最有利于生产,原因可能为:温度过高,_______ ;温度过低,_______
(4)两次通入 的离子反应相同,其离子方程式为
的离子反应相同,其离子方程式为_______ ,通 反应后使用了空气吹出法,该方法利用了溴单质
反应后使用了空气吹出法,该方法利用了溴单质_______ 的性质。
Ⅱ.海水提镁
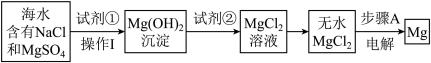
(5)工业上常用于沉淀 的廉价试剂①的俗名是
的廉价试剂①的俗名是_______ 。操作Ⅰ的名称是_______ 。
(6)步骤A的化学方程式为_______ 。
Ⅲ.海带提碘
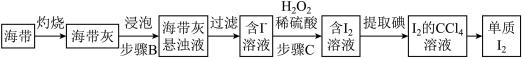
(7)步骤B需搅拌、加热煮沸的目的是_______ 。步骤C中反应的离子方程式为_______
Ⅰ.海水提溴

(1)溴元素在元素周期表中的位置为
(2)吸收塔用二氧化硫和水吸收
 的离子方程式为:
的离子方程式为:(3)蒸馏塔的蒸馏温度应控制在
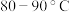 最有利于生产,原因可能为:温度过高,
最有利于生产,原因可能为:温度过高,(4)两次通入
 的离子反应相同,其离子方程式为
的离子反应相同,其离子方程式为 反应后使用了空气吹出法,该方法利用了溴单质
反应后使用了空气吹出法,该方法利用了溴单质Ⅱ.海水提镁

(5)工业上常用于沉淀
 的廉价试剂①的俗名是
的廉价试剂①的俗名是(6)步骤A的化学方程式为
Ⅲ.海带提碘

(7)步骤B需搅拌、加热煮沸的目的是
您最近半年使用:0次
名校
4 . 我国拥有很长的海岸线,海洋资源的开发利用具有广阔前景。全球海水中溴的储藏量丰富,约占地球溴总储藏量的99%,故溴有“海洋元素”之称。
(1)空气吹出法工艺是目前“海水提溴”的最主要方法之一、其工艺流程如图:

步骤①中获得Br2的离子方程式为___________ ;步骤③的化学方程式为___________ ;目的为__________ 。
(2)碘是人体必需的一种微量元素。海洋植物中富含碘元素。实验室模拟从海带中提取碘单质的流程图如图:

① 设计“操作Ⅰ”的主要步骤:溶解、___________ 。
② “试剂a”通常应具有一定的___________ 性。
③ 利用H2O2完成“溶液A”向“溶液B”的转变。配平该反应的化学方程式:___________ 。
___________KI+___________H2O2=___________KOH+___________I2
④ 由于“溶液B”中I2的含量较低,“操作II”能将I2“富集、浓缩”到“有机溶液X”中。
已知:I2在以下试剂中的溶解度都大于水,则“试剂b”可以是___________ 。(选填编号)
⑤“操作II”宜选用的装置是___________ 。(选填编号)
A. B.
B. C.
C. D.
D.
⑥在操作II后,检验提取碘后的水层是否仍含有碘单质的方法是:___________ 。
(1)空气吹出法工艺是目前“海水提溴”的最主要方法之一、其工艺流程如图:

步骤①中获得Br2的离子方程式为
(2)碘是人体必需的一种微量元素。海洋植物中富含碘元素。实验室模拟从海带中提取碘单质的流程图如图:

① 设计“操作Ⅰ”的主要步骤:溶解、
② “试剂a”通常应具有一定的
③ 利用H2O2完成“溶液A”向“溶液B”的转变。配平该反应的化学方程式:
___________KI+___________H2O2=___________KOH+___________I2
④ 由于“溶液B”中I2的含量较低,“操作II”能将I2“富集、浓缩”到“有机溶液X”中。
已知:I2在以下试剂中的溶解度都大于水,则“试剂b”可以是
| 试剂 | A.乙醇 | B.氯仿 | C.四氯化碳 | D.裂化汽油 |
| 相关性质 | 与水互溶不与反应 | 与水不互溶不与I2反应 | 与水不互溶不与I2反应 | 与水不互溶与I2反应 |
A.
 B.
B. C.
C. D.
D.
⑥在操作II后,检验提取碘后的水层是否仍含有碘单质的方法是:
您最近半年使用:0次
名校
解题方法
5 . 海洋资源的利用具有广阔前景。
(1)下图是从海水中提取粗溴的主要流程

①从海水中提取溴的主要步骤是向浓缩的海水中通入氯气,将溴离子氧化,该反应的离子方程式是_______ 。
②可用热空气吹出溴是因为溴的_______ (选填编号)
A.熔点较低 B.熔点较高 C.沸点较低 D.沸点较高
(2)海带灰中富含以 形式存在的碘元素。实验室提取
形式存在的碘元素。实验室提取 的途径如下所示:
的途径如下所示:

①灼烧海带至灰烬时所用的主要仪器名称是_______ 。
②向酸化的滤液中加过氧化氢溶液,写出该反应的离子方程式_______ 。反应结束后,再加入 作萃取剂,振荡、静置,该步操作用到的仪器名称为
作萃取剂,振荡、静置,该步操作用到的仪器名称为_______ ,可以观察到 层呈
层呈_______ 色。
(1)下图是从海水中提取粗溴的主要流程

①从海水中提取溴的主要步骤是向浓缩的海水中通入氯气,将溴离子氧化,该反应的离子方程式是
②可用热空气吹出溴是因为溴的
A.熔点较低 B.熔点较高 C.沸点较低 D.沸点较高
(2)海带灰中富含以
 形式存在的碘元素。实验室提取
形式存在的碘元素。实验室提取 的途径如下所示:
的途径如下所示:
①灼烧海带至灰烬时所用的主要仪器名称是
②向酸化的滤液中加过氧化氢溶液,写出该反应的离子方程式
 作萃取剂,振荡、静置,该步操作用到的仪器名称为
作萃取剂,振荡、静置,该步操作用到的仪器名称为 层呈
层呈
您最近半年使用:0次
2023-03-09更新
|
500次组卷
|
3卷引用:吉林省长春外国语学校2023-2024学年高二上学期开学考试化学试题
名校
6 . 某研究性学习小组利用氯型阴离子交换树脂(RCl)从海带中提取 ,并测定反应
,并测定反应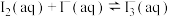 的平衡常数。
的平衡常数。
I.离子交换法提取 的流程如下:
的流程如下:
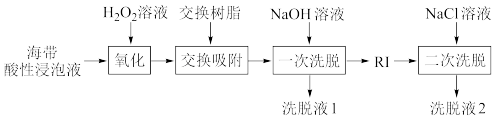
已知:①交换吸附发生反应: ,
,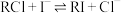 ;
;
②吸附 和
和 达饱和的树脂分别呈淡黄色和黑红色。
达饱和的树脂分别呈淡黄色和黑红色。
③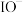 不稳定,易歧化成+5价含氧酸根离子
不稳定,易歧化成+5价含氧酸根离子
(1)“氧化”时 转化为
转化为 ,反应的离子方程式为
,反应的离子方程式为______ 。
(2)“一次洗脱”已经完成的现象是______ 。
(3)向洗脱液1中加入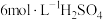 ,可析出碘晶体,写出对应的离子方程式
,可析出碘晶体,写出对应的离子方程式______ 。
(4)将分离出碘晶体的洗脱液合并,置于______ (填仪器名称)中,加入乙醚,振荡,静置,分液。后经______ (填操作名称)回收乙醚。
II.测定反应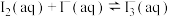 的平衡常数K
的平衡常数K
常温下,取2个碘量瓶分别加入下表中的药品,振荡半小时。取一定体积的上层清液用 溶液进行滴定,测定
溶液进行滴定,测定 和
和 的总浓度。
的总浓度。
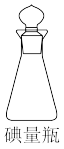
(5)不能用普通锥形瓶代替碘量瓶的原因______ 。
(6)0.5g的碘的不需要精确称取的理由是______ 。
(7)碘量瓶①平衡体系中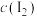 与②中
与②中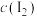 接近。K=
接近。K=______ (写出计算式)。
 ,并测定反应
,并测定反应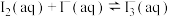 的平衡常数。
的平衡常数。I.离子交换法提取
 的流程如下:
的流程如下:
已知:①交换吸附发生反应:
 ,
,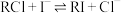 ;
;②吸附
 和
和 达饱和的树脂分别呈淡黄色和黑红色。
达饱和的树脂分别呈淡黄色和黑红色。③
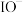 不稳定,易歧化成+5价含氧酸根离子
不稳定,易歧化成+5价含氧酸根离子(1)“氧化”时
 转化为
转化为 ,反应的离子方程式为
,反应的离子方程式为(2)“一次洗脱”已经完成的现象是
(3)向洗脱液1中加入
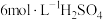 ,可析出碘晶体,写出对应的离子方程式
,可析出碘晶体,写出对应的离子方程式(4)将分离出碘晶体的洗脱液合并,置于
II.测定反应
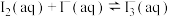 的平衡常数K
的平衡常数K常温下,取2个碘量瓶分别加入下表中的药品,振荡半小时。取一定体积的上层清液用
 溶液进行滴定,测定
溶液进行滴定,测定 和
和 的总浓度。
的总浓度。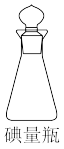
编号 | 250mL碘量瓶① | 250mL碘量瓶② |
药品 | 0.5g研细的碘 60mL | 0.5g研细的碘 60mL |
|
|
|
(5)不能用普通锥形瓶代替碘量瓶的原因
(6)0.5g的碘的不需要精确称取的理由是
(7)碘量瓶①平衡体系中
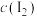 与②中
与②中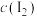 接近。K=
接近。K=
您最近半年使用:0次
2022-12-14更新
|
228次组卷
|
2卷引用:吉林省白山市抚松县第一中学2022-2023学年高三上学期期末考试化学试题
名校
解题方法
7 . 某学习小组按如下实验流程从海带中提取碘单质。
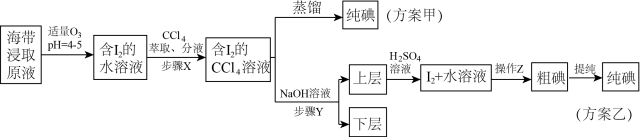
| A.步骤X“分液”时,应打开旋塞,先将水层放出 |
| B.方案甲采用蒸馏法时,碘蒸气先汽化冷凝,在锥形瓶中先得到I2 |
| C.步骤Y中应加入过量的稀NaOH溶液 |
D.加入H2SO4溶液后发生反应的离子方程式为: 5I-+IO +6H+=3I2+3H2O +6H+=3I2+3H2O |
您最近半年使用:0次
2022-10-07更新
|
210次组卷
|
5卷引用:吉林省长春市东北师范大学附属中学2022-2023学年高一下学期期末考试化学试题
8 . 海藻中含有丰富的碘元素(以 形式存在)。实验室中提取碘的流程如图:
形式存在)。实验室中提取碘的流程如图:

(1)实验操作③的名称是_______ ,所用主要仪器名称为_______ 。
(2)提取碘的过程中,可供选择的有机试剂是_______(填编号)。
(3)从碘的有机溶液中得到单质碘的方法是_______ 。
(4)步骤①灼烧海藻时,除需要三脚架外,还需要用到的实验仪器是_______ (从下列仪器中选出所需的仪器,将字母填写在空白处)。
A.烧杯 B.坩埚 C.表面皿 D.泥三角E.酒精灯 F.干燥器
 形式存在)。实验室中提取碘的流程如图:
形式存在)。实验室中提取碘的流程如图:
(1)实验操作③的名称是
(2)提取碘的过程中,可供选择的有机试剂是_______(填编号)。
| A.酒精(沸点78℃) | B.四氯化碳(沸点77℃) |
| C.甘油(沸点290℃) | D.苯(沸点80℃) |
(4)步骤①灼烧海藻时,除需要三脚架外,还需要用到的实验仪器是
A.烧杯 B.坩埚 C.表面皿 D.泥三角E.酒精灯 F.干燥器
您最近半年使用:0次
名校
9 . 海带中含有碘元素,可通过以下步骤提取碘单质:①灼烧;②溶解;③过滤;④氧化;⑤萃取分液等。以上步骤不需要用到的仪器是
A. | B. | C. | D. |
您最近半年使用:0次
2022-03-04更新
|
854次组卷
|
10卷引用:吉林省长春外国语学校2022-2023学年高一下学期6月月考化学试题
吉林省长春外国语学校2022-2023学年高一下学期6月月考化学试题山东省潍坊市2022届高三普通高等学校招生全国统一考试(一模)化学试题福建省龙岩第一中学2021-2022学年高一下学期第二次月考化学试题山东省潍坊市2021-2022学年高一下学期3月阶段测试化学试题福建省厦门市湖滨中学2021-2022学年高一下学期期中考试化学试题广东省昌乐市第一中学2022-2023学年高三上学期期末质量检测化学试题(已下线)题型167 物质的分离与提纯中涉及的仪器选择与使用(已下线)第八章 化学与可持续发展(B卷·能力提升练)-【单元测试】2022-2023学年高一化学分层训练AB卷(人教版2019必修第二册)河北省唐山市第一中学2022-2023学年高三上学期12月月考化学试题(已下线)第八章 化学与可持续发展【单元测试B卷】
真题
名校
10 . 通过下列实验可从I2,的CCl4溶液中回收I2。

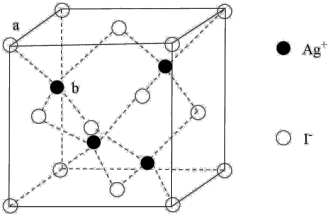
下列说法正确的是


下列说法正确的是
A.NaOH溶液与I2反应的离子方程式:I2+2OH-=I-+IO +H2O +H2O |
| B.通过过滤可将水溶液与CCl4分离 |
| C.向加酸后的上层清液中滴加AgNO3溶液生成AgI沉淀,1个AgI晶胞(如图)中含14个I- |
| D.回收的粗碘可通过升华进行纯化 |
您最近半年使用:0次
2022-01-04更新
|
4857次组卷
|
8卷引用:吉林省长春市第五中学2022-2023学年高二下学期第一学程考试化学试题
吉林省长春市第五中学2022-2023学年高二下学期第一学程考试化学试题2021年新高考江苏化学高考真题(已下线)押江苏卷第9题 化学工艺流程选择题 -备战2022年高考化学临考题号押题(江苏卷)(已下线)易错点32 物质的分离、提纯与检验-备战2023年高考化学考试易错题广东省昌乐市第一中学2022-2023学年高三上学期期末质量检测化学试题河北省衡水市武强中学2022-2023学年高二下学期期末考试化学试题辽宁省沈阳市第二中学2023-2024学年高三上学期期末模拟考试化学试题(已下线)热点06 物质的聚集状态与晶体的常识

 KI
KI




