1 . 下列原理或方法不能达到相应目的或现象的是
| 选项 | 目的或现象 | 原理或方法 |
| A | 去除汽车尾气中NO和CO | 催化转化: |
| B | 利用海带提取碘 | 经灼烧、溶解、过滤、氧化和萃取富集碘元素 |
| C | 维持血液的pH为7.35~7.45 | 血浆中 和 和 的浓度保持动态平衡 的浓度保持动态平衡 |
| D | 消除蚂蚁叮咬引起的皮肤不适 | 可涂抹饱和 溶液 溶液 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
解题方法
2 . 化学创造美好生活。下列应用实例与所述的化学知识没有关联的是
| 选项 | 应用实例 | 化学知识 |
| A | 利用聚苯乙烯制作泡沫包装材料 | 聚苯乙烯燃烧生成 和 和 |
| B | 用 作潜水艇中的供氧剂 作潜水艇中的供氧剂 |  与 与 或 或 反应生成 反应生成 |
| C | 将液态植物油制成人造奶油 | 液态植物油能与 发生加成反应 发生加成反应 |
| D | 从海带灰中提取碘单质 | 海带灰中的 可被氧化 可被氧化 |
| A.A | B.B | C.C | D. |
您最近半年使用:0次
解题方法
3 . 碘是生物必需的一种微量元素,海带、海藻等食物含碘量最为丰富.某小组通过实验提取并测定干海带中碘的含量.回答下列问题:
Ⅰ.从海带中提取碘.该小组同学按如图实验流程进行实验:______ (填仪器名称)。______ (用离子方程式表示)。
Ⅱ.滴定法测海带中碘的含量。
用 滴定
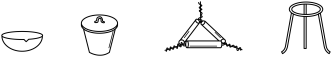
滴定 的水溶液,淀粉溶液作指示剂。原理为:
的水溶液,淀粉溶液作指示剂。原理为: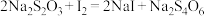 ,
,
(3)用酸式滴定管量取 的水溶液时常需要排出气泡,操作是
的水溶液时常需要排出气泡,操作是__________ 。
(4)小组同学进行了实验测定,在滴定终点附近,反复变回蓝色,一直测不到终点。
猜想1:碘离子被______ 氧化;
猜想2:碘离子被步骤iii中过量的 氧化;
氧化;
②验证猜想
③查阅资料 小组同学认为可能是反应速率不同造成的, 氧化
氧化 的速率
的速率______ (填“快于”或“慢于”) 还原
还原 的速率,导致待测液反复变为蓝色。
的速率,导致待测液反复变为蓝色。
④优化设计 鉴于反应终点无法到达的问题,请提出合理的修正方案____________ 。
⑤完成实验 小组同学修正方案后,取5.000 g干海带进行测定,消耗15.75 mL
 溶液,则干海带中碘的含量为
溶液,则干海带中碘的含量为______ mg/g(保留2位有效数字)。
Ⅰ.从海带中提取碘.该小组同学按如图实验流程进行实验:

Ⅱ.滴定法测海带中碘的含量。
用
 滴定
滴定 的水溶液,淀粉溶液作指示剂。原理为:
的水溶液,淀粉溶液作指示剂。原理为: ,
,(3)用酸式滴定管量取
 的水溶液时常需要排出气泡,操作是
的水溶液时常需要排出气泡,操作是(4)小组同学进行了实验测定,在滴定终点附近,反复变回蓝色,一直测不到终点。

猜想1:碘离子被
猜想2:碘离子被步骤iii中过量的
 氧化;
氧化;②验证猜想
| 序号 | 实验操作 | 实验现象 | 结论 |
| 1 | 取少量原海带浸出液,加入硫酸酸化,再滴加几滴淀粉溶液,鼓入空气 | 待测液始终保持无色 | 猜想1不成立 |
| 2 | 将2mL KI溶液、2滴 KI溶液、2滴  溶液、2滴淀粉溶液和1滴 溶液、2滴淀粉溶液和1滴  溶液混合配制待测液,用 溶液混合配制待测液,用 溶液滴定 溶液滴定 | 猜想2不成立 |
 氧化
氧化 的速率
的速率 还原
还原 的速率,导致待测液反复变为蓝色。
的速率,导致待测液反复变为蓝色。④优化设计 鉴于反应终点无法到达的问题,请提出合理的修正方案
⑤完成实验 小组同学修正方案后,取5.000 g干海带进行测定,消耗15.75 mL

 溶液,则干海带中碘的含量为
溶液,则干海带中碘的含量为
您最近半年使用:0次
2024-04-16更新
|
442次组卷
|
2卷引用:广东省佛山市2024届高三教学质量检测(一)化学试题
名校
解题方法
4 . 某学习小组按如下实验流程进行碘的制取,甲、乙两种实验方案如下:
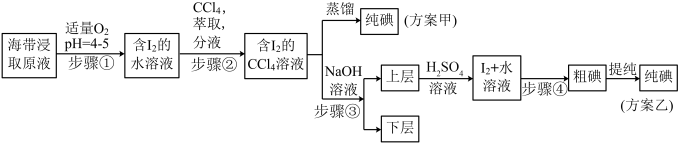
已知: ;酸性条件下,
;酸性条件下, 在水中的溶解度很小。
在水中的溶解度很小。
(1)步骤①中能代替 的最佳物质的电子式为
的最佳物质的电子式为________ 。
(2)步骤②中,萃取后分液漏斗内观察到的现象是________ 。
(3)下列有关步骤③的说法正确的是________(填序号)。
(4)方案乙中,上层液体中加入 溶液,反应的离子方程式为
溶液,反应的离子方程式为________ ,其中步骤④操作的名称是________ ;方案甲中采用蒸馏效果不佳,理由是________ 。

已知:
 ;酸性条件下,
;酸性条件下, 在水中的溶解度很小。
在水中的溶解度很小。(1)步骤①中能代替
 的最佳物质的电子式为
的最佳物质的电子式为(2)步骤②中,萃取后分液漏斗内观察到的现象是
(3)下列有关步骤③的说法正确的是________(填序号)。
| A.应控制NaOH溶液的浓度和体积 | B.将碘转化成离子进入水层 |
| C.主要目的是除去浸取原液中的有机杂质 | D.NaOH溶液可由乙醇代替 |
(4)方案乙中,上层液体中加入
 溶液,反应的离子方程式为
溶液,反应的离子方程式为
您最近半年使用:0次
名校
解题方法
5 . 实验室从干海带中提取碘的流程如图所示.下列各操作所使用的装置正确的是
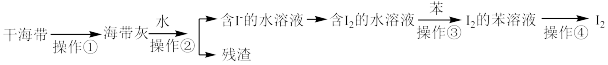
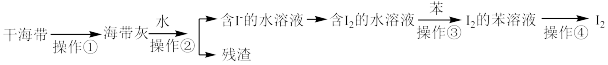
A.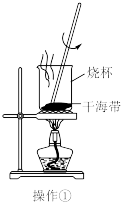 | B. | C. | D. |
您最近半年使用:0次
名校
解题方法
6 . 海洋中蕴含着丰富的化学元素,是人类资源的宝库。
I.某学校兴趣小组在实验室按如下实验流程提取海带中的碘。

(1)海带灼烧的目的是___________ 。海带灰中含有的其他可溶性无机盐,是在___________ (从以上流程中选填实验操作名称)中实现与碘分离。上述实验流程中不需要用到的仪器是___________ (从下列图中选择,写出名称)。

(2)“氧化”时加入3mol·L-1H2SO4和3%H2O2溶液,发生反应的离子方程式为___________ 。
(3)加碘食盐中的碘以KIO3形式存在,证明食盐中存在IO ,必须使用的物质是
,必须使用的物质是___________ (填序号)。
①pH试纸 ②蓝色石蕊试纸 ③碘化钾淀粉试纸 ④蒸馏水 ⑤食醋 ⑥醇
Ⅱ.某学校兴趣小组从海水晒盐后的盐卤(含MgCl2、NaCl、KCl、MgSO4等)中模拟工业生产来提取镁,主要过程如图甲:
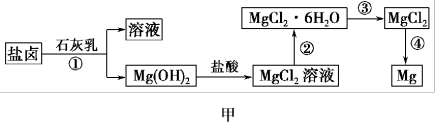
(4)图乙是盐卤中某些物质的溶解度曲线,将盐卤加热到T2℃以上,根据溶解度曲线,首先从盐卤中分离出来的晶体是___________ 。步骤③的具体操作为___________ 。
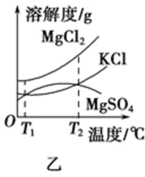
(5)写出步骤④制备金属镁的化学方程式:___________ 。该过程得到的镁蒸气需要在特定的循环中冷却,可选用___________ (填字母)作冷却剂。
A.Ar B.CO2 C.空气 D.O2 E.水蒸气
I.某学校兴趣小组在实验室按如下实验流程提取海带中的碘。

(1)海带灼烧的目的是

(2)“氧化”时加入3mol·L-1H2SO4和3%H2O2溶液,发生反应的离子方程式为
(3)加碘食盐中的碘以KIO3形式存在,证明食盐中存在IO
 ,必须使用的物质是
,必须使用的物质是①pH试纸 ②蓝色石蕊试纸 ③碘化钾淀粉试纸 ④蒸馏水 ⑤食醋 ⑥醇
Ⅱ.某学校兴趣小组从海水晒盐后的盐卤(含MgCl2、NaCl、KCl、MgSO4等)中模拟工业生产来提取镁,主要过程如图甲:

(4)图乙是盐卤中某些物质的溶解度曲线,将盐卤加热到T2℃以上,根据溶解度曲线,首先从盐卤中分离出来的晶体是

(5)写出步骤④制备金属镁的化学方程式:
A.Ar B.CO2 C.空气 D.O2 E.水蒸气
您最近半年使用:0次
7 . 反应①②分别是从海藻灰和某种矿石中提取碘的主要反应:①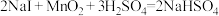
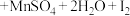 ;②
;② 。下列说法正确的是
。下列说法正确的是
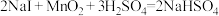
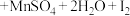 ;②
;② 。下列说法正确的是
。下列说法正确的是| A.两个反应中硫元素均被氧化 |
| B.碘元素在反应①中被还原,在反应②中被氧化 |
C.氧化性: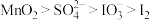 |
D.酸性条件下,I-和 有可能反应生成I2 有可能反应生成I2 |
您最近半年使用:0次
名校
8 . 工业上制备相关物质,涉及的反应原理及部分流程较为合理的是
A.制取镁:海水 Mg(OH)2 Mg(OH)2 MgO MgO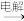 Mg Mg |
B.冶炼铝:铝土矿 NaAlO2 NaAlO2 无水AlCl3 无水AlCl3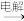 Al Al |
C.制纯碱:饱和NaCl(aq)  NaHCO3(s) NaHCO3(s) 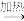 Na2CO3(s) Na2CO3(s) |
D.制碘:海带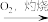 海带灰 海带灰  I2(aq) I2(aq) I2 I2 |
您最近半年使用:0次
2023-09-11更新
|
197次组卷
|
2卷引用:广东省阳江市2023-2024学年高一上学期10月月考化学试题
名校
9 . 人类的生产、生活离不开化学。
(1)铝粉与某些金属的氧化物组成的混合物叫铝热剂,铝热剂在高温下发生的反应叫铝热反应,如: ,反应发生时放出大量的热。
,反应发生时放出大量的热。
①信息中的“某些”指___________ (填“比铝活泼”“比铝不活泼”或“任意”)。
②试写出铝粉与 发生铝热反应的化学方程式:
发生铝热反应的化学方程式:___________ 。
(2)从海水中提取溴的工业流程如图:
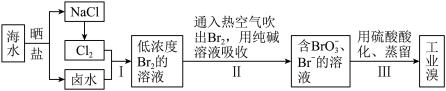
①步骤Ⅰ中发生反应的离子方程式为___________ 。
②步骤Ⅱ用热空气吹出的 被纯碱溶液吸收时,被氧化和被还原的
被纯碱溶液吸收时,被氧化和被还原的 的物质的量之比为
的物质的量之比为___________ 。
(3)海带中含有丰富的碘元素,某化学研究性学习小组用如图流程从海水中提取碘:

①若操作Ⅰ用 溶液(稀硫酸酸化)完成碘元素的转化,则反应的离子方程式为
溶液(稀硫酸酸化)完成碘元素的转化,则反应的离子方程式为___________ 。
②操作Ⅱ的名称为___________ 、___________ ,此过程中可以选用的有机溶剂是___________ (填一种)。
(1)铝粉与某些金属的氧化物组成的混合物叫铝热剂,铝热剂在高温下发生的反应叫铝热反应,如:
 ,反应发生时放出大量的热。
,反应发生时放出大量的热。①信息中的“某些”指
②试写出铝粉与
 发生铝热反应的化学方程式:
发生铝热反应的化学方程式:(2)从海水中提取溴的工业流程如图:

①步骤Ⅰ中发生反应的离子方程式为
②步骤Ⅱ用热空气吹出的
 被纯碱溶液吸收时,被氧化和被还原的
被纯碱溶液吸收时,被氧化和被还原的 的物质的量之比为
的物质的量之比为(3)海带中含有丰富的碘元素,某化学研究性学习小组用如图流程从海水中提取碘:

①若操作Ⅰ用
 溶液(稀硫酸酸化)完成碘元素的转化,则反应的离子方程式为
溶液(稀硫酸酸化)完成碘元素的转化,则反应的离子方程式为②操作Ⅱ的名称为
您最近半年使用:0次
10 . 海带中含有碘元素,从海带中提取碘的实验过程如下所示。
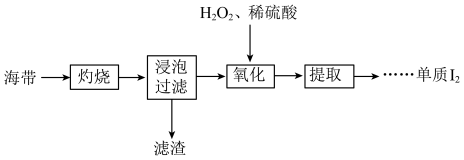
(1)“灼烧”时用到下列仪器中的___________。
(2)“浸泡过滤”后滤液中含有I-,“氧化”的离子方程式为___________ 。
(3)检验“氧化”产生I2的操作:取“氧化”后的少量溶液于试管中,___________ (实验操作及现象)。
(4)“提取”存在以下两种方案。
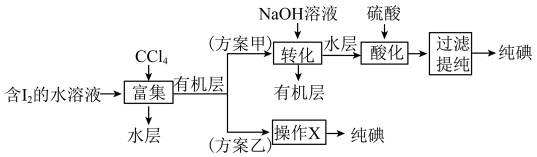
已知: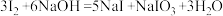 ;酸性条件下,I2在水溶液中的溶解度很小。
;酸性条件下,I2在水溶液中的溶解度很小。
①方案乙中“操作X”的名称是___________ 。
②方案甲中,“酸化”步骤氧化剂与还原剂物质的量之比为___________ 。
③该流程可循环利用的物质是___________ 。
④采用方案乙得到纯碘的产率较低,原因是___________ 。

(1)“灼烧”时用到下列仪器中的___________。
| A.酒精灯 | B.漏斗 | C.蒸发皿 | D.坩埚 |
(3)检验“氧化”产生I2的操作:取“氧化”后的少量溶液于试管中,
(4)“提取”存在以下两种方案。

已知:
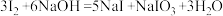 ;酸性条件下,I2在水溶液中的溶解度很小。
;酸性条件下,I2在水溶液中的溶解度很小。①方案乙中“操作X”的名称是
②方案甲中,“酸化”步骤氧化剂与还原剂物质的量之比为
③该流程可循环利用的物质是
④采用方案乙得到纯碘的产率较低,原因是
您最近半年使用:0次



