名校
1 . 某学习小组按如下实验流程从海带中提取碘单质。

已知: ,I2的沸点高于
,I2的沸点高于 ,根据以上流程,判断下列说法正确的是
,根据以上流程,判断下列说法正确的是

已知:
 ,I2的沸点高于
,I2的沸点高于 ,根据以上流程,判断下列说法正确的是
,根据以上流程,判断下列说法正确的是A.步骤X“萃取”时,可用乙醇代替 |
B.加入 溶液后生成1mol I2时转移2NA个e- 溶液后生成1mol I2时转移2NA个e- |
| C.方案甲采用蒸馏法时,碘蒸气先汽化冷凝,在锥形瓶中先得到I2 |
| D.步骤Y后下层液体可循环利用 |
您最近半年使用:0次
名校
解题方法
2 . 海带提碘过程为海带灼烧为海带灰、用水浸取、过滤,所得浸取液中加氧化剂氧化、萃取分液、加NaOH浓溶液反萃取、酸化后过滤得碘单质。上述过程中,用到的玻璃仪器有
①酒精灯、②烧杯、、③坩埚、④分液漏斗、⑤250mL容量瓶、⑥玻璃棒、⑦漏斗、⑧蒸发皿
①酒精灯、②烧杯、、③坩埚、④分液漏斗、⑤250mL容量瓶、⑥玻璃棒、⑦漏斗、⑧蒸发皿
| A.②③④⑦ | B.①②④⑥⑦ | C.②④⑥⑦ | D.①②③④⑥⑦ |
您最近半年使用:0次
2023-09-23更新
|
199次组卷
|
6卷引用:重庆市部分学校2023-2024学年高三一轮复习联考(一)化学试题
名校
解题方法
3 . Ⅰ.将海水淡化与浓海水资源化结合起来是综合利用海水的重要途径之一,一般是先将海水淡化获得淡水,再从剩余的浓海水中通过一系列工艺流程提取其他产品。回答下问题:
(1)请列举一种海水淡化的方法:_______ 。
(2)海水提溴中将Br2从苦卤中吹出,利用了Br2的_______ 性。
Ⅱ.通过传统的海带提碘工艺提取单质碘后,其所得废水中尚残留部分的I2,可用活性炭吸附法加以回收利用。具体流程如图:
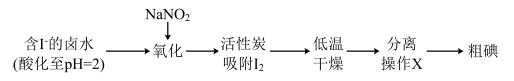
已知:i.pH=2时,NaNO2溶液只能将I-氧化为I2,同时生成NO
ii.将湿润的淀粉-KI试纸伸入盛满氯气的集气瓶中,试纸先变蓝,后褪色
(3)写出氧化含I-的卤水中发生的离子方程式:________ 。
(4)在分离操作X的装置如图所示,电加热器的作用是________ ,得到I2的位置位于该装置中________ 处(填图中选项)。

(5)已知Cl2的氧化性强于NaNO2,但该方法中却选择了价格较高的NaNO2,原因是_______ 。
(6)某工厂排出的废水,经测定含0.012mol/L的游离I2和8×10-4mol/L的H+,若改用加Na2SO3的方法除去I2,发生的化学反应为:Na2SO3+I2+H2O=Na2SO4+2HI,该反应中氧化产物与还原产物的物质的量之比为_______ ,现需处理5L该废水,则需加入0.05mol/L的Na2SO3溶液_______ L才能把I2除尽。
(1)请列举一种海水淡化的方法:
(2)海水提溴中将Br2从苦卤中吹出,利用了Br2的
Ⅱ.通过传统的海带提碘工艺提取单质碘后,其所得废水中尚残留部分的I2,可用活性炭吸附法加以回收利用。具体流程如图:

已知:i.pH=2时,NaNO2溶液只能将I-氧化为I2,同时生成NO
ii.将湿润的淀粉-KI试纸伸入盛满氯气的集气瓶中,试纸先变蓝,后褪色
(3)写出氧化含I-的卤水中发生的离子方程式:
(4)在分离操作X的装置如图所示,电加热器的作用是

(5)已知Cl2的氧化性强于NaNO2,但该方法中却选择了价格较高的NaNO2,原因是
(6)某工厂排出的废水,经测定含0.012mol/L的游离I2和8×10-4mol/L的H+,若改用加Na2SO3的方法除去I2,发生的化学反应为:Na2SO3+I2+H2O=Na2SO4+2HI,该反应中氧化产物与还原产物的物质的量之比为
您最近半年使用:0次
名校
4 . 海洋资源的利用具有非常广阔的前景。
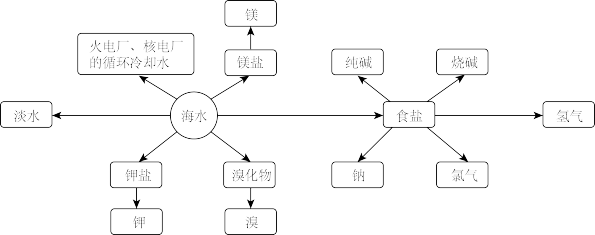
回答下列问题:
Ⅰ.海水制盐
(1)粗盐中可溶性杂质离子包含 、Mg2+、Ca2+。要除去这些杂质离子得到精盐水,加入试剂的顺序可为
、Mg2+、Ca2+。要除去这些杂质离子得到精盐水,加入试剂的顺序可为___________ (填字母)。
a.NaOH溶液、BaCl2溶液、Na2CO3溶液、盐酸
b.NaOH溶液、Na2CO3溶液、BaCl2溶液、盐酸
c.BaCl2溶液、Na2CO3溶液、NaOH溶液、盐酸
(2)精盐水可用于氯碱工业,请写出氯碱工业总反应的离子方程式___________ 。
Ⅱ.海水提溴
(3)工业上常用“吹出法”提溴,请写出用SO2吸收Br2的化学反应方程式___________ 。
(4)含Br2的海水经“空气吹出、SO2吸收、通入氯气”后再蒸馏的目的是___________ 。
Ⅲ.从海带中提取碘的实验过程如下图所示:
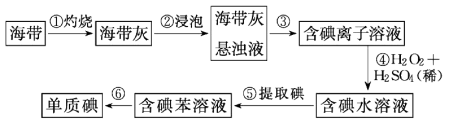
(5)步骤①中灼烧海带时,应将海带放入___________ (填仪器名称)中灼烧。
(6)请写出步骤④反应的离子方程式___________ 。
Ⅳ.海水淡化
(7)实验室模拟蒸馏法淡化海水时,应向蒸馏烧瓶中加入沸石,目的是___________ 。

回答下列问题:
Ⅰ.海水制盐
(1)粗盐中可溶性杂质离子包含
 、Mg2+、Ca2+。要除去这些杂质离子得到精盐水,加入试剂的顺序可为
、Mg2+、Ca2+。要除去这些杂质离子得到精盐水,加入试剂的顺序可为a.NaOH溶液、BaCl2溶液、Na2CO3溶液、盐酸
b.NaOH溶液、Na2CO3溶液、BaCl2溶液、盐酸
c.BaCl2溶液、Na2CO3溶液、NaOH溶液、盐酸
(2)精盐水可用于氯碱工业,请写出氯碱工业总反应的离子方程式
Ⅱ.海水提溴
(3)工业上常用“吹出法”提溴,请写出用SO2吸收Br2的化学反应方程式
(4)含Br2的海水经“空气吹出、SO2吸收、通入氯气”后再蒸馏的目的是
Ⅲ.从海带中提取碘的实验过程如下图所示:

(5)步骤①中灼烧海带时,应将海带放入
(6)请写出步骤④反应的离子方程式
Ⅳ.海水淡化
(7)实验室模拟蒸馏法淡化海水时,应向蒸馏烧瓶中加入沸石,目的是
您最近半年使用:0次
名校
5 . 下列实验装置或操作均正确,且能达到预期目的是


| A.甲检验溶液中是否有K元素 | B.乙吸收HCl |
| C.丙测氯水的pH | D.丁灼烧海带 |
您最近半年使用:0次
名校
6 . 下列有关实验的叙述中,合理的有
①用pH试纸测得某新制氯水的pH为2
②实验室从海带提取单质碘的方法是:取样→灼烧→溶解→过滤→萃取
③用托盘天平称量34.20gNaCl
④用乙醇萃取溶于水中的碘
⑤将pH试纸伸入NaOH溶液中测pH值
⑥证明CH3COOH是弱电解质,可以用同浓度的盐酸和CH3COOH溶液做导电性实验,观察灯泡明亮程度
⑦测定中和反应的反应热时,将碱缓慢倒入酸中,所测温度值偏小
①用pH试纸测得某新制氯水的pH为2
②实验室从海带提取单质碘的方法是:取样→灼烧→溶解→过滤→萃取
③用托盘天平称量34.20gNaCl
④用乙醇萃取溶于水中的碘
⑤将pH试纸伸入NaOH溶液中测pH值
⑥证明CH3COOH是弱电解质,可以用同浓度的盐酸和CH3COOH溶液做导电性实验,观察灯泡明亮程度
⑦测定中和反应的反应热时,将碱缓慢倒入酸中,所测温度值偏小
| A.1项 | B.2项 | C.3项 | D.4项 |
您最近半年使用:0次
名校
7 . 海水是巨大的资源宝库,海水淡化及其综合利用具有重要意义。请回答下列问题:
(1)历史最久,技术和工艺也比较成熟,但成本较高的海水淡化方法是_______ 。
(2)步骤1中,粗盐中含有 、
、 、
、 等杂质离子,精制时常用的试剂有:①稀盐酸;②氯化钡溶液;③氢氧化钠溶液;④碳酸钠溶液。下列加入试剂的顺序正确的是_______(填字母)
等杂质离子,精制时常用的试剂有:①稀盐酸;②氯化钡溶液;③氢氧化钠溶液;④碳酸钠溶液。下列加入试剂的顺序正确的是_______(填字母)
(3)海水提溴工艺中热空气吹出 ,利用了溴的
,利用了溴的_______ 性质;吹出的溴蒸气在吸收塔中被 和水吸收,写出离子方程式
和水吸收,写出离子方程式_______ 。
(4)为了把海水中 转化为
转化为 ,从原料来源及经济效益角度考虑,最好选用
,从原料来源及经济效益角度考虑,最好选用_______ 。
a.氨水 b.氢氧化钙 c.氢氧化钠
(5)写出无水氯化镁制备Mg的化学方程式:_______ 。
(6)在实验室模拟海带提碘的实验过程。灼烧海带时,会用到的主要仪器有酒精灯、三脚架、玻璃棒、_______ 。
(1)历史最久,技术和工艺也比较成熟,但成本较高的海水淡化方法是
(2)步骤1中,粗盐中含有
 、
、 、
、 等杂质离子,精制时常用的试剂有:①稀盐酸;②氯化钡溶液;③氢氧化钠溶液;④碳酸钠溶液。下列加入试剂的顺序正确的是_______(填字母)
等杂质离子,精制时常用的试剂有:①稀盐酸;②氯化钡溶液;③氢氧化钠溶液;④碳酸钠溶液。下列加入试剂的顺序正确的是_______(填字母)| A.①②③④ | B.②③④① | C.④③②① | D.③②④① |
 ,利用了溴的
,利用了溴的 和水吸收,写出离子方程式
和水吸收,写出离子方程式(4)为了把海水中
 转化为
转化为 ,从原料来源及经济效益角度考虑,最好选用
,从原料来源及经济效益角度考虑,最好选用a.氨水 b.氢氧化钙 c.氢氧化钠
(5)写出无水氯化镁制备Mg的化学方程式:
(6)在实验室模拟海带提碘的实验过程。灼烧海带时,会用到的主要仪器有酒精灯、三脚架、玻璃棒、
您最近半年使用:0次
2022-05-12更新
|
496次组卷
|
2卷引用:重庆市巫山大昌中学校2021-2022学年高一下学期期末考试化学试题
8 . 碘和碘化合物的用途广泛,实验室从海带中提取碘的步骤为:①海带灼烧,②溶解过滤,③在滤液中加入稀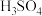 和
和 氧化,④用
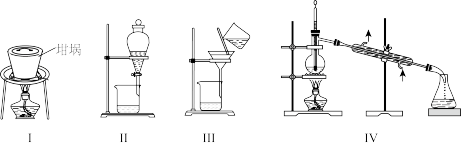
氧化,④用 萃取,⑤蒸馏。下列装置在该实验中不能达到目的的是
萃取,⑤蒸馏。下列装置在该实验中不能达到目的的是
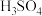 和
和 氧化,④用
氧化,④用 萃取,⑤蒸馏。下列装置在该实验中不能达到目的的是
萃取,⑤蒸馏。下列装置在该实验中不能达到目的的是
| A.用Ⅰ装置灼烧海带 | B.用Ⅱ装置萃取 | C.用Ⅲ装置过滤 | D.用Ⅳ装置蒸馏 |
您最近半年使用:0次
2022-04-09更新
|
370次组卷
|
3卷引用:重庆市2022届高三第二次诊断性考试康德卷化学试题
名校
9 . 下列实验装置与操作都正确的是
| A | B | C | D |
 |  |  |  |
| 灼烧海带 | 稀释浓硫酸 | 分离 和 和 | 提纯 胶体 胶体 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2022-03-10更新
|
363次组卷
|
3卷引用:重庆市巫山县官渡中学2021-2022学年高一下学期期末考试化学试题
名校
解题方法
10 . 下列从海带中提取碘的操作或装置(略去部分夹持仪器)正确的是
A.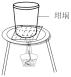 灼烧 灼烧 | B.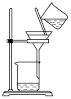 过滤 过滤 |
C. 萃取 萃取 | D. 蒸馏 蒸馏 |
您最近半年使用:0次
2022-02-17更新
|
127次组卷
|
2卷引用:重庆市2021-2022学年高三下学期第六次质量检测(开学考试)化学试题



