名校
1 . 下列有关物质的工业制备过程,在给定条件下能实现的是
A.冶炼铝: |
B.工业制硝酸: |
C.海带提碘: |
D.工业制硫酸: |
您最近半年使用:0次
名校
解题方法
2 . 从海带中提取碘单质,成熟的工艺流程如下,下列关于海带提碘的说法不正确的是


| A.在蒸发皿中灼烧干海带,并用玻璃棒搅拌 |
| B.往含I-的滤液中加入稀硫酸和双氧水后,I-发生氧化反应 |
| C.往碘水中加入几滴淀粉溶液,溶液变蓝色 |
| D.将碘水加入CCl4中,通过萃取、分液得到I2的CCl4溶液 |
您最近半年使用:0次
名校
解题方法
3 . 海洋是资源宝库,下列有关海带提碘的说法错误的是
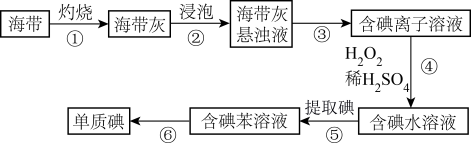

| A.步骤①灼烧海带时需要使用坩埚 |
B.步骤④的化学方程式为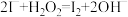 |
| C.灼烧海带时可在容器中滴加少量酒精以促进海带充分燃烧 |
| D.用苯萃取碘水中的碘可实现碘的富集 |
您最近半年使用:0次
名校
解题方法
4 . 某学习小组按如下实验流程探究海带中碘含量的测定和碘的提取。
Ⅰ.碘含量的测定

(1)灼烧海带实验用到的主要的含硅酸盐的仪器有酒精灯、玻璃棒、___________ 、___________ 等。
(2)仪器A的名称为:___________ 。
(3)碘浓度还可用色度计测定吸光度,吸光度越大碘浓度越大。用色度计测得某碘溶液的吸光度后,利用以溶液吸光度为纵坐标、碘浓度(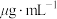 )为横坐标的标准曲线图,可以得出被测溶液碘浓度。为了绘制标准曲线图,取0.10g碘单质,用100mL容量瓶配成碘的
)为横坐标的标准曲线图,可以得出被测溶液碘浓度。为了绘制标准曲线图,取0.10g碘单质,用100mL容量瓶配成碘的 溶液,再从中取出0.10mL加入
溶液,再从中取出0.10mL加入 中配得第一份4.00mL碘的
中配得第一份4.00mL碘的 标准溶液。用色度计测其吸光度,得到标准曲线的第一个坐标点,该坐标点的横坐标是
标准溶液。用色度计测其吸光度,得到标准曲线的第一个坐标点,该坐标点的横坐标是___________ 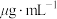 。(注:
。(注: )
)
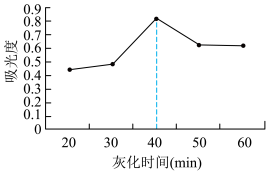
(4)课题组在其他实验条件相同情况下,研究了不同灰化时间(干海带灼烧成灰的时间)对碘提取效果的影响。其结果如图所示。灰化时间超过40min,测得碘的含量逐渐降低,原因是___________ 。
Ⅱ.碘的提取
某同学另取海带原液设计如下实验方案提取碘:
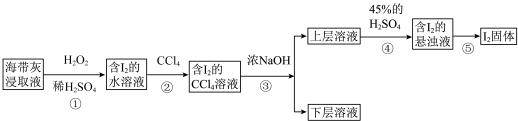
步骤③的离子反应方程式为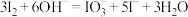
(5)步骤①中发生反应的离子方程式为___________ 。
(6)向含有 的水溶液中加入
的水溶液中加入 振荡静置后的实验现象为
振荡静置后的实验现象为___________ 。
(7)步骤④发生反应的离子方程式为___________ 。
Ⅰ.碘含量的测定

(1)灼烧海带实验用到的主要的含硅酸盐的仪器有酒精灯、玻璃棒、
(2)仪器A的名称为:
(3)碘浓度还可用色度计测定吸光度,吸光度越大碘浓度越大。用色度计测得某碘溶液的吸光度后,利用以溶液吸光度为纵坐标、碘浓度(
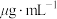 )为横坐标的标准曲线图,可以得出被测溶液碘浓度。为了绘制标准曲线图,取0.10g碘单质,用100mL容量瓶配成碘的
)为横坐标的标准曲线图,可以得出被测溶液碘浓度。为了绘制标准曲线图,取0.10g碘单质,用100mL容量瓶配成碘的 溶液,再从中取出0.10mL加入
溶液,再从中取出0.10mL加入 中配得第一份4.00mL碘的
中配得第一份4.00mL碘的 标准溶液。用色度计测其吸光度,得到标准曲线的第一个坐标点,该坐标点的横坐标是
标准溶液。用色度计测其吸光度,得到标准曲线的第一个坐标点,该坐标点的横坐标是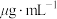 。(注:
。(注: )
)(4)课题组在其他实验条件相同情况下,研究了不同灰化时间(干海带灼烧成灰的时间)对碘提取效果的影响。其结果如图所示。灰化时间超过40min,测得碘的含量逐渐降低,原因是

Ⅱ.碘的提取
某同学另取海带原液设计如下实验方案提取碘:

步骤③的离子反应方程式为
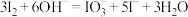
(5)步骤①中发生反应的离子方程式为
(6)向含有
 的水溶液中加入
的水溶液中加入 振荡静置后的实验现象为
振荡静置后的实验现象为(7)步骤④发生反应的离子方程式为
您最近半年使用:0次
名校
解题方法
5 . 海洋资源丰富,其化学资源的开发利用应用广泛。
Ⅰ.工业以浓缩海水为原料提取溴的部分过程如图:
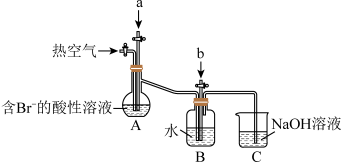
某课外小组在实验室模拟上述过程设计如图装置进行实验(所有橡胶制品均已被保护,夹持装置已略去)。
(1)浓缩海水可以用于提取冶炼金属镁,冶炼Mg的化学方程式为___________ 。
(2)B装置中通入气体b反应的离子方程式为___________ 。
(3)为提取B装置中的溴元素进行如下实验:向反应后B装置的溶液中通入氯气,充分反应得到混合液。从混合液中提取溴单质还需要___________ (填实验操作名称)。
Ⅱ.海带中含丰富的碘。为了从海带中提取碘,某研究性学习小组设计如下实验:

(4)步骤⑤中涉及到的操作名称为___________ ,该步骤还可以选取下列中的哪种试剂替代苯:___________ (填标号)。
A.乙醇 B.四氯化碳 C.乙酸 D.裂化汽油
(5)若要制取127g碘单质,理论上转移电子的物质的量为___________ 。
Ⅰ.工业以浓缩海水为原料提取溴的部分过程如图:

某课外小组在实验室模拟上述过程设计如图装置进行实验(所有橡胶制品均已被保护,夹持装置已略去)。
(1)浓缩海水可以用于提取冶炼金属镁,冶炼Mg的化学方程式为
(2)B装置中通入气体b反应的离子方程式为
(3)为提取B装置中的溴元素进行如下实验:向反应后B装置的溶液中通入氯气,充分反应得到混合液。从混合液中提取溴单质还需要
Ⅱ.海带中含丰富的碘。为了从海带中提取碘,某研究性学习小组设计如下实验:

(4)步骤⑤中涉及到的操作名称为
A.乙醇 B.四氯化碳 C.乙酸 D.裂化汽油
(5)若要制取127g碘单质,理论上转移电子的物质的量为
您最近半年使用:0次
名校
解题方法
6 . 某学习小组按如下实验流程从海带中提取碘单质。
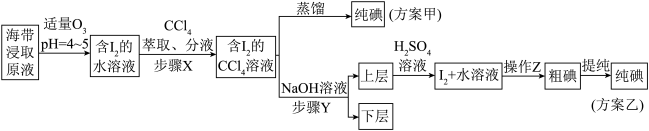
已知: ,
, 的沸点高于
的沸点高于 ,根据以上流程,判断下列说法正确的是
,根据以上流程,判断下列说法正确的是

已知:
 ,
, 的沸点高于
的沸点高于 ,根据以上流程,判断下列说法正确的是
,根据以上流程,判断下列说法正确的是A.步骤X“萃取”时,可用无水乙醇代替 |
B.加入 溶液后发生反应的离子方程式为: 溶液后发生反应的离子方程式为: |
C.方案甲采用蒸馏法时,碘蒸气先汽化冷凝,在锥形瓶中先得到 |
| D.步骤Y后下层液体不可循环利用 |
您最近半年使用:0次
名校
7 . 海洋资源的利用具有非常广阔的前景。
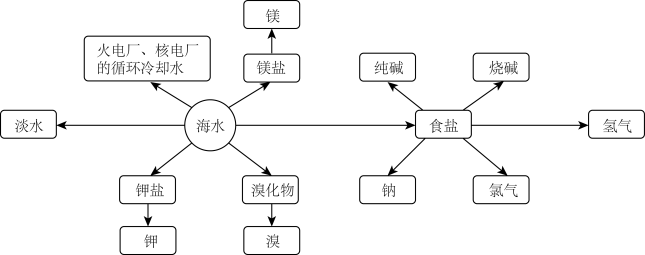
回答下列问题:
Ⅰ.海水制盐
(1)精盐水可用于氯碱工业,请写出氯碱工业总反应的离子方程式___________ 。
Ⅱ.海水提溴
(2)工业上常用“吹出法”提溴,请写出用 吸收
吸收 的化学反应方程式
的化学反应方程式___________ 。
(3)含 的海水经“空气吹出、
的海水经“空气吹出、 吸收、通入氯气”后再蒸馏的目的是
吸收、通入氯气”后再蒸馏的目的是___________ 。
Ⅲ.从海带中提取碘的实验过程如下图所示:
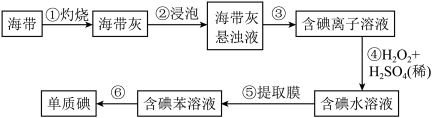
(4)步骤①中灼烧海带时,应将海带放入___________ (填仪器名称)中灼烧。
(5)请写出步骤④反应的离子方程式___________ 。
Ⅳ.海水淡化
(6)实验室模拟蒸馏法淡化海水时,应向蒸馏烧瓶中加入沸石,目的是___________ 。

回答下列问题:
Ⅰ.海水制盐
(1)精盐水可用于氯碱工业,请写出氯碱工业总反应的离子方程式
Ⅱ.海水提溴
(2)工业上常用“吹出法”提溴,请写出用
 吸收
吸收 的化学反应方程式
的化学反应方程式(3)含
 的海水经“空气吹出、
的海水经“空气吹出、 吸收、通入氯气”后再蒸馏的目的是
吸收、通入氯气”后再蒸馏的目的是Ⅲ.从海带中提取碘的实验过程如下图所示:

(4)步骤①中灼烧海带时,应将海带放入
(5)请写出步骤④反应的离子方程式
Ⅳ.海水淡化
(6)实验室模拟蒸馏法淡化海水时,应向蒸馏烧瓶中加入沸石,目的是
您最近半年使用:0次
名校
解题方法
8 . 科学、安全、有效和合理地开发自然资源,对生产、生活有重要价值。请回答下列问题:
(1)活性炭吸附法是工业提取碘的方法之一,其流程如下:
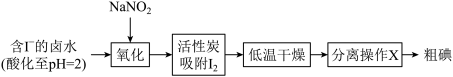
已知: 时,Ⅰ.
时,Ⅰ. 溶液只能将
溶液只能将 氧化为
氧化为 ,同时生成NO
,同时生成NO
Ⅱ.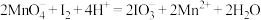
①氧化过程的离子方程式为___________ 。
②根据 的特性,分离操作X为
的特性,分离操作X为___________ ,冷凝得到粗碘。
③酸性 是常用的强氧化剂,但该方法中却选择了价格较高的
是常用的强氧化剂,但该方法中却选择了价格较高的 ,原因是
,原因是___________ 。
④活性炭上吸附的 还能用浓
还能用浓 溶液吸收,每吸收
溶液吸收,每吸收 转移5mol电子,该反应的离子方程式是
转移5mol电子,该反应的离子方程式是___________ 。
(2)以金红石(主要成分为 )为原料,制取Ti的工艺流程如图所示:
)为原料,制取Ti的工艺流程如图所示:
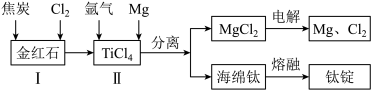
①Ⅰ在高温条件下进行,产物中有一种可燃性无色气体。Ⅰ中反应的化学方程式为___________ 。
②Ⅱ中钛的提取率在不同温度下随时间变化的曲线如图所示,则反应适宜的温度为___________ ℃。

③Ⅱ中氩气的作用是___________ 。
④海绵钛除杂时得到的 可以循环使用,在上述工艺流程中可循环使用的物质还有
可以循环使用,在上述工艺流程中可循环使用的物质还有___________ (填化学式)。
(1)活性炭吸附法是工业提取碘的方法之一,其流程如下:

已知:
 时,Ⅰ.
时,Ⅰ. 溶液只能将
溶液只能将 氧化为
氧化为 ,同时生成NO
,同时生成NOⅡ.
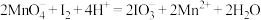
①氧化过程的离子方程式为
②根据
 的特性,分离操作X为
的特性,分离操作X为③酸性
 是常用的强氧化剂,但该方法中却选择了价格较高的
是常用的强氧化剂,但该方法中却选择了价格较高的 ,原因是
,原因是④活性炭上吸附的
 还能用浓
还能用浓 溶液吸收,每吸收
溶液吸收,每吸收 转移5mol电子,该反应的离子方程式是
转移5mol电子,该反应的离子方程式是(2)以金红石(主要成分为
 )为原料,制取Ti的工艺流程如图所示:
)为原料,制取Ti的工艺流程如图所示:
①Ⅰ在高温条件下进行,产物中有一种可燃性无色气体。Ⅰ中反应的化学方程式为
②Ⅱ中钛的提取率在不同温度下随时间变化的曲线如图所示,则反应适宜的温度为

③Ⅱ中氩气的作用是
④海绵钛除杂时得到的
 可以循环使用,在上述工艺流程中可循环使用的物质还有
可以循环使用,在上述工艺流程中可循环使用的物质还有
您最近半年使用:0次
2023-05-23更新
|
639次组卷
|
3卷引用:黑龙江省勃利县高级中学2022-2023学年高一下学期5月月考化学试题
名校
解题方法
9 . 某学习小组按如下实验流程从海带中提取碘单质。
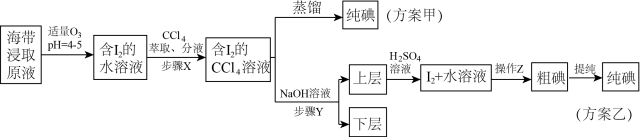
| A.步骤X“分液”时,应打开旋塞,先将水层放出 |
| B.方案甲采用蒸馏法时,碘蒸气先汽化冷凝,在锥形瓶中先得到I2 |
| C.步骤Y中应加入过量的稀NaOH溶液 |
D.加入H2SO4溶液后发生反应的离子方程式为: 5I-+IO +6H+=3I2+3H2O +6H+=3I2+3H2O |
您最近半年使用:0次
2022-10-07更新
|
210次组卷
|
5卷引用:黑龙江省大兴安岭实验中学2023-2024学年高二上学期开学考试化学试卷
名校
解题方法
10 . 碘及其化合物广泛用于医药、染料等方面。回答下列问题:
(1)I2的一种制备方法如图所示:

①生成的沉淀与硝酸反应,生成_____ 后可循环使用。
②通入Cl2的过程中,若氧化产物只有一种,反应的化学方程式为______ ;当n(Cl2)/n(FeI2)>1.5后,单质碘的收率会降低,原因是_______ 。
(2)以NaIO3为原料制备I2的方法是:先向NaIO3溶液中加入计量的NaHSO3,生成碘化物;再向混合溶液中加入NaIO3溶液,反应得到I2。上述制备I2的总反应的离子方程式为______ 。
(3)I2在KI溶液中可发生反应: 。实验室中使用过量的KI与CuSO4溶液反应后,过滤,滤液经水蒸气蒸馏可制得高纯碘。反应中加入过量KI的原因是
。实验室中使用过量的KI与CuSO4溶液反应后,过滤,滤液经水蒸气蒸馏可制得高纯碘。反应中加入过量KI的原因是_______ 。
(1)I2的一种制备方法如图所示:

①生成的沉淀与硝酸反应,生成
②通入Cl2的过程中,若氧化产物只有一种,反应的化学方程式为
(2)以NaIO3为原料制备I2的方法是:先向NaIO3溶液中加入计量的NaHSO3,生成碘化物;再向混合溶液中加入NaIO3溶液,反应得到I2。上述制备I2的总反应的离子方程式为
(3)I2在KI溶液中可发生反应:
 。实验室中使用过量的KI与CuSO4溶液反应后,过滤,滤液经水蒸气蒸馏可制得高纯碘。反应中加入过量KI的原因是
。实验室中使用过量的KI与CuSO4溶液反应后,过滤,滤液经水蒸气蒸馏可制得高纯碘。反应中加入过量KI的原因是
您最近半年使用:0次



