名校
1 . 海洋资源丰富,从海水中获取镁和溴的流程示意图如下:

| A.从经济效益角度考虑,工业上使用的试剂X是氢氧化钠 |
B.可用 代替 代替 吸收含溴的空气 吸收含溴的空气 |
C.直接将 溶液加热蒸干得无水 溶液加热蒸干得无水 |
| D.虚线框内流程的主要目的是减少环境污染 |
您最近半年使用:0次
7日内更新
|
207次组卷
|
3卷引用:2024届内蒙古自治区赤峰市高三一模化学试题
2024届内蒙古自治区赤峰市高三一模化学试题(已下线)通关练02 重要无机化合物的性质及应用-【查漏补缺】2024年高考化学复习冲刺过关(新高考专用)河南省郑州市宇华实验学校2024届高三下学期第三次模拟考试化学试题
2024高三下·全国·专题练习
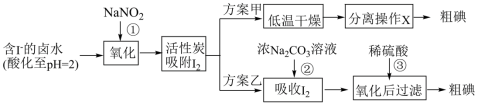
2 . 从海水中可以提取很多有用的物质,例如从海水制盐所得到的卤水中可以提取碘。活性炭吸附法是工业提碘的方法之一,其流程如下:
Ⅱ. ;
;
Ⅲ.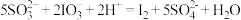 ;
;
方案甲中,根据I2的特性,分离操作X的名称是________ 。
Ⅱ.
 ;
;Ⅲ.
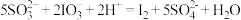 ;
;方案甲中,根据I2的特性,分离操作X的名称是
您最近半年使用:0次
23-24高一·全国·课堂例题
解题方法
3 . 中国有广阔的海岸线,建设发展海洋经济、海水的综合利用大有可为。
Ⅰ.海洋植物中富含一种人体必需的微量元素——碘。实验室模拟从海带中提取碘单质的流程图如下:_______ 中进行。
(2)操作Ⅰ中具体实验步骤:_______
(3)为寻找氯水的替代品,某同学设计了用 代替氯水。请写出此反应的离子方程式:
代替氯水。请写出此反应的离子方程式:_______ 。
Ⅱ.空气吹出法工艺,是目前“海水提溴”的最主要方法之一,其流程如图所示,试回答下列问题:_______ 。
(5)步骤Ⅱ中涉及的离子方程式如下,请在下面横线上填入适当的化学计量数_______ 。
_______ _______
_______ _______
_______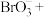 _______
_______ _______
_______
(6)上述流程中吹出的溴蒸气,也可先用二氧化硫水溶液吸收,再用氯气氧化后蒸馏。写出溴与二氧化硫水溶液反应的离子方程式:_______ 。
Ⅲ.镁及其合金是一种用途很广的金属材料,目前60%的镁是从海水中提取的。主要步骤如下: 转化为
转化为 ,试剂①工业上选用
,试剂①工业上选用_______ (填化学式)。
(8)熔融状态的无水 通电后会产生Mg和
通电后会产生Mg和 ,试写出该反应的化学方程式:
,试写出该反应的化学方程式:_______ 。
Ⅰ.海洋植物中富含一种人体必需的微量元素——碘。实验室模拟从海带中提取碘单质的流程图如下:

(2)操作Ⅰ中具体实验步骤:
(3)为寻找氯水的替代品,某同学设计了用
 代替氯水。请写出此反应的离子方程式:
代替氯水。请写出此反应的离子方程式:Ⅱ.空气吹出法工艺,是目前“海水提溴”的最主要方法之一,其流程如图所示,试回答下列问题:

(5)步骤Ⅱ中涉及的离子方程式如下,请在下面横线上填入适当的化学计量数
_______
 _______
_______ _______
_______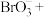 _______
_______ _______
_______
(6)上述流程中吹出的溴蒸气,也可先用二氧化硫水溶液吸收,再用氯气氧化后蒸馏。写出溴与二氧化硫水溶液反应的离子方程式:
Ⅲ.镁及其合金是一种用途很广的金属材料,目前60%的镁是从海水中提取的。主要步骤如下:
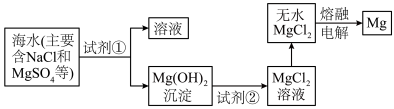
 转化为
转化为 ,试剂①工业上选用
,试剂①工业上选用(8)熔融状态的无水
 通电后会产生Mg和
通电后会产生Mg和 ,试写出该反应的化学方程式:
,试写出该反应的化学方程式:
您最近半年使用:0次
解题方法
4 . 有关化学实验的说法错误的是
| A.实验室储存的镁条着火时,不可以用泡沫灭火器灭火 |
| B.金属汞一旦洒落在实验室地面或桌面时,必须尽可能收集,并深埋处理 |
| C.做蒸馏实验时,应在蒸馏烧瓶中加入沸石,以防暴沸。如果在沸腾前发现忘记加沸石,应立即停止加热,冷却后补加 |
| D.海带中碘元素的提取和检验中,为制取海带灰,可以将海带放在通风处加热灼烧,使其充分灰化 |
您最近半年使用:0次
23-24高一下·全国·课前预习
解题方法
5 . 海水提碘
“提取碘”存在以下两种方案。

①方案乙中“操作X”的名称是_____ 。
②该流程可循环利用的物质是_____ 。
③采用方案乙得到纯碘的产率较低,原因是_____ 。
“提取碘”存在以下两种方案。

①方案乙中“操作X”的名称是
②该流程可循环利用的物质是
③采用方案乙得到纯碘的产率较低,原因是
您最近半年使用:0次
解题方法
6 . 某同学取干海带经下列加工流程,从中提取 。下列说法错误的是
。下列说法错误的是
 。下列说法错误的是
。下列说法错误的是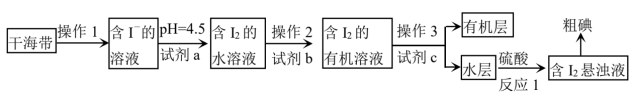

| A.操作1中至少包括灼烧、溶解、过滤等主要过程 |
B.试剂a可以是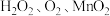 等氧化剂,试剂b可以是 等氧化剂,试剂b可以是 |
| C.操作2和3均用到分液漏斗,振荡萃取时分液漏斗下口要向下倾斜,并不断放气 |
D.反应1每得到127克碘,转移电子数约为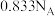 (NA为阿伏加德罗常数的值) (NA为阿伏加德罗常数的值) |
您最近半年使用:0次
7 . 为了从海带浸取液中提取碘,某同学设计了如图实验方案,解答下列问题:
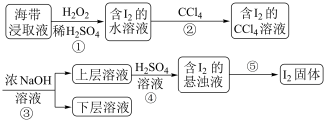
(1) 被称作绿色氧化剂的两个原因
被称作绿色氧化剂的两个原因_______ ;_______
(2)实验操作②的名称为_______ ,操作②需要的仪器除烧杯、玻璃棒外,尚缺少的玻璃仪器有_______ ,碘的 溶液位于
溶液位于_______ 层(填“上”或“下”),呈_______ 色。检验水层是否仍含碘单质的方法是_______ 。
(3)③是将富集在 中的碘单质利用化学转化重新富集在水中,称为反萃取,方程式为
中的碘单质利用化学转化重新富集在水中,称为反萃取,方程式为 ,接下来④发生的反应方程式为
,接下来④发生的反应方程式为_______ 。
(4)本实验中可以循环利用的物质是_______ 。

(1)
 被称作绿色氧化剂的两个原因
被称作绿色氧化剂的两个原因(2)实验操作②的名称为
 溶液位于
溶液位于(3)③是将富集在
 中的碘单质利用化学转化重新富集在水中,称为反萃取,方程式为
中的碘单质利用化学转化重新富集在水中,称为反萃取,方程式为 ,接下来④发生的反应方程式为
,接下来④发生的反应方程式为(4)本实验中可以循环利用的物质是
您最近半年使用:0次
解题方法
8 . 我国拥有很长的海岸线,具有丰富的海洋资源。
Ⅰ.盐卤是海水晒盐后的富含镁盐的溶液,其中除含镁盐外,还含有其他盐类(如图甲所示)。
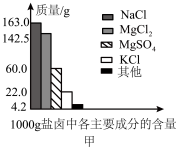
(1)根据图甲所示,写出盐卤中含量最多的盐为___________ (填化学式)其电子式为___________
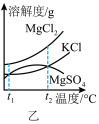
(2)图乙是盐卤中某些物质的溶解度曲线,将盐卤加热到 ℃以上,根据溶解度曲线,首先析出的晶体应是
℃以上,根据溶解度曲线,首先析出的晶体应是___________ 。(填化学式)
(3)如图是常用于混合物的分离和提纯的装置:
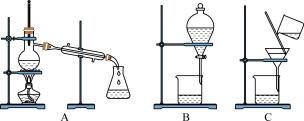
粗盐的提纯应选择图___________ (填字母,下同)装置,若实验中为了除去粗盐中的 、
、 、
、 等杂质离子加入试剂的顺序可以是
等杂质离子加入试剂的顺序可以是___________ 。
A.NaOH、Na2CO3、BaCl2、HCl B.NaOH、BaCl2、Na2CO3、HCl
C.Na2CO3、BaCl2、NaOH、HCl D.BaCl2、NaOH、Na2CO3、HCl
Ⅱ.海带是一种含碘量很高的海藻,从中提取的碘广泛应用于医药、食品和化工。实验室里从海带中提取碘的流程如图。
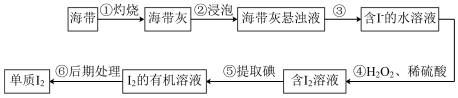
(4)实验步骤①会用到下列仪器中的___________ (填字母)
a.酒精灯 b.蒸发皿 c.坩埚 d.泥三角
(5)设计实验证明第③步操作后滤液中K+的存在,___________ 。
(6)“提取碘”存在以下两种方案。
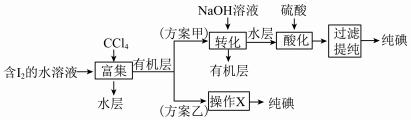
①方案乙中“操作X”的名称是___________ 。
②该流程可循环利用的物质是___________ 。
③采用方案乙得到纯碘的产率较低,原因是___________ 。
Ⅰ.盐卤是海水晒盐后的富含镁盐的溶液,其中除含镁盐外,还含有其他盐类(如图甲所示)。

(1)根据图甲所示,写出盐卤中含量最多的盐为
(2)图乙是盐卤中某些物质的溶解度曲线,将盐卤加热到
 ℃以上,根据溶解度曲线,首先析出的晶体应是
℃以上,根据溶解度曲线,首先析出的晶体应是
(3)如图是常用于混合物的分离和提纯的装置:

粗盐的提纯应选择图
 、
、 、
、 等杂质离子加入试剂的顺序可以是
等杂质离子加入试剂的顺序可以是A.NaOH、Na2CO3、BaCl2、HCl B.NaOH、BaCl2、Na2CO3、HCl
C.Na2CO3、BaCl2、NaOH、HCl D.BaCl2、NaOH、Na2CO3、HCl
Ⅱ.海带是一种含碘量很高的海藻,从中提取的碘广泛应用于医药、食品和化工。实验室里从海带中提取碘的流程如图。

(4)实验步骤①会用到下列仪器中的
a.酒精灯 b.蒸发皿 c.坩埚 d.泥三角
(5)设计实验证明第③步操作后滤液中K+的存在,
(6)“提取碘”存在以下两种方案。

①方案乙中“操作X”的名称是
②该流程可循环利用的物质是
③采用方案乙得到纯碘的产率较低,原因是
您最近半年使用:0次
2023高三·全国·专题练习
9 . 一氯化碘(ICl)是一种卤素互化物。卤素互化物具有强氧化性稀溶液,可与金属直接反应,也可用作有机合成中的碘化剂,一般可由卤素单质直接化合制得。有关一氯化碘制备及性质验证,请回答下列问题:
海藻提碘可得到 的
的 溶液,从其中回收
溶液,从其中回收 的流程如图:
的流程如图:
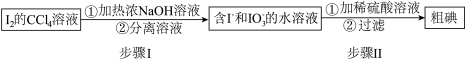
(1)步骤Ⅰ的分离溶液操作中,主要用到的玻璃仪器有烧杯和_______ 。
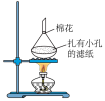
(2)回收获得的粗碘可采用如图所示的简易装置分离提纯。将粉状物放入蒸发皿中并小火加热,碘晶体在扎有小孔的滤纸上凝结,该分离提纯方法的名称是_______ 。
海藻提碘可得到
 的
的 溶液,从其中回收
溶液,从其中回收 的流程如图:
的流程如图:
(1)步骤Ⅰ的分离溶液操作中,主要用到的玻璃仪器有烧杯和
(2)回收获得的粗碘可采用如图所示的简易装置分离提纯。将粉状物放入蒸发皿中并小火加热,碘晶体在扎有小孔的滤纸上凝结,该分离提纯方法的名称是

您最近半年使用:0次
2023高三·全国·专题练习
10 . 全球海水中溴的储藏量丰富,约占地球溴总储藏量的99%,故溴有“海洋元素”之称,海水中溴含量为65mg/L。空气吹出法工艺是目前“海水提溴”的最主要方法之一、其工艺流程如图:
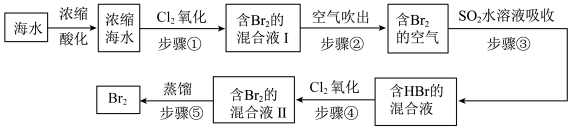
(1)步骤①中获得Br2的离子方程式为____ 。
(2)根据上述反应可判断SO2、Cl2、Br2三种物质氧化性由强到弱的顺序是____ 。
(3)步骤③中若吸收剂为饱和Na2SO3溶液(足量),则完全吸收1molBr2共有___ 个电子转移(用NA的代数式表示)。
碘是人体必需的一种微量元素。海洋植物中富含碘元素。实验室模拟从海带中提取碘单质的流程图如图:

(4)设计“操作Ⅰ”的主要步骤溶解和____ 。
(5)“试剂a”通常应具有一定的____ 性。利用H2O2完成“溶液A”向“溶液B”的转变。写出该反应的化学方程式:________________ 。
(6)由于“溶液B”中I2的含量较低,“操作II”能将I2“富集、浓缩”到“有机溶液X”中。
已知:I2在以下试剂中的溶解度都大于水,则“试剂b”可以是___ 。(选填编号)
(7)“操作II”宜选用的装置是 。(选填编号)
(8)在操作II后,检验提取碘后的水层是否仍含有碘单质的方法是:____ 。
(9)已知:KIO3+5KI+3H2SO4=3K2SO4+3I2+3H2O,I2+2S2O =2I-+S4O
=2I-+S4O ,学生测定某碘盐(含KIO3)中碘元素的含量,其步骤为:
,学生测定某碘盐(含KIO3)中碘元素的含量,其步骤为:
a.准确称取120g食盐,加适量蒸馏水使其完全溶解
b.用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全
c.以淀粉为指示剂,逐滴加入物质的量浓度为2.0×10-3mol·L-1的Na2S2O3溶液50.0mL,恰好反应完全。则所测盐中碘的含量是____ mg•g-1(保留四位小数)。

(1)步骤①中获得Br2的离子方程式为
(2)根据上述反应可判断SO2、Cl2、Br2三种物质氧化性由强到弱的顺序是
(3)步骤③中若吸收剂为饱和Na2SO3溶液(足量),则完全吸收1molBr2共有
碘是人体必需的一种微量元素。海洋植物中富含碘元素。实验室模拟从海带中提取碘单质的流程图如图:

(4)设计“操作Ⅰ”的主要步骤溶解和
(5)“试剂a”通常应具有一定的
(6)由于“溶液B”中I2的含量较低,“操作II”能将I2“富集、浓缩”到“有机溶液X”中。
已知:I2在以下试剂中的溶解度都大于水,则“试剂b”可以是
| 试剂 | A.乙醇 | B.溴水 | C.四氯化碳 | D.裂化汽油 |
| 相关性质 | 与水互溶不与反应 | 与水互溶与I2反应 | 与水不互溶不与I2反应 | 与水不互溶与I2反应 |
(7)“操作II”宜选用的装置是 。(选填编号)
A.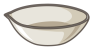 | B. | C.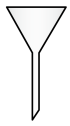 | D.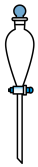 |
(8)在操作II后,检验提取碘后的水层是否仍含有碘单质的方法是:
(9)已知:KIO3+5KI+3H2SO4=3K2SO4+3I2+3H2O,I2+2S2O
 =2I-+S4O
=2I-+S4O ,学生测定某碘盐(含KIO3)中碘元素的含量,其步骤为:
,学生测定某碘盐(含KIO3)中碘元素的含量,其步骤为:a.准确称取120g食盐,加适量蒸馏水使其完全溶解
b.用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全
c.以淀粉为指示剂,逐滴加入物质的量浓度为2.0×10-3mol·L-1的Na2S2O3溶液50.0mL,恰好反应完全。则所测盐中碘的含量是
您最近半年使用:0次



