名校
解题方法
1 . 某兴趣小组利用下列装置,进行与氯气相关的实验。
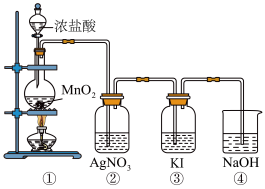
请回答:
(1)写出实验室用上述方法制取氯气的化学方程式_________ 。
(2)利用该原理和装置①进行实验,制得的氯气中往往含有的杂质可依次通入到_________ 、_________ 除去。
(3)装置②中出现白色沉淀,据此现象能否推测装置①中生成Cl2_________ (填“能”或者“否”),请说明理由_________ 。
(4)实验室从海带中提取碘的就是利用装置③的原理,请写出该溶液中发生反应的离子反应方程式_________ 。
(5)图中④所示的溶液是为了减少对环境的污染,请写出该溶液中发生反应的离子反应方程式_________ 。

请回答:
(1)写出实验室用上述方法制取氯气的化学方程式
(2)利用该原理和装置①进行实验,制得的氯气中往往含有的杂质可依次通入到
(3)装置②中出现白色沉淀,据此现象能否推测装置①中生成Cl2
(4)实验室从海带中提取碘的就是利用装置③的原理,请写出该溶液中发生反应的离子反应方程式
(5)图中④所示的溶液是为了减少对环境的污染,请写出该溶液中发生反应的离子反应方程式
您最近一年使用:0次
2 . 海洋资源的综合利用是21世纪世界海洋开发利用的重点领域之一。
(1)模拟工业制备氯气
装置如图所示,接通电源,当观察到石墨电极与滤纸接触的区域有细小的气泡产生时,停止通电。将pH试纸分别放在a、b处滤纸上,观察颜色变化。
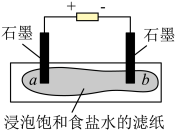
①写出“通电”时发生反应的离子方程式_______ 。
②在上述实验中观察a处pH试纸中心呈白色,边缘有一圈淡淡的红色,b处pH试纸呈_______ 色。
(2)模拟从海水提取食盐后的母液中提取溴的流程如下图:
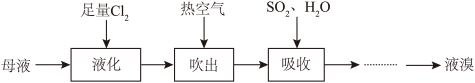
①“吸收”步骤中发生的离子反应方程式为_______ 。
②设计简单的实验验证溴的非金属性比碘强_______ 。(可供选择的试剂:溴水、碘水、NaBr溶液、KI溶液、淀粉溶液)
(3)模拟反萃取法提取碘的实验流程如下图:
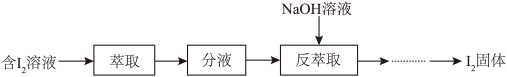
①“萃取”操作中可使用 作为
作为 的萃取剂,其原因除
的萃取剂,其原因除 不与
不与 反应外,还有
反应外,还有_______ 。
②“反萃取”操作时溶液中有 、
、 生成。该步骤发生反应的离子反应方程式:
生成。该步骤发生反应的离子反应方程式:_______ 。
(1)模拟工业制备氯气
装置如图所示,接通电源,当观察到石墨电极与滤纸接触的区域有细小的气泡产生时,停止通电。将pH试纸分别放在a、b处滤纸上,观察颜色变化。

①写出“通电”时发生反应的离子方程式
②在上述实验中观察a处pH试纸中心呈白色,边缘有一圈淡淡的红色,b处pH试纸呈
(2)模拟从海水提取食盐后的母液中提取溴的流程如下图:

①“吸收”步骤中发生的离子反应方程式为
②设计简单的实验验证溴的非金属性比碘强
(3)模拟反萃取法提取碘的实验流程如下图:

①“萃取”操作中可使用
 作为
作为 的萃取剂,其原因除
的萃取剂,其原因除 不与
不与 反应外,还有
反应外,还有②“反萃取”操作时溶液中有
 、
、 生成。该步骤发生反应的离子反应方程式:
生成。该步骤发生反应的离子反应方程式:
您最近一年使用:0次
名校
3 . I.海洋是生命的摇篮,浩瀚的海洋中蕴藏着丰富的资源。人们可以从海水中提取淡水和制得镁、溴等重要的化工产品。
(1)从海水中获得淡水的主要方法有蒸馏法、离子交换法和___________ 。离子交换法净化水的过程如图所示。下列说法正确的是___________ (填序号)。
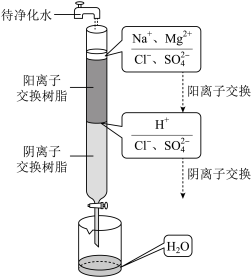
A.经过阳离子交换树脂后,水中阳离子总数
B.通过阴离子交换树脂后,水中只有 被除去
被除去
C.通过净化处理后的水,导电性增强
D.阴离子交换树脂填充段存在反应:
(2)工业上通过 制备Mg,常用的冶炼方法是
制备Mg,常用的冶炼方法是___________ 。制备溴时通入热空气可以吹出溴,是利用了溴的___________ 。
Ⅱ.海带中含有碘元素。从海带中提取碘的实验过程如下图所示:
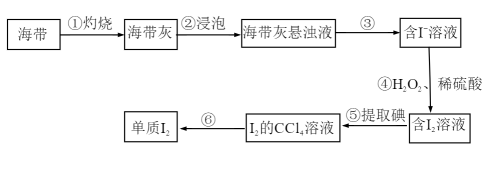
(3)实验步骤①不会用到下列仪器中的___________ (填字母)
a.泥三角 b.250ml容量瓶 c.坩埚 d.漏斗 e.酒精灯
(4)步骤③的操作名称是___________
(5)步骤④中反应的离子方程式为___________
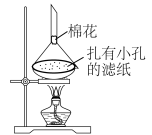
(6)利用如图装置,可以从氯化钠固体中分离出碘单质。简述原理________ ;棉花的作用是________ 。
(1)从海水中获得淡水的主要方法有蒸馏法、离子交换法和

A.经过阳离子交换树脂后,水中阳离子总数
B.通过阴离子交换树脂后,水中只有
 被除去
被除去C.通过净化处理后的水,导电性增强
D.阴离子交换树脂填充段存在反应:

(2)工业上通过
 制备Mg,常用的冶炼方法是
制备Mg,常用的冶炼方法是Ⅱ.海带中含有碘元素。从海带中提取碘的实验过程如下图所示:

(3)实验步骤①不会用到下列仪器中的
a.泥三角 b.250ml容量瓶 c.坩埚 d.漏斗 e.酒精灯
(4)步骤③的操作名称是
(5)步骤④中反应的离子方程式为
(6)利用如图装置,可以从氯化钠固体中分离出碘单质。简述原理

您最近一年使用:0次
名校
解题方法
4 . 海洋是一座巨大的化学资源宝库,从海水中或海产品中提取多种化学物质。
I.试剂级 可用海盐(含泥沙、海藻、
可用海盐(含泥沙、海藻、 等杂质)为原料制备。制备流程如下:
等杂质)为原料制备。制备流程如下:
(1)
焙炒海盐的目的是___________ 。
(2)根据除杂原理、预期沉淀的离子,填写合适的试剂。
其中步骤2和步骤3是否可以颠倒,请给出解释:___________ 。
(3)以氯化钠为原料设计了“黑笔写红字”的趣味实验。滤纸先用氯化钠、无色酚酞的混合液浸湿,然后平铺在一块铂片上,接通电源后,用铅笔在滤纸上写字,会出现红色字迹。下列叙述正确的是___________。

Ⅱ.实验室模拟工业从海藻中提碘的流程如图:
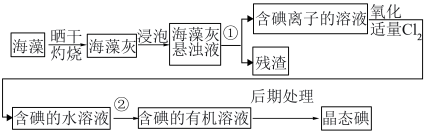
(4)选择合适实验操作名称填入流程图中:①___________ ,②___________ 。(可多选)
A.溶解 B.过滤 C.萃取 D.分液
(5)从“含碘的有机溶液”中回收溶剂,并得到碘单质,可选用如下图装置完成。装置中间部分是“冷凝管”,请描述该装置中有明显的错误,请写出任一种错误___________ 。
(6)
装置 中,温度计所处的正确位置是
中,温度计所处的正确位置是___________ 。(选填编号)

Ⅲ.某化学研究性学习小组模拟工业上从浓缩的海水(海水中富含 )中提取液溴的过程,设计了如下实验装置(夹持装置略去)和操作流程。已知:
)中提取液溴的过程,设计了如下实验装置(夹持装置略去)和操作流程。已知: 的沸点为
的沸点为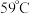 ,微溶于水,有毒。
,微溶于水,有毒。
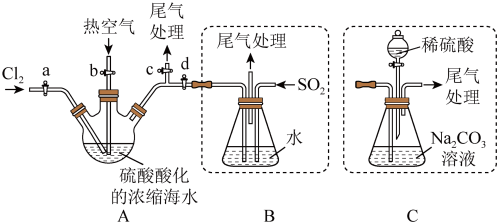
①连接 与B,关闭活塞b、d,,打开活塞a、c,向A中缓慢通入
与B,关闭活塞b、d,,打开活塞a、c,向A中缓慢通入 至反应完全:
至反应完全:
②关闭活塞a、c,打开活塞b、d,向A中鼓入足量热空气:
③进行步骤②的同时,向B中通入足量 ;
;
④关闭活塞b,打开活塞a,再通过A向B中缓慢通入足量 ;
;
⑤将B中所得液体进行萃取分液,蒸馏并收集液溴
请回答下列问题:
(7)步骤②中鼓入热空气的作用为___________ 。
(8)进行步骤③时,B中尾气可用___________吸收处理。
(9)若直接连接A与C,进行步骤①和②,充分反应后,向锥形瓶中流加稀硫酸,再经步骤⑤,也能制得液溴。滴加稀硫酸之前,c中反应生成了NaBrO3、 、
、 ,则该反应的化学方程式为
,则该反应的化学方程式为___________ 。
(10)与B装置相比,采用C装置的优点为___________ 。
I.试剂级
 可用海盐(含泥沙、海藻、
可用海盐(含泥沙、海藻、 等杂质)为原料制备。制备流程如下:
等杂质)为原料制备。制备流程如下:(1)

焙炒海盐的目的是
(2)根据除杂原理、预期沉淀的离子,填写合适的试剂。
| 实验步骤 | 试剂 | 预期沉淀的离子 |
| 步骤1 | 略过量 |  、 、 |
| 步骤2 | 略过量 |  |
| 步骤3 | 略过量 |  |
(3)以氯化钠为原料设计了“黑笔写红字”的趣味实验。滤纸先用氯化钠、无色酚酞的混合液浸湿,然后平铺在一块铂片上,接通电源后,用铅笔在滤纸上写字,会出现红色字迹。下列叙述正确的是___________。

| A.铂片上发生还原反应 |
| B.铂片端作阴极 |
| C.铅笔端有少量的氯气产生 |
| D.a连接的是电源负极 |
Ⅱ.实验室模拟工业从海藻中提碘的流程如图:

(4)选择合适实验操作名称填入流程图中:①
A.溶解 B.过滤 C.萃取 D.分液
(5)从“含碘的有机溶液”中回收溶剂,并得到碘单质,可选用如下图装置完成。装置中间部分是“冷凝管”,请描述该装置中有明显的错误,请写出任一种错误
(6)

装置
 中,温度计所处的正确位置是
中,温度计所处的正确位置是
Ⅲ.某化学研究性学习小组模拟工业上从浓缩的海水(海水中富含
 )中提取液溴的过程,设计了如下实验装置(夹持装置略去)和操作流程。已知:
)中提取液溴的过程,设计了如下实验装置(夹持装置略去)和操作流程。已知: 的沸点为
的沸点为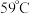 ,微溶于水,有毒。
,微溶于水,有毒。
①连接
 与B,关闭活塞b、d,,打开活塞a、c,向A中缓慢通入
与B,关闭活塞b、d,,打开活塞a、c,向A中缓慢通入 至反应完全:
至反应完全:②关闭活塞a、c,打开活塞b、d,向A中鼓入足量热空气:
③进行步骤②的同时,向B中通入足量
 ;
;④关闭活塞b,打开活塞a,再通过A向B中缓慢通入足量
 ;
;⑤将B中所得液体进行萃取分液,蒸馏并收集液溴
请回答下列问题:
(7)步骤②中鼓入热空气的作用为
(8)进行步骤③时,B中尾气可用___________吸收处理。
| A.水 | B.浓硫酸 | C. 溶液 溶液 | D.饱和 溶液 溶液 |
(9)若直接连接A与C,进行步骤①和②,充分反应后,向锥形瓶中流加稀硫酸,再经步骤⑤,也能制得液溴。滴加稀硫酸之前,c中反应生成了NaBrO3、
 、
、 ,则该反应的化学方程式为
,则该反应的化学方程式为(10)与B装置相比,采用C装置的优点为
您最近一年使用:0次
名校
5 . 海洋化学资源的综合利用对人类的发展意义重大。
Ⅰ.以海水为原料获得的粗盐中含有 、
、 、
、 和难溶性杂质。
和难溶性杂质。
(1)除去粗盐中可溶性杂质,加入试剂的顺序是_______ (填标号),过滤,滴加稀盐酸调节溶液呈中性。
A.


B.


C.


Ⅱ.从海藻中提取碘:
步骤一:制备含碘离子的溶液

(2)实验室焙烧海藻的装置如图,仪器A的名称是_______ 。

步骤二:活性炭吸附法提取碘,其流程如下:
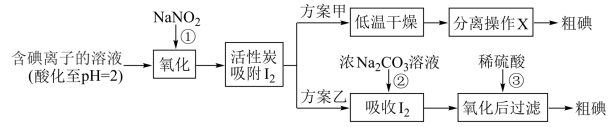
资料显示: 时,
时, 溶液只能将
溶液只能将 氧化为
氧化为 ,同时生成NO。
,同时生成NO。
(3)写出反应①的离子方程式:_______ 。
(4)方案甲中,根据 的特性,分离操作X应为
的特性,分离操作X应为_______ 、_______ 。
(5)方案乙中, 浓溶液吸收
浓溶液吸收 有
有 生成,写出反应②的离子方程式:
生成,写出反应②的离子方程式:_______ 。
(6)方案乙中,已知:反应③充分进行后,过滤,滤液中仍存在少量的 、
、 。为检验滤液中的
。为检验滤液中的 ,请将下列实验方案补充完整。实验中可供选择的试剂:稀
,请将下列实验方案补充完整。实验中可供选择的试剂:稀 、淀粉溶液、
、淀粉溶液、 溶液、
溶液、 。
。
A.将滤液_______ ,直到水层用淀粉溶液检验不出碘单质存在。
B.从水层取少量溶液于试管中,_______ 。
Ⅰ.以海水为原料获得的粗盐中含有
 、
、 、
、 和难溶性杂质。
和难溶性杂质。(1)除去粗盐中可溶性杂质,加入试剂的顺序是
A.



B.



C.



Ⅱ.从海藻中提取碘:
步骤一:制备含碘离子的溶液

(2)实验室焙烧海藻的装置如图,仪器A的名称是

步骤二:活性炭吸附法提取碘,其流程如下:

资料显示:
 时,
时, 溶液只能将
溶液只能将 氧化为
氧化为 ,同时生成NO。
,同时生成NO。(3)写出反应①的离子方程式:
(4)方案甲中,根据
 的特性,分离操作X应为
的特性,分离操作X应为(5)方案乙中,
 浓溶液吸收
浓溶液吸收 有
有 生成,写出反应②的离子方程式:
生成,写出反应②的离子方程式:(6)方案乙中,已知:反应③充分进行后,过滤,滤液中仍存在少量的
 、
、 。为检验滤液中的
。为检验滤液中的 ,请将下列实验方案补充完整。实验中可供选择的试剂:稀
,请将下列实验方案补充完整。实验中可供选择的试剂:稀 、淀粉溶液、
、淀粉溶液、 溶液、
溶液、 。
。A.将滤液
B.从水层取少量溶液于试管中,
您最近一年使用:0次
2023-11-01更新
|
115次组卷
|
2卷引用:江西省上饶广丰中学2023-2024学年高一上学期10月月考化学试题
解题方法
6 .  常用于制药和食品添加剂。以海带为原料提取高纯度碘单质并制备
常用于制药和食品添加剂。以海带为原料提取高纯度碘单质并制备 的一种流程如下:
的一种流程如下:
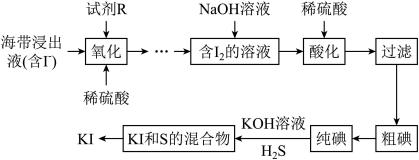
回答下列问题:
(1)“酸化”时稀硫酸的作用是___________ 。
(2)分离 和S的混合物得到
和S的混合物得到 溶液的试剂和方法如下,正确的是
溶液的试剂和方法如下,正确的是___________ (填标号)。
(3)利用下图装置完成 与
与 反应制备
反应制备 。
。

① 溶液的作用是
溶液的作用是___________ (用离子方程式表示)。
②三颈烧瓶中产生 的正确操作顺序为
的正确操作顺序为___________ (填标号)。
a.旋开活塞K,通入 b.加入稀硫酸 c.加入
b.加入稀硫酸 c.加入 溶液
溶液
(4)产品纯度测定。
准确称取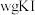 样品溶于水配成
样品溶于水配成 溶液,量取
溶液,量取 溶液于锥形瓶中,加入足量用稀硫酸酸化的
溶液于锥形瓶中,加入足量用稀硫酸酸化的 溶液,摇匀,置于电热板上加热煮沸(常补加热水以保持溶液体积基本不变)。待紫色碘蒸气消失后,再煮沸5分钟,取下放置几分钟,冷却至室温。加入适量的硫酸和磷酸的混合液,用
溶液,摇匀,置于电热板上加热煮沸(常补加热水以保持溶液体积基本不变)。待紫色碘蒸气消失后,再煮沸5分钟,取下放置几分钟,冷却至室温。加入适量的硫酸和磷酸的混合液,用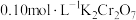 标准溶液反应至完全(还原产物只有
标准溶液反应至完全(还原产物只有 ),消耗标准溶液
),消耗标准溶液 。该
。该 产品的纯度为
产品的纯度为___________ (用含w,V的式子表示)。
 常用于制药和食品添加剂。以海带为原料提取高纯度碘单质并制备
常用于制药和食品添加剂。以海带为原料提取高纯度碘单质并制备 的一种流程如下:
的一种流程如下:
回答下列问题:
(1)“酸化”时稀硫酸的作用是
(2)分离
 和S的混合物得到
和S的混合物得到 溶液的试剂和方法如下,正确的是
溶液的试剂和方法如下,正确的是| 选项 | 试剂 | 方法 |
| a | 二硫化碳 | 分液 |
| b | 酒精 | 分液 |
| c |  溶液 溶液 | 过滤 |
(3)利用下图装置完成
 与
与 反应制备
反应制备 。
。
①
 溶液的作用是
溶液的作用是②三颈烧瓶中产生
 的正确操作顺序为
的正确操作顺序为a.旋开活塞K,通入
 b.加入稀硫酸 c.加入
b.加入稀硫酸 c.加入 溶液
溶液(4)产品纯度测定。
准确称取
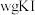 样品溶于水配成
样品溶于水配成 溶液,量取
溶液,量取 溶液于锥形瓶中,加入足量用稀硫酸酸化的
溶液于锥形瓶中,加入足量用稀硫酸酸化的 溶液,摇匀,置于电热板上加热煮沸(常补加热水以保持溶液体积基本不变)。待紫色碘蒸气消失后,再煮沸5分钟,取下放置几分钟,冷却至室温。加入适量的硫酸和磷酸的混合液,用
溶液,摇匀,置于电热板上加热煮沸(常补加热水以保持溶液体积基本不变)。待紫色碘蒸气消失后,再煮沸5分钟,取下放置几分钟,冷却至室温。加入适量的硫酸和磷酸的混合液,用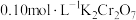 标准溶液反应至完全(还原产物只有
标准溶液反应至完全(还原产物只有 ),消耗标准溶液
),消耗标准溶液 。该
。该 产品的纯度为
产品的纯度为
您最近一年使用:0次
名校
解题方法
7 . 三氯化碘(ICl3)是一种黄色晶体,遇水易分解,熔点:33℃,沸点:73℃,在药物合成中用途非常广泛。某学习小组从海带中提取碘,并用于制备三氯化碘。
(1)从干海带中提取粗碘
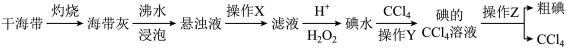
①写出加入过氧化氢后的反应的离子方程式_______ 。
②操作Y用到的玻璃仪器有烧杯、_______ 。
③可以用反萃取法将碘单质从碘的四氯化碳溶液中提取出来,写出向碘的四氯化碳溶液中加入浓氢氧化钠溶液振荡、静置、分液发生的化学方程式_______ 。
(2)利用制得的碘单质制取ICl3
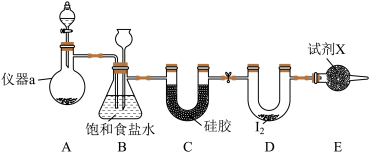
①制备氯气选用的药品为高锰酸钾和浓盐酸,相关反应的离子方程式为_______ 。
②装置B的作用_______ 。
③试剂X为_______ ,X的作用是_______ 。
④氯气与单质碘反应温度稍低于70℃,则装置D适宜的加热方式为_______ 。
(1)从干海带中提取粗碘
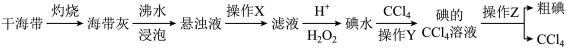
①写出加入过氧化氢后的反应的离子方程式
②操作Y用到的玻璃仪器有烧杯、
③可以用反萃取法将碘单质从碘的四氯化碳溶液中提取出来,写出向碘的四氯化碳溶液中加入浓氢氧化钠溶液振荡、静置、分液发生的化学方程式
(2)利用制得的碘单质制取ICl3

①制备氯气选用的药品为高锰酸钾和浓盐酸,相关反应的离子方程式为
②装置B的作用
③试剂X为
④氯气与单质碘反应温度稍低于70℃,则装置D适宜的加热方式为
您最近一年使用:0次
8 . 围绕海水的综合利用,化学课外兴趣小组进行下列实验:
(1)模拟工业制备氯气
装置如图所示,接通电源,当观察到石墨电极与滤纸接触的区域有细小的气泡产生时,停止通电。将pH试纸分别放在a、b处滤纸上,观察颜色变化。
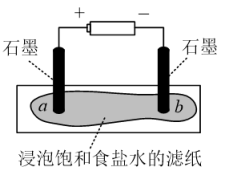
①在上述实验中观察a处pH试纸中心呈白色,边缘有一圈淡淡的红色,b处pH试纸呈___________ 色。
②实验结束后,将滤纸对折,使a、b处充分接触,可将a处残余的Cl2进一步处理。此时发生反应的化学反应方程式是___________ 。
(2)模拟反萃取法提取碘实验流程如下图:
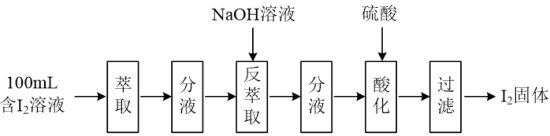
①“萃取”操作时须使用的玻璃仪器有烧杯、玻璃棒和___________ 。
②“反萃取”操作时溶液中有I-、IO 生成。“酸化”步骤发生反应的离子反应方程式为
生成。“酸化”步骤发生反应的离子反应方程式为___________ 。
(3)模拟浓海水提取镁实验流程如下图:
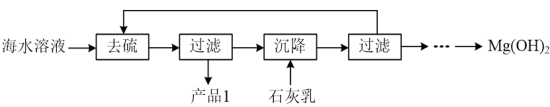
说明:模拟浓海水成分配制的“海水溶液”主要成分如下:
①产品1的化学式为___________ 。
②沉降阶段主要的化学反应方程式为___________ 。
(1)模拟工业制备氯气
装置如图所示,接通电源,当观察到石墨电极与滤纸接触的区域有细小的气泡产生时,停止通电。将pH试纸分别放在a、b处滤纸上,观察颜色变化。

①在上述实验中观察a处pH试纸中心呈白色,边缘有一圈淡淡的红色,b处pH试纸呈
②实验结束后,将滤纸对折,使a、b处充分接触,可将a处残余的Cl2进一步处理。此时发生反应的化学反应方程式是
(2)模拟反萃取法提取碘实验流程如下图:

①“萃取”操作时须使用的玻璃仪器有烧杯、玻璃棒和
②“反萃取”操作时溶液中有I-、IO
 生成。“酸化”步骤发生反应的离子反应方程式为
生成。“酸化”步骤发生反应的离子反应方程式为(3)模拟浓海水提取镁实验流程如下图:

说明:模拟浓海水成分配制的“海水溶液”主要成分如下:
| 离子 | Na+ | Mg2+ | Cl- | SO |
| 浓度/(g·L-1) | 63.7 | 28.8 | 144.6 | 46.4 |
②沉降阶段主要的化学反应方程式为
您最近一年使用:0次
9 . 海带中含有丰富的碘元素(以I-形式存在)。工业中提取碘的流程如图:
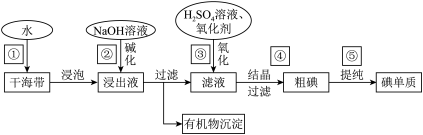
(1)写出步骤③中加硫酸溶液的目的_______ 。
(2)步骤⑤中所涉及的实验操作名称_______ 。
(3)若在实验室中,用分液漏斗、苯(密度比水小,且不溶于水)来提取碘水中的I2,加入少量苯,充分振荡静置后的现象是_______ 。
(4)检验某无色溶液中是否含有I-,所用试剂不合理的是_______ 。
A.淀粉溶液和氯水 B. KBr和稀HCl
C.氯水和四氯化碳 D. KIO3和醋酸
(5)图中有关从海带中提取碘的实验原理和装置能达到实验目的是_____

A.用装置甲灼烧碎海带
B.用装置乙过滤海带灰的浸泡液
C.用装置丙制备用于氧化浸泡液中的氯气
D.用装置丁吸收氧化浸泡液后的尾气

(1)写出步骤③中加硫酸溶液的目的
(2)步骤⑤中所涉及的实验操作名称
(3)若在实验室中,用分液漏斗、苯(密度比水小,且不溶于水)来提取碘水中的I2,加入少量苯,充分振荡静置后的现象是
(4)检验某无色溶液中是否含有I-,所用试剂不合理的是
A.淀粉溶液和氯水 B. KBr和稀HCl
C.氯水和四氯化碳 D. KIO3和醋酸
(5)图中有关从海带中提取碘的实验原理和装置能达到实验目的是

A.用装置甲灼烧碎海带
B.用装置乙过滤海带灰的浸泡液
C.用装置丙制备用于氧化浸泡液中的氯气
D.用装置丁吸收氧化浸泡液后的尾气
您最近一年使用:0次
名校
解题方法
10 . 海带中含有丰富的碘元素(以I-形式存在)。实验中提取碘的流程如图:
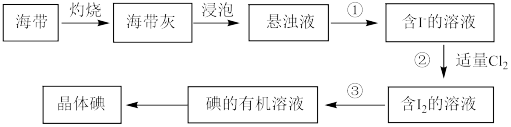
(1)①写出氯原子的原子结构示意图:_______ 。
②写出I-的电子式:_______ 。
③写出步骤②发生的离子方程式_______ 。
(2)①实验①的操作名称_______ 。
②实验③所需要的主要玻璃仪器为_______ 、烧杯。
(3)①实验操作③中,_______ (填“能”或“不能”)用酒精来提取碘。
②实验操作③中,若用苯来提取碘,加入少量苯,充分振荡静置后的现象是_______ 。
A.溶液分层,下层红棕色 B.溶液分层,上层红棕色
C.溶液分层,下层紫红色 D.溶液分层,上层紫红色
(4)检验某无色溶液中是否含有I-,所用试剂不合理的是_______ 。
A.淀粉溶液和氯水 B.稀硝酸和硝酸银溶液
C.氯水和四氯化碳 D.KBr和稀HCl
(5)下列有关从海带中提取碘的实验原理和装置能达到实验目的是( )
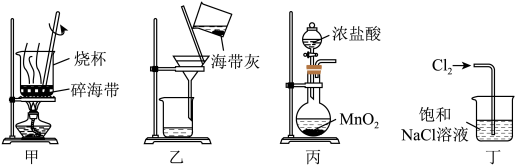
A.用装置甲灼烧碎海带
B.用装置乙过滤海带灰的浸泡液
C.用装置丙制备用于氧化浸泡液中的氯气
D.用装置丁吸收氧化浸泡液中后的尾气

(1)①写出氯原子的原子结构示意图:
②写出I-的电子式:
③写出步骤②发生的离子方程式
(2)①实验①的操作名称
②实验③所需要的主要玻璃仪器为
(3)①实验操作③中,
②实验操作③中,若用苯来提取碘,加入少量苯,充分振荡静置后的现象是
A.溶液分层,下层红棕色 B.溶液分层,上层红棕色
C.溶液分层,下层紫红色 D.溶液分层,上层紫红色
(4)检验某无色溶液中是否含有I-,所用试剂不合理的是
A.淀粉溶液和氯水 B.稀硝酸和硝酸银溶液
C.氯水和四氯化碳 D.KBr和稀HCl
(5)下列有关从海带中提取碘的实验原理和装置能达到实验目的是

A.用装置甲灼烧碎海带
B.用装置乙过滤海带灰的浸泡液
C.用装置丙制备用于氧化浸泡液中的氯气
D.用装置丁吸收氧化浸泡液中后的尾气
您最近一年使用:0次



