三氯化碘(ICl3)是一种黄色晶体,遇水易分解,熔点:33℃,沸点:73℃,在药物合成中用途非常广泛。某学习小组从海带中提取碘,并用于制备三氯化碘。
(1)从干海带中提取粗碘
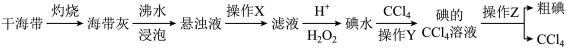
①写出加入过氧化氢后的反应的离子方程式_______ 。
②操作Y用到的玻璃仪器有烧杯、_______ 。
③可以用反萃取法将碘单质从碘的四氯化碳溶液中提取出来,写出向碘的四氯化碳溶液中加入浓氢氧化钠溶液振荡、静置、分液发生的化学方程式_______ 。
(2)利用制得的碘单质制取ICl3
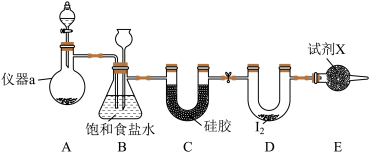
①制备氯气选用的药品为高锰酸钾和浓盐酸,相关反应的离子方程式为_______ 。
②装置B的作用_______ 。
③试剂X为_______ ,X的作用是_______ 。
④氯气与单质碘反应温度稍低于70℃,则装置D适宜的加热方式为_______ 。
(1)从干海带中提取粗碘
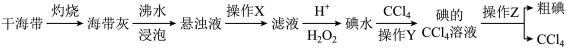
①写出加入过氧化氢后的反应的离子方程式
②操作Y用到的玻璃仪器有烧杯、
③可以用反萃取法将碘单质从碘的四氯化碳溶液中提取出来,写出向碘的四氯化碳溶液中加入浓氢氧化钠溶液振荡、静置、分液发生的化学方程式
(2)利用制得的碘单质制取ICl3

①制备氯气选用的药品为高锰酸钾和浓盐酸,相关反应的离子方程式为
②装置B的作用
③试剂X为
④氯气与单质碘反应温度稍低于70℃,则装置D适宜的加热方式为
更新时间:2021-04-27 10:26:29
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】实验室里用如图所示仪器和药品来制取纯净的无水氯化铜(Cu+Cl2 CuCl2)。图中A、B、C、D、E、F表示玻璃管接口,接口的弯曲和伸长等部分未画出。根据要求填写下列各小题空白。
CuCl2)。图中A、B、C、D、E、F表示玻璃管接口,接口的弯曲和伸长等部分未画出。根据要求填写下列各小题空白。
(1)如果所制气体从左向右流向时,上述各仪器装置的正确连接顺序是(填各装置的序号)
③接_____ 接_______ 接_______ 接______ 接______ ,其中②与④装置相连时,玻璃管接口(用装置中字母表示)应是________ 接________ 。
(2)装置②的作用是_______________________________________________________ ;
装置④的作用是__________________________________________________________ 。
(3)实验开始时,应首先检验装置的________ ,实验结束时,应先熄灭________ 处(填装置序号) 的酒精灯。
(4)在装置⑥的广口瓶中,发生反应的化学方程式为________________________________
 CuCl2)。图中A、B、C、D、E、F表示玻璃管接口,接口的弯曲和伸长等部分未画出。根据要求填写下列各小题空白。
CuCl2)。图中A、B、C、D、E、F表示玻璃管接口,接口的弯曲和伸长等部分未画出。根据要求填写下列各小题空白。 | 序号 | ① | ② | ③ | ④ | ⑤ | ⑥ |
| 仪器及 装置图 | 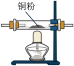 | 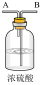 |  | 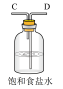 | 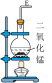 | 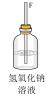 |
③接
(2)装置②的作用是
装置④的作用是
(3)实验开始时,应首先检验装置的
(4)在装置⑥的广口瓶中,发生反应的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】为了探究Cl2、SO2同时通入H2O中发生的反应,某校化学兴趣小组同学设计了如图所示的实验装置。

(1)该化学兴趣小组的同学为制取Cl2、SO2气体,现采用Na2SO3与70%的硫酸为原料制取SO2,采用MnO2和浓盐酸(12mol•L-1)为原料制取Cl2。在此实验中,F仪器的作用是____ ;发生装置B应选择以下三种装置中的____ (填序号)。

(2)D装置中发生主要反应的离子方程式_____ 。怎样证明发生该反应_____ 。
(3)为验证通入D装置中的气体是Cl2过量还是SO2过量,兴趣小组的同学准备了以下试剂:
①氯化铁溶液 ②氯化亚铁溶液 ③硫氰化钾溶液 ④酸性高锰酸钾溶液
若Cl2过量,取适量D中溶液滴加至盛有____ (填一个序号,下同)试剂的试管内,再加入____ 试剂。发生的现象是_____ 。若SO2过量,取适量D中溶液滴加至盛有_____ 试剂的试管内,发生的现象是_____ 。

(1)该化学兴趣小组的同学为制取Cl2、SO2气体,现采用Na2SO3与70%的硫酸为原料制取SO2,采用MnO2和浓盐酸(12mol•L-1)为原料制取Cl2。在此实验中,F仪器的作用是

(2)D装置中发生主要反应的离子方程式
(3)为验证通入D装置中的气体是Cl2过量还是SO2过量,兴趣小组的同学准备了以下试剂:
①氯化铁溶液 ②氯化亚铁溶液 ③硫氰化钾溶液 ④酸性高锰酸钾溶液
若Cl2过量,取适量D中溶液滴加至盛有
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】氯气是氯碱工业的主要产品之一,常作强氧化剂,可与有机物和无机物进行反应生成多种氯化物。某兴趣小组在实验室中对以下反应进行了探究。回答下列问题:
Ⅰ、三氯化硼(BCl3)的制备,
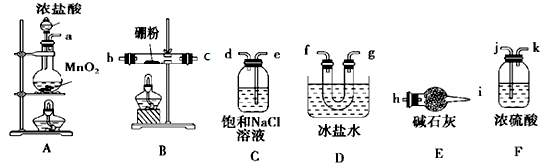
查阅资料:已知:①BCl3的沸点为12.5 ℃,熔点为-107.3 ℃; ②2B+6HCl 2BCl3↑+3H2↑;
2BCl3↑+3H2↑;
③BCl3遇水观察到大量的白雾。
(1)检验发生装置A的气密性的实验具体方法是_____________________________________
(2)按气流方向连接各装置的接口,顺序为_______
a→( )→( )→( )→( )→( )→( )→ ( ) → ( ) →h。
(3)装置D的作用是________________ ;装置E的作用是___________________________ ,实验中若不用装置C,可能产生的后果是____________ 。
(4)BCl3遇水反应的化学方程式为:_____________________________ 。
Ⅱ、SO2与漂粉精溶液的反应
(5)pH试纸颜色的变化说明漂粉精溶液具有的性质是_____________________________ 。
(6)现象2中溶液变为黄绿色的原因是:随溶液酸性的增强,漂粉精的有效成分和Cl- 发生反应。该反应的离子方程式为________________________ 。
(7)用离子方程式解释现象3中黄绿色褪去的原因_______________________ 。
Ⅰ、三氯化硼(BCl3)的制备,

查阅资料:已知:①BCl3的沸点为12.5 ℃,熔点为-107.3 ℃; ②2B+6HCl
 2BCl3↑+3H2↑;
2BCl3↑+3H2↑;③BCl3遇水观察到大量的白雾。
(1)检验发生装置A的气密性的实验具体方法是
(2)按气流方向连接各装置的接口,顺序为
a→( )→( )→( )→( )→( )→( )→ ( ) → ( ) →h。
(3)装置D的作用是
(4)BCl3遇水反应的化学方程式为:
Ⅱ、SO2与漂粉精溶液的反应
| 操作 | 现象 |
| 取4g 漂粉精固体,加入100mL 水,测漂粉精溶液的pH | pH 试纸先变蓝(约为12),后褪色 |
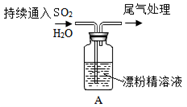 | 1.液面上方出现白雾; 2.稍后,出现浑浊,溶液变为黄绿色; 3.稍后,产生大量白色沉淀,黄绿色褪去 |
(6)现象2中溶液变为黄绿色的原因是:随溶液酸性的增强,漂粉精的有效成分和Cl- 发生反应。该反应的离子方程式为
(7)用离子方程式解释现象3中黄绿色褪去的原因
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】氮、硫的化合物与人类生活和生产有着密切的联系。
Ⅰ.氨既是一种重要的化工产品,又是一种重要的化工原料。图1为合成氨以及氨氧化制硝酸的流程示意图。

(1)合成塔中发生反应的化学方程式为_____ 氧化炉中发生反应的化学方程式为_____ 。
(2)A为_____ ;向吸收塔中通入A的作用_____ 。
(3)工业生产中为了盛装大量浓硝酸,可选择_____ (填字母)作为罐体材料。
a.铜 b.铂 c.铝 d.镁
Ⅱ.浓硫酸与木炭在加热条件下可发生化学反应,为检验反应的产物,某同学设计了如图2所示的实验。请据此回答下列问题:
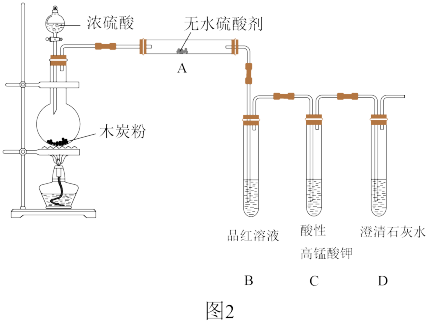
(4)浓硫酸与木炭反应的化学方程式:_____ 。
(5)装置B中的现象_____ ;证明产物中有_____ 。
(6)装置C的作用是_____ 。
Ⅰ.氨既是一种重要的化工产品,又是一种重要的化工原料。图1为合成氨以及氨氧化制硝酸的流程示意图。

(1)合成塔中发生反应的化学方程式为
(2)A为
(3)工业生产中为了盛装大量浓硝酸,可选择
a.铜 b.铂 c.铝 d.镁
Ⅱ.浓硫酸与木炭在加热条件下可发生化学反应,为检验反应的产物,某同学设计了如图2所示的实验。请据此回答下列问题:

(4)浓硫酸与木炭反应的化学方程式:
(5)装置B中的现象
(6)装置C的作用是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】硫酸亚铁可用于治疗缺铁性贫血。利用黄铜矿(CuFeS2)制备硫酸亚铁并回收铜的工艺流程如图所示:
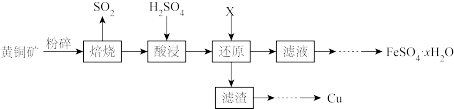
(1)①焙烧生成的SO2可用柠檬酸-柠檬酸钠溶液进行吸收,该过程采用逆流接触法进行吸收的原因是_______ 。
②还可用电化学氧化法处理SO2,同时生成H2SO4,写出SO2参与反应的电极反应式:_______ 。
(2)还原过程中加入的X为_____ (填化学式),该过程发生反应的离子方程式是_______ 。
(3)滤渣的主要成分是_______ (填化学式)。
(4)①向滤液中加入稀硫酸后经蒸发浓缩、冷却结晶、过滤可得绿矾晶体,加入稀硫酸的目的是_______ 。
②为测定产品FeSO4·xH2O中结晶水的数量,称取14g产品配制成250mL待测液,准确量取25.00mL待测液于锥形瓶中加稀硫酸酸化,用0.0500mol·L-1KMnO4标准溶液滴定至终点,重复三次,平均消耗KMnO4溶液的体积为20.00mL,则x=_______ 。

(1)①焙烧生成的SO2可用柠檬酸-柠檬酸钠溶液进行吸收,该过程采用逆流接触法进行吸收的原因是
②还可用电化学氧化法处理SO2,同时生成H2SO4,写出SO2参与反应的电极反应式:
(2)还原过程中加入的X为
(3)滤渣的主要成分是
(4)①向滤液中加入稀硫酸后经蒸发浓缩、冷却结晶、过滤可得绿矾晶体,加入稀硫酸的目的是
②为测定产品FeSO4·xH2O中结晶水的数量,称取14g产品配制成250mL待测液,准确量取25.00mL待测液于锥形瓶中加稀硫酸酸化,用0.0500mol·L-1KMnO4标准溶液滴定至终点,重复三次,平均消耗KMnO4溶液的体积为20.00mL,则x=
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】下图中,B、D、E、F、G是氧化物且B为红棕色固体,F、K是氢化物且F为常温常压下常见无色液体,C、H是日常生活中最常见的金属单质,J是黄绿色气体。O是白色沉淀且B、H、L、M、N、O中含有同种元素,I是基础化学工业的重要产品(图中部分反应物和生成物没有列出)。
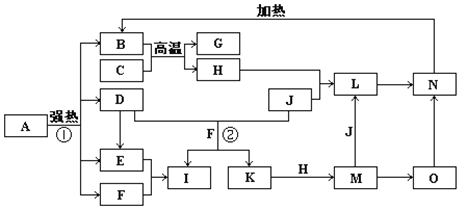
请按要求回答:
(1)写出G、L的化学式G:_____________________ ,L:______________________
(2)反应②的离子方程式________________________________________________ 。
(3)写出反应M→L的离子方程式为________________________________________ 。
(4)若将O敞口久置,变质过程中的现象为___________________________________
发生的化学方程式为__________________________________________________ 。

请按要求回答:
(1)写出G、L的化学式G:
(2)反应②的离子方程式
(3)写出反应M→L的离子方程式为
(4)若将O敞口久置,变质过程中的现象为
发生的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】某同学采用硫铁矿焙烧取硫后的烧渣(主要成分为Fe2O3、SiO2、Al2O3,不考虑其他杂质)制取七水合硫酸亚铁(FeSO4·7H2O)晶体,设计了如下流程:
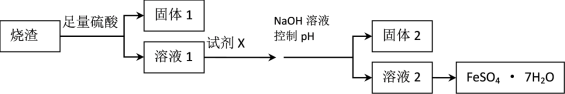
已知:(1)常温下,金属离子开始沉淀和沉淀完全时的pH 见下表。
(2)七水合硫酸亚铁(FeSO4·7H2O)的溶解度
(1)溶解烧渣选用足量硫酸,写出Fe2O3与硫酸反应的离子方程式_______________ ;检验溶液1中含有Fe3+的实验方法是___________________ ;
(2)固体1是制作单晶硅的主要原料,写出该反应的化学方程式___________________ ;
(3)试剂X是__________________ ;固体2是___________________ ;
(4)加入NaOH溶液控制pH应不超过_________________ ;
(5)从溶液2中获得晶体的的方法为______________ , _____________ 过滤、洗涤、干燥。
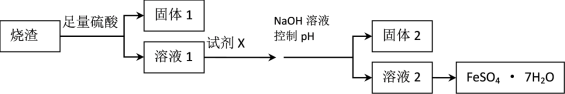
已知:(1)常温下,金属离子开始沉淀和沉淀完全时的pH 见下表。
| 开始形成氢氧化物沉淀的pH | 完全形成氢氧化物沉淀的pH | |
| Fe2+ | 7.0 | 9.0 |
| Fe3+ | 1.9 | 3.2 |
| Al3+ | 3.3 | 5.0 |
| 温度/℃ | 10 | 20 | 30 | 40 | 50 |
| FeSO4·7H2O溶解度(g) | 15.5 | 26.5 | 32.9 | 40.2 | 48.9 |
(2)固体1是制作单晶硅的主要原料,写出该反应的化学方程式
(3)试剂X是
(4)加入NaOH溶液控制pH应不超过
(5)从溶液2中获得晶体的的方法为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】葡萄是一种常见水果,可以生食或制作葡萄干,除此之外,葡萄还可用于酿酒。
(1)检验葡萄汁含有葡萄糖的方法是:向其中加碱调至碱性,再加入新制的Cu(OH)2并加热,其现象是________ 。
(2)葡萄在酿酒过程中,葡萄糖转化为酒精的过程如下,补充完成下列化学方程式:C6H12O6(葡萄糖)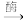 2
2_________ + 2 C2H5OH
(3)葡萄酒密封储存过程中会生成有香味的酯类,酯类也可以通过化学实验来制备,实验室可用如图所示装置制备乙酸乙酯:
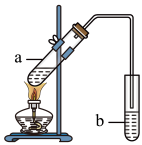
①试管a中生成乙酸乙酯的化学方程式是__________ 。
②试管b中盛放的试剂是饱和____________ 溶液。
③实验开始时,试管b中的导管不伸入液面下的原因是________ 。
④若要分离出试管b中的乙酸乙酯,需要用到的仪器是_______ (填字母)。
A.普通漏斗 B.分液漏斗 C.长颈漏斗
(1)检验葡萄汁含有葡萄糖的方法是:向其中加碱调至碱性,再加入新制的Cu(OH)2并加热,其现象是
(2)葡萄在酿酒过程中,葡萄糖转化为酒精的过程如下,补充完成下列化学方程式:C6H12O6(葡萄糖)
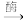 2
2(3)葡萄酒密封储存过程中会生成有香味的酯类,酯类也可以通过化学实验来制备,实验室可用如图所示装置制备乙酸乙酯:

①试管a中生成乙酸乙酯的化学方程式是
②试管b中盛放的试剂是饱和
③实验开始时,试管b中的导管不伸入液面下的原因是
④若要分离出试管b中的乙酸乙酯,需要用到的仪器是
A.普通漏斗 B.分液漏斗 C.长颈漏斗
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】 是重要的化工产品,某小组设计如下实验装置制备氯化铁并探究其性质。
是重要的化工产品,某小组设计如下实验装置制备氯化铁并探究其性质。
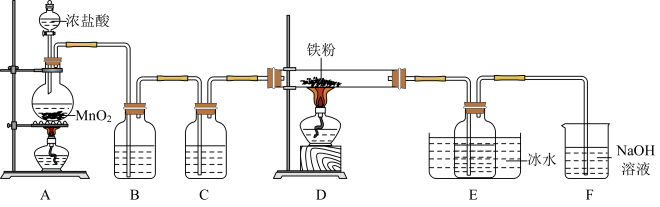
已知: 易升华、遇水蒸气易潮解。回答下列问题:
易升华、遇水蒸气易潮解。回答下列问题:
(1)盛装浓盐酸的仪器是_______ (填名称),B装置中试剂是_______ ,C装置的作用是_______ 。
(2)A装置中发生反应的离子方程式为_______ 。
(3)E装置中冰水浴的作用是_______ 。
(4)上述实验装置存在两处缺陷:一是制备产品的导气管太细,易堵塞;二是_______ 。
(5)经改进,继续完成实验。实验完毕后,取产品探究其性质:
根据上述实验现象,_______ (填“能”或“不能”)确定产品中是否含有铁单质,理由是_______ (用离子方程式表示)。
 是重要的化工产品,某小组设计如下实验装置制备氯化铁并探究其性质。
是重要的化工产品,某小组设计如下实验装置制备氯化铁并探究其性质。
已知:
 易升华、遇水蒸气易潮解。回答下列问题:
易升华、遇水蒸气易潮解。回答下列问题:(1)盛装浓盐酸的仪器是
(2)A装置中发生反应的离子方程式为
(3)E装置中冰水浴的作用是
(4)上述实验装置存在两处缺陷:一是制备产品的导气管太细,易堵塞;二是
(5)经改进,继续完成实验。实验完毕后,取产品探究其性质:
| 实验 | 操作 | 现象 |
| ① | 取少量固体溶于蒸馏水,滴加KSCN溶液 | 溶液变红色 |
| ② | 取少量固体溶于稀硫酸 | 固体溶解,无气泡产生 |
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】海洋资源的利用具有广阔前景。
I.海洋植物如海带、海藻中含有丰富的碘元素,碘元素以碘离子的形式存在。实验室从海带中提取碘的流程如下:

(1)步骤①灼烧海带时,盛放海带的仪器名称是_______ 。
(2)步骤④中反应的离子方程式为_______ 。
(3)步骤⑤的操作为:向含I2的水溶液加入有机试剂,用力震荡后静置分层后分液,则可以选择的有机试剂是_______(填标号)。
II.为除去粗盐中含有的可溶性杂质硫酸钠、氯化钙和氯化镁,某同学利用给定试剂NaOH溶液、BaCl2溶液、 溶液和盐酸,设计了如图实验流程:
溶液和盐酸,设计了如图实验流程:
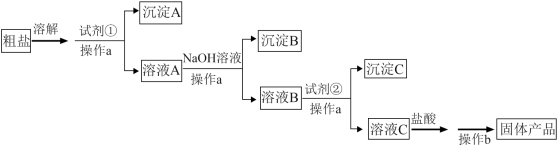
(4)操作a和操作b的名称依次是_______ 、_______ 试剂①是_______ 。
(5)加入试剂②后,发生反应的离子方程式是_______ 。
(6)加入盐酸的作用是_______ 。你设计的流程和该同学的一样吗?简述不同之处_______ (若一样则此空不填)。
I.海洋植物如海带、海藻中含有丰富的碘元素,碘元素以碘离子的形式存在。实验室从海带中提取碘的流程如下:

(1)步骤①灼烧海带时,盛放海带的仪器名称是
(2)步骤④中反应的离子方程式为
(3)步骤⑤的操作为:向含I2的水溶液加入有机试剂,用力震荡后静置分层后分液,则可以选择的有机试剂是_______(填标号)。
| A.四氯化碳 | B.酒精 | C.苯 | D.醋酸 |
II.为除去粗盐中含有的可溶性杂质硫酸钠、氯化钙和氯化镁,某同学利用给定试剂NaOH溶液、BaCl2溶液、
 溶液和盐酸,设计了如图实验流程:
溶液和盐酸,设计了如图实验流程:
(4)操作a和操作b的名称依次是
(5)加入试剂②后,发生反应的离子方程式是
(6)加入盐酸的作用是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】海藻中含有丰富的碘元素,海藻灼烧后碘元素通常以I-的形式存在。实验室从海藻灰中提取I2的流程如图所示:
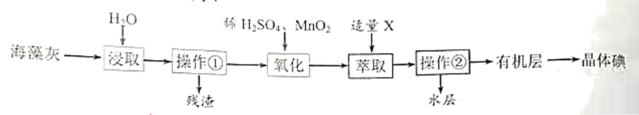
(1)操作①为___________ ,操作②为___________ 。
(2)氧化时发生反应的离子方程式为___________ 。
(3)试剂X可以选择___________ (选填字母)
A.酒精 B.四氯化碳 C.盐酸 D.苯
(4)实验室进行操作②需要的玻璃仪器有烧杯、玻璃棒和___________ 。

(1)操作①为
(2)氧化时发生反应的离子方程式为
(3)试剂X可以选择
A.酒精 B.四氯化碳 C.盐酸 D.苯
(4)实验室进行操作②需要的玻璃仪器有烧杯、玻璃棒和
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】球上99%的溴存在于海水中,故溴也被称为海洋元素,溴主要用于制造汽油抗爆剂、药品、试剂和农药等。以海水提盐后得到的苦卤为原料,提取溴的流程如图所示。
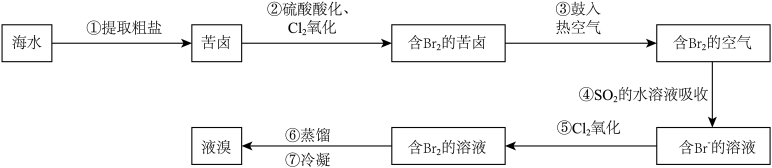
已知:Br2+SO2+2H2O= H2SO4+2HBr。
(1)苦卤可用作提取溴的原料的原因是:_______ 。
(2)写出步骤②中通入Cl2反应的离子方程式:_______ 。
(3)步骤③用热空气将溴吹出制成粗溴,是因为_______(填编号)。
(4)步骤④将Br2转化为Br-,是利用了SO2的_______ 性。
(5)设计一个简单实验,说明溴的活动性大于碘单质:_______ 。

已知:Br2+SO2+2H2O= H2SO4+2HBr。
(1)苦卤可用作提取溴的原料的原因是:
(2)写出步骤②中通入Cl2反应的离子方程式:
(3)步骤③用热空气将溴吹出制成粗溴,是因为_______(填编号)。
| A.Br2的化学性质稳定 | B.Br2沸点低,易挥发 |
| C.Br2易升华 | D.Br2不溶于水 |
(5)设计一个简单实验,说明溴的活动性大于碘单质:
您最近一年使用:0次



