名校
1 . 下列有关实验操作、现象和目的或结论的说法正确的是
选项 | 操作 | 目的或结论 |
A | 将Fe(NO3)2晶体溶于稀硫酸后,滴加KSCN溶液,观察溶液是否变红 | 检验Fe(NO3)2样品是否已被氧化而变质 |
B | 海带提碘实验中,为了制取海带灰的浸取液,需要煮沸海带灰和水的混合物1~2min | 主要目的是去除溶液中的氧气,避免氧气氧化碘离子 |
C | 在试管中依次加入2mL浓硫酸、3mL乙醇和2mL乙酸,用酒精灯缓慢加热 | 制备乙酸乙酯 |
D | 向盛有少量Mg(OH)2固体的试管中加入适量NH4Cl浓溶液,充分振荡,白色固体溶解 | NH4+与Mg(OH)2溶解出的OH-结合,导致Mg(OH)2溶解 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2017-03-15更新
|
886次组卷
|
2卷引用:2017届四川省成都市第七中学高三二诊模拟考试理综化学试卷
名校
2 . 下列各实验中所选用的实验仪器(规格、数量不限,加持装置略去),能完成相应实验的是
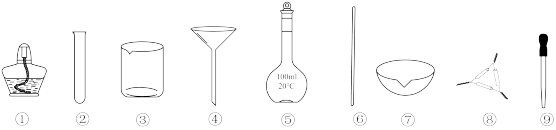

| A.用稀硫酸除去硫酸钡中的少量碳酸钡,只选用③和⑥ |
B.制备 并用于与葡萄糖反应得到银镜,只选用①、②、③和⑨ 并用于与葡萄糖反应得到银镜,只选用①、②、③和⑨ |
| C.将海带灼烧灰化,只选用①、⑦和⑧ |
D.用 的浓硫酸配制 的浓硫酸配制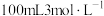 的稀硫酸,只选用③、⑤、⑥和⑨ 的稀硫酸,只选用③、⑤、⑥和⑨ |
您最近一年使用:0次
2021-12-25更新
|
195次组卷
|
3卷引用:山东省菏泽市东明县第一中学2021~2022学年高三上学期期中考试化学试题
山东省菏泽市东明县第一中学2021~2022学年高三上学期期中考试化学试题重庆市缙云教育联盟2021-2022学年高二12月月考化学试题(已下线)3.3 醛 酮-2021-2022学年高二化学课后培优练(人教版2019选择性必修3)
11-12高三上·浙江绍兴·阶段练习
3 . 下列结论均出自《实验化学》中的实验,其中不正确的是
| A.硫酸铜溶液中加入过量浓氨水,可得到深蓝色透明溶液 |
| B.当锌完全溶解后,铁与酸反应产生氢气的速率会显著减慢,此现象可作为判断镀锌铁皮中锌镀层是否完全被反应掉的依据 |
| C.提取海带中碘元素时为保证I-完全氧化为I2,加入的氧化剂(H2O2或新制氯水)均应过量 |
| D.制备硫酸亚铁铵晶体时,最后在蒸发皿中蒸发浓缩溶液时,只需小火加热至溶液表面出现晶膜为止,不能将溶液全部蒸干 |
您最近一年使用:0次
4 . 实验室模拟工业制法从卤水中的碘(主要以I-形式存在)提取碘产品的工艺流程如下:
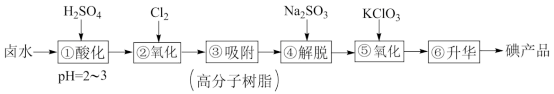
回答下列问题:
(1)实验室中常用二氧化锰跟浓盐酸反应制备干燥纯净的氯气,所用装置如图所示:
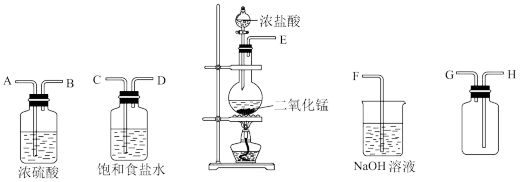
①写出气体发生装置制取氯气的化学方程式___________ 。
②连接上述仪器的正确顺序(填各接口处的字母)是:___________ 。
___________接___________;___________接___________;___________接___________;___________接___________。
③装置中,饱和食盐水的作用是___________ 。
(2)设计步骤③和④的目的是___________ 。
(3)步骤④解脱反应的离子方程式为___________ 。
(4)若②和⑤中分别得到等量I2,则消耗的m(Cl2):m(KClO3)=___________ 。

回答下列问题:
(1)实验室中常用二氧化锰跟浓盐酸反应制备干燥纯净的氯气,所用装置如图所示:

①写出气体发生装置制取氯气的化学方程式
②连接上述仪器的正确顺序(填各接口处的字母)是:
___________接___________;___________接___________;___________接___________;___________接___________。
③装置中,饱和食盐水的作用是
(2)设计步骤③和④的目的是
(3)步骤④解脱反应的离子方程式为
(4)若②和⑤中分别得到等量I2,则消耗的m(Cl2):m(KClO3)=
您最近一年使用:0次
5 . 围绕海水的综合利用,化学课外兴趣小组进行下列实验:
(1)模拟工业制备氯气
装置如图所示,接通电源,当观察到石墨电极与滤纸接触的区域有细小的气泡产生时,停止通电。将pH试纸分别放在a、b处滤纸上,观察颜色变化。
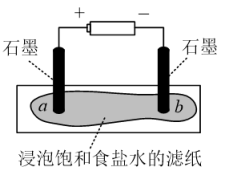
①在上述实验中观察a处pH试纸中心呈白色,边缘有一圈淡淡的红色,b处pH试纸呈___________ 色。
②实验结束后,将滤纸对折,使a、b处充分接触,可将a处残余的Cl2进一步处理。此时发生反应的化学反应方程式是___________ 。
(2)模拟反萃取法提取碘实验流程如下图:
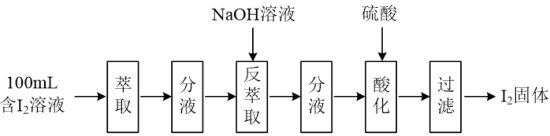
①“萃取”操作时须使用的玻璃仪器有烧杯、玻璃棒和___________ 。
②“反萃取”操作时溶液中有I-、IO 生成。“酸化”步骤发生反应的离子反应方程式为
生成。“酸化”步骤发生反应的离子反应方程式为___________ 。
(3)模拟浓海水提取镁实验流程如下图:
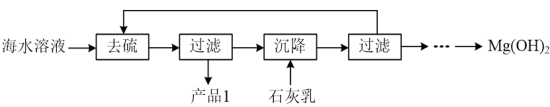
说明:模拟浓海水成分配制的“海水溶液”主要成分如下:
①产品1的化学式为___________ 。
②沉降阶段主要的化学反应方程式为___________ 。
(1)模拟工业制备氯气
装置如图所示,接通电源,当观察到石墨电极与滤纸接触的区域有细小的气泡产生时,停止通电。将pH试纸分别放在a、b处滤纸上,观察颜色变化。

①在上述实验中观察a处pH试纸中心呈白色,边缘有一圈淡淡的红色,b处pH试纸呈
②实验结束后,将滤纸对折,使a、b处充分接触,可将a处残余的Cl2进一步处理。此时发生反应的化学反应方程式是
(2)模拟反萃取法提取碘实验流程如下图:

①“萃取”操作时须使用的玻璃仪器有烧杯、玻璃棒和
②“反萃取”操作时溶液中有I-、IO
 生成。“酸化”步骤发生反应的离子反应方程式为
生成。“酸化”步骤发生反应的离子反应方程式为(3)模拟浓海水提取镁实验流程如下图:

说明:模拟浓海水成分配制的“海水溶液”主要成分如下:
| 离子 | Na+ | Mg2+ | Cl- | SO |
| 浓度/(g·L-1) | 63.7 | 28.8 | 144.6 | 46.4 |
②沉降阶段主要的化学反应方程式为
您最近一年使用:0次
名校
解题方法
6 . 海带中含有丰富的碘元素(以I-形式存在)。实验中提取碘的流程如图:_______ 。
②写出I-的电子式:_______ 。
③写出步骤②发生的离子方程式_______ 。
(2)①实验①的操作名称_______ 。
②实验③所需要的主要玻璃仪器为_______ 、烧杯。
(3)①实验操作③中,_______ (填“能”或“不能”)用酒精来提取碘。
②实验操作③中,若用苯来提取碘,加入少量苯,充分振荡静置后的现象是_______ 。
A.溶液分层,下层红棕色 B.溶液分层,上层红棕色
C.溶液分层,下层紫红色 D.溶液分层,上层紫红色
(4)检验某无色溶液中是否含有I-,所用试剂不合理的是_______ 。
A.淀粉溶液和氯水 B.稀硝酸和硝酸银溶液
C.氯水和四氯化碳 D.KBr和稀HCl
(5)下列有关从海带中提取碘的实验原理和装置能达到实验目的是( )
B.用装置乙过滤海带灰的浸泡液
C.用装置丙制备用于氧化浸泡液中的氯气
D.用装置丁吸收氧化浸泡液中后的尾气
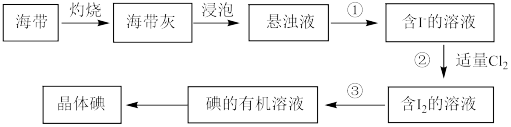
②写出I-的电子式:
③写出步骤②发生的离子方程式
(2)①实验①的操作名称
②实验③所需要的主要玻璃仪器为
(3)①实验操作③中,
②实验操作③中,若用苯来提取碘,加入少量苯,充分振荡静置后的现象是
A.溶液分层,下层红棕色 B.溶液分层,上层红棕色
C.溶液分层,下层紫红色 D.溶液分层,上层紫红色
(4)检验某无色溶液中是否含有I-,所用试剂不合理的是
A.淀粉溶液和氯水 B.稀硝酸和硝酸银溶液
C.氯水和四氯化碳 D.KBr和稀HCl
(5)下列有关从海带中提取碘的实验原理和装置能达到实验目的是
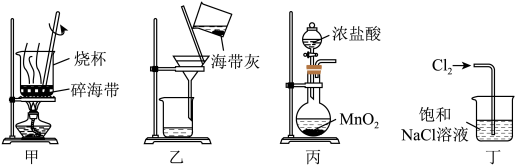
B.用装置乙过滤海带灰的浸泡液
C.用装置丙制备用于氧化浸泡液中的氯气
D.用装置丁吸收氧化浸泡液中后的尾气
您最近一年使用:0次
2020-12-09更新
|
264次组卷
|
2卷引用:上海市向明中学2020-2021学年高一上学期期中考试化学试题
名校
解题方法
7 . 三氯化碘(ICl3)是一种黄色晶体,遇水易分解,熔点:33℃,沸点:73℃,在药物合成中用途非常广泛。某学习小组从海带中提取碘,并用于制备三氯化碘。
(1)从干海带中提取粗碘
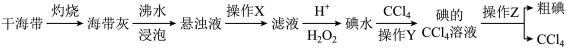
①写出加入过氧化氢后的反应的离子方程式_______ 。
②操作Y用到的玻璃仪器有烧杯、_______ 。
③可以用反萃取法将碘单质从碘的四氯化碳溶液中提取出来,写出向碘的四氯化碳溶液中加入浓氢氧化钠溶液振荡、静置、分液发生的化学方程式_______ 。
(2)利用制得的碘单质制取ICl3
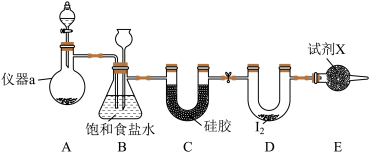
①制备氯气选用的药品为高锰酸钾和浓盐酸,相关反应的离子方程式为_______ 。
②装置B的作用_______ 。
③试剂X为_______ ,X的作用是_______ 。
④氯气与单质碘反应温度稍低于70℃,则装置D适宜的加热方式为_______ 。
(1)从干海带中提取粗碘
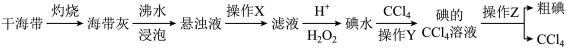
①写出加入过氧化氢后的反应的离子方程式
②操作Y用到的玻璃仪器有烧杯、
③可以用反萃取法将碘单质从碘的四氯化碳溶液中提取出来,写出向碘的四氯化碳溶液中加入浓氢氧化钠溶液振荡、静置、分液发生的化学方程式
(2)利用制得的碘单质制取ICl3

①制备氯气选用的药品为高锰酸钾和浓盐酸,相关反应的离子方程式为
②装置B的作用
③试剂X为
④氯气与单质碘反应温度稍低于70℃,则装置D适宜的加热方式为
您最近一年使用:0次
8 . 海带中含有丰富的碘元素(以I-形式存在)。工业中提取碘的流程如图:
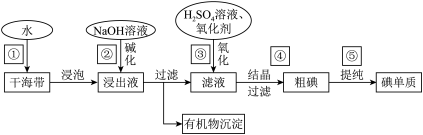
(1)写出步骤③中加硫酸溶液的目的_______ 。
(2)步骤⑤中所涉及的实验操作名称_______ 。
(3)若在实验室中,用分液漏斗、苯(密度比水小,且不溶于水)来提取碘水中的I2,加入少量苯,充分振荡静置后的现象是_______ 。
(4)检验某无色溶液中是否含有I-,所用试剂不合理的是_______ 。
A.淀粉溶液和氯水 B. KBr和稀HCl
C.氯水和四氯化碳 D. KIO3和醋酸
(5)图中有关从海带中提取碘的实验原理和装置能达到实验目的是_____

A.用装置甲灼烧碎海带
B.用装置乙过滤海带灰的浸泡液
C.用装置丙制备用于氧化浸泡液中的氯气
D.用装置丁吸收氧化浸泡液后的尾气

(1)写出步骤③中加硫酸溶液的目的
(2)步骤⑤中所涉及的实验操作名称
(3)若在实验室中,用分液漏斗、苯(密度比水小,且不溶于水)来提取碘水中的I2,加入少量苯,充分振荡静置后的现象是
(4)检验某无色溶液中是否含有I-,所用试剂不合理的是
A.淀粉溶液和氯水 B. KBr和稀HCl
C.氯水和四氯化碳 D. KIO3和醋酸
(5)图中有关从海带中提取碘的实验原理和装置能达到实验目的是

A.用装置甲灼烧碎海带
B.用装置乙过滤海带灰的浸泡液
C.用装置丙制备用于氧化浸泡液中的氯气
D.用装置丁吸收氧化浸泡液后的尾气
您最近一年使用:0次
名校
9 . “海带提碘”中,下列关于装置和操作的说法正确的是
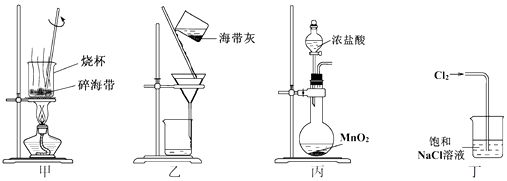

| A.用装置甲灼烧碎海带 |
| B.用装置乙过滤海带灰的浸泡液 |
| C.用装置丙制备Cl2,用于氧化浸泡液中I- |
| D.用装置丁吸收尾气中的Cl2 |
您最近一年使用:0次
2020-12-08更新
|
502次组卷
|
3卷引用:华南师范大学附属中学2021届高三综合测试二化学试题
名校
解题方法
10 . 某化学实验兴趣小组的同学从海带中提取碘单质的实验流程图如图:

(1)完成步骤①需要装置______ 。(I 或 II)
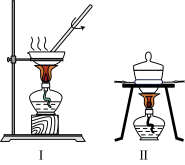
(2)步骤③的实验操作______ 。
(3)步骤④中涉及的离子反应为______ 。
(4)海带灰中的硫酸盐、碳酸盐在步骤______ (①~⑤)中实现与 I2分离。
(5)已知在含少量 I-的溶液中,H2O2会较快分解,反应能量变化如图:

① H2O2分解过程中,I-的作用是______ 。
②加入 I-可以看到双氧水分解过程中有两个反应历程,其中第1个反应历程是______ (填“吸热”或“放热”)反应。
③有、无 I-______ (填“能”或“不能”)改变了总反应的能量变化。
(6)通过查阅资料,发现一种新型氧化剂氧化碘离子的方法如下。
I.制备新型氧化剂:利用亚硝酸钠(NaNO2)与H2O2作为混合试剂与 I-反应,制备新型氧化剂 HIO3。
II.制取 I2:在酸性条件下,氧化剂HIO3与滤液中的 I-反应生成 I2,该反应离子方程式是5I-+IO3-+6H+=3I2 +3H2O。
①1mol氧化剂 HIO3与 I-完全反应时,转移电子的物质的量是______ mol 。
②请将制备氧化剂HIO3的反应离子方程式补充完整:______ H++4______ +______ H2O2+1I-=1______ +4______ ↑+______
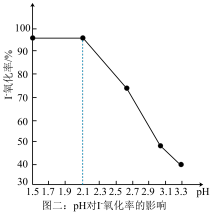
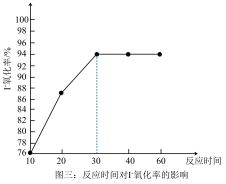
③ 某同学取一定浓度的滤液按照上述资料的方法进行实验,得到如下三组数据图象,根据图象可以得出制取碘的最佳条件______ 。


(1)完成步骤①需要装置

(2)步骤③的实验操作
(3)步骤④中涉及的离子反应为
(4)海带灰中的硫酸盐、碳酸盐在步骤
(5)已知在含少量 I-的溶液中,H2O2会较快分解,反应能量变化如图:

① H2O2分解过程中,I-的作用是
②加入 I-可以看到双氧水分解过程中有两个反应历程,其中第1个反应历程是
③有、无 I-
(6)通过查阅资料,发现一种新型氧化剂氧化碘离子的方法如下。
I.制备新型氧化剂:利用亚硝酸钠(NaNO2)与H2O2作为混合试剂与 I-反应,制备新型氧化剂 HIO3。
II.制取 I2:在酸性条件下,氧化剂HIO3与滤液中的 I-反应生成 I2,该反应离子方程式是5I-+IO3-+6H+=3I2 +3H2O。
①1mol氧化剂 HIO3与 I-完全反应时,转移电子的物质的量是
②请将制备氧化剂HIO3的反应离子方程式补充完整:
③ 某同学取一定浓度的滤液按照上述资料的方法进行实验,得到如下三组数据图象,根据图象可以得出制取碘的最佳条件



您最近一年使用:0次



