解题方法
1 . 溴、碘主要存在于海水中,有“海洋元素”的美称。海水中的碘主要富集在海带中,我国海带产量居世界第一位,除供食用外,大量用于制碘。从海带中提取碘单质,工艺流程如图。
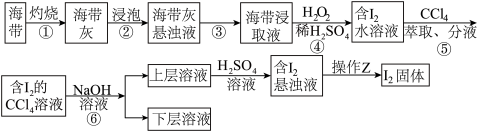
(1)步骤①操作时,除需要酒精灯、三脚架、泥三角外,还需的主要仪器是____ (填名称)。
(2)步骤⑤的具体实验步骤为:
A.把盛有溶液的分液漏斗放在铁架台的铁圈中;
B.检验分液漏斗旋塞和上口的瓶塞是否漏液;
C.把20mL碘水跟5mL四氯化碳加入分液漏斗中,并盖好玻璃塞;
D.倒转漏斗振荡,并不时旋开活塞放气,最后关闭活塞,把分液漏斗放正;
E.旋开活塞,用烧杯接收下层溶液;
F.将分液漏斗上口的玻璃塞打开或使塞上的凹槽对准分液漏斗口上的小孔;
G.从分液漏斗上口倒出上层溶液;
H.静置、分层。
①实验步骤的正确顺序为_____→_____→_____→A→H→_____→_____→_____。____
②静置、分层后的现象为_____ 。
(3)步骤⑤中,某学生选择用CCl4来萃取碘的理由_____ 。
(4)步骤⑥使用的是反萃取法,目的是富集碘元素,该步反应的离子方程式为_____ 。每消耗1molI2转移电子数为_____ 。
(5)某同学制得的粗碘中含有少量Na2SO4,对粗碘进行提纯的装置如图所示,采用的分离方法是_____ ;为得到较多较高纯度的单质碘,A容器中可盛放的试剂为_____ (填字母)。
a.冷水 b.热水 c.热氢氧化钠溶液
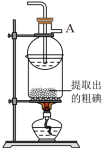

(1)步骤①操作时,除需要酒精灯、三脚架、泥三角外,还需的主要仪器是
(2)步骤⑤的具体实验步骤为:
A.把盛有溶液的分液漏斗放在铁架台的铁圈中;
B.检验分液漏斗旋塞和上口的瓶塞是否漏液;
C.把20mL碘水跟5mL四氯化碳加入分液漏斗中,并盖好玻璃塞;
D.倒转漏斗振荡,并不时旋开活塞放气,最后关闭活塞,把分液漏斗放正;
E.旋开活塞,用烧杯接收下层溶液;
F.将分液漏斗上口的玻璃塞打开或使塞上的凹槽对准分液漏斗口上的小孔;
G.从分液漏斗上口倒出上层溶液;
H.静置、分层。
①实验步骤的正确顺序为_____→_____→_____→A→H→_____→_____→_____。
②静置、分层后的现象为
(3)步骤⑤中,某学生选择用CCl4来萃取碘的理由
(4)步骤⑥使用的是反萃取法,目的是富集碘元素,该步反应的离子方程式为
(5)某同学制得的粗碘中含有少量Na2SO4,对粗碘进行提纯的装置如图所示,采用的分离方法是
a.冷水 b.热水 c.热氢氧化钠溶液

您最近一年使用:0次
名校
解题方法
2 . 海洋资源的利用具有广阔前景。
(1)无需经过化学变化就能从海水中获得的物质是___________ (填序号)。
A.食盐 B.淡水 C.烧碱 D.纯碱 E.溴
(2)大量的镁从海水中提取,一种工业制备无水氯化镁的工艺流程如下:
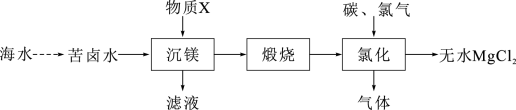
工业上常用“沉镁”物质X的是___________ ,“氯化”过程中的气态副产物常用作还原剂,“氯化”发生的化学方程式是___________ 。
(3)海带中含有碘元素。实验室提取碘的步骤如下所示:

①灼烧海带至灰烬时所用的主要仪器名称是_______ 。海带灰中含有硫酸镁、碳酸钠等,在实验步骤___________ (填序号)中实现与碘分离。
②写出步骤④反应的离子方程式_______ 。反应结束后,再加入CCl4作萃取剂,振荡、静置,可以观察到CCl4层呈___________ 色。
③请设计实验检验用CCl4提取碘后的水溶液中是否还含有碘单质___________ (包括实验步骤、现象及结论)。
(1)无需经过化学变化就能从海水中获得的物质是
A.食盐 B.淡水 C.烧碱 D.纯碱 E.溴
(2)大量的镁从海水中提取,一种工业制备无水氯化镁的工艺流程如下:

工业上常用“沉镁”物质X的是
(3)海带中含有碘元素。实验室提取碘的步骤如下所示:

①灼烧海带至灰烬时所用的主要仪器名称是
②写出步骤④反应的离子方程式
③请设计实验检验用CCl4提取碘后的水溶液中是否还含有碘单质
您最近一年使用:0次
2022-09-21更新
|
348次组卷
|
3卷引用:陕西师范大学附属中学2021-2022学年高一下学期期中考试化学试题
解题方法
3 . 食盐中的加碘剂选用的是碘酸钾( )。实验室可用采用如图实验流程制备碘酸钾。
)。实验室可用采用如图实验流程制备碘酸钾。

(1)操作①的名称为______ 。
(2)操作②包括萃取、______ ,萃取后分液漏斗内的现象______ 。
(3)试剂X是18电子分子,写出溶液M与X反应的离子反应方程式为______ 。
(4)由单质碘制备碘酸钾的化学方程式为______ 。
(5)同学甲认为操作③可以用蒸馏的方法,但同学乙认为不可以,原因是______ ;于是改用下列分离法,具体流程如下:
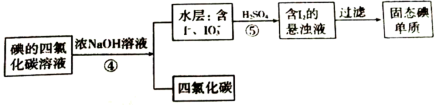
该分离方法叫______ 法,写出反应⑤离子反应方程式______ 。
 )。实验室可用采用如图实验流程制备碘酸钾。
)。实验室可用采用如图实验流程制备碘酸钾。
(1)操作①的名称为
(2)操作②包括萃取、
(3)试剂X是18电子分子,写出溶液M与X反应的离子反应方程式为
(4)由单质碘制备碘酸钾的化学方程式为
(5)同学甲认为操作③可以用蒸馏的方法,但同学乙认为不可以,原因是

该分离方法叫
您最近一年使用:0次
2021-04-10更新
|
212次组卷
|
2卷引用:山东新高考质量测评联盟2020-2021学年高一4月联考化学试题
名校
4 . I.海洋是生命的摇篮,浩瀚的海洋中蕴藏着丰富的资源。人们可以从海水中提取淡水和制得镁、溴等重要的化工产品。
(1)从海水中获得淡水的主要方法有蒸馏法、离子交换法和___________ 。离子交换法净化水的过程如图所示。下列说法正确的是___________ (填序号)。
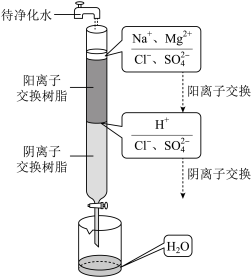
A.经过阳离子交换树脂后,水中阳离子总数
B.通过阴离子交换树脂后,水中只有 被除去
被除去
C.通过净化处理后的水,导电性增强
D.阴离子交换树脂填充段存在反应:
(2)工业上通过 制备Mg,常用的冶炼方法是
制备Mg,常用的冶炼方法是___________ 。制备溴时通入热空气可以吹出溴,是利用了溴的___________ 。
Ⅱ.海带中含有碘元素。从海带中提取碘的实验过程如下图所示:
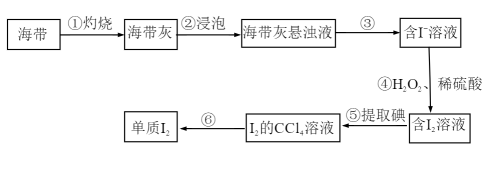
(3)实验步骤①不会用到下列仪器中的___________ (填字母)
a.泥三角 b.250ml容量瓶 c.坩埚 d.漏斗 e.酒精灯
(4)步骤③的操作名称是___________
(5)步骤④中反应的离子方程式为___________
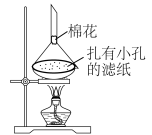
(6)利用如图装置,可以从氯化钠固体中分离出碘单质。简述原理________ ;棉花的作用是________ 。
(1)从海水中获得淡水的主要方法有蒸馏法、离子交换法和

A.经过阳离子交换树脂后,水中阳离子总数
B.通过阴离子交换树脂后,水中只有
 被除去
被除去C.通过净化处理后的水,导电性增强
D.阴离子交换树脂填充段存在反应:

(2)工业上通过
 制备Mg,常用的冶炼方法是
制备Mg,常用的冶炼方法是Ⅱ.海带中含有碘元素。从海带中提取碘的实验过程如下图所示:

(3)实验步骤①不会用到下列仪器中的
a.泥三角 b.250ml容量瓶 c.坩埚 d.漏斗 e.酒精灯
(4)步骤③的操作名称是
(5)步骤④中反应的离子方程式为
(6)利用如图装置,可以从氯化钠固体中分离出碘单质。简述原理

您最近一年使用:0次
名校
解题方法
5 . 海水的综合利用
海水的综合利用主要包括海水直接利用、海水淡化和海水中化学元素的利用三个方面。其中,海水中化学元素的利用是指从海水中提取钠、镁、氯、溴等元素,以及从海洋植物如海带中提取碘等。
(1)海水中含量最多的卤素是___________ 。
A.氟 B.氯 C.溴 D.碘
(2)海洋中蕴藏着巨大的化学资源。下列有关海水综合利用的说法正确的是___________ 。
A.蒸发海水可以得到单质碘
B.蒸馏海水可以得到淡水
C.利用活泼金属钾可置换海水中的镁
D.电解海水可以制得金属钠
(3)下列有关从海水中提取镁的说法错误的是___________ 。
A.贝壳在海水提取镁的生产流程中,主要经历了 的过程
的过程
B.工业生产中利用电解熔融 制备镁
制备镁
C.在从海水中提取镁的工业流程中, 可循环使用,用于制备盐酸,再溶解
可循环使用,用于制备盐酸,再溶解
D.利用 将海水中的
将海水中的 转化为
转化为 沉淀,然后电解
沉淀,然后电解 制备纯镁
制备纯镁
(4)下图是海水提溴的工艺流程,下列说法错误的是___________ 。
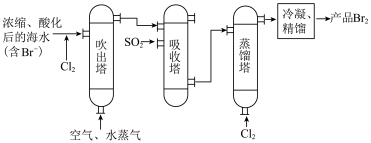
A.在海水中加“酸和氯气”,酸的作用是中和海水中的碱性物质
B .“吹出塔”中热空气的作用是将多余的氯气吹出
C.“吸收塔”中发生的反应为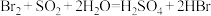
D.以上流程“吹出塔”和“吸收塔”内的反应是为了富集海水中的溴
(5)从海水中提取的粗盐精制后,通过电解饱和食盐水得到一系列化工产品。
①请写出电解饱和食盐水的化学方程式___________ 。
②检验阳极产物时可选用___________ ,向阴极附近溶液滴加紫色石蕊试液呈___________ 色。
③实验测得产生的 体积(标准状况下)为5.60mL,若电解后溶液的体积为50.0mL,则溶液中NaOH的物质的量浓度为
体积(标准状况下)为5.60mL,若电解后溶液的体积为50.0mL,则溶液中NaOH的物质的量浓度为___________  。
。
(6)实验室模拟工业从海藻中提碘的流程如图:
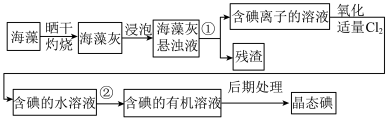
①选择合适实验操作名称填入流程图中:①___________ ,②___________ 。
A.溶解 B.过滤 C.萃取 D.分液
从“含碘的有机溶液”中回收溶剂,并得到碘单质,可选用如图装置完成。
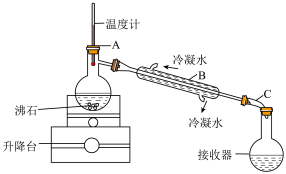
②装置中间部分是“冷凝管”,该装置中有一处明显的错误是___________ 。
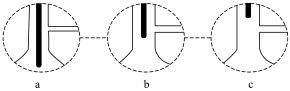
③装置A中,温度计所处的正确位置是___________ 。(选填编号)
海水的综合利用主要包括海水直接利用、海水淡化和海水中化学元素的利用三个方面。其中,海水中化学元素的利用是指从海水中提取钠、镁、氯、溴等元素,以及从海洋植物如海带中提取碘等。
(1)海水中含量最多的卤素是
A.氟 B.氯 C.溴 D.碘
(2)海洋中蕴藏着巨大的化学资源。下列有关海水综合利用的说法正确的是
A.蒸发海水可以得到单质碘
B.蒸馏海水可以得到淡水
C.利用活泼金属钾可置换海水中的镁
D.电解海水可以制得金属钠
(3)下列有关从海水中提取镁的说法错误的是
A.贝壳在海水提取镁的生产流程中,主要经历了
 的过程
的过程B.工业生产中利用电解熔融
 制备镁
制备镁C.在从海水中提取镁的工业流程中,
 可循环使用,用于制备盐酸,再溶解
可循环使用,用于制备盐酸,再溶解
D.利用
 将海水中的
将海水中的 转化为
转化为 沉淀,然后电解
沉淀,然后电解 制备纯镁
制备纯镁(4)下图是海水提溴的工艺流程,下列说法错误的是

A.在海水中加“酸和氯气”,酸的作用是中和海水中的碱性物质
B .“吹出塔”中热空气的作用是将多余的氯气吹出
C.“吸收塔”中发生的反应为
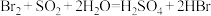
D.以上流程“吹出塔”和“吸收塔”内的反应是为了富集海水中的溴
(5)从海水中提取的粗盐精制后,通过电解饱和食盐水得到一系列化工产品。
①请写出电解饱和食盐水的化学方程式
②检验阳极产物时可选用
③实验测得产生的
 体积(标准状况下)为5.60mL,若电解后溶液的体积为50.0mL,则溶液中NaOH的物质的量浓度为
体积(标准状况下)为5.60mL,若电解后溶液的体积为50.0mL,则溶液中NaOH的物质的量浓度为 。
。(6)实验室模拟工业从海藻中提碘的流程如图:

①选择合适实验操作名称填入流程图中:①
A.溶解 B.过滤 C.萃取 D.分液
从“含碘的有机溶液”中回收溶剂,并得到碘单质,可选用如图装置完成。

②装置中间部分是“冷凝管”,该装置中有一处明显的错误是
③装置A中,温度计所处的正确位置是

您最近一年使用:0次
解题方法
6 .  常用于制药和食品添加剂。以海带为原料提取高纯度碘单质并制备
常用于制药和食品添加剂。以海带为原料提取高纯度碘单质并制备 的一种流程如下:
的一种流程如下:
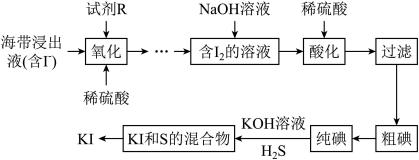
回答下列问题:
(1)“酸化”时稀硫酸的作用是___________ 。
(2)分离 和S的混合物得到
和S的混合物得到 溶液的试剂和方法如下,正确的是
溶液的试剂和方法如下,正确的是___________ (填标号)。
(3)利用下图装置完成 与
与 反应制备
反应制备 。
。

① 溶液的作用是
溶液的作用是___________ (用离子方程式表示)。
②三颈烧瓶中产生 的正确操作顺序为
的正确操作顺序为___________ (填标号)。
a.旋开活塞K,通入 b.加入稀硫酸 c.加入
b.加入稀硫酸 c.加入 溶液
溶液
(4)产品纯度测定。
准确称取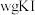 样品溶于水配成
样品溶于水配成 溶液,量取
溶液,量取 溶液于锥形瓶中,加入足量用稀硫酸酸化的
溶液于锥形瓶中,加入足量用稀硫酸酸化的 溶液,摇匀,置于电热板上加热煮沸(常补加热水以保持溶液体积基本不变)。待紫色碘蒸气消失后,再煮沸5分钟,取下放置几分钟,冷却至室温。加入适量的硫酸和磷酸的混合液,用
溶液,摇匀,置于电热板上加热煮沸(常补加热水以保持溶液体积基本不变)。待紫色碘蒸气消失后,再煮沸5分钟,取下放置几分钟,冷却至室温。加入适量的硫酸和磷酸的混合液,用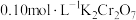 标准溶液反应至完全(还原产物只有
标准溶液反应至完全(还原产物只有 ),消耗标准溶液
),消耗标准溶液 。该
。该 产品的纯度为
产品的纯度为___________ (用含w,V的式子表示)。
 常用于制药和食品添加剂。以海带为原料提取高纯度碘单质并制备
常用于制药和食品添加剂。以海带为原料提取高纯度碘单质并制备 的一种流程如下:
的一种流程如下:
回答下列问题:
(1)“酸化”时稀硫酸的作用是
(2)分离
 和S的混合物得到
和S的混合物得到 溶液的试剂和方法如下,正确的是
溶液的试剂和方法如下,正确的是| 选项 | 试剂 | 方法 |
| a | 二硫化碳 | 分液 |
| b | 酒精 | 分液 |
| c |  溶液 溶液 | 过滤 |
(3)利用下图装置完成
 与
与 反应制备
反应制备 。
。
①
 溶液的作用是
溶液的作用是②三颈烧瓶中产生
 的正确操作顺序为
的正确操作顺序为a.旋开活塞K,通入
 b.加入稀硫酸 c.加入
b.加入稀硫酸 c.加入 溶液
溶液(4)产品纯度测定。
准确称取
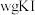 样品溶于水配成
样品溶于水配成 溶液,量取
溶液,量取 溶液于锥形瓶中,加入足量用稀硫酸酸化的
溶液于锥形瓶中,加入足量用稀硫酸酸化的 溶液,摇匀,置于电热板上加热煮沸(常补加热水以保持溶液体积基本不变)。待紫色碘蒸气消失后,再煮沸5分钟,取下放置几分钟,冷却至室温。加入适量的硫酸和磷酸的混合液,用
溶液,摇匀,置于电热板上加热煮沸(常补加热水以保持溶液体积基本不变)。待紫色碘蒸气消失后,再煮沸5分钟,取下放置几分钟,冷却至室温。加入适量的硫酸和磷酸的混合液,用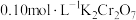 标准溶液反应至完全(还原产物只有
标准溶液反应至完全(还原产物只有 ),消耗标准溶液
),消耗标准溶液 。该
。该 产品的纯度为
产品的纯度为
您最近一年使用:0次
7 . 海洋资源的综合利用是21世纪世界海洋开发利用的重点领域之一。
(1)模拟工业制备氯气
装置如图所示,接通电源,当观察到石墨电极与滤纸接触的区域有细小的气泡产生时,停止通电。将pH试纸分别放在a、b处滤纸上,观察颜色变化。
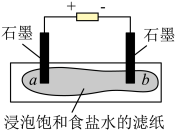
①写出“通电”时发生反应的离子方程式_______ 。
②在上述实验中观察a处pH试纸中心呈白色,边缘有一圈淡淡的红色,b处pH试纸呈_______ 色。
(2)模拟从海水提取食盐后的母液中提取溴的流程如下图:
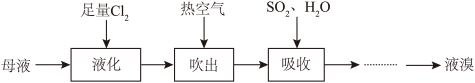
①“吸收”步骤中发生的离子反应方程式为_______ 。
②设计简单的实验验证溴的非金属性比碘强_______ 。(可供选择的试剂:溴水、碘水、NaBr溶液、KI溶液、淀粉溶液)
(3)模拟反萃取法提取碘的实验流程如下图:
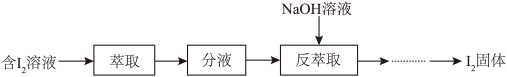
①“萃取”操作中可使用 作为
作为 的萃取剂,其原因除
的萃取剂,其原因除 不与
不与 反应外,还有
反应外,还有_______ 。
②“反萃取”操作时溶液中有 、
、 生成。该步骤发生反应的离子反应方程式:
生成。该步骤发生反应的离子反应方程式:_______ 。
(1)模拟工业制备氯气
装置如图所示,接通电源,当观察到石墨电极与滤纸接触的区域有细小的气泡产生时,停止通电。将pH试纸分别放在a、b处滤纸上,观察颜色变化。

①写出“通电”时发生反应的离子方程式
②在上述实验中观察a处pH试纸中心呈白色,边缘有一圈淡淡的红色,b处pH试纸呈
(2)模拟从海水提取食盐后的母液中提取溴的流程如下图:

①“吸收”步骤中发生的离子反应方程式为
②设计简单的实验验证溴的非金属性比碘强
(3)模拟反萃取法提取碘的实验流程如下图:

①“萃取”操作中可使用
 作为
作为 的萃取剂,其原因除
的萃取剂,其原因除 不与
不与 反应外,还有
反应外,还有②“反萃取”操作时溶液中有
 、
、 生成。该步骤发生反应的离子反应方程式:
生成。该步骤发生反应的离子反应方程式:
您最近一年使用:0次
名校
8 . 金属矿物资源以及海水资源的利用具有非常广阔的前景。
(1).赤铁矿(主要成分Fe2O3)冶炼得到的铁屑和海带中提取的碘可以用于生产KI,其工艺流程如图所示:
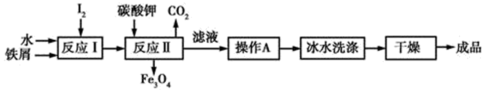
①用冰水洗涤的目的是:a. 除去附着在KI表面的可溶性杂质; b._____________ 。
②反应I生成了铁与碘的化合物X,若X中铁元素与碘元素的质量比为21:127,则X的化学式为____________ ;反应II中1 mol X完全反应生成89.6 L(标准状况)CO2,写出反应II的化学方程式:______________________ 。
(2)其课外小组在实验室设计以下装置(夹持装置已略去);进行实验,模拟海水提溴的部分过程。
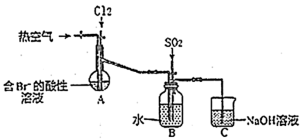
①A装置中通入Cl2气体一段时间后,停止通入,改通入热空气。通入热空气的目的是______________ 。
②反应过程中,B装置中有生成 。写出B中发生反应的离子方程式
。写出B中发生反应的离子方程式______________ 。
③该小组欲从装置B反应后的溶液中制备并分离出溴单质,实验方案为___________ (已知Br2的沸点是59℃,易溶于有机溶剂CCl4)。
(1).赤铁矿(主要成分Fe2O3)冶炼得到的铁屑和海带中提取的碘可以用于生产KI,其工艺流程如图所示:

①用冰水洗涤的目的是:a. 除去附着在KI表面的可溶性杂质; b.
②反应I生成了铁与碘的化合物X,若X中铁元素与碘元素的质量比为21:127,则X的化学式为
(2)其课外小组在实验室设计以下装置(夹持装置已略去);进行实验,模拟海水提溴的部分过程。

①A装置中通入Cl2气体一段时间后,停止通入,改通入热空气。通入热空气的目的是
②反应过程中,B装置中有生成
 。写出B中发生反应的离子方程式
。写出B中发生反应的离子方程式③该小组欲从装置B反应后的溶液中制备并分离出溴单质,实验方案为
您最近一年使用:0次
名校
解题方法
9 . 三氯化碘(ICl3)是一种黄色晶体,遇水易分解,熔点:33℃,沸点:73℃,在药物合成中用途非常广泛。某学习小组从海带中提取碘,并用于制备三氯化碘。
(1)从干海带中提取粗碘
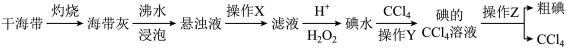
①写出加入过氧化氢后的反应的离子方程式_______ 。
②操作Y用到的玻璃仪器有烧杯、_______ 。
③可以用反萃取法将碘单质从碘的四氯化碳溶液中提取出来,写出向碘的四氯化碳溶液中加入浓氢氧化钠溶液振荡、静置、分液发生的化学方程式_______ 。
(2)利用制得的碘单质制取ICl3
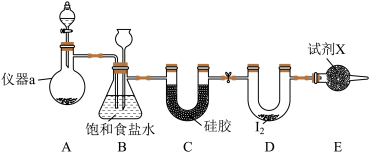
①制备氯气选用的药品为高锰酸钾和浓盐酸,相关反应的离子方程式为_______ 。
②装置B的作用_______ 。
③试剂X为_______ ,X的作用是_______ 。
④氯气与单质碘反应温度稍低于70℃,则装置D适宜的加热方式为_______ 。
(1)从干海带中提取粗碘
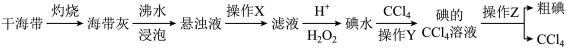
①写出加入过氧化氢后的反应的离子方程式
②操作Y用到的玻璃仪器有烧杯、
③可以用反萃取法将碘单质从碘的四氯化碳溶液中提取出来,写出向碘的四氯化碳溶液中加入浓氢氧化钠溶液振荡、静置、分液发生的化学方程式
(2)利用制得的碘单质制取ICl3

①制备氯气选用的药品为高锰酸钾和浓盐酸,相关反应的离子方程式为
②装置B的作用
③试剂X为
④氯气与单质碘反应温度稍低于70℃,则装置D适宜的加热方式为
您最近一年使用:0次
10 . 海带中含有丰富的碘元素(以I-形式存在)。工业中提取碘的流程如图:
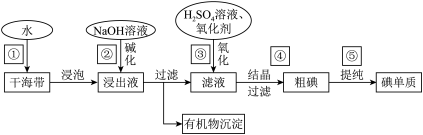
(1)写出步骤③中加硫酸溶液的目的_______ 。
(2)步骤⑤中所涉及的实验操作名称_______ 。
(3)若在实验室中,用分液漏斗、苯(密度比水小,且不溶于水)来提取碘水中的I2,加入少量苯,充分振荡静置后的现象是_______ 。
(4)检验某无色溶液中是否含有I-,所用试剂不合理的是_______ 。
A.淀粉溶液和氯水 B. KBr和稀HCl
C.氯水和四氯化碳 D. KIO3和醋酸
(5)图中有关从海带中提取碘的实验原理和装置能达到实验目的是_____

A.用装置甲灼烧碎海带
B.用装置乙过滤海带灰的浸泡液
C.用装置丙制备用于氧化浸泡液中的氯气
D.用装置丁吸收氧化浸泡液后的尾气

(1)写出步骤③中加硫酸溶液的目的
(2)步骤⑤中所涉及的实验操作名称
(3)若在实验室中,用分液漏斗、苯(密度比水小,且不溶于水)来提取碘水中的I2,加入少量苯,充分振荡静置后的现象是
(4)检验某无色溶液中是否含有I-,所用试剂不合理的是
A.淀粉溶液和氯水 B. KBr和稀HCl
C.氯水和四氯化碳 D. KIO3和醋酸
(5)图中有关从海带中提取碘的实验原理和装置能达到实验目的是

A.用装置甲灼烧碎海带
B.用装置乙过滤海带灰的浸泡液
C.用装置丙制备用于氧化浸泡液中的氯气
D.用装置丁吸收氧化浸泡液后的尾气
您最近一年使用:0次



