名校
解题方法
1 . 如图是从含碘CCl4溶液得到碘的实验过程,则下列说法正确的是
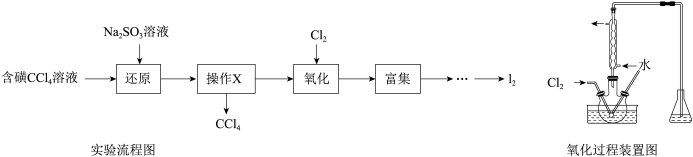

| A.含碘CCl4溶液颜色为红棕色 |
| B.操作X为蒸馏 |
| C.氧化时,应控制在较高温度下进行 |
| D.锥形瓶里盛放的溶液可以为NaHCO3溶液 |
您最近一年使用:0次
解题方法
2 . 下图流程是“海带提碘”实验中的部分流程,有关说法正确的是
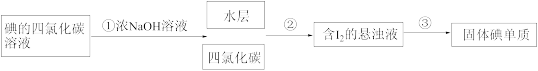
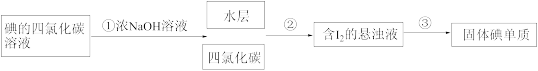
| A.流程①为反萃取,目的是富集碘 |
B.①发生的离子反应方程式为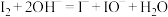 |
| C.②可以使用硝酸提供酸性条件 |
| D.③所需的玻璃仪器有普通漏斗与烧杯 |
您最近一年使用:0次
3 . 下列说法正确的是
A.高温下 与 与 反应生成 反应生成 和 和 | B.乙烯在一定条件下可直接氯化为氯乙烯 |
C.工业上以 和石灰水为原料生产漂白粉 和石灰水为原料生产漂白粉 | D.以海水提取食盐后的母液为原料生产碘单质 |
您最近一年使用:0次
4 . 用离子交换法从海带中提取碘是一种较为先进的制碘工艺应用技术。
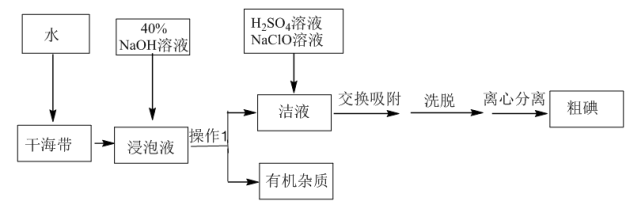
已知: 交换吸附原理:
交换吸附原理: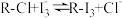 。试回答下列问题:
。试回答下列问题:
(1)操作Ⅰ的正确图示为_______。
(2)在清液中加入 和
和 溶液后,溶液最终变为棕红色,该步骤中
溶液后,溶液最终变为棕红色,该步骤中 的量要适中,请说明原因
的量要适中,请说明原因_______ 。
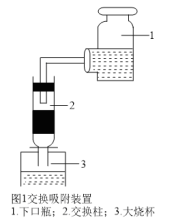
(3)其中交换吸附装置如图1所示,交换柱内装有氯型阴离子交换树脂( 表示),待溶液转化原理为:
表示),待溶液转化原理为: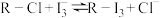 ,全部通过后,树脂颜色变为黑红色,再通过洗脱,离心分离后得到粗碘。已知洗脱分两步进行
,全部通过后,树脂颜色变为黑红色,再通过洗脱,离心分离后得到粗碘。已知洗脱分两步进行
第一步:取8~10%的 溶液
溶液 注入交换柱中。碱性洗脱原理为:
注入交换柱中。碱性洗脱原理为:
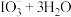 。往碱性洗脱液中滴加
。往碱性洗脱液中滴加 溶液,烧杯底部会析出一层泥状粗碘。
溶液,烧杯底部会析出一层泥状粗碘。
第二步:取10%的 溶液
溶液 注入上述交换柱中。氯化钠洗脱原理为:
注入上述交换柱中。氯化钠洗脱原理为: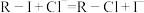 。再往氯化钠洗脱液中滴加
。再往氯化钠洗脱液中滴加 溶液使之酸化,再滴加
溶液使之酸化,再滴加 溶液,溶液由无色转变棕黑色浑浊。
溶液,溶液由无色转变棕黑色浑浊。
①根据交换吸附及洗脱过程可知强碱性阴离子交换树脂也可以对 进行交换吸附,那实验中将
进行交换吸附,那实验中将 转化成
转化成 的原因可能是
的原因可能是_______ 。
②往氯化钠洗脱液中滴加 溶液使之酸化,再滴加
溶液使之酸化,再滴加 溶液反应的离子方程式
溶液反应的离子方程式_______ 。
(4)置换碘量法是分析氧化性试剂的一种常用分析方法,基本过程如下:
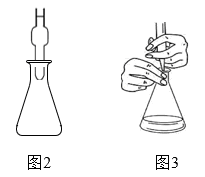
a.取3只碘量瓶,用移液管分别量取一定体积的供试品(氧化性物质)溶液于碘量瓶(图2)中
b.加入稍过量的碘化钾溶液,盖上盖子,并加纯水液封,静置或微热一段时间
c.打开瓶塞,按图3方式用标准 溶液进行滴定,重复3次
溶液进行滴定,重复3次
d.另取3只碘量瓶,用移液管分别量取一定体积准确浓度的基准液 溶液于其中
溶液于其中
e.计算标准液的浓度
f.空白实验
过程中涉及的反应过程如下:
供试品(氧化性物质)
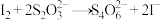

①上述操作合理的顺序是:_______ 。
 _______
_______ _______
_______ _______
_______ _______
_______ _______
_______ (部分步骤可以重复)
(部分步骤可以重复)
②碘量瓶加盖并加纯水液封的主要目的是_______ 。
③已知 易受空气和微生物作用而分解,若无上述操作中的d步骤及相关操作,则测定的供试品的含量会
易受空气和微生物作用而分解,若无上述操作中的d步骤及相关操作,则测定的供试品的含量会_______ 。(填“偏大”、“偏小”或“不变”)

已知:
 交换吸附原理:
交换吸附原理: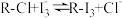 。试回答下列问题:
。试回答下列问题:(1)操作Ⅰ的正确图示为_______。
A.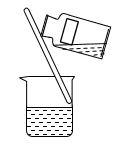 | B.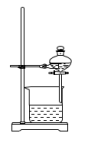 | C.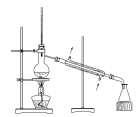 | D.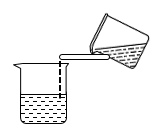 |
 和
和 溶液后,溶液最终变为棕红色,该步骤中
溶液后,溶液最终变为棕红色,该步骤中 的量要适中,请说明原因
的量要适中,请说明原因(3)其中交换吸附装置如图1所示,交换柱内装有氯型阴离子交换树脂(
 表示),待溶液转化原理为:
表示),待溶液转化原理为: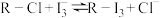 ,全部通过后,树脂颜色变为黑红色,再通过洗脱,离心分离后得到粗碘。已知洗脱分两步进行
,全部通过后,树脂颜色变为黑红色,再通过洗脱,离心分离后得到粗碘。已知洗脱分两步进行第一步:取8~10%的
 溶液
溶液 注入交换柱中。碱性洗脱原理为:
注入交换柱中。碱性洗脱原理为:
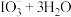 。往碱性洗脱液中滴加
。往碱性洗脱液中滴加 溶液,烧杯底部会析出一层泥状粗碘。
溶液,烧杯底部会析出一层泥状粗碘。第二步:取10%的
 溶液
溶液 注入上述交换柱中。氯化钠洗脱原理为:
注入上述交换柱中。氯化钠洗脱原理为: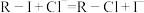 。再往氯化钠洗脱液中滴加
。再往氯化钠洗脱液中滴加 溶液使之酸化,再滴加
溶液使之酸化,再滴加 溶液,溶液由无色转变棕黑色浑浊。
溶液,溶液由无色转变棕黑色浑浊。
①根据交换吸附及洗脱过程可知强碱性阴离子交换树脂也可以对
 进行交换吸附,那实验中将
进行交换吸附,那实验中将 转化成
转化成 的原因可能是
的原因可能是②往氯化钠洗脱液中滴加
 溶液使之酸化,再滴加
溶液使之酸化,再滴加 溶液反应的离子方程式
溶液反应的离子方程式(4)置换碘量法是分析氧化性试剂的一种常用分析方法,基本过程如下:
a.取3只碘量瓶,用移液管分别量取一定体积的供试品(氧化性物质)溶液于碘量瓶(图2)中
b.加入稍过量的碘化钾溶液,盖上盖子,并加纯水液封,静置或微热一段时间
c.打开瓶塞,按图3方式用标准
 溶液进行滴定,重复3次
溶液进行滴定,重复3次d.另取3只碘量瓶,用移液管分别量取一定体积准确浓度的基准液
 溶液于其中
溶液于其中e.计算标准液的浓度
f.空白实验

过程中涉及的反应过程如下:
供试品(氧化性物质)

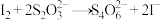

①上述操作合理的顺序是:
 _______
_______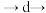 _______
_______ _______
_______ _______
_______ _______
_______ (部分步骤可以重复)
(部分步骤可以重复)②碘量瓶加盖并加纯水液封的主要目的是
③已知
 易受空气和微生物作用而分解,若无上述操作中的d步骤及相关操作,则测定的供试品的含量会
易受空气和微生物作用而分解,若无上述操作中的d步骤及相关操作,则测定的供试品的含量会
您最近一年使用:0次
5 . 海洋化工产品为化学工业生产体系输送了大量的基础原料,为人类的可持续发展做出了重要贡献。下列提取海洋资源的方法不正确的是
| A.将海水蒸发结晶得到氯化钠晶体 |
| B.利用空气从浓缩的海水中氧化出溴 |
C.在海带浸取液中加入 制备碘 制备碘 |
| D.利用熟石灰从海水中沉淀氢氧化镁 |
您最近一年使用:0次
6 . 溴、碘主要存在于海水中,有“海洋元素”的美称。从海带中提取碘单质,工艺流程如下图。
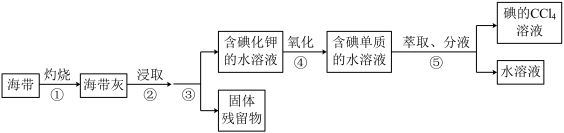
下列操作错误的是

下列操作错误的是
| A | B | C | D |
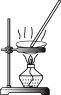 | 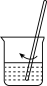 | 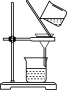 | 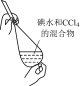 |
| 步骤①操作 | 步骤②操作 | 步骤③操作 | 步骤⑤中振荡萃取操作 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
7 . 从海产品(如海带)中提取碘是工业获取碘的重要途径。其流程如下:

下列说法中不正确的是

下列说法中不正确的是
| A.碘元素在海带中以游离态存在 |
| B.使海带中的碘进入水中也可将海带灼烧成灰再加水浸取 |
C.用 代替 代替 不会产生污染,且能防止 不会产生污染,且能防止 被进一步氧化 被进一步氧化 |
| D.碘单质容易华,可以利用升华法提纯含有氯化钠杂质的碘单质 |
您最近一年使用:0次
名校
解题方法
8 . Ⅰ.将海水淡化与浓海水资源化结合起来是综合利用海水的重要途径之一,一般是先将海水淡化获得淡水,再从剩余的浓海水中通过一系列工艺流程提取其他产品。回答下问题:
(1)请列举一种海水淡化的方法:_______ 。
(2)海水提溴中将Br2从苦卤中吹出,利用了Br2的_______ 性。
Ⅱ.通过传统的海带提碘工艺提取单质碘后,其所得废水中尚残留部分的I2,可用活性炭吸附法加以回收利用。具体流程如图:
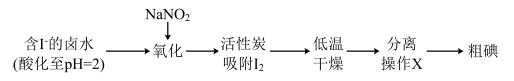
已知:i.pH=2时,NaNO2溶液只能将I-氧化为I2,同时生成NO
ii.将湿润的淀粉-KI试纸伸入盛满氯气的集气瓶中,试纸先变蓝,后褪色
(3)写出氧化含I-的卤水中发生的离子方程式:________ 。
(4)在分离操作X的装置如图所示,电加热器的作用是________ ,得到I2的位置位于该装置中________ 处(填图中选项)。

(5)已知Cl2的氧化性强于NaNO2,但该方法中却选择了价格较高的NaNO2,原因是_______ 。
(6)某工厂排出的废水,经测定含0.012mol/L的游离I2和8×10-4mol/L的H+,若改用加Na2SO3的方法除去I2,发生的化学反应为:Na2SO3+I2+H2O=Na2SO4+2HI,该反应中氧化产物与还原产物的物质的量之比为_______ ,现需处理5L该废水,则需加入0.05mol/L的Na2SO3溶液_______ L才能把I2除尽。
(1)请列举一种海水淡化的方法:
(2)海水提溴中将Br2从苦卤中吹出,利用了Br2的
Ⅱ.通过传统的海带提碘工艺提取单质碘后,其所得废水中尚残留部分的I2,可用活性炭吸附法加以回收利用。具体流程如图:

已知:i.pH=2时,NaNO2溶液只能将I-氧化为I2,同时生成NO
ii.将湿润的淀粉-KI试纸伸入盛满氯气的集气瓶中,试纸先变蓝,后褪色
(3)写出氧化含I-的卤水中发生的离子方程式:
(4)在分离操作X的装置如图所示,电加热器的作用是

(5)已知Cl2的氧化性强于NaNO2,但该方法中却选择了价格较高的NaNO2,原因是
(6)某工厂排出的废水,经测定含0.012mol/L的游离I2和8×10-4mol/L的H+,若改用加Na2SO3的方法除去I2,发生的化学反应为:Na2SO3+I2+H2O=Na2SO4+2HI,该反应中氧化产物与还原产物的物质的量之比为
您最近一年使用:0次
解题方法
9 . 碘是人体必需的微量元素,幼儿缺碘可导致发育迟缓、呆傻等多种疾病。海带中含有较多的碘元素,以下是从海带中提取碘并测定碘含量的实验方案。
提示:海带灰中碘元素以 形式存在。
形式存在。
实验一:海带中碘元素的检验
步骤Ⅰ:准确称取20.0g干海带,去除表面附着物、洗净、剪碎,用酒精浸润,灼烧完全至灰烬,停止加热、冷却。
步骤Ⅱ:将海带灰全部转移到小烧杯中,加入 蒸馏水搅拌,煮沸2~3分钟,过滤,洗涤,将滤液转移至
蒸馏水搅拌,煮沸2~3分钟,过滤,洗涤,将滤液转移至 容量瓶中定容。
容量瓶中定容。
步骤Ⅲ:取步骤IⅡ容量瓶中的溶液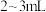 于试管中,加入几滴
于试管中,加入几滴
 溶液酸化,再加入
溶液酸化,再加入 3%的
3%的 溶液和几滴淀粉溶液,观察现象。
溶液和几滴淀粉溶液,观察现象。
实验二:海带中碘元素含量的测定
步骤Ⅳ:取步骤Ⅱ容量瓶中溶液 于锥形瓶中,逐滴加入饱和溴水到呈浅黄色,放置一段时间使其充分反应后加热煮沸至黄色褪去,冷却后加入
于锥形瓶中,逐滴加入饱和溴水到呈浅黄色,放置一段时间使其充分反应后加热煮沸至黄色褪去,冷却后加入 10%
10% 溶液,摇匀,立即用
溶液,摇匀,立即用 的
的 标准溶液滴定反应至浅黄色,加入几滴淀粉溶液作指示剂,继续滴定到溶液刚好褪色,达到反应终点。重复以上操作2~3次,测得平均消耗
标准溶液滴定反应至浅黄色,加入几滴淀粉溶液作指示剂,继续滴定到溶液刚好褪色,达到反应终点。重复以上操作2~3次,测得平均消耗 标准溶液
标准溶液 。
。
涉及的有关反应有:①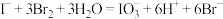
②
③
请按要求完成下列问题:
(1)步骤Ⅰ中用酒精浸润海带的作用是_______ ,灼烧海带的实验中需要的实验仪器有酒精灯、铁架台、泥三角、玻璃棒和_______ (填仪器名称)。
(2)说明海带中有碘元素的实验现象是_______ ,写出步骤中发生的离子反应方程式_______ 。
(3)根据以上数据计算每千克海带中含碘量约为_______  。
。
提示:海带灰中碘元素以
 形式存在。
形式存在。实验一:海带中碘元素的检验
步骤Ⅰ:准确称取20.0g干海带,去除表面附着物、洗净、剪碎,用酒精浸润,灼烧完全至灰烬,停止加热、冷却。
步骤Ⅱ:将海带灰全部转移到小烧杯中,加入
 蒸馏水搅拌,煮沸2~3分钟,过滤,洗涤,将滤液转移至
蒸馏水搅拌,煮沸2~3分钟,过滤,洗涤,将滤液转移至 容量瓶中定容。
容量瓶中定容。步骤Ⅲ:取步骤IⅡ容量瓶中的溶液
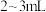 于试管中,加入几滴
于试管中,加入几滴
 溶液酸化,再加入
溶液酸化,再加入 3%的
3%的 溶液和几滴淀粉溶液,观察现象。
溶液和几滴淀粉溶液,观察现象。实验二:海带中碘元素含量的测定
步骤Ⅳ:取步骤Ⅱ容量瓶中溶液
 于锥形瓶中,逐滴加入饱和溴水到呈浅黄色,放置一段时间使其充分反应后加热煮沸至黄色褪去,冷却后加入
于锥形瓶中,逐滴加入饱和溴水到呈浅黄色,放置一段时间使其充分反应后加热煮沸至黄色褪去,冷却后加入 10%
10% 溶液,摇匀,立即用
溶液,摇匀,立即用 的
的 标准溶液滴定反应至浅黄色,加入几滴淀粉溶液作指示剂,继续滴定到溶液刚好褪色,达到反应终点。重复以上操作2~3次,测得平均消耗
标准溶液滴定反应至浅黄色,加入几滴淀粉溶液作指示剂,继续滴定到溶液刚好褪色,达到反应终点。重复以上操作2~3次,测得平均消耗 标准溶液
标准溶液 。
。涉及的有关反应有:①
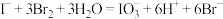
②

③

请按要求完成下列问题:
(1)步骤Ⅰ中用酒精浸润海带的作用是
(2)说明海带中有碘元素的实验现象是
(3)根据以上数据计算每千克海带中含碘量约为
 。
。
您最近一年使用:0次
名校
解题方法
10 . 实验室中下列做法正确的是
| A.浓硝酸保存在带橡胶塞的棕色细口瓶中 |
| B.酸液不慎滴到皮肤,立刻用大量清水冲洗,然后涂上1%的硼酸 |
| C.海带提碘实验中,制取海带灰,可以放在通风处加热灼烧,使其充分灰化 |
| D.实验后,将产生的实验废液及时用自来水稀释后倒入下水道 |
您最近一年使用:0次



