名校
解题方法
1 . 碘是人体必需的生命元素,对人类的生长发育起着重要作用。碘主要存在于海草(如海带)、海水和盐矿中。某小组同学设计如下实验流程模拟从海草中提取碘。
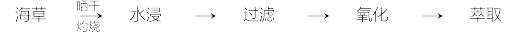
(1)灼烧海草时,除需要三脚架外,还需要用到的下列仪器有_____ (填标号字母)。
A.烧杯 B.坩埚 C.表面皿 D.泥三角 E.酒精灯 F.干燥管
(2)“氧化” 是关键步骤。小组同学设计实验探究 KI 溶液的氧化反应,实验记录如表所示:
①实验Ⅰ中溶液变为浅黄色所发生反应的离子方程式是:_________________ 。
②对比实验 I 和 II,探究实验 II 反应后“溶液不变蓝”的原因,小组同学提出两种假设:
假设 1:NaClO 溶液显碱性,I2在碱性溶液发生歧化反应 3I2 +6OH-= IO3-+ 5I-+ 3H2O。
假设 2:NaClO 溶液有强氧化性,可氧化 I2。
(a)NaClO 溶液显碱性的原因:__________ (用离子方程式表示)。
(b)设计实验 III,证实假设 2 成立,所用装置如图所示,甲溶液是___________ ,实验现象是______________ 。

③小组同学又设计了如下实验:
(a)分析实验Ⅳ、Ⅴ和Ⅵ,得出影响氧气氧化 KI 溶液的反应速率的因素有 ____ 、_____ 。
(b)试解释与实验Ⅵ相比,实验Ⅴ速率较慢的原因_____________ 。
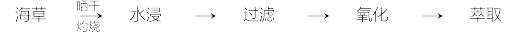
(1)灼烧海草时,除需要三脚架外,还需要用到的下列仪器有
A.烧杯 B.坩埚 C.表面皿 D.泥三角 E.酒精灯 F.干燥管
(2)“氧化” 是关键步骤。小组同学设计实验探究 KI 溶液的氧化反应,实验记录如表所示:
| 序号 | 实验 | 操作 | 现象 |
| Ⅰ |  | 先加 0.5 mL 0.5 mol/L NaClO 溶液,后滴几滴淀粉溶液 | 溶液先变为浅黄色后溶液变蓝 |
| Ⅱ |  | 先加 0.5 mL 0.5 mol/L KI 溶液后滴几滴淀粉溶液 | 先溶液保持无色后溶液也不变蓝,且 pH=10 |
②对比实验 I 和 II,探究实验 II 反应后“溶液不变蓝”的原因,小组同学提出两种假设:
假设 1:NaClO 溶液显碱性,I2在碱性溶液发生歧化反应 3I2 +6OH-= IO3-+ 5I-+ 3H2O。
假设 2:NaClO 溶液有强氧化性,可氧化 I2。
(a)NaClO 溶液显碱性的原因:
(b)设计实验 III,证实假设 2 成立,所用装置如图所示,甲溶液是

③小组同学又设计了如下实验:
| 序号 | 实验 | 操作 | 现象 |
| Ⅳ |  | 敞口试管 | 2 小时后滴加淀粉溶液才出现蓝色 |
| Ⅴ | 敞口试管 水浴 70℃ | 20 min 溶液保持无色,冷却至室温后滴加淀粉溶液出现蓝色 | |
| Ⅵ | 密闭试管 水浴 70℃ | 溶液迅速出现黄色,且黄色逐渐加,冷却至室温后滴加淀粉溶液出现蓝色 |
(b)试解释与实验Ⅵ相比,实验Ⅴ速率较慢的原因
您最近一年使用:0次
解题方法
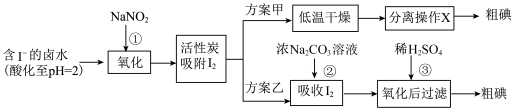
2 . 从海水中可以提取很多有用的物质,例如从海水制盐所得到的卤水中可以提取碘。活性炭吸附法是工业提碘的方法之一,其流程如下:
资料显示:Ⅰ. pH=2时,NaNO2溶液只能将 I-氧化为I2,同时生成NO
Ⅱ. I2+5Cl2+6H2O === 2HIO3+10HCl
Ⅲ. 5 +2
+2 +2H+ = I2+5
+2H+ = I2+5 +H2O
+H2O
(1)反应①的离子方程式____________________ 。
(2)方案甲中,根据I2的特性,分离操作X的方法是____________ 。
(3)已知:反应②中每吸收3mol I2转移5mol电子,离子方程式是__________ 。
(4)Cl2、酸性KMnO4等都是常用的强氧化剂,但该工艺中氧化卤水中的I-却选择了价格较高的NaNO2,原因是_______________________ 。
(5)方案乙中,已知反应③过滤后,滤液中仍存在少量的I2、I-、 。请
。请分别 检验滤液中的I-、 ,将实验方案补充完整。实验中可供选择的试剂:稀H2SO4、淀粉溶液、Fe2(SO4)3溶液、Na2SO3溶液
,将实验方案补充完整。实验中可供选择的试剂:稀H2SO4、淀粉溶液、Fe2(SO4)3溶液、Na2SO3溶液
a.滤液用CCl4多次萃取、分液,直到水层用淀粉溶液检验不出碘单质存在。
b._____________________ 。
资料显示:Ⅰ. pH=2时,NaNO2溶液只能将 I-氧化为I2,同时生成NO
Ⅱ. I2+5Cl2+6H2O === 2HIO3+10HCl
Ⅲ. 5
 +2
+2 +2H+ = I2+5
+2H+ = I2+5 +H2O
+H2O (1)反应①的离子方程式
(2)方案甲中,根据I2的特性,分离操作X的方法是
(3)已知:反应②中每吸收3mol I2转移5mol电子,离子方程式是
(4)Cl2、酸性KMnO4等都是常用的强氧化剂,但该工艺中氧化卤水中的I-却选择了价格较高的NaNO2,原因是
(5)方案乙中,已知反应③过滤后,滤液中仍存在少量的I2、I-、
 。请
。请 ,将实验方案补充完整。实验中可供选择的试剂:稀H2SO4、淀粉溶液、Fe2(SO4)3溶液、Na2SO3溶液
,将实验方案补充完整。实验中可供选择的试剂:稀H2SO4、淀粉溶液、Fe2(SO4)3溶液、Na2SO3溶液a.滤液用CCl4多次萃取、分液,直到水层用淀粉溶液检验不出碘单质存在。
b.
您最近一年使用:0次
3 . 下列实验不能达到目的的是
| 选项 | 目的 | 实验 |
| A | 检验海带中是否含有碘元素 | 向海带灰浸取液中滴加淀粉溶液 |
| B | 除去溴苯中混有的Br2 | 加入稀NaOH溶液洗涤、分液 |
| C | 证明SO2具有还原性 | 将SO2通入酸性KMnO4溶液中 |
| D | 证明醋酸是弱酸 | 测定0.1 mol/L醋酸溶液的pH |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
4 . 某兴趣小组设计了如下实验测定海带中碘元素的含量,依次经过以下四个步骤,下列图示装置和原理能达到实验目的的是
A.灼烧海带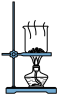 |
B.将海带灰溶解后分离出不溶性杂质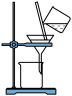 |
C.制备Cl2,并将I-氧化为I2 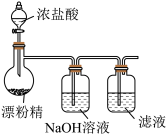 |
D.以淀粉为指示剂,用Na2SO3标准溶液滴定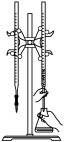 |
您最近一年使用:0次
2020-04-19更新
|
332次组卷
|
5卷引用:【全国百强校】湖北省黄冈中学2019届高三下学期5月第二次模拟考试理科综合化学试题
解题方法
5 . 海带是一种富含生物碘的海洋植物,碘是人体必需的微量元素,人体内碘的含量直接影响身体健康,为了防止缺碘,通常向食盐中加入碘酸钾(KIO3),以补充人体对碘的需求。已知:
以下为某兴趣小组从海带提取碘单质的过程:
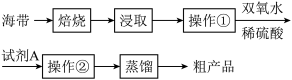
(1)实验室中焙烧海带时不能用到的仪器有________(填写相应的字母)。
(2)向浸取液中加入足量的双氧水和稀硫酸时所发生反应的离子方程式为:____________ 。
(3)操作①中除用到玻璃棒外,还需要的玻璃仪器有_____________________ ;
(4)试剂A的名称为_________ (从上表给出的试剂中选择)。
(5)操作②的名称为__________ 。
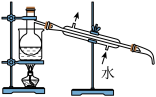
(6)下图是进行蒸馏时的部分仪器,图中缺少玻璃仪器的名称是_____________ 。
(7)工业上可用碘制取碘酸钾,其反应为:I2+2KClO3=2KIO3+Cl2↑,下列有关叙述不正确的是_________________。
| 乙醇 | 四氯化碳 | 裂化汽油 | 碘(晶体) | |
| 密度/g·cm-3 | 0.789 | 1.595 | 0.71~0.76 | 4.93 |
| 沸点/℃ | 78.5 | 76.8 | 25~232 | 184.35 |

(1)实验室中焙烧海带时不能用到的仪器有________(填写相应的字母)。
| A.泥三角 |
| B.三脚架 |
| C.烧杯 |
| D.坩埚 |
| E.蒸发皿 |
| F.酒精灯 |
(3)操作①中除用到玻璃棒外,还需要的玻璃仪器有
(4)试剂A的名称为
(5)操作②的名称为
(6)下图是进行蒸馏时的部分仪器,图中缺少玻璃仪器的名称是

(7)工业上可用碘制取碘酸钾,其反应为:I2+2KClO3=2KIO3+Cl2↑,下列有关叙述不正确的是_________________。
| A.氧化性:I2>Cl2 |
| B.每生成1 mol KIO3转移电子5 mol |
| C.该反应是置换反应 |
| D.反应物和生成物中均含有共价键 |
您最近一年使用:0次



