名校
解题方法
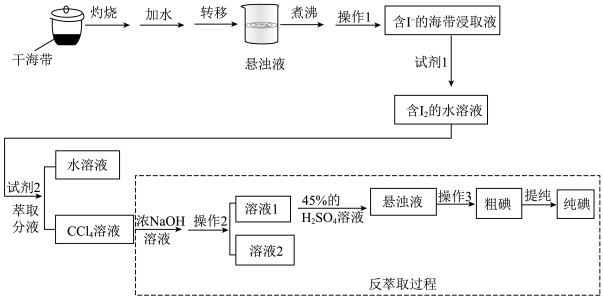
1 . 海带中含有丰富的碘元素,常用作提取碘单质的原料。在实验室我们进行了海带提碘实验,实验流程如下图所示。
已知:①碘易溶于CCl4
②3I2+6NaOH=5NaI+NaIO3+3H2O___________ ,操作2选用装置___________ 。(填“序号”)___________ 。
a.稀硫酸溶液 b.氯水 c.NaOH溶液 d.CCl4
写出试剂1参与反应的离子方程式:___________
(3)加入试剂2后观察到的现象是___________ 。
(4)反萃取第一步加入足量浓NaOH溶液在分液漏斗中进行,振荡并及时放气,判断碘元素由有机层完全进入水层的现象是___________ 。分液后取___________ (填“上层”或“下层”)加入45%的H2SO4溶液
(5)写出加入45%的H2SO4溶液发生反应的离子方程式___________ 。反萃取过程中消耗NaOH和H2SO4的物质的量之比为___________ 。
已知:①碘易溶于CCl4
②3I2+6NaOH=5NaI+NaIO3+3H2O
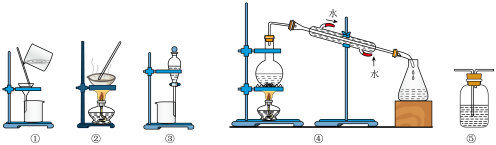
a.稀硫酸溶液 b.氯水 c.NaOH溶液 d.CCl4
写出试剂1参与反应的离子方程式:
(3)加入试剂2后观察到的现象是
(4)反萃取第一步加入足量浓NaOH溶液在分液漏斗中进行,振荡并及时放气,判断碘元素由有机层完全进入水层的现象是
(5)写出加入45%的H2SO4溶液发生反应的离子方程式
您最近一年使用:0次
解题方法
2 . 开发和利用海洋资源是当前科学研究的一项重要任务,如图是某化工厂对海洋资源综合利用的流程图:
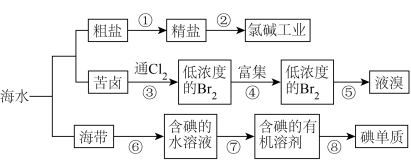
请回答下列问题:
(1)粗盐中含有泥沙、 、
、 、
、 等杂质,精制时一般步骤如下:
等杂质,精制时一般步骤如下:
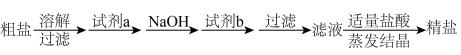
加入的试剂a、b分别是___________ 、___________ 。
(2)③中发生反应的离子方程式为___________ ,可推断氧化性:
___________  (填“>”或“<”)。
(填“>”或“<”)。
(3)⑥通常分三个步骤:
第1步:灼烧,将足量海带灼烧成灰烬;
第2步: 溶液的获取;
溶液的获取;
第3步:氧化。
下列仪器在第1步中不会用到的有___________ 。
A.试管B.瓷坩埚C.坩埚钳D.铁三脚架E.泥三角F.酒精灯G.烧杯H.量筒
第3步中最好选用的氧化剂是___________ 。
A.浓硫酸B.新制氯水C.酸性高锰酸钾D.
(4)⑦中所用的操作方法有___________ 、___________ 。

请回答下列问题:
(1)粗盐中含有泥沙、
 、
、 、
、 等杂质,精制时一般步骤如下:
等杂质,精制时一般步骤如下:
加入的试剂a、b分别是
(2)③中发生反应的离子方程式为

 (填“>”或“<”)。
(填“>”或“<”)。(3)⑥通常分三个步骤:
第1步:灼烧,将足量海带灼烧成灰烬;
第2步:
 溶液的获取;
溶液的获取;第3步:氧化。
下列仪器在第1步中不会用到的有
A.试管B.瓷坩埚C.坩埚钳D.铁三脚架E.泥三角F.酒精灯G.烧杯H.量筒
第3步中最好选用的氧化剂是
A.浓硫酸B.新制氯水C.酸性高锰酸钾D.

(4)⑦中所用的操作方法有
您最近一年使用:0次
名校
3 . 海水是巨大的资源宝库,工业上从海水中获取某些重要化工原料的流程如下图示。 、
、 和
和 等。回答下列问题:
等。回答下列问题:
(1)请列举除蒸馏法外海水淡化的一种方法:____________________ 。
(2)试剂1最好选用__________ (填编号)。
a. b.
b. c.
c. d.NaOH
d.NaOH
(3)提取溴单质时,往苦卤中通入氯气和酸,其酸化的目的是____________________ 。
(4)将吹出后的含 的空气按一定速率通入吸收塔,用
的空气按一定速率通入吸收塔,用 和水进行吸收,吸收后的空气进行循环利用。
和水进行吸收,吸收后的空气进行循环利用。
①流程中可用热空气吹出溴的原因为_____________________ 。
②“吸收塔”内发生反应的离子方程式:_____________________ 。
③流程中不是将酸和氯气氧化后的苦卤直接蒸馏,而是经过“空气吹出”、“二氧化硫吸收”、“氢气氧化”再蒸馏得到液溴,目的是_____________________ 。
(5)检验吸收塔里的溶液是否含 的方法是
的方法是_______________________ 。
(6)海带灰中富含以 形式存在的碘元素。实验室提取
形式存在的碘元素。实验室提取 的途径如图所示:
的途径如图所示:__________ (填一种仪器名称)中加热灼烧。
②向酸化的滤液中加入过氧化氢溶液,可将 氧化为
氧化为 ,请写出该反应的离子方程式:
,请写出该反应的离子方程式:__________________ 。

 、
、 和
和 等。回答下列问题:
等。回答下列问题:(1)请列举除蒸馏法外海水淡化的一种方法:
(2)试剂1最好选用
a.
 b.
b. c.
c. d.NaOH
d.NaOH(3)提取溴单质时,往苦卤中通入氯气和酸,其酸化的目的是
(4)将吹出后的含
 的空气按一定速率通入吸收塔,用
的空气按一定速率通入吸收塔,用 和水进行吸收,吸收后的空气进行循环利用。
和水进行吸收,吸收后的空气进行循环利用。①流程中可用热空气吹出溴的原因为
②“吸收塔”内发生反应的离子方程式:
③流程中不是将酸和氯气氧化后的苦卤直接蒸馏,而是经过“空气吹出”、“二氧化硫吸收”、“氢气氧化”再蒸馏得到液溴,目的是
(5)检验吸收塔里的溶液是否含
 的方法是
的方法是(6)海带灰中富含以
 形式存在的碘元素。实验室提取
形式存在的碘元素。实验室提取 的途径如图所示:
的途径如图所示: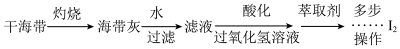
②向酸化的滤液中加入过氧化氢溶液,可将
 氧化为
氧化为 ,请写出该反应的离子方程式:
,请写出该反应的离子方程式:
您最近一年使用:0次
4 . 海带中含有丰富的碘,某中学实验小组为了提取和检验海带灰中的碘,设计了以下实验流程。(已知:海带灰中的碘元素主要以 形式存在)
形式存在)
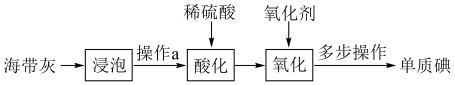
(1)“浸泡”时需充分搅拌,并将悬浊液煮沸2~3分钟,主要的目的是___________ (写一条即可)。
(2)操作a需要用到的玻璃仪器,除烧杯外,还需要___________ 。
(3)“酸化”时需要稀硫酸,回答下列有关问题:
①配制 稀硫酸,需要质量分数为98%的浓硫酸(密度:
稀硫酸,需要质量分数为98%的浓硫酸(密度: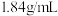 )的体积约为
)的体积约为___________  。(已知:用量筒取用浓硫酸)
。(已知:用量筒取用浓硫酸)
②配制过程的部分操作如下图,则操作步骤的正确顺序为___________ 。(用字母序号表示)
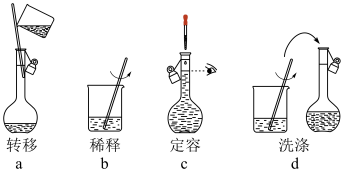
③下列有关配制上述稀硫酸的描述正确的是___________
A.稀释时将蒸馏水缓缓注入盛有浓硫酸的烧杯中
B.溶液未冷却至室温,立即转移、定容
C.定容时俯视容量瓶的刻度线,导致所配溶液的浓度偏大
D.将所配的稀硫酸分装于带橡胶塞的广口瓶中
(4)“氧化”时氧化剂的选择将影响实验结果。
①若选用 ,“氧化”时发生反应的离子方程式为
,“氧化”时发生反应的离子方程式为___________ 。
②若选用 ,过量的
,过量的 可将碘单质氧化成
可将碘单质氧化成 ,其反应的化学方程式为
,其反应的化学方程式为___________ 。
(5)检验“氧化”后的水溶液中是否含有单质碘的实验操作方法___________ 。
 形式存在)
形式存在)
(1)“浸泡”时需充分搅拌,并将悬浊液煮沸2~3分钟,主要的目的是
(2)操作a需要用到的玻璃仪器,除烧杯外,还需要
(3)“酸化”时需要稀硫酸,回答下列有关问题:
①配制
 稀硫酸,需要质量分数为98%的浓硫酸(密度:
稀硫酸,需要质量分数为98%的浓硫酸(密度: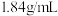 )的体积约为
)的体积约为 。(已知:用量筒取用浓硫酸)
。(已知:用量筒取用浓硫酸)②配制过程的部分操作如下图,则操作步骤的正确顺序为

③下列有关配制上述稀硫酸的描述正确的是
A.稀释时将蒸馏水缓缓注入盛有浓硫酸的烧杯中
B.溶液未冷却至室温,立即转移、定容
C.定容时俯视容量瓶的刻度线,导致所配溶液的浓度偏大
D.将所配的稀硫酸分装于带橡胶塞的广口瓶中
(4)“氧化”时氧化剂的选择将影响实验结果。
①若选用
 ,“氧化”时发生反应的离子方程式为
,“氧化”时发生反应的离子方程式为②若选用
 ,过量的
,过量的 可将碘单质氧化成
可将碘单质氧化成 ,其反应的化学方程式为
,其反应的化学方程式为(5)检验“氧化”后的水溶液中是否含有单质碘的实验操作方法
您最近一年使用:0次
解题方法
5 . 碘及其化合物广泛用于医药、染料等方面。回答下列问题:
Ⅰ. 的一种制备方法如下图所示:
的一种制备方法如下图所示:

(1)“富集”步骤中,生成的黄色固体为______ (填化学式)。
(2)“氧化”步骤中的离子方程式为______ 。
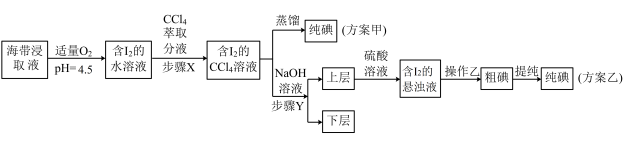
Ⅱ.下图是利用海带浸取原液制备 的甲、乙两种实验方案:
的甲、乙两种实验方案:
已知:① ;
;
②碘微溶于水,从 左右开始升华;
左右开始升华; 的沸点是
的沸点是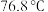 。
。
(3)海带浸取原液在酸性条件下被 氧化的离子方程式是
氧化的离子方程式是______ 。
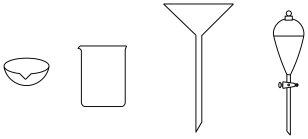
(4)步骤 需要用到的仪器有
需要用到的仪器有______ (从下列图中选择,写出仪器名称)。
(5)“含 的悬浊液”中,水溶液的主要溶质是
的悬浊液”中,水溶液的主要溶质是______ (填化学式)。
(6)操作乙的名称是______ 。
(7)方案甲中采用“蒸馏”不合理,理由是______ 。
Ⅰ.
 的一种制备方法如下图所示:
的一种制备方法如下图所示:
(1)“富集”步骤中,生成的黄色固体为
(2)“氧化”步骤中的离子方程式为
Ⅱ.下图是利用海带浸取原液制备
 的甲、乙两种实验方案:
的甲、乙两种实验方案:
已知:①
 ;
;②碘微溶于水,从
 左右开始升华;
左右开始升华; 的沸点是
的沸点是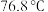 。
。(3)海带浸取原液在酸性条件下被
 氧化的离子方程式是
氧化的离子方程式是(4)步骤
 需要用到的仪器有
需要用到的仪器有
(5)“含
 的悬浊液”中,水溶液的主要溶质是
的悬浊液”中,水溶液的主要溶质是(6)操作乙的名称是
(7)方案甲中采用“蒸馏”不合理,理由是
您最近一年使用:0次
6 . 碘是人体必需的微量元素,人体的碘完全依赖于自然环境的供应,并且必须每天摄入。
(1)紫菜中含有丰富的碘(假设以KI的形式存在),使用无水氯化铁,设计一个简单的实验,制备少量的单质碘。写出实验步骤和相关的化学方程式__________ ;_________ 。
(2)市面上不时出现假碘盐,请你设计一种试纸,在试纸上就可以通过简单的操作(包括加入水或某种化学药品)方便快速地鉴别盐是否含有碘(设含碘盐中加入的是NalO3)。说明你选用何种类型的纸张,试纸的制作方法__________ ,鉴定真假加碘盐的步骤以及反应的离子方程式________ ;__________ 。
(1)紫菜中含有丰富的碘(假设以KI的形式存在),使用无水氯化铁,设计一个简单的实验,制备少量的单质碘。写出实验步骤和相关的化学方程式
(2)市面上不时出现假碘盐,请你设计一种试纸,在试纸上就可以通过简单的操作(包括加入水或某种化学药品)方便快速地鉴别盐是否含有碘(设含碘盐中加入的是NalO3)。说明你选用何种类型的纸张,试纸的制作方法
您最近一年使用:0次
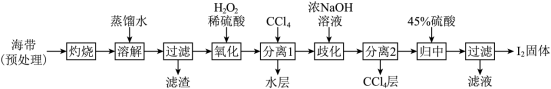
7 . 碘是国防、工业、农业、医药等部门和行业所依赖的重要原料,海水提碘是从海藻中提取元素碘的技术。
Ⅰ.海带提碘(海带中碘元素以I-形式存在)_______ ,设计实验检验氧化后所得溶液是否含I2时,可取样于试管,滴加_______ (填试剂名称)。
(2)加入浓NaOH溶液充分振荡,发生的歧化反应中氧化剂和还原剂物质的量之比为_______ ;向分离得到的含I-和 的水溶液中加入45%硫酸,发生归中反应的离子方程式为
的水溶液中加入45%硫酸,发生归中反应的离子方程式为_______ 。
Ⅱ.获取重要的还原剂-HI
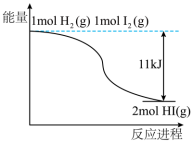
(3)H2和I2反应生成HI过程能量变化如图所示,1molH2(g)、1molHI(g)分子中化学键断裂时分别要吸收能量436kJ、299kJ,则1molI2(g)分子中化学键断裂时需吸收的能量为_______ kJ。
(4)优质的锂碘电池可用于心脏起搏器延续患者的生命,它的正极材料是聚2-乙烯吡啶(简写P2VP)和I2的复合物,电解质是固态薄膜状的碘化锂,电池的总反应为 ,其工作原理如图所示:
,其工作原理如图所示:_______ ;
②放电时,转移0.6×6.02×1023个电子,负极质量减少_______ g。
Ⅰ.海带提碘(海带中碘元素以I-形式存在)
(2)加入浓NaOH溶液充分振荡,发生的歧化反应中氧化剂和还原剂物质的量之比为
 的水溶液中加入45%硫酸,发生归中反应的离子方程式为
的水溶液中加入45%硫酸,发生归中反应的离子方程式为Ⅱ.获取重要的还原剂-HI
(3)H2和I2反应生成HI过程能量变化如图所示,1molH2(g)、1molHI(g)分子中化学键断裂时分别要吸收能量436kJ、299kJ,则1molI2(g)分子中化学键断裂时需吸收的能量为
(4)优质的锂碘电池可用于心脏起搏器延续患者的生命,它的正极材料是聚2-乙烯吡啶(简写P2VP)和I2的复合物,电解质是固态薄膜状的碘化锂,电池的总反应为
 ,其工作原理如图所示:
,其工作原理如图所示: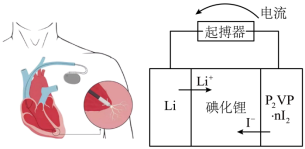
②放电时,转移0.6×6.02×1023个电子,负极质量减少
您最近一年使用:0次
名校
解题方法
8 . 氢气在工业上可用于海水提溴、海带提碘。
Ⅰ.海水提溴工业流程如下图。
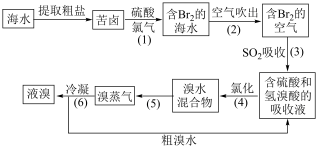
(1)骤(1)中,加硫酸的目的是___________ ;步骤(2)利用了溴的什么物理性质?___________ 。该空气的温度一般控制在80~90℃,温度过高有何不妥?___________ 。
(2)步骤(3)反应中,氧化产物是___________ 。该反应的离子方程式为___________ 。
(3)步骤(2)(3)(4)的目的是___________ 。
(4)步骤(5)、(6)的操作名称依次为___________ 、___________ 。
Ⅱ.海藻中含有丰富的碘元素。实验室中提取碘的流程如下:

(5)步骤①的目的是___________ 。欲确认步骤③中的反应已发生,可取样,加___________ (试剂名称)。
(6)在实验室中进行步骤④操作需要的仪器是___________ 。步骤⑤的名称为___________ 。
(7)关于海水提溴、海藻提碘,下列说法正确的是___________;
Ⅰ.海水提溴工业流程如下图。

(1)骤(1)中,加硫酸的目的是
(2)步骤(3)反应中,氧化产物是
(3)步骤(2)(3)(4)的目的是
(4)步骤(5)、(6)的操作名称依次为
Ⅱ.海藻中含有丰富的碘元素。实验室中提取碘的流程如下:

(5)步骤①的目的是
(6)在实验室中进行步骤④操作需要的仪器是
(7)关于海水提溴、海藻提碘,下列说法正确的是___________;
| A.都需经过浓缩、氧化、提取 |
B.海水提溴的浓缩原理是蒸发,提高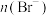 |
C.都可通氯气将 、 、 分别还原为 分别还原为 、 、 |
D.海藻提碘可采用 萃取 萃取 ,海水提溴没有萃取操作 ,海水提溴没有萃取操作 |
您最近一年使用:0次
名校
9 . 碘在科研与生活中有重要作用。
Ⅰ.实验室按如下实验流程提取海带中的碘。___________ (从下列图中选择,写出名称)。___________ 。
(3)海带灰中含有的其他可溶性无机盐,是在___________ (从以上流程中选填实验操作名称)中实现与碘分离。
Ⅱ.测定反应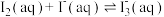 的平衡常数K
的平衡常数K
常温下,取2个碘量瓶分别加入下表中的药品,振荡半小时,均有少量固体不溶。取一定体积的上层清液,加入淀粉作指示剂,用c1 mol L-1 Na2S2O3溶液进行滴定(发生反应
L-1 Na2S2O3溶液进行滴定(发生反应 ),测定
),测定 和
和 的总浓度,进而可以测得K。
的总浓度,进而可以测得K。
(注:在本实验中,认为碘在水中和KI溶液中达到饱和时,它们的碘分子浓度c(I2)相等)
(4)Na2S2O3溶液也可以滴定 的原因是
的原因是___________ (用平衡移动原理回答);滴定终点的实验现象为___________ 。
(5)实验I中,c( )=
)=___________ mol/L(用含c1、c2、c3或c4的式子表示,下同),反应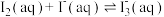 的平衡常数K=
的平衡常数K=___________ 。
(6)若所加的碘偏少,导致实验I中碘量瓶振荡半小时后无固体剩余(不饱和),而实验Ⅱ的碘量瓶中仍有固体不溶,则测得的K将___________ (填“偏大”、“偏小”或“无影响”)。
Ⅰ.实验室按如下实验流程提取海带中的碘。


(3)海带灰中含有的其他可溶性无机盐,是在
Ⅱ.测定反应
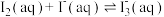 的平衡常数K
的平衡常数K常温下,取2个碘量瓶分别加入下表中的药品,振荡半小时,均有少量固体不溶。取一定体积的上层清液,加入淀粉作指示剂,用c1 mol
 L-1 Na2S2O3溶液进行滴定(发生反应
L-1 Na2S2O3溶液进行滴定(发生反应 ),测定
),测定 和
和 的总浓度,进而可以测得K。
的总浓度,进而可以测得K。(注:在本实验中,认为碘在水中和KI溶液中达到饱和时,它们的碘分子浓度c(I2)相等)
| 碘量瓶 (实验Ⅰ) | 碘量瓶 (实验Ⅱ) | |
| 药品 | 0.5 g研细的碘,100 mL c2 mol L-1 KI L-1 KI | 0.5 g研细的碘,100 mL H2O |
| I2和I3-的总浓度 | c3 mol L-1 L-1 | c4 mol L-1 L-1 |
 的原因是
的原因是(5)实验I中,c(
 )=
)=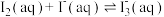 的平衡常数K=
的平衡常数K=(6)若所加的碘偏少,导致实验I中碘量瓶振荡半小时后无固体剩余(不饱和),而实验Ⅱ的碘量瓶中仍有固体不溶,则测得的K将
您最近一年使用:0次
名校
解题方法
10 . 海洋植物如海带、海藻中含有丰富的碘元素,其中碘元素以碘离子的形式存在。实验室里从海带中提取碘的流程如图。
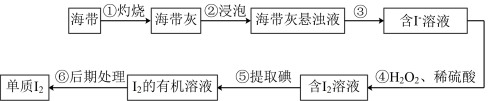
(1)步骤①所用硅酸盐仪器除酒精灯、瓷坩埚外,还有___________ 。
(2)写出步骤④中主要反应的离子方程式:___________ 。
(3)步骤⑤操作的名称为___________ ;若该步骤用的有机溶剂为苯,则得到 的有机溶液的操作为充分振荡放气后,静置分层,
的有机溶液的操作为充分振荡放气后,静置分层,___________ ,该步骤还可选择的有关试剂是___________ (填标号)。
a.酒精 b.四氯化碳 c.饱和食盐水
(4)流程中后期处理用反萃取法:
碘的有机溶液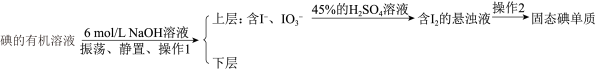
①碘单质与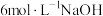 溶液(即浓溶液)发生反应的离子方程式为
溶液(即浓溶液)发生反应的离子方程式为___________ ,该反应中氧化剂与还原剂的质量之比为___________ 。
(2) 与
与 在
在 的
的 溶液中能发生反应,反应的化学方程式为
溶液中能发生反应,反应的化学方程式为___________ 。
(5)实验室常用碘量法测定某溶液中 的含量。取
的含量。取 该溶液,加入
该溶液,加入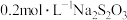 溶液,充分反应后,消耗
溶液,充分反应后,消耗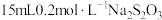 溶液。则该溶液中
溶液。则该溶液中 的含量是
的含量是___________  。(离子方程式为
。(离子方程式为 )
)

(1)步骤①所用硅酸盐仪器除酒精灯、瓷坩埚外,还有
(2)写出步骤④中主要反应的离子方程式:
(3)步骤⑤操作的名称为
 的有机溶液的操作为充分振荡放气后,静置分层,
的有机溶液的操作为充分振荡放气后,静置分层,a.酒精 b.四氯化碳 c.饱和食盐水
(4)流程中后期处理用反萃取法:
碘的有机溶液
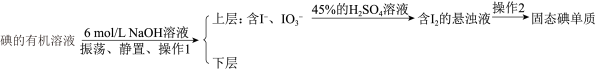
①碘单质与
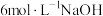 溶液(即浓溶液)发生反应的离子方程式为
溶液(即浓溶液)发生反应的离子方程式为(2)
 与
与 在
在 的
的 溶液中能发生反应,反应的化学方程式为
溶液中能发生反应,反应的化学方程式为(5)实验室常用碘量法测定某溶液中
 的含量。取
的含量。取 该溶液,加入
该溶液,加入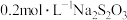 溶液,充分反应后,消耗
溶液,充分反应后,消耗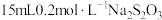 溶液。则该溶液中
溶液。则该溶液中 的含量是
的含量是 。(离子方程式为
。(离子方程式为 )
)
您最近一年使用:0次



