名校
解题方法
1 . 海洋资源的利用具有非常广阔的前景,从海水中可提取多种化工原料。
Ⅰ.如图是从海水中提取镁的简单流程,回答下列问题:

(1)工业上常用于沉淀 的试剂A是
的试剂A是___________ ,操作A的名称是___________ 。
(2)由无水 制取Mg的化学方程式是
制取Mg的化学方程式是___________ 。
Ⅱ.海水中Br含量为 ,工业上常用“吹出法”从海水中提溴,工艺流程示意图如图,回答下列问题:
,工业上常用“吹出法”从海水中提溴,工艺流程示意图如图,回答下列问题:
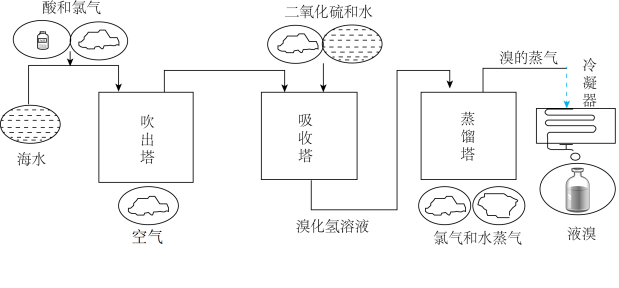
(3)鼓入热空气将生成的溴吹出,利用了 的
的___________ 性。
(4)吸收塔中 的吸收率可达95%,吸收塔中主要反应的方程式是
的吸收率可达95%,吸收塔中主要反应的方程式是 。也有工艺是在吹出
。也有工艺是在吹出 后用碳酸钠溶液吸收,生成溴化钠和溴酸钠,该反应的离子方程式是
后用碳酸钠溶液吸收,生成溴化钠和溴酸钠,该反应的离子方程式是___________ 。
Ⅲ.海带中含有丰富的碘。为了从海带中提取碘,某研究性学习小组设计如下实验:

(5)步骤①中灼烧海带时,应将海带放入___________ (填仪器名称)中灼烧。
(6)步骤④发生的离子反应方程式为___________ 。
(7)实验室常用碘量法测定溶液中 的含量。取200mL样品,加入
的含量。取200mL样品,加入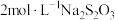 溶液,发生反应
溶液,发生反应 ,充分反应后,消耗
,充分反应后,消耗 溶液100mL。则该样品中
溶液100mL。则该样品中 的含量是
的含量是___________  。
。
Ⅰ.如图是从海水中提取镁的简单流程,回答下列问题:

(1)工业上常用于沉淀
 的试剂A是
的试剂A是(2)由无水
 制取Mg的化学方程式是
制取Mg的化学方程式是Ⅱ.海水中Br含量为
 ,工业上常用“吹出法”从海水中提溴,工艺流程示意图如图,回答下列问题:
,工业上常用“吹出法”从海水中提溴,工艺流程示意图如图,回答下列问题:
(3)鼓入热空气将生成的溴吹出,利用了
 的
的(4)吸收塔中
 的吸收率可达95%,吸收塔中主要反应的方程式是
的吸收率可达95%,吸收塔中主要反应的方程式是 。也有工艺是在吹出
。也有工艺是在吹出 后用碳酸钠溶液吸收,生成溴化钠和溴酸钠,该反应的离子方程式是
后用碳酸钠溶液吸收,生成溴化钠和溴酸钠,该反应的离子方程式是Ⅲ.海带中含有丰富的碘。为了从海带中提取碘,某研究性学习小组设计如下实验:

(5)步骤①中灼烧海带时,应将海带放入
(6)步骤④发生的离子反应方程式为
(7)实验室常用碘量法测定溶液中
 的含量。取200mL样品,加入
的含量。取200mL样品,加入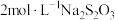 溶液,发生反应
溶液,发生反应 ,充分反应后,消耗
,充分反应后,消耗 溶液100mL。则该样品中
溶液100mL。则该样品中 的含量是
的含量是 。
。
您最近一年使用:0次
名校
2 . 海洋植物如海带,海藻中含有丰富的碘元素,碘元素以碘离子的形式存在。实验室里从海藻中提取碘的流程如下:(已知: )。
)。
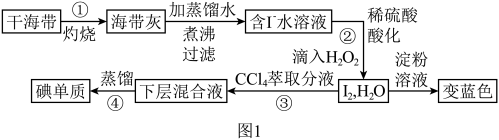
(1)以上步骤不需要用到的仪器是_______。
(2)选用试剂 的理由是_______。
的理由是_______。
(3)写出步骤②中反应的离子方程式_______ 。
(4)工业制备过程中,步骤④很难达到目的,常对图1步骤④进行如下改进:
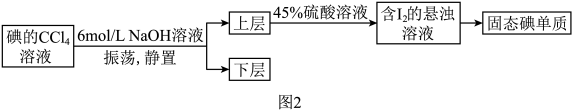
写出上述流程中加入45%硫酸溶液一步反应的离子方程式_______ 。
(5)向盛有KI溶液的试管中加入少许CCl4后滴加氯水,CCl4层变成紫色。如果继续向试管中滴加氯水,振荡,CCl4层会逐渐变浅,最后变成无色。完成下列填空:
①已知碘元素最终变为无色HIO3。上述整个过程中的还原剂有_______ 。
②若把KI成KBr,则CCl4层变为_______ 色,继续滴加氯水,CCl4层的颜色没有变化。Cl2、HIO3、HBrO3氧化性由强到弱的顺序是_______ 。
 )。
)。
(1)以上步骤不需要用到的仪器是_______。
A. | B. | C. | D. |
 的理由是_______。
的理由是_______。A. 不溶于水 不溶于水 | B. 的密度比水大 的密度比水大 |
C.碘在 中比在水中溶解度更大 中比在水中溶解度更大 | D. 与碘水不反应 与碘水不反应 |
(4)工业制备过程中,步骤④很难达到目的,常对图1步骤④进行如下改进:

写出上述流程中加入45%硫酸溶液一步反应的离子方程式
(5)向盛有KI溶液的试管中加入少许CCl4后滴加氯水,CCl4层变成紫色。如果继续向试管中滴加氯水,振荡,CCl4层会逐渐变浅,最后变成无色。完成下列填空:
①已知碘元素最终变为无色HIO3。上述整个过程中的还原剂有
②若把KI成KBr,则CCl4层变为
您最近一年使用:0次
解题方法
3 .  常用于制药和食品添加剂。以海带为原料提取高纯度碘单质并制备
常用于制药和食品添加剂。以海带为原料提取高纯度碘单质并制备 的一种流程如下:
的一种流程如下:
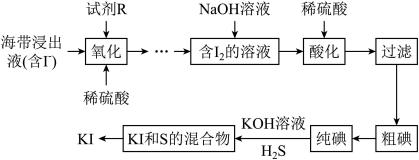
回答下列问题:
(1)“酸化”时稀硫酸的作用是___________ 。
(2)分离 和S的混合物得到
和S的混合物得到 溶液的试剂和方法如下,正确的是
溶液的试剂和方法如下,正确的是___________ (填标号)。
(3)利用下图装置完成 与
与 反应制备
反应制备 。
。

① 溶液的作用是
溶液的作用是___________ (用离子方程式表示)。
②三颈烧瓶中产生 的正确操作顺序为
的正确操作顺序为___________ (填标号)。
a.旋开活塞K,通入 b.加入稀硫酸 c.加入
b.加入稀硫酸 c.加入 溶液
溶液
(4)产品纯度测定。
准确称取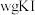 样品溶于水配成
样品溶于水配成 溶液,量取
溶液,量取 溶液于锥形瓶中,加入足量用稀硫酸酸化的
溶液于锥形瓶中,加入足量用稀硫酸酸化的 溶液,摇匀,置于电热板上加热煮沸(常补加热水以保持溶液体积基本不变)。待紫色碘蒸气消失后,再煮沸5分钟,取下放置几分钟,冷却至室温。加入适量的硫酸和磷酸的混合液,用
溶液,摇匀,置于电热板上加热煮沸(常补加热水以保持溶液体积基本不变)。待紫色碘蒸气消失后,再煮沸5分钟,取下放置几分钟,冷却至室温。加入适量的硫酸和磷酸的混合液,用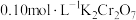 标准溶液反应至完全(还原产物只有
标准溶液反应至完全(还原产物只有 ),消耗标准溶液
),消耗标准溶液 。该
。该 产品的纯度为
产品的纯度为___________ (用含w,V的式子表示)。
 常用于制药和食品添加剂。以海带为原料提取高纯度碘单质并制备
常用于制药和食品添加剂。以海带为原料提取高纯度碘单质并制备 的一种流程如下:
的一种流程如下:
回答下列问题:
(1)“酸化”时稀硫酸的作用是
(2)分离
 和S的混合物得到
和S的混合物得到 溶液的试剂和方法如下,正确的是
溶液的试剂和方法如下,正确的是| 选项 | 试剂 | 方法 |
| a | 二硫化碳 | 分液 |
| b | 酒精 | 分液 |
| c |  溶液 溶液 | 过滤 |
(3)利用下图装置完成
 与
与 反应制备
反应制备 。
。
①
 溶液的作用是
溶液的作用是②三颈烧瓶中产生
 的正确操作顺序为
的正确操作顺序为a.旋开活塞K,通入
 b.加入稀硫酸 c.加入
b.加入稀硫酸 c.加入 溶液
溶液(4)产品纯度测定。
准确称取
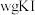 样品溶于水配成
样品溶于水配成 溶液,量取
溶液,量取 溶液于锥形瓶中,加入足量用稀硫酸酸化的
溶液于锥形瓶中,加入足量用稀硫酸酸化的 溶液,摇匀,置于电热板上加热煮沸(常补加热水以保持溶液体积基本不变)。待紫色碘蒸气消失后,再煮沸5分钟,取下放置几分钟,冷却至室温。加入适量的硫酸和磷酸的混合液,用
溶液,摇匀,置于电热板上加热煮沸(常补加热水以保持溶液体积基本不变)。待紫色碘蒸气消失后,再煮沸5分钟,取下放置几分钟,冷却至室温。加入适量的硫酸和磷酸的混合液,用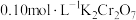 标准溶液反应至完全(还原产物只有
标准溶液反应至完全(还原产物只有 ),消耗标准溶液
),消耗标准溶液 。该
。该 产品的纯度为
产品的纯度为
您最近一年使用:0次
名校
4 . 碘在工农业生产和日常生活中有重要用途。图为海带制碘的流程图。
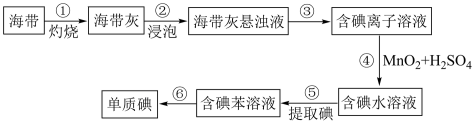
(1)步骤③的实验操作名称是_______ ,步骤①的目的是_______ ,实验室中步骤⑤操作选用的主要玻璃仪器是_______ (填仪器名称)。
(2)若步骤⑤采用四氯化碳来提取碘,将四氯化碳加入含碘水溶液并振荡、静置,将观察到的现象是_______ 。

(1)步骤③的实验操作名称是
(2)若步骤⑤采用四氯化碳来提取碘,将四氯化碳加入含碘水溶液并振荡、静置,将观察到的现象是
您最近一年使用:0次
名校
解题方法
5 . 海带中含有丰富的碘元素,从海带中提取碘,可经过以下实验步骤完成。
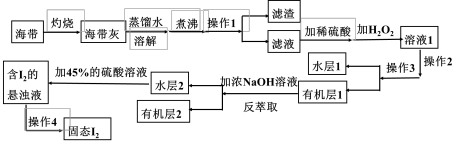
回答下列问题:
(1)灼烧的目的是___________ 。
(2)操作2和操作3用到的玻璃仪器有___________ 。
(3)若有机层1在下层,则有机层2主要成分可能为___________ 。
(4)加入H2O2,发生反应的离子方程式为___________ 。
(5)用铂丝蘸取少量水层2中溶液在酒精灯上灼烧,可观察到___________ 色。
(6)反萃取过程发生反应的离子方程式为___________ 。

回答下列问题:
(1)灼烧的目的是
(2)操作2和操作3用到的玻璃仪器有
(3)若有机层1在下层,则有机层2主要成分可能为
(4)加入H2O2,发生反应的离子方程式为
(5)用铂丝蘸取少量水层2中溶液在酒精灯上灼烧,可观察到
(6)反萃取过程发生反应的离子方程式为
您最近一年使用:0次
6 . Ⅰ.请回答实验室制取蒸馏水的有关问题。
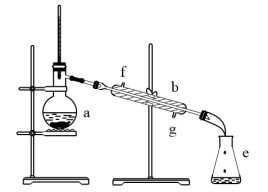
(1)写出下列仪器的名称:a.___________ b. ___________
(2)若利用该装置分离四氯化碳和酒精的混合物,还缺少的仪器是___________ ,将仪器补充完整后进行实验。冷却水由___________ (填f或g,下同)口通入,___________ 口流出。
(3)实验开始几分钟后,发现忘记添加沸石,此时应该进行的操作是___________ 。
Ⅱ.海洋植物如海带、海藻中含有大量的碘元素,请回答提取碘的有关问题。

(4)图中操作⑤,还可选择的试剂是___________
(5)操作⑤需要使用的主要玻璃仪器为___________ 。
(6)操作⑤的萃取环节结束后,分液漏斗中上层液体呈___________ 色;打开分液漏斗活塞,将下层液体从下口放出时,却未见液体流下,原因可能是___________ 。

(1)写出下列仪器的名称:a.
(2)若利用该装置分离四氯化碳和酒精的混合物,还缺少的仪器是
(3)实验开始几分钟后,发现忘记添加沸石,此时应该进行的操作是
Ⅱ.海洋植物如海带、海藻中含有大量的碘元素,请回答提取碘的有关问题。

(4)图中操作⑤,还可选择的试剂是___________
| A.酒精 | B.四氯化碳 | C.醋酸 | D.汽油 |
(6)操作⑤的萃取环节结束后,分液漏斗中上层液体呈
您最近一年使用:0次
解题方法
7 . 已知 悬浊液,加入Fe粉
悬浊液,加入Fe粉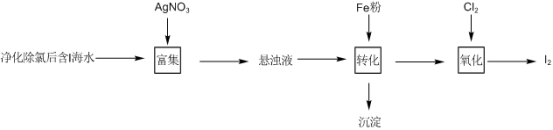 进行转化反应的离子方程式为
进行转化反应的离子方程式为_______ ,生成的沉淀与硝酸反应,生成_______ 后可循环使用。
 悬浊液,加入Fe粉
悬浊液,加入Fe粉 进行转化反应的离子方程式为
进行转化反应的离子方程式为
您最近一年使用:0次
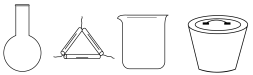
8 . 碘元素是我们身体必不可少的一种微量元素。海带中含有碘元素,从海带中提取碘的实验过程如图所示:

回答下列问题
(1)“灼烧”中用到下列仪器中的_______ (填仪器名称)。
(2) 的电子式为
的电子式为_______ ,“滤液”中发生反应的离子方程式为_______ 。
(3)“萃取”操作需用到分液漏斗,该仪器使用前应进行的操作为_______ , 的
的 溶液应从分液漏斗的
溶液应从分液漏斗的_______ (填“上口”或“下口”)放出。
(4)某小组发现该实验的成功率不高,很容易出现萃取后有机层出现无色或者出现淡粉色的现象。为了提高海带提碘实验的成功率,小组同学对该实验中引起碘元素流失的操作步骤进行了探究。
提出假设 实验中不同浸取温度和不同洗涤液对碘元素流失有影响。
设计方案并完成实验 灼烧海带30min后,用15.00mL蒸馏水浸取,进行实验:
已知: 溶液颜色越深,数值A越大,且
溶液颜色越深,数值A越大,且 。
。
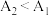 可能的原因为
可能的原因为_______ ,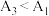 可能的原因为
可能的原因为_______ 。
(5)海带中含有钙元素。写出一种含钙元素物质的化学式及其用途:_______ 。

回答下列问题
(1)“灼烧”中用到下列仪器中的

(2)
 的电子式为
的电子式为(3)“萃取”操作需用到分液漏斗,该仪器使用前应进行的操作为
 的
的 溶液应从分液漏斗的
溶液应从分液漏斗的(4)某小组发现该实验的成功率不高,很容易出现萃取后有机层出现无色或者出现淡粉色的现象。为了提高海带提碘实验的成功率,小组同学对该实验中引起碘元素流失的操作步骤进行了探究。
提出假设 实验中不同浸取温度和不同洗涤液对碘元素流失有影响。
设计方案并完成实验 灼烧海带30min后,用15.00mL蒸馏水浸取,进行实验:
| 序号 | 浸取温度/℃ | 洗涤液 | 稀硫酸溶液滴数 | 氧化剂 |  溶液颜色深浅数值A 溶液颜色深浅数值A |
| 1 | 常温 | 20滴50%的乙醇 | 15滴 | 1.00mL10% |  |
| 2 | 常温 | 20滴蒸馏水 | 15滴 | 1.00mL10% |  |
| 3 | 加热 | 20滴50%的乙醇 | 15滴 | 1.00mL10% |  |
 溶液颜色越深,数值A越大,且
溶液颜色越深,数值A越大,且 。
。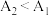 可能的原因为
可能的原因为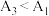 可能的原因为
可能的原因为(5)海带中含有钙元素。写出一种含钙元素物质的化学式及其用途:
您最近一年使用:0次
9 . 加碘食盐中加入的碘酸钾是一种白色结晶粉末,常温下很稳定,加热至560℃开始分解。工业生产碘酸钾的流程如图:

(1)检验加碘食盐中的碘元素,某学生利用碘酸钾与碘化钾在酸性条件下发生反应。用四氯化碳萃取所生成的碘时,主要用到的玻璃仪器有____ 。
(2)从滤液中得到KIO3成品的操作为____ ,操作时除不断用玻璃棒搅拌外,还需要注意的事项有____ 。

(1)检验加碘食盐中的碘元素,某学生利用碘酸钾与碘化钾在酸性条件下发生反应。用四氯化碳萃取所生成的碘时,主要用到的玻璃仪器有
(2)从滤液中得到KIO3成品的操作为
您最近一年使用:0次
20-21高一上·全国·课时练习
10 . 海带提取碘的过程如下:
海带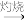 海带灰
海带灰 滤液
滤液 碘水
碘水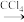 碘的CCl4溶液
碘的CCl4溶液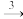 单质碘
单质碘
(1)1、3的操作名称分别是___________ 、___________ 。
(2)A所需加入的物质是___________ ,发生的离子方程式是___________ 。
(3)CCl4的作用是___________ ,CCl4加入到碘水中,充分振荡后静置,用___________ (仪器名称)可分离得到碘的CCl4溶液,对应操作称为___________ 。
海带
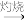 海带灰
海带灰 滤液
滤液 碘水
碘水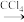 碘的CCl4溶液
碘的CCl4溶液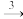 单质碘
单质碘(1)1、3的操作名称分别是
(2)A所需加入的物质是
(3)CCl4的作用是
您最近一年使用:0次



