四川省泸州市泸县第一中学2019届高三下学期三诊模拟理科综合化学试题
四川
高三
一模
2019-04-19
680次
整体难度:
适中
考查范围:
常见无机物及其应用、有机化学基础、认识化学科学、化学实验基础、物质结构与性质、化学反应原理
四川省泸州市泸县第一中学2019届高三下学期三诊模拟理科综合化学试题
四川
高三
一模
2019-04-19
680次
整体难度:
适中
考查范围:
常见无机物及其应用、有机化学基础、认识化学科学、化学实验基础、物质结构与性质、化学反应原理
一、单选题 添加题型下试题
单选题
|
适中(0.65)
名校
1. 中国传统文化中的“笔、墨、纸、砚”被称为“文房四宝”。下列说法错误的是
| A.毛笔中羊毫的主要成分是蛋白质 |
| B.墨中炭黑性质稳定可使古代字画长期保存而不褪色 |
| C.宣纸制作工序中的“加碱蒸煮”主要发生化学变化 |
| D.砚石中含有二氧化硅,结构式为O=Si=O |
【知识点】 二氧化硅的组成、结构解读 淀粉、纤维素的水解 蛋白质
您最近一年使用:0次
2018-06-06更新
|
735次组卷
|
4卷引用:四川省宜宾市高2018届高三第三次诊断考试化学试题
四川省宜宾市高2018届高三第三次诊断考试化学试题四川省宜宾市第四中学2019届高三二诊模拟考试理综-化学试题四川省泸州市泸县第一中学2019届高三下学期三诊模拟理科综合化学试题(已下线)2019年5月12日《每日一题》四轮复习—— 每周一测
单选题
|
适中(0.65)
名校
2. 检查司机是否酒后驾车的反应原理是:C2H5OH+4CrO3+6H2SO4=2Cr2(SO4)3+2CO2↑+9H2O。NA表示阿伏伽德罗常数的值,下列说法正确的是
| A.0.1 mol C2H5OH中含OH-数目为0.1 NA |
| B.25℃时,pH=1的H2SO4溶液中含有H+的数目为0.1 NA |
| C.1.8 g H2O中含有共用电子对数目为0.2 NA |
| D.生成4.48 L CO2气体时,转移电子数目为1.2 NA |
您最近一年使用:0次
2018-06-06更新
|
606次组卷
|
6卷引用:四川省宜宾市高2018届高三第三次诊断考试化学试题
四川省宜宾市高2018届高三第三次诊断考试化学试题辽宁省沈阳铁路实验中学2017-2018学年高二6月月考化学试题(已下线)2018年高考题及模拟题汇编 专题02 化学计量与化学计算(已下线)学科网2019年高考化学一轮复习讲练测1.1 物质的量 气体摩尔体积 讲四川省宜宾市第四中学2019届高三二诊模拟考试理综-化学试题四川省泸州市泸县第一中学2019届高三下学期三诊模拟理科综合化学试题
单选题
|
适中(0.65)
名校
解题方法
3. 对伞花烃(a)常用作染料、医药、香料的中间体,a可转化为b(如图)。下列说法错误的是( )
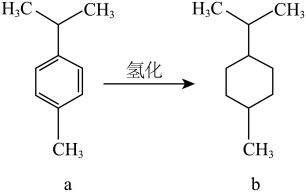
| A.常温下对伞花烃呈液态且难溶于水 |
| B.b物质的一氯代物有5种(不考虑立体异构) |
| C.对伞花烃分子中最多有9个碳原子共平面 |
| D.图中氢化反应既是加成反应也是还原反应 |
您最近一年使用:0次
2020-04-12更新
|
1411次组卷
|
14卷引用:【全国市级联考】四川省泸州市2018届高三第三次教学质量诊断考试理综化学试题
【全国市级联考】四川省泸州市2018届高三第三次教学质量诊断考试理综化学试题【全国市级联考】四川省泸州市2018届高三第三次教学质量诊断考试理科综合化学试题【全国百强校】四川省棠湖中学2017-2018学年高二下学期期中考试理综化学试题四川省宜宾市第四中学2019届高三二诊模拟考试理综-化学试题四川省泸州市泸县第一中学2019届高三下学期三诊模拟理科综合化学试题安徽省金汤白泥乐槐六校2018-2019学年高二上学期第二次联考化学试题专题4.2 有机化学基础(综合提升卷)——巅峰冲刺2020年高考化学二轮专项提升第二章 烃和卤代烃——C挑战 模拟高考(人教版选修5)(人教2019)选择性必修3第二章 C高考挑战区(鲁科版2019)选3第1章 C高考挑战区山东省威海乳山市银滩高级中学2021-2022学年高二下学期3月月考化学试题北京市陈经纶中学2022-2023学年高二下学期期中考试化学试题湖北省沙市中学2022-2023学年高二下学期5月月考化学试题山东省威海市乳山市银滩高级中学2023-2024学年高二3月月考化学试题
单选题
|
适中(0.65)
名校
4. 按图装置进行实验,下列现象能推断出结论的是( )
| 选项 | 试剂X | Y中试剂及现象 | 结论 | 装置 |
| A | 一种盐 | 酚酞溶液未变红 | 该盐不可能是铵盐 | 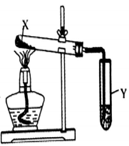 |
| B | 小苏打和纯碱 | 石灰水变浑浊 | 纯碱比小苏打稳定 | |
| C | 氢氧化钙与氯化铵 | 硝酸银溶液中先产生沉淀后溶解 | Ag2O能溶于氨水 | |
| D | 氯酸钾与二氧化锰 | 淀粉、碘化钾和硫酸的混合溶液变蓝 | 反应产生了Cl2 |
| A.A | B.B | C.C | D.D |
【知识点】 物质含量的测定 化学实验探究 物质性质实验方案的设计解读
您最近一年使用:0次
2018-05-04更新
|
306次组卷
|
3卷引用:【全国市级联考】四川省泸州市2018届高三第三次教学质量诊断考试理综化学试题
单选题
|
适中(0.65)
名校
5. A、B、C、D、E 是五种原子序数依次增大的短周期主族元素,B的原子核外电子层数为n,核电荷数为2n2-1,原子最外层电子数为2n+1;A与C同主族但不相邻;D原子最外层电子数等于电子层数的2倍。下列说法不正确的是
| A.C元素位于第3周期第IA族 |
| B.E的含氧酸的酸性大于D的含氧酸的酸性 |
| C.B、E均能与A形成18个电子的化合物 |
| D.B的气态氢化物与其最高价氧化物对应的水化物反应生成盐 |
您最近一年使用:0次
2018-05-01更新
|
253次组卷
|
3卷引用:【全国市级联考】山东省日照市2018届高三4月校际联合期中考试理综化学试题
单选题
|
适中(0.65)
名校
6. 在实验室中,以一定浓度的乙醛—Na2SO4溶液为电解质溶液,模拟乙醛废水的处理过程(如图),乙醛在两电极分别转化为乙醇和乙酸。下列对电解过程的分析正确的是


| A.以铅蓄电池为电源,则a极为Pb电极 |
| B.石墨Ⅱ电极附近的pH逐渐减小 |
| C.阳极反应为CH3CHO+H2O-2e-=CH3COOH+2H+ |
| D.每处理含8.8g乙醛的废水,转移电子的数目为0.4NA |
您最近一年使用:0次
2018-05-26更新
|
642次组卷
|
5卷引用:【全国市级联考】四川省广安、眉山、内江、遂宁2018届高三第三次诊断性考试理综化学试题
单选题
|
适中(0.65)
名校
7. 常温下,用0. 1000 mol·L-1的盐酸滴定20.00 mL未知浓度的Na2CO3溶液,溶液的pH与所加盐酸的体积关系如图所示(饱和H2CO3溶液pH=5.6)。下列有关叙述正确的是
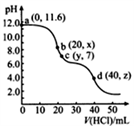

| A.若c(Na2CO3)=0.1000 mol·L-1,则H2CO3的Ka2数量级约为10-6 |
| B.c点处溶液中一定有:c(Na+)=2c(CO32-)+c(HCO3-) |
| C.a、c两点水的c(OH-)之比为10-11.6 :10-7 |
| D.若z=5.6,则d点有c(Na+)=c(Cl-)>c(H2CO3)>c(OH-) |
您最近一年使用:0次
2018-05-26更新
|
417次组卷
|
3卷引用:【全国市级联考】四川省广安、眉山、内江、遂宁2018届高三第三次诊断性考试理综化学试题
二、解答题 添加题型下试题
解答题-实验探究题
|
适中(0.65)
名校
8. TiC14是制备钛及其化合物的重要中间体,某小组同学利用下列装置在实验室制备TiCl4,设计实验如下(夹持装置略去):
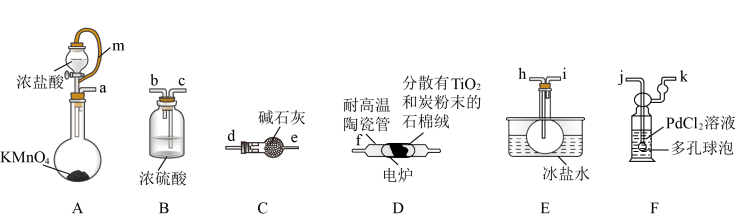
已知:①PdC12溶液捕获CO时,生成金属单质和两种酸性气体化合物。
②
请回答下列问题:
(1)按照气流由左到右的方向,上述装置合理的连接顺序为a→____ →____ →f→g→___ →____ →_____ →_____ →_____ (填仪器接口字母)。
(2)根据完整的实验装置进行实验,实验步骤如下:检查装置气密性后,装入药品;_____________ (按正确的顺序填入下列操作的序号)。
①关闭分液漏斗活塞 ②打开分液漏斗活塞
③停止加热,充分冷却 ④加热装置D中陶瓷管
(3)装置D中除生成TiCl4外,同时生成一种气态不成盐氧化物,该反应的化学方程式为________ 。
(4)设计实验证明装置E中收集到的液体中含有TiCl4:__________________________ 。
(5)装置F中发生反应的化学方程式为_____________ 。用其他方法也可代替装置F,可以是______ (写出一种即可)。
(6)制得的TiC14产品中常含有少量CC14,从产品中分离出TiC14的操作名称为_________________ 。

已知:①PdC12溶液捕获CO时,生成金属单质和两种酸性气体化合物。
②
| 化合物 | 熔点/℃ | 沸点/℃ | 密度/g·cm-3 | 水溶性 |
| TiCl4 | -25 | 136 | 1.5 | 易水解生成难溶于水的物质,能溶于有机溶剂 |
| CCl4 | -25 | 76.8 | 1.6 | 难溶于水 |
(1)按照气流由左到右的方向,上述装置合理的连接顺序为a→
(2)根据完整的实验装置进行实验,实验步骤如下:检查装置气密性后,装入药品;
①关闭分液漏斗活塞 ②打开分液漏斗活塞
③停止加热,充分冷却 ④加热装置D中陶瓷管
(3)装置D中除生成TiCl4外,同时生成一种气态不成盐氧化物,该反应的化学方程式为
(4)设计实验证明装置E中收集到的液体中含有TiCl4:
(5)装置F中发生反应的化学方程式为
(6)制得的TiC14产品中常含有少量CC14,从产品中分离出TiC14的操作名称为
您最近一年使用:0次
9. 含氮化合物在材料方面的应用越来越广泛。
(1) 甲胺(CH3NH2)是合成太阳能敏化剂的原料。工业合成甲胺原理:
CH3OH(g)+ NH3(g) CH3NH2(g)+H2O(g) △H
CH3NH2(g)+H2O(g) △H
①已知键能指断开1mol气态键所吸收的能量或形成1mol气态键所释放的能量。几种化学键的键能如下表所示:
则该合成反应的△H=______________ 。
②一定条件下,在体积相同的甲、乙、丙、丁四个容器中,起始投入物质如下:
达到平衡时,甲、乙、丙、丁容器中的CH3OH转化率由大到小的顺序为_______________ 。
(2) 工业上利用镓(Ga) 与NH3在高温下合成固体半导体材料氮化镓(GaN),其反应原理 为2Ga(s)+2NH3(g) 2GaN(s)+3H2(g) △H=-30.81kJ·mol-1。
2GaN(s)+3H2(g) △H=-30.81kJ·mol-1。
①在密闭容器中充入一定量的Ga与NH3发生反应,实验测得反应体系与温度、压强的相关曲线如图所示。图中A点与C点的化学平衡常数分别为KA和KC,下列关系正确的是_________ (填代号)。

a.纵轴a表示NH3的转化率b.纵轴a 表示NH3的体积分数c.T1<T2d.KA<Kc
②镓在元素周期表位于第四周期第ⅢA 族,化学性质与铝相似。氮化镓性质稳定,不溶于水,但能缓慢溶解在热的NaOH溶液中,该反应的离子方程式为_____________________ 。
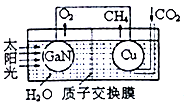
(3) 用氮化镓与铜组成如图所示的人工光合系统,利用该装置成功地以CO2和H2O为原料合成CH4。铜电极表面发生的电极反应式为___________ 。两电极放出O2和CH4相同条件下的体积比为________ ,为提高该人工光合系统的工作效率,可向装置中加入少量的__________ (填“盐酸”或“硫酸”)。
(1) 甲胺(CH3NH2)是合成太阳能敏化剂的原料。工业合成甲胺原理:
CH3OH(g)+ NH3(g)
 CH3NH2(g)+H2O(g) △H
CH3NH2(g)+H2O(g) △H①已知键能指断开1mol气态键所吸收的能量或形成1mol气态键所释放的能量。几种化学键的键能如下表所示:
| 化学键 | C-H | C-O | H-O | N-H | C-N |
| 键能/kJ·mol-1 | 413 | 351 | 463 | 393 | 293 |
②一定条件下,在体积相同的甲、乙、丙、丁四个容器中,起始投入物质如下:
| NH3(g)/mol | CH3OH(g)/mol | 反应条件 | |
| 甲 | 1 | 1 | 498K,恒容 |
| 乙 | 1 | 1 | 598K,恒容 |
| 丙 | 1 | 1 | 598K,恒压 |
| 丁 | 2 | 3 | 598K,恒容 |
(2) 工业上利用镓(Ga) 与NH3在高温下合成固体半导体材料氮化镓(GaN),其反应原理 为2Ga(s)+2NH3(g)
 2GaN(s)+3H2(g) △H=-30.81kJ·mol-1。
2GaN(s)+3H2(g) △H=-30.81kJ·mol-1。①在密闭容器中充入一定量的Ga与NH3发生反应,实验测得反应体系与温度、压强的相关曲线如图所示。图中A点与C点的化学平衡常数分别为KA和KC,下列关系正确的是

a.纵轴a表示NH3的转化率b.纵轴a 表示NH3的体积分数c.T1<T2d.KA<Kc
②镓在元素周期表位于第四周期第ⅢA 族,化学性质与铝相似。氮化镓性质稳定,不溶于水,但能缓慢溶解在热的NaOH溶液中,该反应的离子方程式为

(3) 用氮化镓与铜组成如图所示的人工光合系统,利用该装置成功地以CO2和H2O为原料合成CH4。铜电极表面发生的电极反应式为
您最近一年使用:0次
2018-03-24更新
|
512次组卷
|
3卷引用:山东省烟台市2018届高三下学期高考诊断性测试理综-化学试题
三、填空题 添加题型下试题
填空题
|
适中(0.65)
名校
10. 硫酸锌可用于制造锌钡白、印染媒染剂等。用锌白矿(主要成分为ZnO,还含有FeO、CuO、SiO2等杂质)制备ZnSO4·7H2O的流程如下。
已知:Ksp[Fe(OH)3]=4.0×10−38,Ksp[Cu(OH)2]=2.2×10−20

(1)“滤渣1”的主要成分是__________ (填化学式)。“酸浸”过程中,为了提高锌元素浸出速率,可采取的措施有:①适当提高酸的浓度,②__________ (填一种)。
(2)“氧化”过程中,发生氧化还原反应的离子方程式是___________ 。
(3)“沉淀”过程中,加入ZnO产生Fe(OH)3沉淀的原因是___________ 。
(4)加入适量ZnO固体,若只析出Fe(OH)3沉淀而未析出Cu(OH)2沉淀,且测得沉淀后的溶液中 c(Fe3+)=4.0×10−14 mol/L,此时溶液中c(Cu2+)的取值范围是________ mol/L。
(5)加入适量锌粉的作用是________ 。
(6)由滤液得到ZnSO4•7H2O的操作依次为____ 、过滤、洗涤、干燥。实验室中过滤操作需要使用的玻璃仪器有烧杯、____ 、____ 。
已知:Ksp[Fe(OH)3]=4.0×10−38,Ksp[Cu(OH)2]=2.2×10−20

(1)“滤渣1”的主要成分是
(2)“氧化”过程中,发生氧化还原反应的离子方程式是
(3)“沉淀”过程中,加入ZnO产生Fe(OH)3沉淀的原因是
(4)加入适量ZnO固体,若只析出Fe(OH)3沉淀而未析出Cu(OH)2沉淀,且测得沉淀后的溶液中 c(Fe3+)=4.0×10−14 mol/L,此时溶液中c(Cu2+)的取值范围是
(5)加入适量锌粉的作用是
(6)由滤液得到ZnSO4•7H2O的操作依次为
您最近一年使用:0次
2018-01-27更新
|
761次组卷
|
4卷引用:四川省宜宾市2018届高三第一次诊断性考试理科综合化学试题2
四、解答题 添加题型下试题
解答题-结构与性质
|
较难(0.4)
名校
解题方法
11. 铁氰化钾,化学式为K3[Fe(CN)6],主要应用于制药、电镀、造纸、钢铁生产等工业。其煅烧分解生成KCN、FeC2、N2、(CN)2等物质。
(1)基态K原子核外电子排布简写式为___________ 。 K3[Fe(CN)6]中所涉及的元素的基态原子核外未成对电子数最多的是_________ ,各元素的第一电离能由大到小的顺序为_________ 。
(2)(CN)2分子中存在碳碳键,则分子中σ键与π键数目之比为_______ 。KCN与盐酸作用可生成HCN,HCN的中心原子的杂化轨道类型为_________ 。
(3)CO能与金属Fe形成Fe(CO)5,该化合物熔点为253 K,沸点为为376 K,其固体属于_____ 晶体。
(4)右图是金属单质常见的两种堆积方式的晶胞模型。
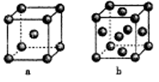
①铁采纳的是a堆积方式.铁原子的配位数为_____ ,该晶体中原子总体积占晶体体积的比值为____ (用含π的最简代数式表示)。
②常见的金属铝采纳的是b堆积方式,铝原子的半径为r pm,则其晶体密度为_____ g·cm-3(用含有r、NA的最简代数式表示)。
(1)基态K原子核外电子排布简写式为
(2)(CN)2分子中存在碳碳键,则分子中σ键与π键数目之比为
(3)CO能与金属Fe形成Fe(CO)5,该化合物熔点为253 K,沸点为为376 K,其固体属于
(4)右图是金属单质常见的两种堆积方式的晶胞模型。

①铁采纳的是a堆积方式.铁原子的配位数为
②常见的金属铝采纳的是b堆积方式,铝原子的半径为r pm,则其晶体密度为
您最近一年使用:0次
2017-12-28更新
|
642次组卷
|
3卷引用:四川省内江市2018届高三第一次模拟考试理科综合化学试题
解答题-有机推断题
|
适中(0.65)
名校
12. 聚合物H (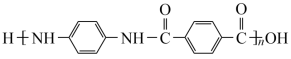 )是一种聚酰胺纤维,广泛用于各种刹车片,其合成路线如下:
)是一种聚酰胺纤维,广泛用于各种刹车片,其合成路线如下:
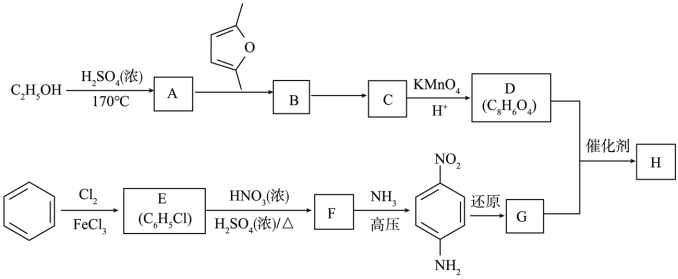
已知:①C、D、G均为芳香族化合物,分子中均只含两种不同化学环境的氢原子。
②Diels﹣Alder反应: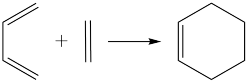 。
。
(1)生成A的反应类型是________ 。D的名称是______ 。F中所含官能团的名称是______ 。
(2)B的结构简式是______ ;“B→C”的反应中,除C外,另外一种产物是______ 。
(3)D+G→H的化学方程式是___________________________________________ 。
(4)Q是D的同系物,相对分子质量比D大14,则Q可能的结构有_____ 种,其中核磁共振氢谱有4组峰,且峰面积比为1:2:2:3的结构简式为__________________________________ (任写一种)。
(5)已知:乙炔与1,3﹣丁二烯也能发生Diels﹣Alder反应。请以1,3﹣丁二烯和乙炔为原料,选用必要的无机试剂合成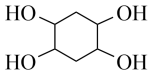 ,写出合成路线
,写出合成路线_______________________ (用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)。
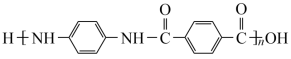 )是一种聚酰胺纤维,广泛用于各种刹车片,其合成路线如下:
)是一种聚酰胺纤维,广泛用于各种刹车片,其合成路线如下:
已知:①C、D、G均为芳香族化合物,分子中均只含两种不同化学环境的氢原子。
②Diels﹣Alder反应:
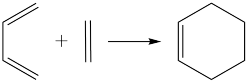 。
。(1)生成A的反应类型是
(2)B的结构简式是
(3)D+G→H的化学方程式是
(4)Q是D的同系物,相对分子质量比D大14,则Q可能的结构有
(5)已知:乙炔与1,3﹣丁二烯也能发生Diels﹣Alder反应。请以1,3﹣丁二烯和乙炔为原料,选用必要的无机试剂合成
 ,写出合成路线
,写出合成路线
您最近一年使用:0次
2020-04-28更新
|
331次组卷
|
19卷引用:四川省宜宾市高2018届高三第三次诊断考试化学试题
四川省宜宾市高2018届高三第三次诊断考试化学试题【全国百强校】湖北省荆州中学2018届高三全真模拟考试(二)理综化学试题辽宁省沈阳铁路实验中学2017-2018学年高二6月月考化学试题【全国校级联考】广东省中山一中、仲元中学等七校2019届高三第一次(8月)联考理综化学试题【全国百强校】宁夏回族自治区银川市第一中学2019届高三上学期第三次月考理科综合化学试题【全国百强校】甘肃省兰州市第一中学2019届高三上学期期中考试化学试题内蒙古巴彦淖尔一中2019届高三上学期第二次月考理综化学试题西藏自治区林芝二高2019届高三上学期第四次月考化学试题【市级联考】辽宁省抚顺市2019届高三下学期第一次模拟考试理科综合化学试题四川省泸州市泸县第一中学2019届高三下学期三诊模拟理科综合化学试题【全国百强校】河北省武邑中学2019届高三下学期第一次模拟考试化学试题【校级联考】湖北省宜昌市夷陵中学、襄阳五中、钟祥一中2019届高三5月模拟考试理科综合化学试题安徽省宿州市2020年高三年级理综模拟卷(四)化学试题(已下线)《2020年新高考政策解读与配套资源》2020年山东新高考化学全真模拟卷(三)(已下线)考点19 有机合成与推断-2020年高考化学命题预测与模拟试题分类精编山东省青岛市平度市2020届高三3月高考模拟化学试卷山东省济南市大学城实验高级中学2021届高三1月阶段性考试化学试题云南民族大学附属中学2019-2020学年高二下学期期中考试化学试题海南省琼海市嘉积第三中学2021-2022学年高三下学期第三次月考化学科试题
试卷分析
整体难度:适中
考查范围:常见无机物及其应用、有机化学基础、认识化学科学、化学实验基础、物质结构与性质、化学反应原理
试卷题型(共 12题)
题型
数量
单选题
7
解答题
4
填空题
1
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.65 | 二氧化硅的组成、结构 淀粉、纤维素的水解 蛋白质 | |
| 2 | 0.65 | 结合气体物质与NA相关推算 结合氧化还原反应知识与NA相关推算 | |
| 3 | 0.65 | 有机反应类型 有机分子中原子共面的判断 芳香烃空间结构 多官能团有机物的结构与性质 | |
| 4 | 0.65 | 物质含量的测定 化学实验探究 物质性质实验方案的设计 | |
| 5 | 0.65 | 元素周期律、元素周期表的推断 根据物质性质进行元素种类推断 “位构性”关系理解及应用 结合物质计算的元素周期律、元素周期表相关推断 | |
| 6 | 0.65 | 电解原理的应用 电解原理的理解及判断 电解池电极反应式及化学方程式的书写与判断 | |
| 7 | 0.65 | 盐溶液中微粒间的电荷守恒、物料守恒、质子守恒原理 盐溶液中离子浓度大小的比较 | |
| 二、解答题 | |||
| 8 | 0.65 | 仪器使用与实验安全 物质的分离、提纯 物质制备的探究 综合实验设计与评价 | 实验探究题 |
| 9 | 0.65 | 根据△H=反应物的键能之和-生成物的键能之和进行计算 化学平衡的移动及其影响因素 化学平衡的有关计算 原电池 | 原理综合题 |
| 11 | 0.4 | 电离能 利用杂化轨道理论判断化学键杂化类型 配合物的结构与性质 晶胞的有关计算 | 结构与性质 |
| 12 | 0.65 | 羧酸 根据题给物质选择合适合成路线 有机推断综合考查 酰胺的性质与应用 | 有机推断题 |
| 三、填空题 | |||
| 10 | 0.65 | 溶度积常数相关计算 | |



