河南省九师联盟5月联考-理综化学试题
河南
高三
模拟预测
2020-05-24
1134次
整体难度:
适中
考查范围:
常见无机物及其应用、有机化学基础、认识化学科学、物质结构与性质、化学反应原理、化学实验基础
河南省九师联盟5月联考-理综化学试题
河南
高三
模拟预测
2020-05-24
1134次
整体难度:
适中
考查范围:
常见无机物及其应用、有机化学基础、认识化学科学、物质结构与性质、化学反应原理、化学实验基础
一、单选题 添加题型下试题
单选题
|
较易(0.85)
名校
解题方法
1. 苏颂《本草图经》有关不灰木(火浣布)有如下描述:“不灰木,出上党,今泽、潞山中皆有之,盖石类也。其色青白如烂木,烧之不燃,以此得名。或云滑石之根也,出滑石[Mg3(Si4O10)(OH)2]处皆有”。“不灰木”成分可能是
| A.纤维素 | B.硅酸盐 | C.氧化铁 | D.动物毛皮 |
您最近一年使用:0次
2020-05-22更新
|
228次组卷
|
4卷引用:河南省九师联盟5月联考-理综化学试题
河南省九师联盟5月联考-理综化学试题(已下线)小题必刷17 碳、硅与无机非金属材料——2021年高考化学一轮复习小题必刷(通用版)吉林省松原市实验高级中学2021届高三5月月考化学试题甘肃省嘉峪关市第一中学2020-2021学年高一下学期期中考试化学试题
单选题
|
适中(0.65)
名校
解题方法
2. 化合物(a)与(b)的结构简式如图所示。下列叙述正确的是
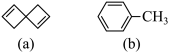

| A.(a)与(b)互为同分异构体 |
| B.(a)分子中所有碳原子均共面 |
| C.(b)的一氯取代物共有3种 |
| D.(a)与(b)均能使Br2/CC14褪色 |
【知识点】 同分异构体的数目的确定解读 有机分子中原子共面的判断解读
您最近一年使用:0次
2020-05-22更新
|
606次组卷
|
7卷引用:河南省九师联盟5月联考-理综化学试题
河南省九师联盟5月联考-理综化学试题四川省阆中中学2020届高三全景模拟(最后一考)理综化学试题吉林省吉林市2021届高三上学期第二次调研测试(1月)化学试题云南省玉溪市一中2020-2021学年高二下学期4月月考化学试题(已下线)2021年高考化学押题预测卷(新课标Ⅲ卷)(02)(含考试版、答题卡、参考答案、全解全析)(已下线)重点6 常见有机物及其应用-2021年高考化学【热点·重点·难点】专练(新高考)深圳市宝安区2021-2022学年高三上学期第一次调研化学试题
单选题
|
适中(0.65)
3. 设NA为阿伏加 德罗常数的值。下列说法正确的是
| A.标准状况下,2.24L三氯甲烷中含氢原子数为0.1NA |
| B.0.1mol•L-1Na2SO3溶液中,含硫元素的粒子数目之和为0.1NA |
| C.8.0gNH4NO3发生反应5NH4NO3= 4N2+2HNO3+9H2O,转移电子数为0.3NA |
D.0.1molP35Cl3与足量37Cl2发生反应:PCl3+Cl2 PCl5,产物中P—37Cl键数为0.2NA PCl5,产物中P—37Cl键数为0.2NA |
【知识点】 阿伏加德罗常数的应用解读
您最近一年使用:0次
单选题
|
适中(0.65)
解题方法
4. 硼烯是继石墨烯之后又一种“神奇纳米材料”,具有优良的导电、导热性能。科学家已成功合成多种结构的硼烯,如图为“皱褶”式硼烯的结构,下列说法正确的是


| A.“皱褶”式硼烯中含B、H两种元素 |
| B.“皱褶”式硼烯中硼原子达到8电子稳定结构 |
| C.硼的最高价氧化物对应水化物的酸性比碳酸的强 |
| D.硼烯有望代替石墨烯作锂离子电池的电极材料 |
【知识点】 同周期元素性质递变规律理解及应用解读 核外电子排布规律解读
您最近一年使用:0次
单选题
|
适中(0.65)
名校
解题方法
5. 等体积两种一元酸“酸1”和“酸2”分别用等浓度的KOH溶液滴定,滴定曲线如图所示。下列说法错误的是


| A.“酸1”比“酸2”的酸性强 |
| B.“酸2”的浓度为0.01mol•L-1 |
| C.“酸2”的Ka的数量级约为10-5 |
| D.滴定“酸1”和“酸2”均可用酚酞作指示剂 |
【知识点】 酸碱中和滴定的综合考查解读
您最近一年使用:0次
2020-05-22更新
|
294次组卷
|
5卷引用:河南省九师联盟5月联考-理综化学试题
河南省九师联盟5月联考-理综化学试题山西大学附属中学2020-2021学年高二上学期期中考试化学试题选择性必修1(SJ)专题3易错疑难集训(一)(已下线)考点27 水的电离和溶液的pH-备战2023年高考化学一轮复习考点帮(全国通用)河南省叶县高级中学2022-2023学年高二上学期9月月考化学试题
单选题
|
适中(0.65)
名校
解题方法
6. 某新型离子电池电解质的化学组成为 W5.7XY4.7Z1.3(各元素的化合价均为最高正价或最低负价),已知 W、X、Y、Z为原子序数依次增大的短周期主族元素,X、Y、Z位于同周期,W 原子的核外电子总数与Y原子的最外层电子数之和等于9,Y 的最高正价与最低负价代数和为4。下列说法错误的是
| A.常见单质的沸点:Y>Z |
| B.W 的单质能与冷水反应 |
| C.X与Z原子序数之和是Y 核电荷数的2倍 |
| D.W、X、Y、Z的简单离子均能促进水的电离 |
【知识点】 元素周期律、元素周期表的推断 “位构性”关系理解及应用解读
您最近一年使用:0次
2020-05-22更新
|
242次组卷
|
2卷引用:河南省九师联盟5月联考-理综化学试题
单选题
|
适中(0.65)
解题方法
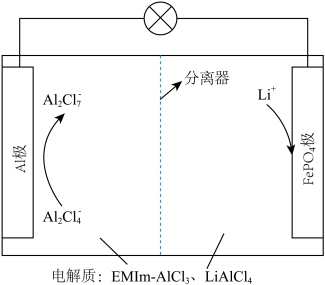
7. 一种用离子液体作电解液的混合动力电池放电原理图如图所示,已知充放电时的电池反应为4LiA12C17+3LiFePO4(s) A1+3FePO4+7LiA1C14。下列说法正确的是
A1+3FePO4+7LiA1C14。下列说法正确的是
 A1+3FePO4+7LiA1C14。下列说法正确的是
A1+3FePO4+7LiA1C14。下列说法正确的是
| A.放电时,向正极迁移的是 Al3+ |
| B.放电时,A1极上的电势比FePO4极上的高 |
| C.充电时,阴极反应式:A12C17-+6e- = 2A1+7C1- |
| D.充电时,阳极反应式:LiFePO4—e- = FePO4+Li+ |
【知识点】 原电池电极反应式书写解读 二次电池
您最近一年使用:0次
二、解答题 添加题型下试题
8. 以含镍废硫酸盐(含 Ni2+ 、Fe2+ 、Cu2+ 、Co2+ 、A13+ 、Mn2+ 、Cr3+ 、Mg2+ 、Zn2+ 等)为原料制取NiSO4·6H2O 的工艺流程如下:
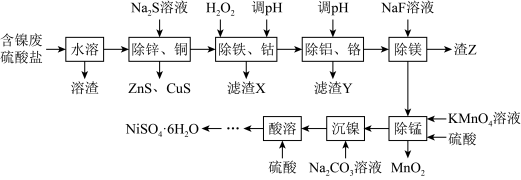
相关金属离子形成氢氧化物沉淀的pH 范围如下:
回答下列问题:
(1)已知1gKsp(CuS)= -47.6,1gKsp(ZnS)= -23.8,则反应ZnS+Cu2+ CuS+Zn2+的平衡常数对数值1gK=
CuS+Zn2+的平衡常数对数值1gK= ________________________ 。
(2)“除铁、钴”时,加入H2O2的目的是______________ ,得到的渣X为________ 。
(3) “除铝、铬”时,调pH 范围为_________ ;滤渣Y 中含Cr(OH)3,其性质与 A1(OH)3 类似,写出Cr(OH)3与NaOH反应的化学方程式: __________________ 。
(4)“除锰”时,发生反应的离子方程式为___________________________ 。
(5)“酸溶”得到溶液制备 NiSO4·6H2O晶体,还需进行的操作工艺是___________ 。

相关金属离子形成氢氧化物沉淀的pH 范围如下:
| 金属离子 | Co2+ | Co3+ | Fe2+ | Fe3+ | A13+ | Cr3+ | Ni2+ |
| 开始沉淀的pH | 7.2 | 0.23 | 6.3 | 1.5 | 4.1 | 4.3 | 6.9 |
| 沉淀完全的pH | 9.2 | 1.1 | 8.3 | 2.8 | 5.4 | 5.6 | 8.9 |
回答下列问题:
(1)已知1gKsp(CuS)= -47.6,1gKsp(ZnS)= -23.8,则反应ZnS+Cu2+
 CuS+Zn2+的平衡常数对数值1gK=
CuS+Zn2+的平衡常数对数值1gK= (2)“除铁、钴”时,加入H2O2的目的是
(3) “除铝、铬”时,调pH 范围为
(4)“除锰”时,发生反应的离子方程式为
(5)“酸溶”得到溶液制备 NiSO4·6H2O晶体,还需进行的操作工艺是
您最近一年使用:0次
解答题-实验探究题
|
适中(0.65)
解题方法
9. CS(NH2)2(硫脲,白色而有光泽的晶体,溶于水,20℃时溶解度为13.6g;在150 ℃时转变成 NH4SCN)是用于制造药物、染料、金属矿物的浮选剂等的原料。某化学实验小组同学用Ca(HS)2与CaCN2(石灰氮)合成硫脲并探究其性质

(1)制备Ca(HS)2溶液,所用装置如图(已知酸性:H2CO3>H2S):
①装置a中反应发生的操作为______________________________________ ;装置b中盛放的试剂是__________________ 。
②装置c中的长直导管的作用是____________________________________ ,三颈烧瓶中通入CO2 不能过量,原因是 ______________________________ 。
(2)制备硫脲:将CaCN2与Ca(HS)2溶液混合,加热至80℃时,可合成硫脲,同时生成一种常见的碱,合适的加热方式是___________________________ ;该反应的化学方程式为___________________________________________________________________ 。
(3)探究硫脲的性质:
①取少量硫脲溶于水并加热,验证有NH4SCN生成,可用的试剂是_____________ (填化学式,下同)
②向盛有少量硫脲的试管中加入NaOH溶液,有NH3放出,检验该气体的方法为__________________________________________________ 。
③可用酸性KMnO4溶液滴定硫脲,已知MnO4- 被还原为Mn2+,CS(NH2)2被氧化为CO2、N2及SO42— ,该反应中氧化剂与还原剂的物质的量之比为_____________ 。

(1)制备Ca(HS)2溶液,所用装置如图(已知酸性:H2CO3>H2S):
①装置a中反应发生的操作为
②装置c中的长直导管的作用是
(2)制备硫脲:将CaCN2与Ca(HS)2溶液混合,加热至80℃时,可合成硫脲,同时生成一种常见的碱,合适的加热方式是
(3)探究硫脲的性质:
①取少量硫脲溶于水并加热,验证有NH4SCN生成,可用的试剂是
②向盛有少量硫脲的试管中加入NaOH溶液,有NH3放出,检验该气体的方法为
③可用酸性KMnO4溶液滴定硫脲,已知MnO4- 被还原为Mn2+,CS(NH2)2被氧化为CO2、N2及SO42— ,该反应中氧化剂与还原剂的物质的量之比为
您最近一年使用:0次
三、填空题 添加题型下试题
填空题
|
较难(0.4)
名校
10. 热化学碘硫循环可用于大规模制氢气,HI分解和SO2水溶液还原I2均是其中的主要反应。回答下列问题:
(1)碘硫热化学循环中,SO2的水溶液还原I2的反应包括:SO2+I2+2H2O 3H++HSO4- +2I- 、I-+I2
3H++HSO4- +2I- 、I-+I2 I3-。若起始时n(I2)=n(SO2)=1mol,I- 、I3- 、H+ 、HSO4-的物质的量随(
I3-。若起始时n(I2)=n(SO2)=1mol,I- 、I3- 、H+ 、HSO4-的物质的量随( )的变化如图所示:
)的变化如图所示:

图中表示的微粒:a为_____________ ,d为____________________ 。
(2)起始时 HI的物质的量为1mol,总压强为0.1MPa下,发生反应 HI(g)
 H2(g)+
H2(g)+ I2(g) 平衡时各物质的物质的量随温度变化如图所示:
I2(g) 平衡时各物质的物质的量随温度变化如图所示:

①该反应的△H__________________ (“>”或“<”)0。
②600℃时,平衡分压p(I2)=______ MPa,反应的平衡常数Kp=_____________ (Kp为以分压表示的平衡常数)。
(3)反应 H2(g)+I2(g) 2HI(g)的反应机理如下:
2HI(g)的反应机理如下:
第一步:I2 2I(快速平衡)
2I(快速平衡)
第二步:I+H2 H2I(快速平衡)
H2I(快速平衡)
第三步:H2I+I 2HI (慢反应)
2HI (慢反应)
①第一步反应_____________ (填 “放出”或“吸收”)能量。
②只需一步完成的反应称为基元反应,基元反应如aA+dD = gG+hH 的速率方程,v= kca(A)•cd(D),k为常数;非基元反应由多个基元反应组成,非基元反应的速率方程可由反应机理推定。H2(g)与I2(g)反应生成 HI(g)的速率方程为v=________ (用含k1、k-1、k2…的代数式表示)。
(1)碘硫热化学循环中,SO2的水溶液还原I2的反应包括:SO2+I2+2H2O
 3H++HSO4- +2I- 、I-+I2
3H++HSO4- +2I- 、I-+I2 I3-。若起始时n(I2)=n(SO2)=1mol,I- 、I3- 、H+ 、HSO4-的物质的量随(
I3-。若起始时n(I2)=n(SO2)=1mol,I- 、I3- 、H+ 、HSO4-的物质的量随( )的变化如图所示:
)的变化如图所示:
图中表示的微粒:a为
(2)起始时 HI的物质的量为1mol,总压强为0.1MPa下,发生反应 HI(g)

 H2(g)+
H2(g)+ I2(g) 平衡时各物质的物质的量随温度变化如图所示:
I2(g) 平衡时各物质的物质的量随温度变化如图所示:
①该反应的△H
②600℃时,平衡分压p(I2)=
(3)反应 H2(g)+I2(g)
 2HI(g)的反应机理如下:
2HI(g)的反应机理如下:第一步:I2
 2I(快速平衡)
2I(快速平衡) 第二步:I+H2
 H2I(快速平衡)
H2I(快速平衡)第三步:H2I+I
 2HI (慢反应)
2HI (慢反应)①第一步反应
②只需一步完成的反应称为基元反应,基元反应如aA+dD = gG+hH 的速率方程,v= kca(A)•cd(D),k为常数;非基元反应由多个基元反应组成,非基元反应的速率方程可由反应机理推定。H2(g)与I2(g)反应生成 HI(g)的速率方程为v=
【知识点】 化学平衡的移动解读 化学平衡常数的有关计算解读
您最近一年使用:0次
2020-05-22更新
|
782次组卷
|
3卷引用:河南省九师联盟5月联考-理综化学试题
四、解答题 添加题型下试题
解答题-结构与性质
|
适中(0.65)
名校
解题方法
11. iCo2S4@g-C3N4-CNT是一类很有发展前途的化合物电催化剂。回答下列问题:
(1)基态Co2+的价层电子排布图(轨道表达式)为_________ ;基态S原子电子占据最高能级的电子云轮廓图为______________ 形。
(2)g-C3N4(结构片段如图1,环上化学键与苯环类似)可由三聚氰胺(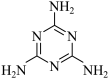 )与(NH4)2SO4共热制得。
)与(NH4)2SO4共热制得。
①g-C3N4分子中环上的氮原子、碳原子杂化方式依次为________ 、_____ 。
②SO42—的空间构型为__________________ 。
③三聚氰胺分子中含σ键______ 个,它不溶于冷水,溶于热水,其主要原因是 ______________________ 。
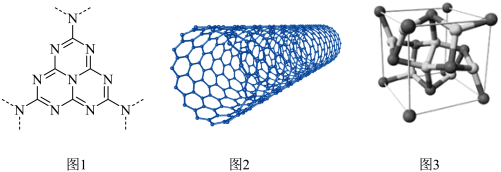
(3)碳纳米管(CNT,结构如图2)具有良好的导电性,其原因是______________ 。
(4)CoS2具有 AB2型立方结构(如图3),晶胞参数为553.4pm。设NA为阿伏加 德罗常数的值,则晶体的密度为________________ g•cm—3(列出计算式) 。
(1)基态Co2+的价层电子排布图(轨道表达式)为
(2)g-C3N4(结构片段如图1,环上化学键与苯环类似)可由三聚氰胺(
 )与(NH4)2SO4共热制得。
)与(NH4)2SO4共热制得。①g-C3N4分子中环上的氮原子、碳原子杂化方式依次为
②SO42—的空间构型为
③三聚氰胺分子中含σ键

(3)碳纳米管(CNT,结构如图2)具有良好的导电性,其原因是
(4)CoS2具有 AB2型立方结构(如图3),晶胞参数为553.4pm。设NA为阿伏加 德罗常数的值,则晶体的密度为
您最近一年使用:0次
2020-05-22更新
|
333次组卷
|
2卷引用:河南省九师联盟5月联考-理综化学试题
解答题-有机推断题
|
适中(0.65)
名校
解题方法
12. 孟鲁司特钠可用于抗新型冠状病毒肺炎,其制备中间体G 的一种合成路线如下:
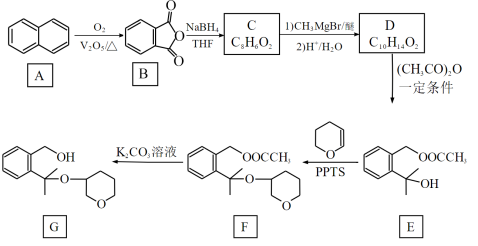
已知:① B、C除苯环外还含有一个五元环,D的苯环上只有两个取代基;
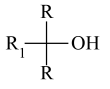
②RX RMgX
RMgX
回答下列问题:
(1)A 的化学名称是____________________ 。
(2)F中含氧官能团名称是____________________________ 。
(3)B的结构简式为______________________________________ 。
(4)D生成E同时生成乙酸的化学方程式为___________________________________ 。
(5)E生成F的反应类型是________________ 。
(6)化合物 W 与G 互为同分异构体,能发生水解反应,其核磁共振氢谱有四组峰且峰面积之比为9:9:2:2,则 W 的结构简式为_____________________ (写一种) 。
(7)设计以苯甲酸和乙醇为起始原料制备3-苯基-3-戊醇(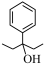 )的合成路线:
)的合成路线: _____________________________________________ (无机试剂及有机溶剂任用) 。

已知:① B、C除苯环外还含有一个五元环,D的苯环上只有两个取代基;
②RX
 RMgX
RMgX

回答下列问题:
(1)A 的化学名称是
(2)F中含氧官能团名称是
(3)B的结构简式为
(4)D生成E同时生成乙酸的化学方程式为
(5)E生成F的反应类型是
(6)化合物 W 与G 互为同分异构体,能发生水解反应,其核磁共振氢谱有四组峰且峰面积之比为9:9:2:2,则 W 的结构简式为
(7)设计以苯甲酸和乙醇为起始原料制备3-苯基-3-戊醇(
 )的合成路线:
)的合成路线:
您最近一年使用:0次
试卷分析
整体难度:适中
考查范围:常见无机物及其应用、有机化学基础、认识化学科学、物质结构与性质、化学反应原理、化学实验基础
试卷题型(共 12题)
题型
数量
单选题
7
解答题
4
填空题
1
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.85 | 几种常见硅酸盐矿物 | |
| 2 | 0.65 | 同分异构体的数目的确定 有机分子中原子共面的判断 | |
| 3 | 0.65 | 阿伏加德罗常数的应用 | |
| 4 | 0.65 | 同周期元素性质递变规律理解及应用 核外电子排布规律 | |
| 5 | 0.65 | 酸碱中和滴定的综合考查 | |
| 6 | 0.65 | 元素周期律、元素周期表的推断 “位构性”关系理解及应用 | |
| 7 | 0.65 | 原电池电极反应式书写 二次电池 | |
| 二、解答题 | |||
| 8 | 0.65 | 沉淀转化 溶度积常数相关计算 物质分离、提纯综合应用 常见无机物的制备 | 工业流程题 |
| 9 | 0.65 | 常见无机物的制备 物质制备的探究 综合实验设计与评价 | 实验探究题 |
| 11 | 0.65 | 物质结构与性质综合考查 电子排布式 利用杂化轨道理论判断化学键杂化类型 晶胞的有关计算 | 结构与性质 |
| 12 | 0.65 | 有机推断综合考查 | 有机推断题 |
| 三、填空题 | |||
| 10 | 0.4 | 化学平衡的移动 化学平衡常数的有关计算 | |



