黑龙江农垦建三江管理局第一高级中学2020-2021学年高一上学期12月月考化学试题
黑龙江
高一
阶段练习
2021-01-09
230次
整体难度:
容易
考查范围:
认识化学科学、物质结构与性质、常见无机物及其应用、化学实验基础、化学与STSE
一、单选题 添加题型下试题
| A.SO2、SiO2、CaO均为酸性氧化物 | B.稀豆浆、鸡蛋清、氯化铁溶液均为胶体 |
| C.烧碱、硫酸、酒精均为电解质 | D.澄清石灰水、盐酸、氨水均为混合物 |
【知识点】 酸、碱、盐、氧化物的概念及其相互联系解读 胶体 电解质与非电解质
A.Cu2+、Na+、Cl-、 | B.Ag+、K+、 、Cl- 、Cl- |
C.Mg2+、Na+、 、Cl- 、Cl- | D.Na+、K+、Cl-、 |
【知识点】 限定条件下的离子共存解读
| A.Na2SO4溶液加入少量BaCl2固体 | B.Ba(OH)2溶液加入少量CuSO4固体 |
| C.NaOH溶液通入少量MgCl2固体 | D.H2O中加入少量NaCl固体 |
| A.I->Fe2+>Cl->SO2 | B.Cl->Fe2+>SO2>I- |
| C.Fe2+>I->Cl->SO2 | D.SO2>I->Fe2+>Cl- |
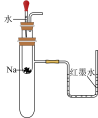
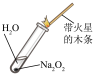
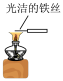
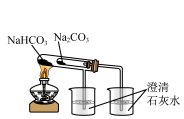
7. 下列实验装置能达到实验目的的是
①验证 和水反应是否为放热反应 和水反应是否为放热反应 | ②检验 与 与 反应有 反应有 生成 生成 | ③观察 的焰色试验 的焰色试验 | ④比较 、 、 的稳定性 的稳定性 |
|
|
|
|
| A.①② | B.①③ | C.②④ | D.③④ |
| A.10 mL 0.1 mol/L的AlCl3溶液 | B.20 mL 0.1mol/L CaCl2溶液 |
| C.30 mL 0.2 mol/L的KCl溶液 | D.100 mL 0.25 mol/L的NaCl溶液 |
【知识点】 物质的量浓度计算-与溶质成分有关的计算解读
| A.Ag失去电子 | B.H2O是氧化产物 |
| C.X为Ag2S | D.每生成1molX转移电子数2NA |
【知识点】 氧化还原反应基本概念
| A.向水中通入氯气:Cl2+H2O⇌2H++Cl﹣+ClO﹣ |
B.氯化铝溶液中加入过量氨水:Al3++4NH3·H2O= +4 +4 +2H2O +2H2O |
C.碳酸氢钠溶液加过量澄清石灰水:2HCO +Ca2++2OH﹣═CaCO3↓+2H2O+CO +Ca2++2OH﹣═CaCO3↓+2H2O+CO |
| D.金属钠与硫酸铜溶液反应:2Na+2H2O+Cu2+═2Na++Cu(OH)2↓+H2↑ |
【知识点】 离子方程式的正误判断解读
A.向饱和 溶液中通入过量的 溶液中通入过量的 |
B.向澄清石灰水中持续通入 |
C.向 溶液中逐滴加入过量的稀 溶液中逐滴加入过量的稀 溶液 溶液 |
D.向 胶体中逐滴加入过量的稀盐酸 胶体中逐滴加入过量的稀盐酸 |
| A.足量MnO2与40 mL 10 mol·L-1的浓盐酸充分反应,生成的氯气分子数为0.1NA |
| B.标况下,11.2L H2O中含10NA个质子 |
| C.标况下,2.24LCO和CO2混合气体中含有的碳原子数目为0.1NA |
| D.1L0.1mol/LNaHCO3溶液中含有氧原子数0.3NA |
| A.取金属钠可以用手拿,实验用不完的金属钠应该放在废液缸中或水槽中 |
| B.在蒸发皿中完成金属钠燃烧实验后发现生成黑色固体氧化钠 |
| C.用镊子夹住一小块铝箔,在酒精灯内焰上加热至熔化,轻轻晃动有液态铝滴落 |
| D.金属钠着火时用干沙土灭火 |
【知识点】 钠的化学性质 铝与氧气的反应解读 氧化铝的物理性质与用途解读
A.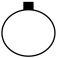 | B. | C. | D. |
【知识点】 阿伏加德罗定律 阿伏加德罗定律及其推论解读 阿伏加德罗定律的应用解读
| A.硝酸银溶液 | B.硫酸铜溶液 | C.稀硫酸 | D.硫酸铁溶液 |
【知识点】 铁与非氧化性酸的反应解读 铁与铁离子反应解读
| A.Fe3O4是黑色固体,有磁性 |
| B.Fe2O3既不溶于水也不溶于酸 |
| C.FeO是碱性氧化物,可与H2O反应生成Fe(OH)2 |
| D.FeO、Fe2O3、Fe3O4中铁的化合价相同 |
【知识点】 铁的氧化物
二、填空题 添加题型下试题
①H2SO4
②NH4NO3
(2)写出下列反应的离子方程式
①氢氧化钡和稀硫酸反应:
②碳酸氢钠溶液和稀盐酸反应:
(3)宇航员常用过氧化钠作供氧剂,写出过氧化钠与二氧化碳反应的化学方程式并用双线桥法表示电子转移的方向和数目:
(4)将氯气溶于一定浓度的氢氧化钠溶液可制得“84消毒液”,反应的离子方程式为
(5)有以下物质:①铁红②Al③C④稀硫酸⑤浓硫酸⑥NaOH溶液⑦Al2(SO4)3既能跟④又能跟⑥反应的是
(2)在标准状况下,8gCO2和CO组成的混合气体,其体积为5.6L,则此混合气体中CO2的质量分数为
(3)用托盘天平称取5.0gCuSO4·5H2O晶体,溶于水配成100mL溶液,其物质的量浓度为
Ⅱ.欲用
 的浓硫酸(密度为
的浓硫酸(密度为 )配制成浓度为
)配制成浓度为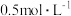 的稀硫酸480ml。
的稀硫酸480ml。(1)选用的主要仪器有:①玻璃棒,②烧杯,③量筒,④胶头滴管,⑤
(2)请将下列各操作相应的序号按要求填在横线上。
A.用量筒量取浓硫酸 B.反复颠倒摇匀 C.用胶头滴管加蒸馏水至刻度线
D.稀释浓硫酸 E.将溶液转入容量瓶
其正确的操作顺序依次为
(3)简要回答下列问题:
①所需浓硫酸的体积为
②定容时必须使溶液凹液面与刻度线相切,若仰视会使浓度
【知识点】 物质的量浓度的计算 配制一定物质的量浓度溶液的综合考查解读
三、解答题 添加题型下试题

按要求回答下列问题。
(1)写出A装置制取氯气的化学方程式:
(2)①装置B中盛放的试剂名称为
②装置D和E中出现的不同现象说明:
③写出装置G中发生反应的离子方程式
(3)实验室也可以用高锰酸钾和浓盐酸反应制取氯气,反应的化学方程式如下:
2KMnO4+16HCl(浓)=2KCl+MnCl2+5Cl2↑+8H2O
①该反应中浓盐酸体现出来的性质为
②氧化剂与还原剂之比是
③若反应中转移了0.4mol电子,则产生的气体在标准状况下体积为
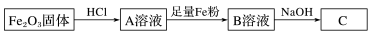
(1)向A、B溶液中分别滴入几滴KSCN溶液, A溶液颜色:
(2)写出上述过程中有关反应的离子方程式:A→B
(3)B→C(暴露在空气中)可看到的现象是
(4)将A的饱和溶液制成胶体的操作
【知识点】 铁三角转化条件分析及判断解读
试卷分析
试卷题型(共 22题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.94 | 酸、碱、盐、氧化物的概念及其相互联系 胶体 电解质与非电解质 | |
| 2 | 0.94 | 几组常见同素异形体 “四素”比较 | |
| 3 | 0.85 | 限定条件下的离子共存 | |
| 4 | 0.85 | 氧化还原反应的规律 | |
| 5 | 0.85 | 物质水溶液的导电性 | |
| 6 | 0.85 | 常见氧化剂与还原剂 氧化性、还原性强弱的比较 氧化还原反应的规律 | |
| 7 | 0.65 | 焰色试验 过氧化钠与水的反应 碳酸钠与碳酸氢钠性质的比较 物质性质实验方案的设计 | |
| 8 | 0.85 | 物质的量浓度计算-与溶质成分有关的计算 | |
| 9 | 0.94 | 氧化还原反应基本概念 | |
| 10 | 0.65 | 离子方程式的正误判断 | |
| 11 | 0.85 | 胶体的性质和应用 碳酸钠与碳酸氢钠的相互转化 氢氧化铝与强碱反应 铝盐与强碱溶液反应 | |
| 12 | 0.94 | 铁合金 铜合金 金属材料 常见合金的组成 | |
| 13 | 0.65 | 物质的转化 铁盐 | |
| 14 | 0.85 | 阿伏加德罗常数的求算 阿伏加德罗常数的应用 结合物质结构基础知识与NA相关推算 | |
| 15 | 0.85 | 钠的化学性质 铝与氧气的反应 氧化铝的物理性质与用途 | |
| 16 | 0.94 | 阿伏加德罗定律 阿伏加德罗定律及其推论 阿伏加德罗定律的应用 | |
| 17 | 0.94 | 铁与非氧化性酸的反应 铁与铁离子反应 | |
| 18 | 0.94 | 铁的氧化物 | |
| 二、填空题 | |||
| 19 | 0.85 | 离子方程式的书写 单线桥、双线桥分析氧化还原反应 氯气与碱溶液反应 铝与强碱溶液反应 | |
| 20 | 0.85 | 物质的量浓度的计算 配制一定物质的量浓度溶液的综合考查 | |
| 三、解答题 | |||
| 21 | 0.65 | 氯气的化学性质 氯气的实验室制法 | 实验探究题 |
| 22 | 0.85 | 铁三角转化条件分析及判断 | 实验探究题 |


 、
、
 、
、 → CO2
→ CO2