广东省梅州市大埔县虎山中学2021-2022学年高二上学期第一次段考(10月)化学试题
广东
高二
阶段练习
2021-11-04
49次
整体难度:
容易
考查范围:
化学反应原理、竞赛
广东省梅州市大埔县虎山中学2021-2022学年高二上学期第一次段考(10月)化学试题
广东
高二
阶段练习
2021-11-04
49次
整体难度:
容易
考查范围:
化学反应原理、竞赛
一、单选题 添加题型下试题
单选题
|
较易(0.85)
名校
解题方法
1. 下列事实能说明影响化学反应速率的决定性因素是反应物本身性质的是
| A.Cu能与浓硝酸反应,但不能与浓盐酸反应 |
| B.Cu与浓硝酸反应比与稀硝酸反应快 |
C. 与 与 在常温、常压下不反应,放电时可反应 在常温、常压下不反应,放电时可反应 |
| D.Fe与浓盐酸反应比与稀盐酸反应快 |
您最近一年使用:0次
2021-07-31更新
|
441次组卷
|
20卷引用:2016-2017学年北大附中河南分校高二上第一次月考化学卷
2016-2017学年北大附中河南分校高二上第一次月考化学卷2016-2017学年天津市河东区高二上学期期中质检化学试卷湖南省衡阳县2017-2018学年高二上期期末考试化学试题黑龙江省齐齐哈尔市第八中学2018-2019学年高二上学期9月月考化学试题【全国百强校】甘肃省静宁县第一中学2018-2019学年高二上学期10月月考化学试题甘肃省岷县第二中学2018-2019学年高二上学期期中考试化学试题河北省大名县第一中学2019-2020学年高二9月月考化学试题河北省邯郸大名一中2019-2020学年高二上学期第一次月考化学试题吉林省通化市梅河口市博文学校2019-2020学年高二上学期第一次月考化学试题青海省西宁市第十四中学2019-2020学年高二上学期期末考试化学试题湖北松滋市言程中学2020-2021学年高二上学期期中考试化学试题选择性必修1(SJ)专题2第一单元课时2 影响化学反应速率的因素(已下线)2.1.2 影响化学反应速率的因素-2021-2022学年高二化学课后培优练(苏教版2019选择性必修1)广东省梅州市大埔县虎山中学2021-2022学年高二上学期第一次段考(10月)化学试题福建省南安市柳城中学2021-2022学年高二上学期第一次月考化学试题宁夏六盘山高级中学2021-2022学年高二上学期期中考试化学试题(资助班)(已下线)6.1.2 化学反应速率(第2课时 影响化学反应速率的因素)-【帮课堂】2021-2022学年高一化学同步精品讲义(沪科版2020必修第二册)(已下线)第06讲 影响化学反应速率的因素(word讲义)-【帮课堂】2022-2023学年高二化学同步精品讲义(人教2019选择性必修1)宁夏永宁县永宁中学2021-2022学年高二上学期期中考试化学试题2.1.2影响化学反应速率的因素 课后
单选题
|
较易(0.85)
名校
2. 下列关于化学反应平衡常数的叙述正确的是
| A.在任何条件下,平衡常数是一个恒定值 |
| B.改变反应物或生成物的浓度,可改变平衡常数 |
| C.化学反应平衡常数随反应温度而改变 |
| D.平衡常数大表示该反应速度快 |
【知识点】 化学平衡常数的影响因素及应用解读 化学平衡
您最近一年使用:0次
2021-08-13更新
|
414次组卷
|
2卷引用:第27届(2013年)高中学生化学竞赛天津市预赛试题
单选题
|
较易(0.85)
名校
3. 下列说法正确的是
| A.需要加热的化学反应都是吸热反应 |
| B.物质的燃烧反应都是放热反应 |
| C.原电池是将电能转化为化学能的一种装置 |
| D.水力发电是将化学能转化为电能的过程 |
您最近一年使用:0次
单选题
|
适中(0.65)
名校
4. 下列说法不正确的是
| A.应用盖斯定律,可计算某些难以直接测量的反应焓变 |
| B.化学键的断裂与形成是化学反应中能量变化的主要原因 |
| C.反应物能量高于生成物能量的反应是吸热反应 |
| D.同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件的ΔH相同 |
您最近一年使用:0次
2021-10-26更新
|
87次组卷
|
2卷引用:广东省梅州市大埔县虎山中学2021-2022学年高二上学期第一次段考(10月)化学试题
单选题
|
适中(0.65)
名校
5. 根据下列热化学方程式:
①C(s)+O2=CO2(g) ΔH1=-393.5 kJ·mol-1
②H2(g)+1/2O2(g)=H2O(l) ΔH2=-285.8 kJ·mol-1
③CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l) ΔH3=-870.3kJ·mol-1
可计算出2C(s)+2H2(g)+O2(g)=CH3COOH(l)的反应热
①C(s)+O2=CO2(g) ΔH1=-393.5 kJ·mol-1
②H2(g)+1/2O2(g)=H2O(l) ΔH2=-285.8 kJ·mol-1
③CH3COOH(l)+2O2(g)=2CO2(g)+2H2O(l) ΔH3=-870.3kJ·mol-1
可计算出2C(s)+2H2(g)+O2(g)=CH3COOH(l)的反应热
| A.ΔH=244.1 kJ·mol-1 | B.ΔH=-488.3 kJ·mol-1 |
| C.ΔH=-996.6 kJ·mol-1 | D.ΔH=996.6 kJ·mol-1 |
【知识点】 化学反应热的计算 盖斯定律与热化学方程式解读
您最近一年使用:0次
2019-10-13更新
|
414次组卷
|
24卷引用:2011届吉林省第一中学高三上学期第二次教学质量检测化学卷
(已下线)2011届吉林省第一中学高三上学期第二次教学质量检测化学卷(已下线)2011届黑龙江省哈尔滨六中高三上学期期末考试化学试卷(已下线)2010—2011学年广东省广州六中高二上学期期末考试化学试卷卷(已下线)2013届山东省济宁市鱼台一中高三上学期期中考试化学试卷(已下线)2012-2013学年甘肃省武威第五中学高二11月月考化学试卷(已下线)2012-2013学年黑龙江省集贤县第一中学高二上学期期末考试化学试卷(已下线)2013-2014学年江苏常州市某重点高中高二上学期第四次月考化学试卷(已下线)2013-2014学年天津市南开区高二上学期期末考试化学试卷(已下线)2014~2015学年江西四校9月联考高二化学试卷2016届山东省枣庄市滕州十一中高三上学期期末模拟化学试卷(已下线)同步君 人教版 选修4 第1章 第3节 反应热的计算2016-2017学年河北省景县中学高二上学期摸底化学试卷广东省阳东广雅学校2017-2018学年高二9月月考化学试题高中化学人教版 选修四 第一章 化学反应与能量 第三节 化学反应热的计算 化学反应热的计算第二课时(反应热的计算)河北省承德市第二中学2017-2018学年高二上学期第一次月考化学试题广西宾阳县宾阳中学2019-2020学年高二9月月考化学试题山东省济南外国语学校三箭分校2019-2020学年高二上学期期中考试化学试题吉林省公主岭市范家屯镇第一中学2020届高三上学期第二次月考化学试题吉林省长春市第二十九中学2019-2020学年高一下学期线上检测化学试题福建省永安市第三中学2020-2021学年高二10月月考化学(学考班)试题湖南省湘潭电机子弟中学2019-2020学年高二下学期期中考试化学(理)试题广东省梅州市大埔县虎山中学2021-2022学年高二上学期第一次段考(10月)化学试题广东省惠州市博罗县博罗中学2023-2024学年高二上学期高二10月月考化学试题青海省西宁市海湖中学2023-2024学年高二下学期开学考试化学试卷
单选题
|
较易(0.85)
名校
6. 以下说法中正确的是:
| A.ΔH<0的反应均是自发反应 |
| B.自发进行的反应一定能随时自动发生 |
| C.冰在室温下自动熔化成水,这是熵增的过程 |
| D.MgCO3(s)=MgO(s)+CO2(g)高温下,不能自发 |
您最近一年使用:0次
2019-11-17更新
|
113次组卷
|
2卷引用:辽宁省大连市2019-2020学年高二上学期期中考试化学试题
单选题
|
适中(0.65)
名校
解题方法
7. 反应3Fe(s)+4H2O(g)  Fe3O4(s)+4H2(g)在一容积可变的密闭容器中进行,下列条件的改变对其化学反应速率几乎无影响的是
Fe3O4(s)+4H2(g)在一容积可变的密闭容器中进行,下列条件的改变对其化学反应速率几乎无影响的是
 Fe3O4(s)+4H2(g)在一容积可变的密闭容器中进行,下列条件的改变对其化学反应速率几乎无影响的是
Fe3O4(s)+4H2(g)在一容积可变的密闭容器中进行,下列条件的改变对其化学反应速率几乎无影响的是| A.保持容积不变,增加H2O(g)的物质的量 | B.将容器的容积缩小一半 |
| C.保持容积不变,充入Ar使压强增大 | D.保持压强不变,充入Ar使容积增大 |
【知识点】 影响化学反应速率的外因
您最近一年使用:0次
2022-07-09更新
|
599次组卷
|
24卷引用:2015-2016学年吉林省松原市油田高中高一下期中化学试卷
2015-2016学年吉林省松原市油田高中高一下期中化学试卷福建省南安第一中学2017-2018学年高二上学期期中考试化学试题西藏拉萨那曲第二高级中学2020-2021学年高二上学期期中考试化学试题(已下线)课时35 化学反应速率及影响因素-2022年高考化学一轮复习小题多维练(全国通用)上海交通大学附属中学2021-2022高二上学期开学摸底测试化学试题河北深州市长江中学2021-2022学年高二上学期10月月考化学(理)试题广东省梅州市大埔县虎山中学2021-2022学年高二上学期第一次段考(10月)化学试题(已下线)专题10 化学反应速率与化学平衡-备战2022年高考化学学霸纠错(全国通用)贵州省毕节市金沙县第一中学2021-2022学年高二上学期期中考试化学试题重庆市第七中学校2021-2022学年高二上学期期中考试化学试题江西省九江市第一中学2021-2022学年高二上学期期中考试化学试题(已下线)考点21 化学反应速率-备战2023年高考化学一轮复习考点帮(全国通用)重庆市沙坪坝实验中学校2021-2022学年高二上学期12月月考化学试题浙江省宁波市咸祥中学2021-2022学年高一下学期期中考试化学试题吉林省吉林市2022-2023学年高二上学期期中调研测试化学试题河南省兰考县第二高级中学2021-2022学年高二上学期期中考试化学试题江苏省淮安市涟水县第一中学2022-2023学年高二上学期第二次阶段检测化学试题甘肃省定西市文峰中学2021-2022学年高二上学期期中考试化学(理科)试题浙江省嘉兴市海盐第二高级中学2021-2022学年高二上学期(10月)阶段检测化学试题(已下线)第七章 化学反应速率与化学平衡 第40练 化学反应速率四川省凉山彝族自治州2022-2023学年高二上学期期末检测化学试题浙江省宁波效实中学2022-2023学年高一下学期期中考试化学(选考班)试题(已下线)考点21 化学反应速率(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)江西省景德镇市2023-2024学年高二上学期11月期中考试化学试题
单选题
|
较易(0.85)
名校
8. 对可逆反应4NH3(g)+5O2(g)  4NO(g)+6H2O(g),下列叙述正确的是
4NO(g)+6H2O(g),下列叙述正确的是
 4NO(g)+6H2O(g),下列叙述正确的是
4NO(g)+6H2O(g),下列叙述正确的是| A.达到化学平衡时,3υ正(NH3)=2υ逆(H2O) |
| B.若单位时间内生成4x mol NO的同时,消耗4x mol NH3,则反应达到平衡状态 |
| C.达到化学平衡时,若压缩容器体积,则正反应速率增大,逆反应速率减小 |
| D.反应达到平衡后,保持恒温恒容条件向容器中充入一定量的He,则NH3的转化率减小 |
您最近一年使用:0次
2021-09-29更新
|
287次组卷
|
3卷引用:重庆市暨华中学校2020-2021学年高二上学期第二次月考化学试题
单选题
|
较易(0.85)
名校
9. 已知可逆反应: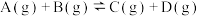
 ,在某密闭体系中进行该反应,反应过程中能量变化如图所示。下列说法正确的是
,在某密闭体系中进行该反应,反应过程中能量变化如图所示。下列说法正确的是
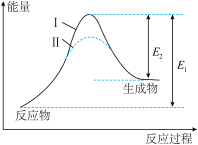
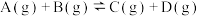
 ,在某密闭体系中进行该反应,反应过程中能量变化如图所示。下列说法正确的是
,在某密闭体系中进行该反应,反应过程中能量变化如图所示。下列说法正确的是
A.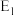 为逆反应的活化能, 为逆反应的活化能, 为正反应的活化能 为正反应的活化能 |
| B.曲线Ⅱ使用了催化剂,降低了反应的焓变 |
C.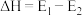 ,该反应为吸热反应 ,该反应为吸热反应 |
| D.活化能越大,反应越容易进行 |
您最近一年使用:0次
2021-07-31更新
|
1252次组卷
|
10卷引用:选择性必修1(SJ)专题2第一单元课时2 影响化学反应速率的因素
选择性必修1(SJ)专题2第一单元课时2 影响化学反应速率的因素(已下线)第2章 化学反应速率与化学平衡(基础过关卷)-【高效检测】2021-2022学年高二化学章末测试卷(人教版2019选择性必修1)吉林省永吉县第四中学2021-2022学年高二上学期第一次月考化学试题辽宁省辽东南协作体2021-2022学年高二上学期第一次月考化学试题广东省梅州市大埔县虎山中学2021-2022学年高二上学期第一次段考(10月)化学试题2.1.2影响化学反应速率的因素 课后黑龙江省鹤岗市第一中学2022-2023学年高二上学期11月期中考试化学试题宁夏吴忠中学2023-2024学年高二上学期11月期中考试化学试题云南省大理市大理白族自治州民族中学2023-2024学年高二上学期12月月考化学试题新疆维吾尔自治区喀什市第十四中学2023-2024学年高二上学期1月期末质量检测化学试题
单选题
|
适中(0.65)
10. 在密闭容器中,一定条件下,进行如下反应:NO(g)+CO(g)⇌ N2(g)+CO2(g) ΔH=-373.2kJ·mol-1,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是
N2(g)+CO2(g) ΔH=-373.2kJ·mol-1,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是
 N2(g)+CO2(g) ΔH=-373.2kJ·mol-1,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是
N2(g)+CO2(g) ΔH=-373.2kJ·mol-1,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是| A.加催化剂同时升高温度 | B.加催化剂同时增大压强 |
| C.升高温度同时充入N2 | D.降低温度同时增大压强 |
您最近一年使用:0次
2021-10-26更新
|
469次组卷
|
14卷引用:广东省梅州市大埔县虎山中学2021-2022学年高二上学期第一次段考(10月)化学试题
广东省梅州市大埔县虎山中学2021-2022学年高二上学期第一次段考(10月)化学试题浙江省磐安县第二中学2021-2022学年高二10月份竞赛化学试题吉林省通化县综合高级中学2021-2022学年高二上学期期中考试化学试题辽宁师范大学附属中学2021-2022学年高二上学期10月月考化学试题重庆市沙坪坝实验中学校2021-2022学年高二上学期10月月考化学试题西藏林芝市第二高级中学2021-2022学年高二上学期期中考试理综化学试题黑龙江省齐齐哈尔市恒昌中学校2022-2023学年高二上学期第一次月考化学试题广东省广州市第二中学2022-2023学年高二上学期期中考试化学试题黑龙江省哈尔滨市第一六二中学校2022-2023学年高二上学期第一次月考化学试题新疆奇台县第一中学2022-2023学年高二上学期期中考试化学试题浙江省嘉兴市海盐第二高级中学2021-2022学年高二上学期(10月)阶段检测化学试题河南省新教材2022-2023学年高二上学期第三次阶段性模拟测试化学试题云南省昌宁县第一中学2022-2023学年高二下学期期末考试化学试题浙江省宁波市奉化区2023-2024学年高二上学期期末检测化学试题



