10. 氮及其化合物的研究对于生态环境保护和工农业生产发展非常重要。请回答下列问题:
(1)煤燃烧产生的烟气中含有氮的氧化物NO
x,用CH
4催化还原NO
x可消除氮氧化物的污染。
已知:
①CH
4(g)+ 2NO
2(g)= N
2(g)+CO
2(g)+ 2H
2O(g)
△H=-865.0 kJ·mol
-l②2NO(g)+O
2(g)= 2NO
2(g)
△H=-112.5 kJ·mol
-1③适量的N
2和O
2完全反应,每生成2.24 L(标准状况下)NO时,吸收8.9 kJ的热量。
则CH
4(g)+4NO(g)= 2N
2(g)+ CO
2(g)+ 2H
2O(g)
△H=
___________kJ·mol
-1(2)已知合成氨反应N
2(g)+ 3H
2(g)

2NH
3(g)
△H= -92 kJ·mol
-l,科研小组模拟不同条件下的合成氨反应,向刚性容器中充入10.0 mol N
2和20.0 molH
2,不同温度下平衡混合物中氨气的体积分数与总压强(p)的关系如图,T
1、T
2、T
3由小到大的排序为
___________;在T
2、50MPa条件下,A点v
正___________ v
逆(填“>”“<”或“=”);在温度T
2压强50MPa时,平衡常数K
p=
___________MPa
-2(列出表达式,分压=总压×物质的量分数)。

(3)将1mol的N
2和3mol的H
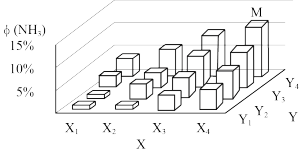
2通入密闭容器中进行反应,在一定温度和压强下达到平衡时氨气的体积分数ϕ (NH
3)的变化趋势如图所示(其中X
1→X
4逐渐减小,Y
1→Y
4逐渐增大):图中X轴表示的外界条件为
___________,判断的理由是
____。
(4)利用反应6NO
2 + 8NH
3 = 7N
2+ 12H
2O构成电池,能实现有效消除氮氧化物的排放,减轻环境污染,装置如下图所示:

写出电极B的电极反应式:
___________。