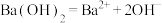湖北省黄冈市蕲春县第四高级中学2022-2023学年高一上学期期中质量检测化学试题
湖北
高一
期中
2022-12-02
140次
整体难度:
容易
考查范围:
认识化学科学、常见无机物及其应用、化学实验基础、化学与STSE
湖北省黄冈市蕲春县第四高级中学2022-2023学年高一上学期期中质量检测化学试题
湖北
高一
期中
2022-12-02
140次
整体难度:
容易
考查范围:
认识化学科学、常见无机物及其应用、化学实验基础、化学与STSE
一、单选题 添加题型下试题
单选题
|
容易(0.94)
名校
解题方法
您最近一年使用:0次
2022-10-10更新
|
561次组卷
|
10卷引用:河南省新乡市2022~2023学年高一上学期选科调研第一次测试化学试题
河南省新乡市2022~2023学年高一上学期选科调研第一次测试化学试题辽宁省协作校2022-2023学年高一上学期第一次月考化学试题河南省社旗县第一高级中学2022-2023学年高一上学期9月月考化学试题湖南省长沙市地质中学2022-2023学年高一上学期期中考试化学试题重庆市万州纯阳中学2022-2023学年高一上学期期中考试化学试题湖北省黄冈市蕲春县第四高级中学2022-2023学年高一上学期期中质量检测化学试题辽宁省名校联盟2022-2023学年高一3月联考化学试题广西南宁市第五十六中学2022-2023学年高一上学期期中考试化学试题黑龙江省牡丹江市第二高级中学2023-2024学年高一上学期10月月考化学试题湖南省平江县第三中学2023-2024学年高一上学期期中考试化学试题
单选题
|
容易(0.94)
2. 中秋月饼的包装盒内常可看到如图所示的脱氧保鲜剂(其主要成分有 、铁粉、碳粉、
、铁粉、碳粉、 、NaCl),关于其主要成分的分类不包括
、NaCl),关于其主要成分的分类不包括

 、铁粉、碳粉、
、铁粉、碳粉、 、NaCl),关于其主要成分的分类不包括
、NaCl),关于其主要成分的分类不包括
| A.碱 | B.单质 | C.盐 | D.氧化物 |
【知识点】 无机物质的分类
您最近一年使用:0次
2022-10-11更新
|
113次组卷
|
2卷引用:河北省沧州市部分学校2022-2023学年高一上学期10月选科调考第一次联考化学试题
单选题
|
容易(0.94)
解题方法
3. 丁达尔效应是由英国物理学家约翰·丁达尔在1869年研究发现的,是一种光的散射现象。当光束通过下列物质时,不会出现丁达尔效应的是
| A.云、雾 | B.氢氧化钡溶液 | C.有色玻璃 | D.氢氧化铁胶体 |
您最近一年使用:0次
2022-10-29更新
|
147次组卷
|
3卷引用:河南省百所名校2022-2023学年高一上学期10月联考化学试题
单选题
|
较易(0.85)
4. 某种矿泉水的主要矿物质成分及含量(单位为 )为
)为 、
、 、
、 、
、 等,则该矿泉水
等,则该矿泉水
 )为
)为 、
、 、
、 、
、 等,则该矿泉水
等,则该矿泉水| A.不导电 | B.能导电 | C.是非电解质 | D.是电解质 |
【知识点】 电解质、非电解质概念解读
您最近一年使用:0次
2022-10-11更新
|
73次组卷
|
2卷引用:河北省沧州市部分学校2022-2023学年高一上学期10月选科调考第一次联考化学试题
单选题
|
容易(0.94)
名校
5. 下列化学反应不是氧化还原反应的是是
A. | B. |
C. | D.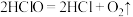 |
【知识点】 氧化还原反应定义、本质及特征解读
您最近一年使用:0次
2022-10-11更新
|
578次组卷
|
4卷引用:河北省沧州市部分学校2022-2023学年高一上学期10月选科调考第一次联考化学试题
单选题
|
适中(0.65)
名校
您最近一年使用:0次
2022-10-11更新
|
142次组卷
|
3卷引用:河北省沧州市部分学校2022-2023学年高一上学期10月选科调考第一次联考化学试题
单选题
|
较易(0.85)
解题方法
7. 根据物质的组成和性质,可以通过化学变化实现物质之间的转化。下列转化不能一步实现的是
A. | B.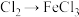 | C. | D. |
【知识点】 物质的转化 氧化还原反应定义、本质及特征解读
您最近一年使用:0次
2022-10-29更新
|
110次组卷
|
3卷引用:河南省百所名校2022-2023学年高一上学期10月联考化学试题
单选题
|
较易(0.85)
解题方法
您最近一年使用:0次
2022-10-29更新
|
250次组卷
|
5卷引用:河南省百所名校2022-2023学年高一上学期10月联考化学试题
单选题
|
较易(0.85)
名校
解题方法
9. 小明将某无色溶液滴到红色石蕊试纸上,发现试纸显蓝色,在此无色溶液中能大量共存的一组离子是
A. 、 、 、 、 、 、 | B. 、 、 、 、 、 、 |
C. 、 、 、 、 、 、 | D. 、 、 、 、 、 、 |
【知识点】 离子反应的发生条件解读 限定条件下的离子共存解读
您最近一年使用:0次
2022-10-29更新
|
166次组卷
|
4卷引用:河南省百所名校2022-2023学年高一上学期10月联考化学试题
单选题
|
适中(0.65)
名校
解题方法
10. 2022年6月5日,“神舟十四号”载人飞船成功发射。为了使宇航员在飞船中得到一个稳定的、良好的生存环境,一般会在飞船内安装盛有 颗粒的装置。下列关于
颗粒的装置。下列关于 的叙述正确的是
的叙述正确的是
 颗粒的装置。下列关于
颗粒的装置。下列关于 的叙述正确的是
的叙述正确的是A. 只能作氧化剂 只能作氧化剂 |
B. 中的阴、阳离子数目之比为1∶1 中的阴、阳离子数目之比为1∶1 |
C. 能与酸反应,是碱性氧化物 能与酸反应,是碱性氧化物 |
D.等质量的 分别与足量 分别与足量 、 、 反应,转移的电子数相同 反应,转移的电子数相同 |
您最近一年使用:0次
2022-10-29更新
|
352次组卷
|
7卷引用:河南省百所名校2022-2023学年高一上学期10月联考化学试题
单选题
|
适中(0.65)
解题方法
11. 浩瀚的大海美丽而富饶。海洋是一个巨大的化学资源宝库,含有80多种元素,钠和氯是其中含量较高的元素。下列关于钠和氯及其化合物的离子方程式的书写正确的是
A.将氯气通入水中: |
B.将一小块钠放入水中: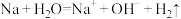 |
C.向 溶液中通入少量氯气: 溶液中通入少量氯气: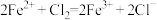 |
D.向碳酸氢钠溶液中加入稀硫酸: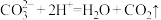 |
【知识点】 离子方程式的书写解读 离子方程式的正误判断解读
您最近一年使用:0次
2022-10-29更新
|
203次组卷
|
3卷引用:河南省百所名校2022-2023学年高一上学期10月联考化学试题
12.  与浓盐酸的反应是实验室制备氯气的方法之一、
与浓盐酸的反应是实验室制备氯气的方法之一、
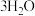 ,下列说法正确的是
,下列说法正确的是
 与浓盐酸的反应是实验室制备氯气的方法之一、
与浓盐酸的反应是实验室制备氯气的方法之一、
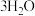 ,下列说法正确的是
,下列说法正确的是A.还原性: |
| B.HCl在反应中只表现出还原性 |
| C.被氧化的氯原子与被还原的氯原子的个数之比为5:1 |
D.用双线桥法表示电子得失情况: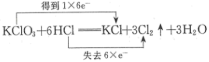 |
您最近一年使用:0次
2022-10-29更新
|
237次组卷
|
4卷引用:河南省百所名校2022-2023学年高一上学期10月联考化学试题
单选题
|
适中(0.65)
名校
解题方法
13. 化学是一门以实验为基础的学科。下列实验方案操作正确且能够达到实验目的的是
| 选项 | 实验目的 | 实验方案 |
| A | 除去 中的少量HCl 中的少量HCl | 将混合气体通过盛有氢氧化钠溶液的洗气瓶 |
| B | 证明 与 与 反应是放热反应 反应是放热反应 | 用棉花包裹 粉末后,滴加几滴水,棉花燃烧说明该反应是放热反应 粉末后,滴加几滴水,棉花燃烧说明该反应是放热反应 |
| C | 观察钠与水反应的现象 | 用手从煤油中取出金属钠,切下绿豆大小的钠,小心放入装有适量水的烧杯中 |
| D | 检验NaCl溶液中的阳离子 | 用玻璃棒蘸取溶液,在酒精灯外焰上灼烧,观察火焰的颜色 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-10-29更新
|
335次组卷
|
6卷引用:河南省百所名校2022-2023学年高一上学期10月联考化学试题
单选题
|
较易(0.85)
名校
解题方法
14. 某实验小组通过如图所示实验,探究 与水的反应,并观察到以下现象:
与水的反应,并观察到以下现象:

下列说法中错误的是
 与水的反应,并观察到以下现象:
与水的反应,并观察到以下现象:
下列说法中错误的是
| A.④中现象可能是由于溶液中含有漂白性物质造成的 |
B.⑤中 的主要作用是作催化剂 的主要作用是作催化剂 |
C.②中的反应生成了 |
| D.③④中的现象,说明NaOH有漂白性 |
您最近一年使用:0次
2022-10-12更新
|
309次组卷
|
2卷引用:广西梧州市高级中学2022~2023学年高一上学期10月考试化学试题
单选题
|
较难(0.4)
名校
解题方法
15. 不同温度下,硝酸铵受热分解的产物不同:① ;②
;②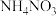
 ;③
;③
 ;④
;④
 。下列说法正确的是
。下列说法正确的是
 ;②
;②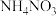
 ;③
;③
 ;④
;④
 。下列说法正确的是
。下列说法正确的是| A.上述反应均为分解反应,且均属于氧化还原反应 |
B.反应②中被氧化和被还原的氮原子数之比为 |
C.反应③中生成1个 ,转移的电子数为10 ,转移的电子数为10 |
D.反应④中氧化产物与还原产物的分子数之比为 |
【知识点】 氧化还原反应基本概念 基于氧化还原反应守恒规律的计算解读
您最近一年使用:0次
2022-10-10更新
|
704次组卷
|
6卷引用:河南省新乡市2022~2023学年高一上学期选科调研第一次测试化学试题
二、填空题 添加题型下试题
填空题
|
较易(0.85)
解题方法
16. 室温下,现有9种物质:①CaO固体②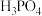 溶液③
溶液③ ④
④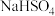 固体⑤
固体⑤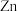 ⑥
⑥ ⑧
⑧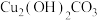 固体⑨
固体⑨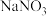 固体。根据所学知识回答下列问题:
固体。根据所学知识回答下列问题:
(1)上述物质中属于碱性氧化物的有_______ (填标号,下同),属于钠盐的有_______ 。
(2)上述物质在所处的状态下,可以导电的有_______ (填标号)。
(3)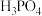 的化学名称为
的化学名称为_______ 。
(4)④在水中的电离方程式为_______ 。
(5)⑥→⑦仅通过一步反应可实现,化学方程式为 ,该反应中氧化性:⑥
,该反应中氧化性:⑥_______ (填“>”“<”或“=”)⑦。
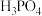 溶液③
溶液③ ④
④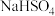 固体⑤
固体⑤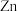 ⑥
⑥ ⑧
⑧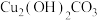 固体⑨
固体⑨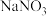 固体。根据所学知识回答下列问题:
固体。根据所学知识回答下列问题:(1)上述物质中属于碱性氧化物的有
(2)上述物质在所处的状态下,可以导电的有
(3)
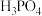 的化学名称为
的化学名称为(4)④在水中的电离方程式为
(5)⑥→⑦仅通过一步反应可实现,化学方程式为
 ,该反应中氧化性:⑥
,该反应中氧化性:⑥
您最近一年使用:0次
2022-10-20更新
|
120次组卷
|
3卷引用:河南省创新联盟2022-2023学年高一上学期第一次模拟选科考试化学试题
三、解答题 添加题型下试题
解答题-实验探究题
|
适中(0.65)
解题方法
17. 氯气、“84”消毒液、漂白粉等都是含氯的消毒剂,某化学兴趣小组利用如图装置制备“84”消毒液、漂白粉,并收集纯净干燥的氯气。回答下列问题:
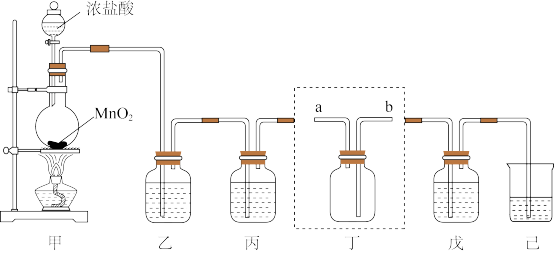
(1)盛装浓盐酸的仪器的名称为_______ ,装置甲中发生反应的化学方程式为_______ 。
(2)装置丁用来收集纯净且干燥的氯气,进气口为_______ (填标号);装置乙和丙盛装的试剂分别是_______ 、_______ 。(填名称)
(3)将氯气通入装置己中制备漂白液,则装置己中发生反应的离子方程式为_______ ,有同学认为装置己还有一个作用,该作用为_______ ,发挥该作用时_______ (填“能”或“不能”)用澄清石灰水代替。
(4)装置戊中盛装石灰乳用来制备漂白粉,漂白粉的有效成分为_______ (填化学式),漂白粉长时间暴露在空气中容易发生变质的原因为_______ (结合化学方程式说明)。

(1)盛装浓盐酸的仪器的名称为
(2)装置丁用来收集纯净且干燥的氯气,进气口为
(3)将氯气通入装置己中制备漂白液,则装置己中发生反应的离子方程式为
(4)装置戊中盛装石灰乳用来制备漂白粉,漂白粉的有效成分为
您最近一年使用:0次
2022-10-29更新
|
247次组卷
|
4卷引用:河南省百所名校2022-2023学年高一上学期10月联考化学试题
四、填空题 添加题型下试题
填空题
|
适中(0.65)
解题方法
18. 碳酸钠俗称纯碱,用途非常广泛,我国化学家侯德榜发明了“侯氏制碱法”。下列实验操作a中以NaCl饱和溶液和 饱和溶液为原料制备
饱和溶液为原料制备 的原理为
的原理为 。
。
请回答下列问题:

(1)图中涉及的①~⑧八种物质中,能导电的物质有_______ (填序号,下同),属于电解质的有_______ 。
(2)反应Ⅱ的化学方程式为_______ ,它属于四种基本反应类型中的_______ 反应。
(3)用离子方程式表示操作a制备 的原理:
的原理:_______ ,该反应能发生的原因是_______ 。
(4)若向 溶液中加入足量的
溶液中加入足量的 ,该反应的离子方程式为
,该反应的离子方程式为_______ 。
 饱和溶液为原料制备
饱和溶液为原料制备 的原理为
的原理为 。
。请回答下列问题:

(1)图中涉及的①~⑧八种物质中,能导电的物质有
(2)反应Ⅱ的化学方程式为
(3)用离子方程式表示操作a制备
 的原理:
的原理:(4)若向
 溶液中加入足量的
溶液中加入足量的 ,该反应的离子方程式为
,该反应的离子方程式为
您最近一年使用:0次
2022-10-18更新
|
355次组卷
|
4卷引用:河南省信阳市2022-2023学年高一上学期阶段性测试(一)化学试题
五、解答题 添加题型下试题
解答题-原理综合题
|
较难(0.4)
解题方法
19. 一方面,磷矿藏在地球上分布不均匀且储量有限;另一方面,污水中含有较多的磷元素。因此在污水处理生物污泥中的蓝铁矿[Fe3(PO4)2·nH2O]因其潜在的特殊用途以及经济价值而备受关注。蓝铁矿在自然水体中形成的过程如图。

(1)水处理时,加入的高铁酸钾(K2FeO4)作为净水消毒剂,发生反应的化学方程式为4K2FeO4+10H2O=4Fe(OH)3(胶体)+8KOH+3O2↑。
①K2FeO4中Fe的化合价为_______ 价,上述反应涉及的物质中属于盐的是_______ 。
②高铁酸钾可用于净水消毒的原因是_______ 。
(2)在甲烷厌氧氧化菌的作用下,氢氧化铁和甲烷发生如下反应,配平该离子方程式:________ _______Fe(OH)3+______CH4+_______H+ ______Fe2++_______HCO
______Fe2++_______HCO +_______H2O,
+_______H2O,
该反应中的氧化产物为_______ (填离子符号),被氧化的原子与被还原的原子的数目之比为_______ 。
(3)无氧条件下加热,蓝铁矿(无杂质)发生分解:Fe3(PO4)2·nH2O Fe3(PO4)2+nH2O,蓝铁矿的质量由5.02g减小为3.58g,则n=
Fe3(PO4)2+nH2O,蓝铁矿的质量由5.02g减小为3.58g,则n=_______ ,蓝铁矿的相对分子质量为_______ 。

(1)水处理时,加入的高铁酸钾(K2FeO4)作为净水消毒剂,发生反应的化学方程式为4K2FeO4+10H2O=4Fe(OH)3(胶体)+8KOH+3O2↑。
①K2FeO4中Fe的化合价为
②高铁酸钾可用于净水消毒的原因是
(2)在甲烷厌氧氧化菌的作用下,氢氧化铁和甲烷发生如下反应,配平该离子方程式:
 ______Fe2++_______HCO
______Fe2++_______HCO +_______H2O,
+_______H2O,该反应中的氧化产物为
(3)无氧条件下加热,蓝铁矿(无杂质)发生分解:Fe3(PO4)2·nH2O
 Fe3(PO4)2+nH2O,蓝铁矿的质量由5.02g减小为3.58g,则n=
Fe3(PO4)2+nH2O,蓝铁矿的质量由5.02g减小为3.58g,则n=
您最近一年使用:0次
2022-10-10更新
|
805次组卷
|
3卷引用:河南省新乡市2022~2023学年高一上学期选科调研第一次测试化学试题
试卷分析
整体难度:适中
考查范围:认识化学科学、常见无机物及其应用、化学实验基础、化学与STSE
试卷题型(共 19题)
题型
数量
单选题
15
填空题
2
解答题
2
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.94 | 物理变化与化学变化 | |
| 2 | 0.94 | 无机物质的分类 | |
| 3 | 0.94 | 胶体 胶体的性质和应用 | |
| 4 | 0.85 | 电解质、非电解质概念 | |
| 5 | 0.94 | 氧化还原反应定义、本质及特征 | |
| 6 | 0.65 | 电离方程式 | |
| 7 | 0.85 | 物质的转化 氧化还原反应定义、本质及特征 | |
| 8 | 0.85 | 钠与水反应原理 钠与盐溶液的反应 | |
| 9 | 0.85 | 离子反应的发生条件 限定条件下的离子共存 | |
| 10 | 0.65 | 过氧化钠 电子转移计算 | |
| 11 | 0.65 | 离子方程式的书写 离子方程式的正误判断 | |
| 12 | 0.65 | 氧化还原反应的几组概念 单线桥、双线桥分析氧化还原反应 氧化性、还原性强弱的比较 氧化还原反应有关计算 | |
| 13 | 0.65 | 焰色试验 钠与水反应原理 过氧化钠与水的反应 | |
| 14 | 0.85 | 过氧化钠与水的反应 | |
| 15 | 0.4 | 氧化还原反应基本概念 基于氧化还原反应守恒规律的计算 | |
| 二、填空题 | |||
| 16 | 0.85 | 酸、碱、盐、氧化物的概念及其相互联系 物质水溶液的导电性 电离方程式 氧化性、还原性强弱的比较 | |
| 18 | 0.65 | 非电解质、电解质物质类别判断 离子反应的发生及书写 碳酸钠与碳酸氢钠性质的比较 纯碱的生产 | |
| 三、解答题 | |||
| 17 | 0.65 | 氯气 氯气的实验室制法 氯气与碱溶液反应 物质制备的探究 | 实验探究题 |
| 19 | 0.4 | 氧化还原反应基本概念 氧化还原反应有关计算 氧化还原反应方程式的配平 氧化还原反应在生活、生产中的应用 | 原理综合题 |