10. N
2O是一种强温室气体,且易形成颗粒性污染物,N
2O的综合治理是当前重要的研究课题。
I.CO用于处理大气污染物N
2O的反应为CO(g)+N
2O(g)

CO
2(g)+N
2(g)。在Zn
+作用下该反应的具体过程如图1所示,反应过程中能量变化情况如图2所示。

(1)总反应:CO(g)+N
2O(g)

CO
2(g)+N
2(g) ΔH=
__________kJ·mol
-1;该总反应的决速步是反应
______(填“①”或“②”)。
(2)在总压为100 kPa的恒容密闭容器中,充入一定量的CO(g)和N
2O(g)发生上述反应,在不同条件下达到平衡时,在T
1K时N
2O的平衡转化率随
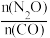
的变化关系,及在
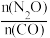
=1时N
2O的平衡转化率随

的变化关系如图3所示:
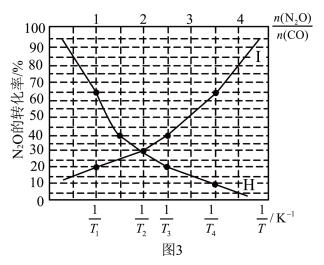
①表示N
2O的转化率随

的变化为曲线
___________(填“I”或“H”);说明理由
_____________。
②该反应在T
4时,该反应的分压平衡常数K
p=
__________ (计算结果保留两位有效数字)。
③其他条件不变,缩小体积,若总压变为200kPa, N
2O的平衡转化率将
_____________(填“增大”、“减小”或“不变”)。
Ⅱ.研究N
2O的分解反应2N
2O=2N
2+O
2对环境保护有重要意义。
(3)碘蒸气存在能大幅度提高N
2O的分解速率,反应历程为:
第一步I
2(g)

2I(g) 快速平衡,平衡常数为K
第二步I(g)+N
2O(g)→N
2(g)+IO(g) υ=k
1·c(N
2O)·c(I)慢反应
第三步IO(g)+N
2O(g)→N
2(g)+O
2(g)+

I
2(g) 快反应
其中可近似认为第二步反应不影响第一步的平衡,实验表明,含碘时N
2O分解速率方程υ=k·c(N
2O)· [c (I
2)]
0.5 (k为速率常数)。
①k=
_____________(用含K和k
1的代数式表示)。
②下列表述正确的是
_______________。
a.IO为反应的中间产物
b.碘蒸气的浓度大小不会影响N
2O的分解速率
c.第二步对总反应速率起决定作用
d.碰撞理论认为,催化剂不会改变活化分子百分数