8. Cu
2O主要在玻璃、搪瓷工业中作红色颜料。阿伏加德罗常数(N
A)是化学中重要的物理常数。某实验小组利用下图装置电化学合成Cu
2O并采用量气法测定阿伏加德罗常数的值(夹持装置略)。
实验步骤为:
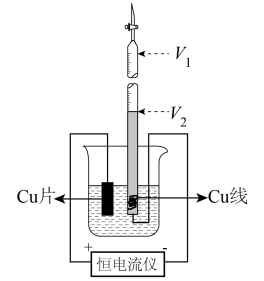
Ⅰ.向烧杯中加入pH为12(用NaOH溶液调节)的2mol/LNaCl溶液。向50mL聚四氟乙烯滴定管(作为量气管用)中加满上述NaCl溶液,然后将其倒置在烧杯中,调节液面高度,读出量气管中液面位置V
1。
Ⅱ.用砂纸打磨Cu片表面,洗涤干净,用滤纸擦干后插入烧杯内。
Ⅲ.取一段Cu线,把Cu线一端的绝缘层剥掉并弯成螺旋状,插入量气管的倒口中。
Ⅳ.将Cu片和Cu线分别连接恒电流仪的两极,进行电解实验。
Ⅴ.电解结束后,读出量气管中液面位置V
2,离心分离出烧杯中的Cu
2O固体,并用适量蒸馏水洗涤。
回答下列问题:
(1)量气管不采用酸式滴定管的原因是
_______。该小组进行了多次平行实验,在每次实验中,量气管中液面位置V
1应尽可能控制在同一位置,目的是
_______。
(2)步骤Ⅱ中,Cu片打磨前,表面黑色物质的主要成分为
_______(写化学式)。
(3)步骤Ⅲ中,Cu线裸露部分应全部放在量气管内,目的是
_______。
(4)电解时,Cu片附近首先析出白色的CuCl,进而转化为Cu
2O。该条件下CuCl转化为Cu
2O的离子方程式为
_______。
(5)某次实验,电解电流为100.0mA,电解时间为722s,测量的体积折合成H
2的物质的量为
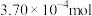
,则N
A值为
_______(用科学计数法表示,保留2位小数,已知单个电子的电量约为
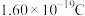
)。
(6)步骤Ⅴ中,可通过检测洗出液中是否存在Cl
-来判断洗涤是否完成。检测的方法是
_____。