压轴题01 离子方程式与离子共存的判断

命题预测 | 本专题考查类型主要涉及点为离子方程式的书写及正误判断、溶液中的离子共存。而离子共存增加了限制条件和隐含条件以及加大对氧化还原反应的考查,综合程度增加,区分度加大。在无机推断及化工流程题中考查信息型离子方程式的书写。 从命题趋势看,预计2024年命题以实际问题为情境(如工农业生产、日常生活、科学实验、环境保护、检验检测等),设计学科内的综合题并推出创新的题型,是主流趋势。 |
高频考法 | (1)离子方程式正误判断 (2)附加条件的离子共存 (3)离子检验与推断 (4)离子方程式与工艺流程 |


一、离子方程式正误判断的基本方法

二、“四步法”突破离子能否大量共存

三、离子的检验方法与推断
1.常见阳离子的检验

2.常见阴离子的检验

四、离子推断的四项基本原则
肯定性 原则 | 根据实验现象推出溶液中肯定存在或肯定不存在的离子(记住常见的有色离子:Fe2+、Fe3+、Cu2+、MnO4- ) |
互斥性 原则 | 在肯定某些离子的同时,结合离子共存规律,否定一些离子存在(要注意题目中的隐含条件,如酸性、碱性、指示剂的变化、与铝反应产生氢气、水的电离情况等) |
电中性 原则 | 溶液呈电中性,一定既有阳离子、又有阴离子,且溶液中正、负电荷总数相等(利用这一原则可确定一些隐含的离子) |
进出性 原则 | 通常是在实验过程中使用,是指在实验过程中反应生成的离子或引入的离子对后续实验的干扰 |

 01 离子方程式综合考查
01 离子方程式综合考查
(2024·吉林白山·二模)
A.证明氧化性: : :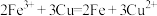 |
B.稀硫酸与 溶液混合: 溶液混合: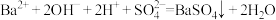 |
C. 在酸性环境下不能稳定存在: 在酸性环境下不能稳定存在: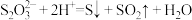 |
D. 与烧碱溶液反应制水玻璃: 与烧碱溶液反应制水玻璃: |
 02 与量有关离子方程式正误判断
02 与量有关离子方程式正误判断
(2024·陕西榆林·二模)
| A | 向饱和 溶液中通入过量 溶液中通入过量 | 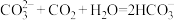 |
| B |  溶液中加入过量的 溶液中加入过量的 溶液 溶液 | 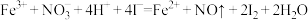 |
| C |  溶液与过量石灰水反应 溶液与过量石灰水反应 |  |
| D |  溶液中通入少量 溶液中通入少量 气体 气体 | 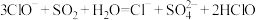 |
| A.A | B.B | C.C | D.D |
 03 限定条件的离子共存判断
03 限定条件的离子共存判断
(2024·天津·一模)
A.乙醇溶液中: 、 、 、 、 、 、 |
B.滴加酚酞显红色的溶液中: 、 、 、 、 、 、 |
C.使甲基橙变红的溶液中: 、 、 、 、 、 、 |
D.所含溶质为 的溶液中: 的溶液中: 、 、 、 、 、 、 |
【知识点】 限定条件下的离子共存解读
 04 离子推断
04 离子推断
(2024·安徽淮北·一模)
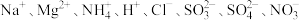 ,取溶液分别进行如下实验:
,取溶液分别进行如下实验:①加入
 酸化的
酸化的 溶液产生白色沉淀;
溶液产生白色沉淀;②加入淀粉
 溶液,呈蓝色;
溶液,呈蓝色;③加入
 溶液产生白色沉淀,加热后产生有刺激性气味的气体。
溶液产生白色沉淀,加热后产生有刺激性气味的气体。下列说法错误的是
A.由①②可知一定有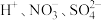 |
B.若将①中的试剂换成盐酸酸化的 溶液,不影响成分的判断 溶液,不影响成分的判断 |
C.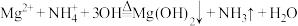 |
D.不能确定有无 |
 05 离子反应与工艺流程
05 离子反应与工艺流程
(2024·辽宁·一模)
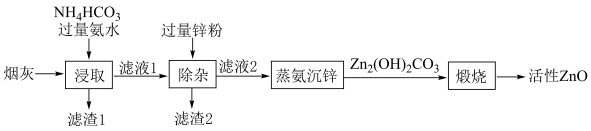
| A.由滤液1中的阳离子主要含有[Zn(NH3)4]2+、[Cu(NH3)4]2+、NH4+可知,滤渣1中含有FeO 和MnO2 |
| B.“除杂”工序反应的离子方程式:Zn+[Cu(NH3)4]2+ =Cu + [Zn(NH3)4]2+ |
| C.“蒸氨沉锌”、“煅烧”时产生的气体可返回到“浸取”工序中循环使用 |
D.从m kg烟灰中得到活性ZnO a kg,则ZnO 的回收率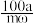 % % |

(2024·江西·一模)
A.能使甲基橙变红的溶液:S2-、 、 、 、Na+ 、Na+ |
B.常温下,由水电离的c(H+)=10-12的溶液中:Be2+、 、K+、Cl- 、K+、Cl- |
C.在水溶液中: 、 、 、Ba2+、F- 、Ba2+、F- |
D.在漂白液中:OH-、Rb+、 、 、 |
【知识点】 限定条件下的离子共存解读 水的电离
(2024·安徽黄山·一模)
| 粒子组 | 判断和分析 | |
| A |  、 、 、 、 、 、 | 能大量共存,粒子间不反应 |
| B |  、 、 、 、 、 、 | 不能大量共存,因发生反应: |
| C |  、 、 、 、 、 、 | 不能大量共存,因发生反应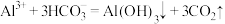 |
| D |  、 、 、 、 、 、 | 能大量共存,粒子间不反应 |
| A.A | B.B | C.C | D.D |
(2023·吉林长春·一模)
| 选项 | 实验操作及现象 | 实验结论 |
| A | 取少量 样品溶于水,加入 样品溶于水,加入 溶液,再加入足量盐酸,产生白色沉淀 溶液,再加入足量盐酸,产生白色沉淀 | 原样品已变质 |
| B | 向某溶液中滴加浓盐酸,将产生气体通入石蕊试液,溶液先变红后褪色 | 溶液中含有 或 或 |
| C | 向溶有 的 的 溶液中通入气体X,出现白色沉淀 溶液中通入气体X,出现白色沉淀 | 气体X不一定是氧化性气体 |
| D | 在某固体试样加水后的溶液中,滴加 溶液,没有产生使湿润红色石蕊试纸变蓝的气体 溶液,没有产生使湿润红色石蕊试纸变蓝的气体 | 该固体试样中不可能存在 |
| A.A | B.B | C.C | D.D |
(2024·陕西咸阳·一模)
| 选项 | 微粒组 | 试剂M | 发生反应的离子方程式 |
| A | Fe3+、H+、 、 、 | 通入少量SO2 | 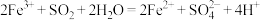 |
| B |  、Fe2+、 、Fe2+、 、Na+ 、Na+ | 少量硫酸 | 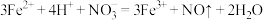 |
| C | Cl-、Na+、 、K+ 、K+ | 过量醋酸溶液 | 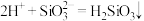 |
| D | K+、 、 、 、 、 | 适量HNO3溶液 | 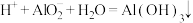 |
| A.A | B.B | C.C | D.D |
(2024·湖南长沙·一模)
 、
、 、
、 、
、 、
、 、
、 。取少量样品进行如下实验:
。取少量样品进行如下实验:①混合物溶于水,得到澄清透明溶液A;
②取--定量溶液A于试管中,加入少量酸性高锰酸钾溶液,溶液不褪色;
③取少量溶液A进行焰色实验,火焰呈黄色;
④取少量溶液A加入过量的氨水,生成白色沉淀。
根据实验现象可判断该样品确定存在的是
A. 、 、 | B.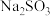 、 、 |
C. 、 、 | D. 、 、 |
【知识点】 离子反应在化合物组成的分析、鉴定的应用解读 焰色试验解读
(2024·北京西城·一模)
(2024·福建泉州·一模)

A.过程①: |
B.过程②总反应式: |
C.过程③: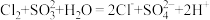 |
D. 溶于水: 溶于水: |
【知识点】 离子方程式的正误判断解读 氧化还原反应方程式的书写与配平解读 氯气 铵盐
(2024·北京·一模)
| A.用Na2S去除废水中的Hg2+:Hg2++S2-=HgS↓ |
| B.用醋酸溶解水垢中的碳酸钙:CaCO3+2CH3COOH=Ca2++2CH3COO-+CO2↑+H2O |
C.实验室用二氧化锰和浓盐酸共热制氯气:MnO2+4H++2Cl- Mn2++Cl2↑+2H2O Mn2++Cl2↑+2H2O |
| D.铜在NH3环境中被腐蚀:2Cu+O2+2NH3·H2O=2Cu2++2NH3+4OH- |
(2024·河北邢台·模拟预测)
A.铅蓄电池充电时阴极的电极反应式: |
B.以铁为电极电解 溶液的阳极的电极反应式: 溶液的阳极的电极反应式: |
C.把铜粉加入含双氧水的氨水中,溶液变蓝: |
D.在 溶液中滴加少量 溶液中滴加少量 溶液: 溶液: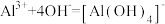 |
(2024·湖南益阳·三模)
A.电解饱和的 溶液: 溶液: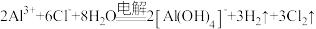 |
B.漂粉精的制备: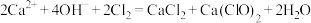 |
C.乙醛的银镜反应: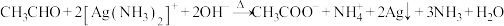 |
D.向胆矾溶液中加入过量的浓氨水: |
(2024·北京·模拟预测)
已知:①图1表示将FeSO4溶液逐滴滴加到含少量NaOH的NaClO溶液中的pH变化;②图2表示NaClO溶液中含氯微粒的物质的量分数与pH的关系[注:饱和NaClO溶液的pH约为11; Ksp[Fe(OH)3]=2.8×10−39]。
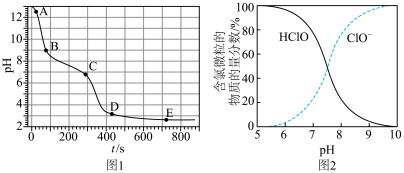
A.A点溶液的pH约为13,主要原因是ClO− + H2O HClO + OH− HClO + OH− |
| B.AB段pH显著下降的原因是5ClO-+2Fe2+ + 5H2O=Cl−+ 2Fe(OH)3↓+ 4HClO |
| C.CD段较BC段pH下降快的主要原因是HClO+2Fe2+ +5H2O=2Fe(OH)3↓+Cl-+ 5H+ |
| D.反应进行至400s时溶液中产生Cl2的原因是:ClO-+ Cl-+2H+=Cl2↑+ H2O |
(2024·北京·模拟预测)
A.用酸性KMnO4标准液滴定草酸:16H++5 +2 +2 = 2Mn2++8H2O+10CO2 ↑ = 2Mn2++8H2O+10CO2 ↑ |
B.用NaClO溶液吸收少量SO2: 2ClO- +SO2+H2O=2HClO+ |
C.向NH4HCO3溶液中加入含Mn2+的溶液生成MnCO3:Mn2++ =MnCO3↓+ H+ =MnCO3↓+ H+ |
D.用稀硝酸洗涤试管内壁的银镜: 3Ag+4H++ = 3Ag++NO↑+2H2O = 3Ag++NO↑+2H2O |
(2024·四川成都·二模)
A.用 溶液腐蚀印刷电路板: 溶液腐蚀印刷电路板: |
B. 溶液与少量 溶液与少量 溶液反应: 溶液反应: |
C.用 溶液吸收 溶液吸收 气体: 气体: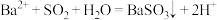 |
D.将 通入含 通入含 的溶液中: 的溶液中: |
(2024·陕西榆林·一模)
A.醋酸除去茶壶中的水垢: |
B. 使酸性 使酸性 溶液褪色: 溶液褪色: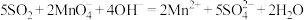 |
C. 溶液中通入少量 溶液中通入少量 |
D. 溶液中通入少量 溶液中通入少量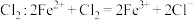 |
(2024·浙江宁波·二模)
A.1.0mol/L氨水溶液( )中: )中: 、 、 、 、 |
B.1.0mol/L氯化钠溶液( )中: )中: 、 、 、 、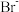 |
C.0.1mol/L碳酸钠溶液( )中: )中: 、 、 、 、 |
D.0.1mol/L酸性高锰酸钾溶液( )中: )中: 、 、 、 、 |
【知识点】 限定条件下的离子共存解读
(2023·黑龙江·模拟预测)
 、
、 、
、 、
、 、
、 、
、 、
、 、
、 中的若干种,且各离子浓度相等,为确定其成分,依次进行下列实验。①取少量溶液X,向其中加入足量的氢氧化钠溶液,有白色沉淀A产生;微热闻到刺激性气味。②过滤①中的混合物,向滤液中加入足量的氢氧化钡溶液,有白色沉淀B产生,再加入足量的稀硝酸,沉淀不溶解。根据上述实验,以下说法不正确的是
中的若干种,且各离子浓度相等,为确定其成分,依次进行下列实验。①取少量溶液X,向其中加入足量的氢氧化钠溶液,有白色沉淀A产生;微热闻到刺激性气味。②过滤①中的混合物,向滤液中加入足量的氢氧化钡溶液,有白色沉淀B产生,再加入足量的稀硝酸,沉淀不溶解。根据上述实验,以下说法不正确的是A.刺激性气味气体是 |
B.溶液X中是否含 、 、 需要通过焰色试验确定 需要通过焰色试验确定 |
| C.白色沉淀A和白色沉淀B都是纯净物 |
D.溶液X中一定没有 ,但一定含有 ,但一定含有 |
【知识点】 限定条件下的离子共存解读 离子的检验
(2024·河北张家口·一模)
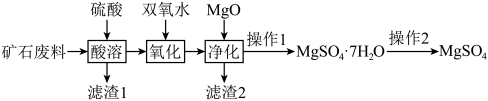
| A.滤渣1的成分为SiO2 |
B.“氧化”时发生反应的离子方程式为: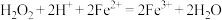 |
| C.“净化”时加入MgO是为了调节溶液的pH使杂质离子沉淀 |
| D.“操作2”可直接将MgSO4·7H2O加热失水制备MgSO4 |
(2024·浙江嘉兴·二模)
A.向银氨溶液中加入过量盐酸: |
B. 溶液中加入 溶液中加入 产生沉淀: 产生沉淀: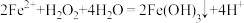 |
C.将二氧化硫通入氢硫酸中产生黄色沉淀: |
D.乙醇与 酸性溶液反应: 酸性溶液反应: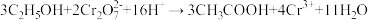 |
(2024·安徽黄山·二模)
A.侯氏制碱法中制备NaHCO3:NH3+CO2+H2O=HCO +NH +NH |
B.酸性条件下催化电解 制 制 的阴极电极反应式为:2CO2+12e−+12H+=CH3CH2OH+3H2O 的阴极电极反应式为:2CO2+12e−+12H+=CH3CH2OH+3H2O |
C.向苯酚钠溶液中通入少量二氧化碳: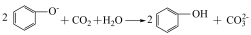 |
D.碳酸铵与氢氧化钙溶液反应:CO +Ca2+=CaCO3↓ +Ca2+=CaCO3↓ |
(2024·湖南长沙·二模)
 、Ba2+、Fe2+、Mg2+、Cl-、
、Ba2+、Fe2+、Mg2+、Cl-、 、
、 、
、 中的一种或几种。取该溶液进行连续实验,实验过程如图所示,下列有关推理错误的是
中的一种或几种。取该溶液进行连续实验,实验过程如图所示,下列有关推理错误的是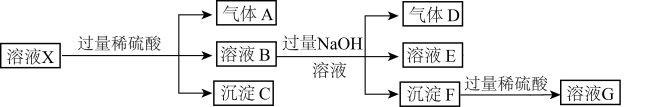
A.溶液X中一定不存在的阴离子为 和 和 |
B.生成气体A的离子方程式为3Fe2++ +4H+=3Fe3++NO↑+2H2O +4H+=3Fe3++NO↑+2H2O |
| C.气体D能使湿润的红色石蕊试纸变蓝 |
| D.溶液G中一定含有的阳离子为H+、Mg2+、Fe3+、Fe2+ |



 溶液与
溶液与

 :
:


