解题方法
1 . 实验室以一种工业废渣(主要成分为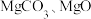 和
和 )为原料制备
)为原料制备 ,其实验流程如下:
,其实验流程如下:

(1)“酸浸”时能提高浸出速率的方法有___________ 、___________ (答两条即可)。
(2)“滤渣I”主要成分是___________ (填化学式)。
(3)“反应”步骤中,碳酸钠与硫酸镁反应生成 的化学方程式:
的化学方程式:___________ 。
(4)“洗涤”过程中所用的乙醇中所含官能团的名称为___________ ,向乙醇中滴加几滴酸性高锰酸钾溶液,溶液仍呈无色,由此说明乙醇具有___________ 性。
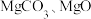 和
和 )为原料制备
)为原料制备 ,其实验流程如下:
,其实验流程如下:
(1)“酸浸”时能提高浸出速率的方法有
(2)“滤渣I”主要成分是
(3)“反应”步骤中,碳酸钠与硫酸镁反应生成
 的化学方程式:
的化学方程式:(4)“洗涤”过程中所用的乙醇中所含官能团的名称为
您最近一年使用:0次
名校
解题方法
2 . 反应C(s)+H2O(g)  CO(g)+H2(g)在一体积可变的容器中进行,则下列条件的改变使其反应速率增大的是
CO(g)+H2(g)在一体积可变的容器中进行,则下列条件的改变使其反应速率增大的是
 CO(g)+H2(g)在一体积可变的容器中进行,则下列条件的改变使其反应速率增大的是
CO(g)+H2(g)在一体积可变的容器中进行,则下列条件的改变使其反应速率增大的是| A.降低温度 | B.将容器的体积缩小一半 |
| C.将容器的体积拉大到原来的2倍 | D.增加C的量 |
您最近一年使用:0次
2024-02-26更新
|
789次组卷
|
4卷引用:新疆乌鲁木齐市第十一中学2023-2024学年高一下学期期中测试化学试卷
23-24高一下·全国·课后作业
名校
3 . 为研究不同状态 块状、粉末状
块状、粉末状 碳酸钙固体与盐酸反应的反应速率,某同学通过实验测定数据得出如图所示的曲线。下列有关说法中正确的
碳酸钙固体与盐酸反应的反应速率,某同学通过实验测定数据得出如图所示的曲线。下列有关说法中正确的
 块状、粉末状
块状、粉末状 碳酸钙固体与盐酸反应的反应速率,某同学通过实验测定数据得出如图所示的曲线。下列有关说法中正确的
碳酸钙固体与盐酸反应的反应速率,某同学通过实验测定数据得出如图所示的曲线。下列有关说法中正确的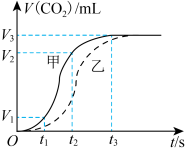
| A.曲线乙表示的是粉末状碳酸钙固体与盐酸反应 |
| B.随着反应进行,盐酸浓度降低,反应速率不断降低 |
C.若用单位时间内 的体积变化来表示该反应的速率,则甲线中 的体积变化来表示该反应的速率,则甲线中 时间内平均反应速率为 时间内平均反应速率为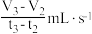 |
D.两次实验,粉末状固体最终生成的 的量更多 的量更多 |
您最近一年使用:0次
2024-02-24更新
|
455次组卷
|
3卷引用:新疆克孜勒苏柯尔克孜自治州第二中学2022-2023学年高一下学期期末考试化学试题
新疆克孜勒苏柯尔克孜自治州第二中学2022-2023学年高一下学期期末考试化学试题(已下线)6.2.1化学反应的速率课后作业提高篇广东省广州市广东番禺中学2023-2024学年高一下学期期中考试化学试题
名校
4 . 下列措施能明显加快反应速率的是
| A.Na与水反应,增加水的用量 |
B.C与 反应中,恒压充入 反应中,恒压充入 |
C.Fe与稀硫酸反应制取 ,改用浓硫酸 ,改用浓硫酸 |
D.大理石和盐酸反应制取 ,将块状大理石改为粉末状 ,将块状大理石改为粉末状 |
您最近一年使用:0次
2023-12-14更新
|
54次组卷
|
2卷引用:新疆兵团第三师图木舒克市鸿德实验学校2023-2024学年高二上学期第二次月考化学试题
解题方法
5 . 等质量的金属锌与足量的硫酸在不同条件下的反应如下表所示,其中放出 最快的一组是
最快的一组是
 最快的一组是
最快的一组是| 组别 | 锌的状态 | 硫酸的浓度 | 反应温度 |
| A | 颗粒状 | 2mol/L | 20℃ |
| B | 颗粒状 | 2mol/L | 55℃ |
| C | 颗粒状 | 4mol/L | 60℃ |
| D | 颗粒状 | 15mol/L | 80℃ |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-12-03更新
|
74次组卷
|
2卷引用:新疆兵团第三师图木舒克市鸿德实验学校2023-2024学年高二上学期第二次月考化学试题
名校
解题方法
6 . 硫酸是重要的化工材料,二氧化硫生成三氧化硫是工业制硫酸的重要反应之一、
(1)将0.050 mol 和0.030 mol
和0.030 mol  放入容积为1 L的密闭容器中,反应
放入容积为1 L的密闭容器中,反应 在一定条件下达到平衡,测得
在一定条件下达到平衡,测得 。
。
①从平衡角度分析,采用过量 的目的是
的目的是___________ ;
②在上述反应达平衡后,在恒温恒容条件下,再向容器内充入0.01 mol 和0.02 mol
和0.02 mol  ,此时反应向
,此时反应向___________ 移动(“正向”或“逆向”)。
③对于气相反应,用某组分(B)的平衡分压(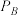 )代替其物质的量浓度(
)代替其物质的量浓度( )也可以表示平衡常数(记作
)也可以表示平衡常数(记作 ),已知:B的平衡分压=总压×平衡时B的物质的量分数,则该温度下
),已知:B的平衡分压=总压×平衡时B的物质的量分数,则该温度下
___________ 。(总压为P0)
④已知: ,若反应温度升高,
,若反应温度升高, 的转化率
的转化率___________ (填“增大”、“减小”或“不变”)。
(2)某课外兴趣小组实验探究影响化学反应速率的因素。
硫代硫酸钠( )俗称大苏打、海波,广泛应用于照相定影等领域。乙同学利用控制变量法探究影响硫代硫酸钠与稀硫酸反应速率的因素时,设计了如下系列实验:
)俗称大苏打、海波,广泛应用于照相定影等领域。乙同学利用控制变量法探究影响硫代硫酸钠与稀硫酸反应速率的因素时,设计了如下系列实验:
①从类别的角度分析,硫代硫酸钠( )属于
)属于________ (填序号)。
A.盐 B.碱 C.酸 D.氧化物
②写出硫代硫酸钠与稀硫酸反应的化学方程式________ 。
③该实验1和2可探究________ 对反应速率的影响,因此 是
是________ 。实验1和3可探究硫酸浓度对反应速率的影响,因此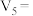
________ 。
④实验中利用了出现黄色沉淀的快慢来比较反应速率的快慢,请你分析为何不采用测量单位时间内产生气体体积的大小进行比较________ 。
(1)将0.050 mol
 和0.030 mol
和0.030 mol  放入容积为1 L的密闭容器中,反应
放入容积为1 L的密闭容器中,反应 在一定条件下达到平衡,测得
在一定条件下达到平衡,测得 。
。①从平衡角度分析,采用过量
 的目的是
的目的是②在上述反应达平衡后,在恒温恒容条件下,再向容器内充入0.01 mol
 和0.02 mol
和0.02 mol  ,此时反应向
,此时反应向③对于气相反应,用某组分(B)的平衡分压(
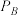 )代替其物质的量浓度(
)代替其物质的量浓度( )也可以表示平衡常数(记作
)也可以表示平衡常数(记作 ),已知:B的平衡分压=总压×平衡时B的物质的量分数,则该温度下
),已知:B的平衡分压=总压×平衡时B的物质的量分数,则该温度下
④已知:
 ,若反应温度升高,
,若反应温度升高, 的转化率
的转化率(2)某课外兴趣小组实验探究影响化学反应速率的因素。
硫代硫酸钠(
 )俗称大苏打、海波,广泛应用于照相定影等领域。乙同学利用控制变量法探究影响硫代硫酸钠与稀硫酸反应速率的因素时,设计了如下系列实验:
)俗称大苏打、海波,广泛应用于照相定影等领域。乙同学利用控制变量法探究影响硫代硫酸钠与稀硫酸反应速率的因素时,设计了如下系列实验:| 实验序号 | 反应温度/℃ |  浓度 浓度 | 稀硫酸 |  | ||
| V/mL | c/(mol/L) | V/mL | c/(mol/L) | V/mL | ||
| 1 | 20 | 10.0 | 0.10 | 10.0 | 0.50 | 0 |
| 2 | 40 |  | 0.10 |  | 0.50 |  |
| 3 | 20 |  | 0.10 | 4.0 | 0.50 |  |
 )属于
)属于A.盐 B.碱 C.酸 D.氧化物
②写出硫代硫酸钠与稀硫酸反应的化学方程式
③该实验1和2可探究
 是
是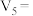
④实验中利用了出现黄色沉淀的快慢来比较反应速率的快慢,请你分析为何不采用测量单位时间内产生气体体积的大小进行比较
您最近一年使用:0次
名校
解题方法
7 . 稀硫酸与过量锌粉反应,为减缓反应速率,且不影响生成氢气的总量,可加入的物质是:
①水②Na2CO3溶液③Na2SO4溶液④CH3COONa溶液⑤少量K2SO4固体⑥几滴CuSO4溶液
①水②Na2CO3溶液③Na2SO4溶液④CH3COONa溶液⑤少量K2SO4固体⑥几滴CuSO4溶液
| A.①②⑥ | B.②③④ | C.①③④ | D.③④⑤ |
您最近一年使用:0次
2023-11-12更新
|
260次组卷
|
5卷引用:新疆生产建设兵团第三师图木舒克市第一中学2023-2024学年高二上学期第二次月考试化学试卷
新疆生产建设兵团第三师图木舒克市第一中学2023-2024学年高二上学期第二次月考试化学试卷浙江省浙南名校联盟2023-2024学年高二上学期11月期中考试化学试题【定心卷】2.1.2 影响化学反应速率的因素随堂练习-人教版2023-2024学年选择性必修1(已下线)寒假作业02 化学反应速率-【寒假分层作业】2024年高二化学寒假培优练(人教版2019)陕西省安康市2023-2024学年高二上学期12月联考化学试题
名校
8 . 某小组利用硫代硫酸钠溶液与稀硫酸反应:Na2S2O3+H2SO4=Na2SO4+S↓+SO2↑+H2O,探究反应条件对速率的影响,下列有关说法不正确的是
| 选项 | 反应温度/℃ | Na2S2O3溶液 | 稀H2SO4 | H2O | ||
| V/mL | c/(mol/L) | V/mL | c/(mol/L) | V/mL | ||
| ① | 25 | 10 | 0.1 | 10 | 0.1 | 0 |
| ② | 25 | 5 | 0.1 | 10 | 0.1 | x |
| ③ | 50 | 10 | 0.1 | 5 | 0.2 | 5 |
| A.可通过产生浑浊的时间判断反应的快慢 |
| B.①②两组实验可探究Na2S2O3浓度对反应速率的影响,则x=5 |
| C.①③两组实验可探究温度对反应速率的影响 |
| D.实验结束后,有少量S附着在试管上,可以用水冲洗干净 |
您最近一年使用:0次
2023-11-10更新
|
77次组卷
|
2卷引用:新疆生产建设兵团第三师图木舒克市第一中学2023-2024学年高二下学期开学考试化学试卷
名校
解题方法
9 . 丙酮碘化反应为兴趣小组在20℃时研究了该反应的反应速。他们在反应开始前加入淀粉溶液,通过观察淀粉溶液褪色时间来度量反应速举的大小。实验数据如下表,其中①~④混合液总体积相同。
下列根据实验数据做出的推理不合理的是
| 序号 | c(丙酮) | c(I2) | c(H+) | 褪色时间/s |
| ① | 2 | 0.002 | 0.5 | 40 |
| ② | 1 | 0.002 | 0.5 | 80 |
| ③ | 2 | 0.001 | 0.5 | 20 |
| ④ | 2 | 0.002 | 0.25 | 80 |
| A.实验①中,ν(I2)=5×10-5mol·L-1·s-1 |
| B.由实验①②可知c(丙酮)越大,反应速率越快 |
| C.由实验①③可知c(I2)越大,反应速率越慢 |
| D.由实验①④可知,c(H+)越大,反应速率越快 |
您最近一年使用:0次
2023-10-29更新
|
123次组卷
|
13卷引用:新疆乌鲁木齐市第八中学2022-2023学年高一下学期期中考试化学试题
新疆乌鲁木齐市第八中学2022-2023学年高一下学期期中考试化学试题北京海淀区2022-2023学年高二上学期期末考试化学试题北京一零一中学2022-2023高二上学期期末考试化学试题北京市首都师范大学附属中学2022-2023学年高二上学期期末考试化学试题辽宁省名校联盟2023-2024学年高二上学期期初考试化学试题辽宁省锦州市黑山县名校联盟试2023-2024学年高二上学期开学考试化学试题辽宁省辽东南协作校2023-2024学年高二上学期10月月考化学试题北京市丰台区2023-2024学年高二上学期期中联考(A卷)化学试题辽宁省大连市第四十八中学2023-2024学年高二上学期10月月考化学试题四川省广元市苍溪中学校2023-2024学年高二上学期10月月考化学试题北京市第十三中学2023-2024学年高二上学期期中考试化学试题(已下线)寒假收官卷01-【寒假分层作业】2024年高二化学寒假培优练(人教版2019)四川省德阳市什邡中学2023-2024学年高二上学期11月期中考试化学试题
名校
解题方法
10 . 我国力争2030年前实现碳达峰,2060年前实现碳中和。 的捕集利用已成为科学家们研究的重要课题。
的捕集利用已成为科学家们研究的重要课题。 加氢可转化为二甲醚
加氢可转化为二甲醚 ,反应原理为:
,反应原理为: 。该反应的能量变化如图所示。
。该反应的能量变化如图所示。
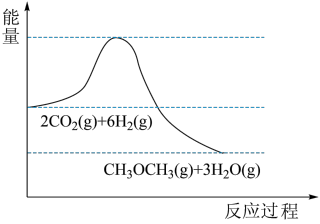
回答问题:
(1)该反应为_____ (填“放热”或“吸热”)反应。
(2)在固定体积的密闭容器中发生该反应,能说明该反应达到平衡状态的是_____ (填字母)。
a. 的含量保持不变
的含量保持不变
b.混合气体的密度不变
c.混合气体的平均相对分子质量不变
d.
(3)在体积为 密闭容器中充入
密闭容器中充入 和
和 ,测得
,测得 、
、 的物质的量随时间变化如图所示。
的物质的量随时间变化如图所示。
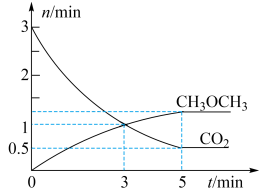

回答下列问题:
① 内,
内,
_____ 。
②反应达到平衡状态时, 的体积分数为
的体积分数为_____ %(保留1位小数)。
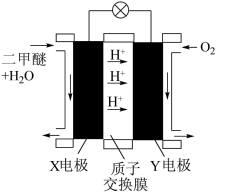
③“二甲醚 酸性燃料池”的工作原理示意图如图所示。X电极反应式
酸性燃料池”的工作原理示意图如图所示。X电极反应式_____ ;若此燃料电池电路中转移 电子,则消耗的
电子,则消耗的 在标准状况下的体积为
在标准状况下的体积为_____ L。
(4)实验室用 溶液与
溶液与 溶液反应探究条件的改变对化学反应速率的影响,设计的实验方案如下表(已知
溶液反应探究条件的改变对化学反应速率的影响,设计的实验方案如下表(已知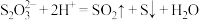 ):
):
①对比实验1和2可探究_____ 因素对化学反应速率的影响。
②对比实验1和3来探究浓度对化学反应速率的影响,则
_____ 。
 的捕集利用已成为科学家们研究的重要课题。
的捕集利用已成为科学家们研究的重要课题。 加氢可转化为二甲醚
加氢可转化为二甲醚 ,反应原理为:
,反应原理为: 。该反应的能量变化如图所示。
。该反应的能量变化如图所示。
回答问题:
(1)该反应为
(2)在固定体积的密闭容器中发生该反应,能说明该反应达到平衡状态的是
a.
 的含量保持不变
的含量保持不变b.混合气体的密度不变
c.混合气体的平均相对分子质量不变
d.

(3)在体积为
 密闭容器中充入
密闭容器中充入 和
和 ,测得
,测得 、
、 的物质的量随时间变化如图所示。
的物质的量随时间变化如图所示。

回答下列问题:
①
 内,
内,
②反应达到平衡状态时,
 的体积分数为
的体积分数为③“二甲醚
 酸性燃料池”的工作原理示意图如图所示。X电极反应式
酸性燃料池”的工作原理示意图如图所示。X电极反应式 电子,则消耗的
电子,则消耗的 在标准状况下的体积为
在标准状况下的体积为
(4)实验室用
 溶液与
溶液与 溶液反应探究条件的改变对化学反应速率的影响,设计的实验方案如下表(已知
溶液反应探究条件的改变对化学反应速率的影响,设计的实验方案如下表(已知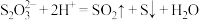 ):
):| 实验序号 | 体积/mL | 温度/℃ | 溶液出现浑浊的时间/s | ||
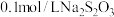 溶液 溶液 | 水 | 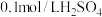 溶液 溶液 | |||
| 1 | 2.0 | 0.0 | 2.0 | 25 | 8 |
| 2 | 2.0 | 0.0 | 2.0 | 50 | 5 |
| 3 | 1.0 | V | 2.0 | 25 | 10 |
②对比实验1和3来探究浓度对化学反应速率的影响,则

您最近一年使用:0次
2023-08-15更新
|
268次组卷
|
2卷引用:新疆生产建设兵团第三师图木舒克市第一中学2023-2024学年高二下学期开学考试化学试卷



