名校
解题方法
1 . 有关反应 N2+3H2 2NH3的说法正确的是
2NH3的说法正确的是
 2NH3的说法正确的是
2NH3的说法正确的是| A.升高温度可减慢反应速率 | B.使用催化剂可提高反应速率 |
| C.达到平衡时,N2的v(正)=v(逆)=0 | D.达到平衡时 H2 转化率可达 100% |
您最近一年使用:0次
解题方法
2 . 回答下列问题:
(1)将除去氧化膜的镁条插入到稀盐酸溶液中,发现生成氢气的速度变化情况如下图所示: 速度变化的主要原因
速度变化的主要原因______________ 。
② 速度变化的主要原因是
速度变化的主要原因是_____________ 。
(2)实验室配制FeSO4溶液,溶解时先要加入少量的稀硫酸,其原因是____________ ;配制完毕后要加入少量铁屑,其目的是______________ 。
(1)将除去氧化膜的镁条插入到稀盐酸溶液中,发现生成氢气的速度变化情况如下图所示:
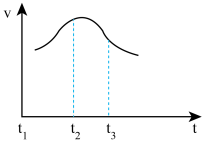
 速度变化的主要原因
速度变化的主要原因②
 速度变化的主要原因是
速度变化的主要原因是(2)实验室配制FeSO4溶液,溶解时先要加入少量的稀硫酸,其原因是
您最近一年使用:0次
名校
解题方法
3 . 等质量的铁与过量的盐酸在不同的实验条件下进行反应,测定反应过程中产生氢气体积V的数据,根据数据绘制得如图,则曲线a、b、c、d所对应的实验组别,有关说法错误的是
| 实验组别 |  | 温度/ ℃ | 形状(Fe) |
| Ⅰ | 2.0 | 30 | 块状 |
| Ⅱ | 2.5 | 30 | 块状 |
| Ⅲ | 2.5 | 50 | 粉末状 |
| Ⅳ | 2.5 | 50 | 块状 |
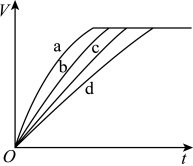
| A.曲线a对应的实验组别为Ⅲ |
| B.对比实验Ⅰ、Ⅱ说明浓度对化学反应速率的影响 |
| C.对比实验Ⅱ、Ⅳ说明温度对化学反应速率的影响 |
| D.曲线a、b、c、d对应的实验组别分别为Ⅳ、Ⅲ、Ⅱ、Ⅰ |
您最近一年使用:0次
2024-04-30更新
|
118次组卷
|
2卷引用:宁夏石嘴山市第三中学2023-2024学年高一下学期4月期中考试化学试题
4 . 钢渣是钢铁行业的固体废弃物,含有2CaO·SiO2、Fe2O3、FeO、Al2O3和V2O3等物质。一种以钢渣粉为原料固定CO2并制备V2O3的工艺流程如图所示。
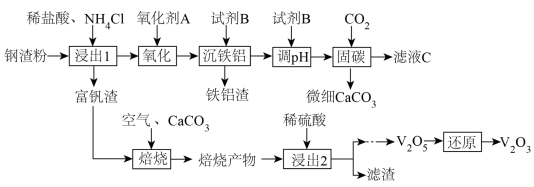
已知钢渣中Ca元素质量分数为30%。V2O3在稀盐酸和NH4Cl混合溶液中不易被浸出。该工艺条件下,有关金属离子开始沉淀和沉淀完全的pH如下表所示:
回答下列问题:
(1)浸出1过程生成的SiO2“包裹”在钢渣表面形成固体膜,阻碍反应物向钢渣扩散。提高浸出率的措施有_______ (除粉碎外,举1例)。该浸出过程不使用稀硫酸代替稀盐酸的原因是_______ 。
(2)为避免引入杂质离子,氧化剂A应为_______ (举1例)。
(3)滤液C的溶质可循环利用,试剂B应为_______ 。
(4)若钢渣粉中含有钒酸钙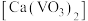 ,加入Na2CO3溶液能够使钒酸钙溶解,是因为存在平衡:
,加入Na2CO3溶液能够使钒酸钙溶解,是因为存在平衡: 。已知
。已知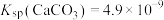 ,
,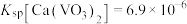 ,则该平衡常数
,则该平衡常数
_______ (结果保留2位有效数字)。
(5)富钒渣焙烧可生成钒钙盐,不同钒钙盐的溶解率随pH变化如图所示。已知浸出2的pH约为2.5,则应控制焙烧条件使该钒钙盐为_______ 。该培烧反应的化学方程式是_______ 。

(6)若Ca的浸出率为90%,理论上1吨钢渣在“固碳”中可固定_______ kgCO2。

已知钢渣中Ca元素质量分数为30%。V2O3在稀盐酸和NH4Cl混合溶液中不易被浸出。该工艺条件下,有关金属离子开始沉淀和沉淀完全的pH如下表所示:
| 金属离子 | Fe3+ | Fe2+ | Al3+ | Ca2+ |
| 开始沉淀的pH | 1.9 | 7.2 | 3.5 | 12.4 |
| 沉淀完全的pH | 2.9 | 8.2 | 5.1 | 13.8 |
(1)浸出1过程生成的SiO2“包裹”在钢渣表面形成固体膜,阻碍反应物向钢渣扩散。提高浸出率的措施有
(2)为避免引入杂质离子,氧化剂A应为
(3)滤液C的溶质可循环利用,试剂B应为
(4)若钢渣粉中含有钒酸钙
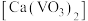 ,加入Na2CO3溶液能够使钒酸钙溶解,是因为存在平衡:
,加入Na2CO3溶液能够使钒酸钙溶解,是因为存在平衡: 。已知
。已知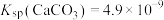 ,
,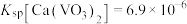 ,则该平衡常数
,则该平衡常数
(5)富钒渣焙烧可生成钒钙盐,不同钒钙盐的溶解率随pH变化如图所示。已知浸出2的pH约为2.5,则应控制焙烧条件使该钒钙盐为

(6)若Ca的浸出率为90%,理论上1吨钢渣在“固碳”中可固定
您最近一年使用:0次
名校
解题方法
5 . 在一定条件下,将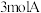 和
和 投入容积
投入容积 且容积不变的密闭容器中,发生如下反应:
且容积不变的密闭容器中,发生如下反应: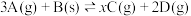 。2min末测得此时容器中
。2min末测得此时容器中 和
和 的浓度为
的浓度为 和
和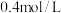 。下列叙述正确的是
。下列叙述正确的是
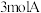 和
和 投入容积
投入容积 且容积不变的密闭容器中,发生如下反应:
且容积不变的密闭容器中,发生如下反应: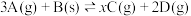 。2min末测得此时容器中
。2min末测得此时容器中 和
和 的浓度为
的浓度为 和
和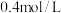 。下列叙述正确的是
。下列叙述正确的是A. |
B.此时 的物质的量分数为 的物质的量分数为 |
C. 内 内 的反应速率为 的反应速率为 |
| D.充入氦气压强增大,化学反应速率加快,平衡逆向移动 |
您最近一年使用:0次
2023-10-12更新
|
197次组卷
|
2卷引用:宁夏青铜峡市宁朔中学2023-2024学年高二上学期期中考试化学试题
名校
解题方法
6 . 某同学根据外界条件对化学反应速率的影响原理,设计了硫代硫酸钠与硫酸反应有关实验,实验过程的数据记录如下表,请结合表中信息,回答有关问题:
(1)写出上述反应的离子方程式___________ 。
(2)能说明温度对该反应速率影响的组合比较是___________ (填实验序号);
(3)C1___________ ;
___________ 。
(4)A和B、A和C的组合比较所研究的问题分别是___________ 、___________ 。
| 实验序号 | 反应温度 | 参加反应的物质 | ||||
 |  |  | ||||
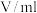 | 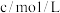 | 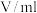 | 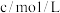 | 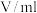 | ||
 |  |  |  |  |  |  |
 |  |  |  |  |  |  |
| C |  |  |  |  |  |  |
 |  |  |  |  |  |  |
(2)能说明温度对该反应速率影响的组合比较是
(3)C1

(4)A和B、A和C的组合比较所研究的问题分别是
您最近一年使用:0次
名校
7 . 为探究锌与0.1 mol/L稀硫酸的反应速率[以υ(H2)表示],对反应物作出如下改变。下列判断正确的是
| A.加入NH4HSO4固体,υ(H2)不变 |
| B.加入少量水,υ(H2)减小 |
| C.把0.1 mol/L稀硫酸改为0.2 mol/L盐酸,υ(H2)增大 |
| D.把稀硫酸改为98%的浓硫酸,υ(H2)增大 |
您最近一年使用:0次
2023-08-27更新
|
771次组卷
|
4卷引用:宁夏青铜峡市宁朔中学2023-2024学年高二上学期期中考试化学试题
名校
8 . 定条件下,发生反应A(g)+B(g) C(g) △H>0,达到平衡后根据下列图像判断:
C(g) △H>0,达到平衡后根据下列图像判断:
A.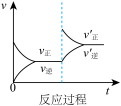 B.
B.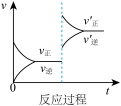 C.
C. D.
D.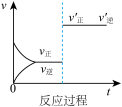 E.
E.
(1)表示升高温度,达到新平衡的是图______ (填“A”、“B”、“C”、“D”或“E”,下同),新平衡中C的质量分数______ (填“增大”、“减小”或“不变”,下同)。
(2)表示降低压强,达到新平衡的是图______ ,A的转化率______ 。
(3)表示减少C的浓度,达到新平衡的是图______ ,表示使用催化剂,达新平衡的是图。
(4)增加A的浓度,达到新平衡的是图______ ,达到平衡后A的转化率______ 。
 C(g) △H>0,达到平衡后根据下列图像判断:
C(g) △H>0,达到平衡后根据下列图像判断:A.
 B.
B. C.
C. D.
D. E.
E.
(1)表示升高温度,达到新平衡的是图
(2)表示降低压强,达到新平衡的是图
(3)表示减少C的浓度,达到新平衡的是图
(4)增加A的浓度,达到新平衡的是图
您最近一年使用:0次
2023-04-24更新
|
264次组卷
|
2卷引用:宁夏青铜峡市宁朔中学2023-2024学年高二上学期期中考试化学试题
名校
解题方法
9 . 某同学探究外界条件对H2O2分解速率的影响实验所用试剂:0.4mol·L-1H2O2溶液、蒸馏水、MnO2粉末、Fe2O3粉。
(1)实验1、2的目的是其他条件相同时,研究___________ 对H2O2分解速率的影响。
(2)表中a处所用试剂为___________ 。对比实验3、4可得出的结论是___________ 。
(3)实验3、5是其他条件相同时,探究浓度对该化学反应速率的影响。b处取用10mL0.4mol·L-1H2O2溶液,还应添加的试剂及用量为___________ 。
(4)控制其他条件相同,印刷电路板的金属粉末用0.4mol·L-1H2O2溶液和3.0mol·L-1 H2SO4溶液处理。
①请配平方程式:___________
___________Cu+___________H2O2+___________H+=___________Cu2++___________H2O
②某同学在不同温度下完成该实验,测得铜的平均溶解速率分别为:
当温度高于40℃时,铜的平均溶解速率随着反应温度的升高而下降,其主要原因是:___________ 。
实验序号 | H2O2浓度(mol·L-1) | v(H2O2溶液)(mL) | 温度 | 催化剂 | 收集112mLO2所需时间(s) |
1 | 0.4 | 20 | 室温 | 无 | 几乎无气体产生 |
2 | 0.4 | 20 | 50℃水浴 | 无 | 296 |
3 | 0.4 | 20 | 室温 | 0.5g a | 45 |
4 | 0.4 | 20 | 室温 | 0.5gMnO2粉末 | 100 |
5 | 0.4 | b | 室温 | a | >45 |
(2)表中a处所用试剂为
(3)实验3、5是其他条件相同时,探究浓度对该化学反应速率的影响。b处取用10mL0.4mol·L-1H2O2溶液,还应添加的试剂及用量为
(4)控制其他条件相同,印刷电路板的金属粉末用0.4mol·L-1H2O2溶液和3.0mol·L-1 H2SO4溶液处理。
①请配平方程式:
___________Cu+___________H2O2+___________H+=___________Cu2++___________H2O
②某同学在不同温度下完成该实验,测得铜的平均溶解速率分别为:
温度(℃) | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
铜的平均溶解速率( | 7.34 | 8.01 | 9.25 | 7.98 | 7.24 | 6.73 | 5.76 |
您最近一年使用:0次
2021-12-02更新
|
183次组卷
|
7卷引用:宁夏六盘山高级中学2021-2022学年高二上学期期中考试化学试题
宁夏六盘山高级中学2021-2022学年高二上学期期中考试化学试题北京市丰台区2020-2021学年高一下学期期中联考化学(A卷)试题(已下线)作业03 化学反应速率-2021年高二化学暑假作业(人教版2019)(已下线)2.2 影响化学反应速率的因素-2021-2022学年高二化学课后培优练(人教版选修4)(已下线)第2章 化学反应速率和化学平衡(选拔卷)-【单元测试】2021-2022学年高二化学尖子生选拔卷(人教版选修4)(已下线)2.1.2 影响化学反应速率的因素(素养提优B练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)安徽省黄山市屯溪第一中学2022-2023学年高二上学期期中质量检测(选择性考试) 化学试题
9-10高二下·海南·期中
名校
解题方法
10 . 在下列影响化学反应速率的外界因素中,肯定能使化学反应速率加快的方法是
①升高温度 ②使用催化剂 ③增大反应物浓度 ④将块状固体反应物磨成粉末 ⑤增大压强
①升高温度 ②使用催化剂 ③增大反应物浓度 ④将块状固体反应物磨成粉末 ⑤增大压强
| A.①②③⑤ | B.①②④⑤ | C.①③④ | D.①②③④ |
您最近一年使用:0次
2021-12-02更新
|
460次组卷
|
19卷引用:宁夏六盘山高级中学2021-2022学年高二上学期期中考试化学试题
宁夏六盘山高级中学2021-2022学年高二上学期期中考试化学试题(已下线)2010年海南省海南中学高二第二学期期中考试化学(文)试卷(已下线)2010-2011学年广东省龙山中学高一下学期期中考试化学试卷(已下线)2011-2012学年吉林省四校高一下学期期中联考化学试卷(已下线)2013-2014学年贵州省重点高中高二上学期期中考试理科化学试卷2014-2015学年黑龙江省伊春市伊春二中高二上学期期中化学试卷2014-2015河南省周口中英文学校高一下学期期中考试化学试卷辽宁省大石桥市第二高级中学2016-2017学年高二学业水平模拟测试化学试题黑龙江省牡丹江市第一高级中学2016-2017学年高一下学期期末考试化学试题山东省德州市第二中学2018-2019学年高一下学期第一次模块检测(A卷)化学试题广西桂林市第十八中学2019-2020学年高二上学期期中考试化学(文)试题重庆市永川景圣中学校2021-2022学年高二上学期第一次月考化学试题湖北省襄阳市第一中学2021-2022学年高一下学期4月月考化学试题重庆市巫山大昌中学校2021-2022学年高一下学期期末考试化学试题黑龙江省鸡西市密山市第四中学2021-2022学年高二上学期期末考试化学试题安徽省宿州市十三所重点中学2022-2023学年高二上学期期中质量检测化学试题四川省绵阳市南山中学实验学校2022-2023学年高一下学期5月月考化学试题西藏林芝市第二高级中学2022-2023学年高一下学期期末考试化学试题湖北省武汉三牛中学2023-2024学年高一下学期3月月考 化学试

 )
)

