名校
解题方法
1 . 等质量的铁与过量的盐酸在不同的实验条件下进行反应,测定反应过程中产生氢气体积V的数据,根据数据绘制得如图,则曲线a、b、c、d所对应的实验组别,有关说法错误的是
| 实验组别 |  | 温度/ ℃ | 形状(Fe) |
| Ⅰ | 2.0 | 30 | 块状 |
| Ⅱ | 2.5 | 30 | 块状 |
| Ⅲ | 2.5 | 50 | 粉末状 |
| Ⅳ | 2.5 | 50 | 块状 |
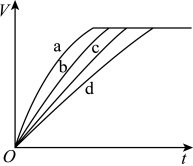
| A.曲线a对应的实验组别为Ⅲ |
| B.对比实验Ⅰ、Ⅱ说明浓度对化学反应速率的影响 |
| C.对比实验Ⅱ、Ⅳ说明温度对化学反应速率的影响 |
| D.曲线a、b、c、d对应的实验组别分别为Ⅳ、Ⅲ、Ⅱ、Ⅰ |
您最近一年使用:0次
2024-04-30更新
|
118次组卷
|
2卷引用:名校期中好题汇编-化学反应与能量(选择题)
名校
解题方法
2 . 在C(s)+CO2(g)=2CO(g)的反应中,现采取下列措施:①缩小体积,增大压强②增加碳的量③通入CO2 ④恒容下充入N2 ⑤恒压下充入N2,上述能够使反应速率增大的措施是
| A.①④ | B.②③⑤ | C.①③ | D.①②④ |
您最近一年使用:0次
名校
解题方法
3 . I.在一定温度下,4L密闭容器内某一反应中气体M、气体N的物质的量随时间变化的曲线如图: 时刻,正逆反应速率大小
时刻,正逆反应速率大小
___________  。(填“>”“=”或“<”)
。(填“>”“=”或“<”)
(2)若 ,计算反应开始至
,计算反应开始至 时刻用M的浓度变化表示的平均反应速率
时刻用M的浓度变化表示的平均反应速率___________ 。
(3) 时刻化学反应达到平衡,反应物的转化率为
时刻化学反应达到平衡,反应物的转化率为___________ 。
(4)如果升高温度,则
___________ (填“增大”“减小”或“不变”)。
Ⅱ.某同学设计如下实验方案探究影响锌与稀硫酸反应速率的因素,有关数据如下表所示:
(5)①本实验待测数据可以是___________ ,实验 和实验
和实验 可以探究
可以探究___________ 对锌与稀硫酸反应速率的影响﹔实验 和实验
和实验 可以探究
可以探究___________ 对锌与稀硫酸反应速率的影响。
②实验发现 比实验
比实验 反应速率快,原因是
反应速率快,原因是___________ 。

 时刻,正逆反应速率大小
时刻,正逆反应速率大小
 。(填“>”“=”或“<”)
。(填“>”“=”或“<”)(2)若
 ,计算反应开始至
,计算反应开始至 时刻用M的浓度变化表示的平均反应速率
时刻用M的浓度变化表示的平均反应速率(3)
 时刻化学反应达到平衡,反应物的转化率为
时刻化学反应达到平衡,反应物的转化率为(4)如果升高温度,则

Ⅱ.某同学设计如下实验方案探究影响锌与稀硫酸反应速率的因素,有关数据如下表所示:
| 序号 | 纯锌粉/g |  硫酸溶液/mL 硫酸溶液/mL | 温度/℃ | 硫酸铜固体/g | 加入蒸馏水/mL |
 | 2.0 | 50.0 | 25 | 0 | 0 |
 | 2.0 | 40.0 | 25 | 0 | 10.0 |
 | 2.0 | 50.0 | 25 | 0.2 | 0 |
 | 2.0 | 50.0 | 35 | 0 | 0 |
(5)①本实验待测数据可以是
 和实验
和实验 可以探究
可以探究 和实验
和实验 可以探究
可以探究②实验发现
 比实验
比实验 反应速率快,原因是
反应速率快,原因是
您最近一年使用:0次
2024-04-28更新
|
334次组卷
|
2卷引用:安徽省合肥市六校联盟2023-2024学年高一下学期4月期中考试化学试题
名校
解题方法
4 . Ⅰ.断开1 mol AB(g)分子中的化学键使其分别生成气态A原子和气态B原子所吸收的能量称为A—B的键能。下表列出了一些化学键的键能(E):
请回答下列问题:
(1)如图表示某反应的能量变化关系,则此反应_______ (填“吸收”或“放出”)_______ kJ能量(用含有a、b的关系式表示)。 O2(g)=H2O(g)放出241.8 kJ能量,则根据所给键能数据可得x=
O2(g)=H2O(g)放出241.8 kJ能量,则根据所给键能数据可得x=_______ 。
(3)历史上曾用“地康法”制氯气,这一方法是用CuCl2作催化剂,在450 ℃时利用空气中的氧气与氯化氢反应制氯气。反应的化学方程式为_______ 。
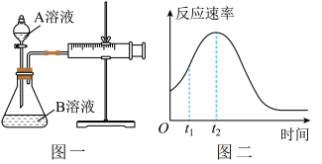
Ⅱ.用酸性KMnO4和H2C2O4(草酸)反应研究影响反应速率的因素,离子方程式为2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O。一实验小组欲通过测定单位时间内生成CO2的速率,探究某种影响化学反应速率的因素,设计实验方案如下(KMnO4溶液已酸化):
(4)该实验探究的是_______ 因素对化学反应速率的影响。如下图一,相同时间内针筒中所得的CO2体积大小关系是_______ (填实验序号)。 =
=_______ (假设混合液体积为50mL)。
(6)除通过测定一定时间内CO2的体积来比较反应速率外,本实验还可通过测定_______ 来比较化学反应速率。
(7)小组同学发现反应速率总是如上图二,其中t1~t2时间内速率变快的主要原因可能是①产物MnSO4是该反应的催化剂、②_______ 。
| 化学键 | H—H | Cl—Cl | O=O | C—Cl | C—H | O—H | H—Cl |
| E/(kJ·mol-1) | 436 | 247 | x | 330 | 413 | 463 | 431 |
(1)如图表示某反应的能量变化关系,则此反应
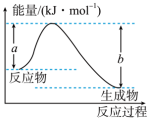
 O2(g)=H2O(g)放出241.8 kJ能量,则根据所给键能数据可得x=
O2(g)=H2O(g)放出241.8 kJ能量,则根据所给键能数据可得x=(3)历史上曾用“地康法”制氯气,这一方法是用CuCl2作催化剂,在450 ℃时利用空气中的氧气与氯化氢反应制氯气。反应的化学方程式为
Ⅱ.用酸性KMnO4和H2C2O4(草酸)反应研究影响反应速率的因素,离子方程式为2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O。一实验小组欲通过测定单位时间内生成CO2的速率,探究某种影响化学反应速率的因素,设计实验方案如下(KMnO4溶液已酸化):
| 实验序号 | A溶液 | B溶液 |
| ① | 20mL 0.1mol·L-1H2C2O4溶液 | 30mL 0.1 mol·L-1KMnO4溶液 |
| ② | 20mL 0.2mol·L-1H2C2O4溶液 | 30mL 0.1mol·L-1KMnO4溶液 |
 =
=(6)除通过测定一定时间内CO2的体积来比较反应速率外,本实验还可通过测定
(7)小组同学发现反应速率总是如上图二,其中t1~t2时间内速率变快的主要原因可能是①产物MnSO4是该反应的催化剂、②
您最近一年使用:0次
2024-04-25更新
|
200次组卷
|
2卷引用:名校期中好题汇编-化学反应与能量(非选择题)
名校
5 . 在生产和生活中,人们关注化学反应进行的快慢和程度,以提高生产效率和调控反应条件。
Ⅰ.合成氨的反应对人类解决粮食问题贡献巨大,反应为 。
。
(1)德国化学家F·Haber利用 和
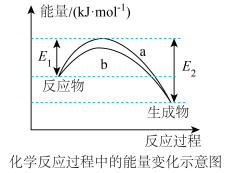
和 在催化剂表面合成氨气而获得诺贝尔奖,该反应的能量变化及微观历程的示意图如下,用
在催化剂表面合成氨气而获得诺贝尔奖,该反应的能量变化及微观历程的示意图如下,用 、
、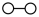 、
、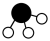 分别
分别 、
、 、
、 。
。_______ 。
A.氢气燃烧 B.氯化铵与 的反应
的反应
C.锌片与稀硫酸的反应 D.钠与冷水的反应
②下列说法正确的是_______ 。
A.使用催化剂,可以加快合成氨的反应速率
B.②→③过程,是吸热过程且只有H-H键断裂
C.③→④过程,N原子和H原子形成了含有极性键的
D.合成氨反应中,反应物断键吸收能量大于生成物成键释放的能量
(2)一定温度下,向恒容的密闭容器中充入一定量的 和
和 发生反应,测得各组分浓度随时间变化如图所示。
发生反应,测得各组分浓度随时间变化如图所示。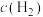 变化的曲线是
变化的曲线是_______ (填“A”“B”或“C”)。
②下列能说明该反应达到平衡状态的是_______ (填序号)。
a.容器中的压强不随时间变化
b.
c.容器中混合气体的密度不随时间变化
d.单位时间内生成3mol 的同时生成2mol
的同时生成2mol
e.容器内 的质量分数不变
的质量分数不变
(3)一定条件下,将2mol 和3mol
和3mol 通入2L的恒容密闭容器中,10min后达到化学平衡,测得
通入2L的恒容密闭容器中,10min后达到化学平衡,测得 的物质的量为2.4mol,则10min内
的物质的量为2.4mol,则10min内 的平均反应速率为
的平均反应速率为_______ , 的转化率是
的转化率是_______ ,混合气中 的物质的量分数是
的物质的量分数是_______ 。
Ⅱ.探究一定条件下反应物浓度对硫代硫酸钠( )与硫酸反应速率的影响。
)与硫酸反应速率的影响。
【查阅资料】
a. 易溶于水,能与硫酸发生反应:
易溶于水,能与硫酸发生反应: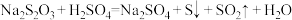
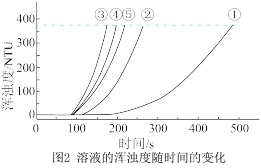
b.浊度计用于测量浑浊度的变化。产生的沉淀越多,浑浊度(单位为NTU)值越大。
【实验过程】
实验数据:
(4)选用浊度计进行测量,原因是 溶液与
溶液与 溶液反应生成了
溶液反应生成了_______ 。
(5)实验③中,x=_______ 。
(6)实验①、②、③的目的是_______ 。
(7)通过比较①、②、③与③、④、⑤两组实验,可推断:反应物浓度的改变对 与硫酸反应的化学反应速率的影响,
与硫酸反应的化学反应速率的影响, 溶液浓度的改变影响更大。该推断的证据是
溶液浓度的改变影响更大。该推断的证据是_______ 。
Ⅰ.合成氨的反应对人类解决粮食问题贡献巨大,反应为
 。
。(1)德国化学家F·Haber利用
 和
和 在催化剂表面合成氨气而获得诺贝尔奖,该反应的能量变化及微观历程的示意图如下,用
在催化剂表面合成氨气而获得诺贝尔奖,该反应的能量变化及微观历程的示意图如下,用 、
、 、
、 分别
分别 、
、 、
、 。
。
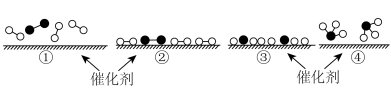
A.氢气燃烧 B.氯化铵与
 的反应
的反应C.锌片与稀硫酸的反应 D.钠与冷水的反应
②下列说法正确的是
A.使用催化剂,可以加快合成氨的反应速率
B.②→③过程,是吸热过程且只有H-H键断裂
C.③→④过程,N原子和H原子形成了含有极性键的

D.合成氨反应中,反应物断键吸收能量大于生成物成键释放的能量
(2)一定温度下,向恒容的密闭容器中充入一定量的
 和
和 发生反应,测得各组分浓度随时间变化如图所示。
发生反应,测得各组分浓度随时间变化如图所示。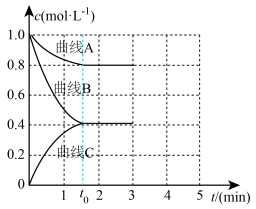
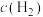 变化的曲线是
变化的曲线是②下列能说明该反应达到平衡状态的是
a.容器中的压强不随时间变化
b.

c.容器中混合气体的密度不随时间变化
d.单位时间内生成3mol
 的同时生成2mol
的同时生成2mol
e.容器内
 的质量分数不变
的质量分数不变(3)一定条件下,将2mol
 和3mol
和3mol 通入2L的恒容密闭容器中,10min后达到化学平衡,测得
通入2L的恒容密闭容器中,10min后达到化学平衡,测得 的物质的量为2.4mol,则10min内
的物质的量为2.4mol,则10min内 的平均反应速率为
的平均反应速率为 的转化率是
的转化率是 的物质的量分数是
的物质的量分数是Ⅱ.探究一定条件下反应物浓度对硫代硫酸钠(
 )与硫酸反应速率的影响。
)与硫酸反应速率的影响。【查阅资料】
a.
 易溶于水,能与硫酸发生反应:
易溶于水,能与硫酸发生反应: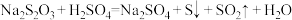
b.浊度计用于测量浑浊度的变化。产生的沉淀越多,浑浊度(单位为NTU)值越大。
【实验过程】
| 实验编号 |  溶液 溶液 |  溶液 溶液 | 蒸馏水 | ||
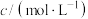 | V/mL | 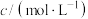 | V/mL | V/mL | |
| ① | 0.1 | 1.5 | 0.1 | 3.5 | 10 |
| ② | 0.1 | 2.5 | 0.1 | 3.5 | 9 |
| ③ | 0.1 | 3.5 | 0.1 | 3.5 | x |
| ④ | 0.1 | 3.5 | 0.1 | 2.5 | 9 |
| ⑤ | 0.1 | 3.5 | 0.1 | 1.5 | 10 |
(4)选用浊度计进行测量,原因是
 溶液与
溶液与 溶液反应生成了
溶液反应生成了(5)实验③中,x=
(6)实验①、②、③的目的是
(7)通过比较①、②、③与③、④、⑤两组实验,可推断:反应物浓度的改变对
 与硫酸反应的化学反应速率的影响,
与硫酸反应的化学反应速率的影响, 溶液浓度的改变影响更大。该推断的证据是
溶液浓度的改变影响更大。该推断的证据是
您最近一年使用:0次
2024-04-25更新
|
308次组卷
|
2卷引用:广东省广州市育才中学2023-2024学年高一下学期 期中考试化学试题
2024高三下·全国·专题练习
解题方法
6 . 某工厂采用如下工艺处理镍钴矿硫酸浸取液(含 和
和 )。实现镍、钴、镁元素的回收。
)。实现镍、钴、镁元素的回收。
回答下列问题:
(1)“氧化”中保持空气通入速率不变, (Ⅱ)氧化率与时间的关系如下。
(Ⅱ)氧化率与时间的关系如下。 体积分数为
体积分数为_______ 时, (Ⅱ)氧化速率最大;继续增大
(Ⅱ)氧化速率最大;继续增大 体积分数时,
体积分数时, (Ⅱ)氧化速率减小的原因是
(Ⅱ)氧化速率减小的原因是_______ 。
 和
和 )。实现镍、钴、镁元素的回收。
)。实现镍、钴、镁元素的回收。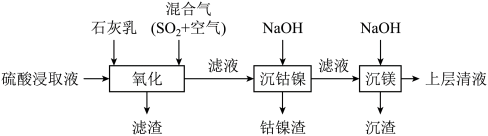
| 物质 |  | 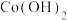 |  |  |
 |  |  |  |  |
(1)“氧化”中保持空气通入速率不变,
 (Ⅱ)氧化率与时间的关系如下。
(Ⅱ)氧化率与时间的关系如下。 体积分数为
体积分数为 (Ⅱ)氧化速率最大;继续增大
(Ⅱ)氧化速率最大;继续增大 体积分数时,
体积分数时, (Ⅱ)氧化速率减小的原因是
(Ⅱ)氧化速率减小的原因是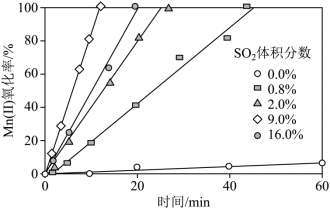
您最近一年使用:0次
名校
解题方法
7 . 为探究过氧化氢分解反应快慢的影响因素,某学习小组设计了下列实验:
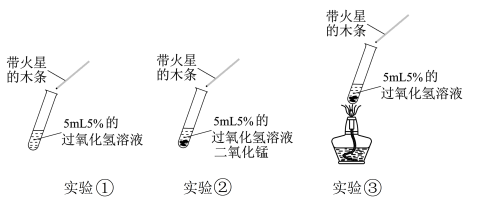
| A.综合实验①、②和③,可得出5%的过氧化氢溶液最适合用于分解制氧气 |
| B.对比实验①和③,可研究升温对过氧化氢分解反应快慢的影响 |
| C.综合实验②和③,可得出过氧化氢分解制氧气的最佳反应条件 |
| D.对比实验①和②,可研究催化剂对化学反应快慢的影响 |
您最近一年使用:0次
2024-04-06更新
|
544次组卷
|
4卷引用:广东省东莞市东华高级中学2023-2024学年高一下学期前段考试化学试题
解题方法
8 . 工业上以软锰矿(主要成分为MnO2,还含有少量Fe2O3等)和辉铜矿(主要成分为Cu2S,还含有少量Si、Ni等氧化物)为原料,制备碳酸锰和胆矾的工艺流程如图所示。
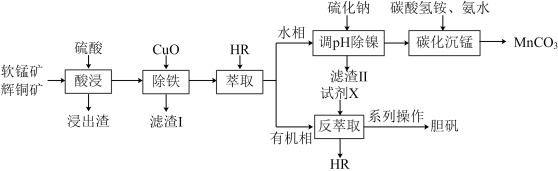
已知:HR萃取Cu2+的原理为Cu2+(aq)+2HR(org) CuR2(org)+2H+(aq)(org为有机相)。
CuR2(org)+2H+(aq)(org为有机相)。
回答下列问题:
(1)为了加快“酸浸”速率,可采取的措施是________ (答出任意两条即可);已知浸出渣中含有单质S,写出“酸浸”时MnO2与Cu2S反应的离子方程式:________ 。
(2)得到“滤渣I”的操作:________ 。
(3)写出“碳化沉锰”过程中发生反应的离子方程式:________ 。
(4)试剂X为________ (填化学式);“系列操作”包括________ 、过滤、洗涤和干燥。

已知:HR萃取Cu2+的原理为Cu2+(aq)+2HR(org)
 CuR2(org)+2H+(aq)(org为有机相)。
CuR2(org)+2H+(aq)(org为有机相)。回答下列问题:
(1)为了加快“酸浸”速率,可采取的措施是
(2)得到“滤渣I”的操作:
(3)写出“碳化沉锰”过程中发生反应的离子方程式:
(4)试剂X为
您最近一年使用:0次
2024高三下·全国·专题练习
解题方法
9 . 金属铼(Re)是重要的新兴金属,应用于国防、石油化工以及电子制造等领域,通过还原高铼酸铵(NH4ReO4)可制取金属铼。以钼精矿(主要成分为钼的硫化物和少量铼的硫化物)制取高铼酸铵的流程如下图所示。回答下列问题:
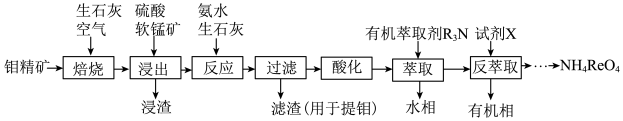
(1)“焙烧”过程加入生石灰的目的___________ 。
(2)“焙烧”常采用高压空气、逆流操作(空气从培烧炉下部通入,矿粉从中上部加入),这样操作的目的是___________ ,请再举出一项提高“焙烧”效率的合理措施:___________ 。
(3)“浸出”中,浸出率与温度的关系如下图所示,浸出率与硫酸浓度的关系如下图所示。工业生产应选择的适宜条件是___________ 。
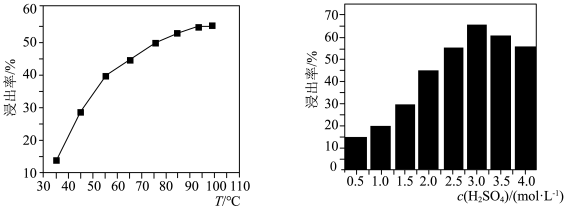

(1)“焙烧”过程加入生石灰的目的
(2)“焙烧”常采用高压空气、逆流操作(空气从培烧炉下部通入,矿粉从中上部加入),这样操作的目的是
(3)“浸出”中,浸出率与温度的关系如下图所示,浸出率与硫酸浓度的关系如下图所示。工业生产应选择的适宜条件是

您最近一年使用:0次
2024高三下·全国·专题练习
10 . 用硫酸浸取镍钴矿时,提高浸取速率的方法为___________ (答出一条即可)。
您最近一年使用:0次



