湖北省荆门市龙泉中学2019届高三上学期12月月考化学试题
湖北
高三
阶段练习
2019-01-18
315次
整体难度:
适中
考查范围:
常见无机物及其应用、有机化学基础、化学与STSE、认识化学科学、化学实验基础、化学反应原理、物质结构与性质
湖北省荆门市龙泉中学2019届高三上学期12月月考化学试题
湖北
高三
阶段练习
2019-01-18
315次
整体难度:
适中
考查范围:
常见无机物及其应用、有机化学基础、化学与STSE、认识化学科学、化学实验基础、化学反应原理、物质结构与性质
一、单选题 添加题型下试题
单选题
|
适中(0.65)
名校
1. 化学和生产生活紧密相关,下列说法错误的是
| A.SO2可以用来漂白纸浆、丝、毛、草帽辫等 |
| B.为使鲜花保鲜,可在箱内放入高锰酸钾溶液浸泡过的硅藻土 |
| C.医药工业上,常以葡萄糖为工业原料合成补钙、补锌药物 |
| D.钛被称为继铁、铝之后的第三金属,但目前主要用于尖端领域,因为钛在自然界中储量少 |
您最近一年使用:0次
单选题
|
适中(0.65)
名校
2. NA为阿伏伽德罗常数的值,下列有关叙述正确的是
| A.18g D2O含有的电子数为10 NA |
| B.S2和S8的混合物共6.4g,其中所含硫原子数一定为0.2NA |
| C.12g石墨烯(单层石墨)中含有六元环的个数为2NA |
| D.在标准状况下,22.4L SO3所含分子数目为NA |
您最近一年使用:0次
单选题
|
适中(0.65)
名校
3. 下列实验操作规范且所选玻璃仪器能达到目的的是
| 目的 | 所选玻璃仪器 | |
| A | 分离苯和四氯化碳的混合物 | 分液漏斗、烧杯、玻璃棒 |
| B | 用碱石灰除去氢气中混有的水蒸气并收集氢气 | 洗气瓶、导气管、集气瓶 |
| C | 用氢氧化钠和醋酸溶液测中和反应的中和热 | 烧杯、玻璃棒、温度计 |
| D | 配制480mL 0.5mol/L CuSO4溶液 | 烧杯、玻璃棒、量筒、500mL容量瓶、胶头滴管 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较难(0.4)
名校
4. 甲、乙、丙、丁、戊五种物质是中学化学常见的物质,它们的转化关系如图所示(某些条件和部分产物已略去)。下列说法不正确的是


| A.若甲为单质,乙为O2,且甲可以与NaOH溶液反应放出H2,则丙不一定是两性氧化物 |
| B.若甲为短周期中最活泼的金属,且戊为碱,则丙生成戊可能是氧化还原反应 |
| C.若甲为硫磺燃烧产物,丁为水,则戊的浓溶液不可用于干燥甲 |
| D.若甲为浓盐酸,乙为MnO2,则戊可能使品红褪色 |
您最近一年使用:0次
2019-01-14更新
|
421次组卷
|
2卷引用:湖北省荆门市龙泉中学2019届高三上学期12月月考化学试题
单选题
|
适中(0.65)
名校
5. 美籍华裔科学家钱永键、日本科学家下村修和美国科学家马丁·沙尔菲因在发现和研究绿色荧光蛋白(GFP)方面做出突出贡献而分享了2008年诺贝尔化学奖。经研究发现GFP中的生色基团结构如图所示,下列有关GFP的说法中正确的是

| A.该有机物属于芳香烃 |
| B.该有机物能发生加成反应、取代反应和氧化反应 |
| C.1mol该有机物分子中含有7mol碳碳双键 |
| D.该有机物所有原子都有可能共平面 |
您最近一年使用:0次
单选题
|
适中(0.65)
名校
6. 如图是一种新型高温可充电电池(电池活性物质为Na和S),则下列说法中正确的是

| A.放电时石墨b上发生的反应为: 2Na++xS+2e−=Na2Sx |
| B.充电时石墨a与外接电源正极相连 |
| C.可将装置中的固体电解质改成NaCl溶液 |
| D.放电时,电子由石墨b经固体电解质向石墨a迁移 |
【知识点】 原电池电极反应式书写解读 新型电池解读 原电池、电解池综合考查解读
您最近一年使用:0次
单选题
|
较难(0.4)
名校
7. 常温下,用AgNO3溶液分别滴定浓度均为0.01mol/L的KCl、K2C2O4溶液,所得的沉淀溶解平衡图象如图所示(不考虑C2O42-的水解)。下列叙述正确的是

| A.Ksp(Ag2C2O4)的数量级为10-7 |
| B.n点表示AgCl的不饱和溶液 |
C.Ag2C2O4+2Cl- 2AgCl+C2O42-的平衡常数为109.04 2AgCl+C2O42-的平衡常数为109.04 |
| D.向c(Cl-)=c(C2O42-)的混合液中滴入AgNO3溶液时,先生成 Ag2C2O4沉淀 |
【知识点】 难溶电解质的溶解平衡 溶度积 溶度积常数相关计算解读
您最近一年使用:0次
二、解答题 添加题型下试题
解答题-实验探究题
|
较难(0.4)
名校
8. 无水SnCl4用作媒染剂和有机氯化催化剂,一种用熔融的金属锡(熔点239.1℃)和氯气反应制备无水 SnCl4的装置如图所示:
已知:无水SnCl4是无色易流动的液体, 熔点-33℃,沸点114.1℃,遇潮湿的空气易水解产生白烟。回答下列问题:
(1)仪器Q的名称是____________ 。实验开始时,①和④两处酒精喷灯,应先点燃_________ 处。
(2)干燥管⑥的作用是________________________________________________ 。若撤除该干燥管,则收集的产品中混有的主要杂质是_____________ (填化学式) 。
(3)装置④采用油浴加热,曲颈甑中发生反应的化学方程式为___________________________ 。
(4)装置③中盛放的试剂名称为___________ 。若去掉装置②,曲颈甑中可能发生的主要副反应的化学方程式为______________________________________ (写一个)。
(5)若收集的SnCl4产品中溶有Cl2,则可采取下列_____________ (填字母)措施加以除去。
A.加NaOH溶液萃取、分液 B.加入足量Sn,再加热蒸馏 C.加入KI冷凝过滤
(6)发生装置①中仪器的配置可能导致空气污染,改进办法是_________________________ 。

已知:无水SnCl4是无色易流动的液体, 熔点-33℃,沸点114.1℃,遇潮湿的空气易水解产生白烟。回答下列问题:
(1)仪器Q的名称是
(2)干燥管⑥的作用是
(3)装置④采用油浴加热,曲颈甑中发生反应的化学方程式为
(4)装置③中盛放的试剂名称为
(5)若收集的SnCl4产品中溶有Cl2,则可采取下列
A.加NaOH溶液萃取、分液 B.加入足量Sn,再加热蒸馏 C.加入KI冷凝过滤
(6)发生装置①中仪器的配置可能导致空气污染,改进办法是
您最近一年使用:0次
解答题-工业流程题
|
较难(0.4)
名校
解题方法
9. 以铬铁矿(主要成分为FeO和Cr2O3,含有Al2O3、SiO2等杂质)为主要原料生产化工原料红矾钠(主要成分Na2Cr2O7·2H2O),其主要工艺流程如下:

查阅资料得知:
ⅰ.常温下,NaBiO3不溶于水,有强氧化性,在碱性条件下,能将Cr3+转化为CrO42-。
ⅱ.
回答下列问题:
(1)反应之前先将矿石粉碎的目的是______________________________________ 。
(2)步骤③加的试剂为_____________ ,此时溶液pH要调到5的目的________________ 。
(3)写出反应④的离子反应方程式____________________________________________ 。
(4)⑤中酸化是使CrO42-转化为Cr2O72-,写出该反应的离子方程式_________________ 。
(5)将溶液H经过蒸发浓缩,冷却结晶,过滤,洗涤,干燥即得红矾钠粗晶体,精制红矾钠粗晶体需要采用的操作是__________________ (填操作名称)。
(6)取一定质量的固体D溶解于200mL的硫酸中,向所得溶液中加入5mol/L的NaOH溶液,生成沉淀的物质的量n与加入NaOH溶液的体积V关系如图所示,则硫酸的浓度为___________ ,固体D中含Fe化合物的物质的量为____________ 。


查阅资料得知:
ⅰ.常温下,NaBiO3不溶于水,有强氧化性,在碱性条件下,能将Cr3+转化为CrO42-。
ⅱ.
| 金属离子 | Fe3+ | Al3+ | Cr3+ | Fe2+ | Bi3+ |
| 开始沉淀的pH | 2.7 | 3.4 | 5.0 | 7.5 | 0.7 |
| 沉淀完全的pH | 3.7 | 4.9 | 5.9 | 9.7 | 4.5 |
回答下列问题:
(1)反应之前先将矿石粉碎的目的是
(2)步骤③加的试剂为
(3)写出反应④的离子反应方程式
(4)⑤中酸化是使CrO42-转化为Cr2O72-,写出该反应的离子方程式
(5)将溶液H经过蒸发浓缩,冷却结晶,过滤,洗涤,干燥即得红矾钠粗晶体,精制红矾钠粗晶体需要采用的操作是
(6)取一定质量的固体D溶解于200mL的硫酸中,向所得溶液中加入5mol/L的NaOH溶液,生成沉淀的物质的量n与加入NaOH溶液的体积V关系如图所示,则硫酸的浓度为

您最近一年使用:0次
解答题-原理综合题
|
适中(0.65)
名校
解题方法
10. 目前,人们对环境保护、新能源的开发很重视。
Ⅰ.(1)汽车尾气中含有CO、NO2等有毒气体,对汽车加装尾气净化装置,可使有毒气体转化为无毒气体:
4CO(g)+2NO2(g) 4CO2(g)+N2(g)。恒温恒容条件下,能够说明该反应已达到平衡状态的是
4CO2(g)+N2(g)。恒温恒容条件下,能够说明该反应已达到平衡状态的是____ (填序号);
A.容器内混合气体颜色不再变化 B.容器内的压强保持不变
C.2v逆(NO2)=v正(N2) D.容器内混合气体平均密度保持不变
(2)以CO2与NH3为原料可合成化肥尿素[化学式为CO(NH2)2]。已知:①2NH3(g)+CO2(g)=NH2CO2NH4(s)ΔH=-l59.5 kJ·mol-1
②NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g) ΔH= +116.5 kJ·mol-1
③H2O(l)=H2O(g)ΔH=+44.0 kJ· mol-1,
写出CO2与NH3合成尿素和液态水的热化学反应方程式_____________________ 。
(3)在饱和的KHCO3电解液中,电解活化CO2制备乙醇的原理如图所示。
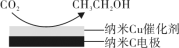
①阴极的电极反应式是___________________________ 。
②从电解后溶液中分离出乙醇的操作方法是____________ (选填字母)。
a.分液 b.过滤 c.蒸馏 d.升华
Ⅱ.工业上利用吸热反应C(s)+2H2O(g) CO2(g)+2H2(g),可制备氢气,氢能源是一种安全高效的新能源。一定条件下,将C(s)和H2O(g)分别加入甲、乙两个密闭容器发生反应,其相关数据如表所示:
CO2(g)+2H2(g),可制备氢气,氢能源是一种安全高效的新能源。一定条件下,将C(s)和H2O(g)分别加入甲、乙两个密闭容器发生反应,其相关数据如表所示:
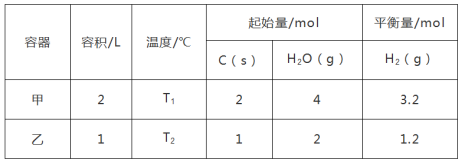
T1℃时,该反应的平衡常数K=_______ ;T1_______ T2(填“>”、“=”或“<”)。
Ⅲ.利用H2和CO2在一定条件下可以合成乙烯:6H2(g)+2CO2(g)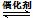 CH2=CH2(g)+4H2O(g),已知不同温度对CO2的平衡转化率及催化剂的催化效率影响如图所示,
CH2=CH2(g)+4H2O(g),已知不同温度对CO2的平衡转化率及催化剂的催化效率影响如图所示,
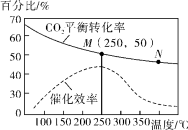
下列有关说法不正确的是________ (填序号)。
①不同条件下反应,N点的速率最大
②M点时平衡常数比N点时平衡常数大
③实际反应应尽可能在较低的温度下进行,以提高CO2的平衡转化率
④温度低于250℃时,随温度升高乙烯的产率减小
Ⅰ.(1)汽车尾气中含有CO、NO2等有毒气体,对汽车加装尾气净化装置,可使有毒气体转化为无毒气体:
4CO(g)+2NO2(g)
 4CO2(g)+N2(g)。恒温恒容条件下,能够说明该反应已达到平衡状态的是
4CO2(g)+N2(g)。恒温恒容条件下,能够说明该反应已达到平衡状态的是A.容器内混合气体颜色不再变化 B.容器内的压强保持不变
C.2v逆(NO2)=v正(N2) D.容器内混合气体平均密度保持不变
(2)以CO2与NH3为原料可合成化肥尿素[化学式为CO(NH2)2]。已知:①2NH3(g)+CO2(g)=NH2CO2NH4(s)ΔH=-l59.5 kJ·mol-1
②NH2CO2NH4(s)=CO(NH2)2(s)+H2O(g) ΔH= +116.5 kJ·mol-1
③H2O(l)=H2O(g)ΔH=+44.0 kJ· mol-1,
写出CO2与NH3合成尿素和液态水的热化学反应方程式
(3)在饱和的KHCO3电解液中,电解活化CO2制备乙醇的原理如图所示。

①阴极的电极反应式是
②从电解后溶液中分离出乙醇的操作方法是
a.分液 b.过滤 c.蒸馏 d.升华
Ⅱ.工业上利用吸热反应C(s)+2H2O(g)
 CO2(g)+2H2(g),可制备氢气,氢能源是一种安全高效的新能源。一定条件下,将C(s)和H2O(g)分别加入甲、乙两个密闭容器发生反应,其相关数据如表所示:
CO2(g)+2H2(g),可制备氢气,氢能源是一种安全高效的新能源。一定条件下,将C(s)和H2O(g)分别加入甲、乙两个密闭容器发生反应,其相关数据如表所示:
T1℃时,该反应的平衡常数K=
Ⅲ.利用H2和CO2在一定条件下可以合成乙烯:6H2(g)+2CO2(g)
 CH2=CH2(g)+4H2O(g),已知不同温度对CO2的平衡转化率及催化剂的催化效率影响如图所示,
CH2=CH2(g)+4H2O(g),已知不同温度对CO2的平衡转化率及催化剂的催化效率影响如图所示,
下列有关说法不正确的是
①不同条件下反应,N点的速率最大
②M点时平衡常数比N点时平衡常数大
③实际反应应尽可能在较低的温度下进行,以提高CO2的平衡转化率
④温度低于250℃时,随温度升高乙烯的产率减小
您最近一年使用:0次
解答题-无机推断题
|
适中(0.65)
名校
11. 下图是元素周期表的一部分,已知a、b、c、d、e、f、g都是周期表中的前四周期元素,它们在周期表中的位置如图所示。
试回答下列问题:
(l)f元素基态原子的价电子排布式为______________ 。
(2)a、b、c的第一电离能由大到小的顺序______________ (用元素符号表示)。
(3)与b元素单质分子互为等电子体的阴离子为______________ 。
(4)下图为a元素某种氧化物的晶胞,其分子中心原子采用_____ 杂化,每个分子周围有___ 个分子与之距离相等且最近。若晶胞棱长为x pm,则该晶体密度的表达式为________ g•cm-3。
(5)g元素的最简单氢化物分子的空间构型为______ ,其沸点比b元素最简单的氢化物_______ (填 “高” 或“低”),其原因是______________________________ 。
(6)向CuSO4溶液中滴加入b元素最简单氢化物的水溶液,先生成蓝色沉淀,后沉淀逐渐溶解,得到深蓝色透明溶液,加入乙醇析出深蓝色晶体的化学式为______________________ 。
(7)已知b的电负性大于氯,则bC13水解反应方程式为______________________________ 。
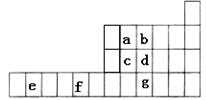
试回答下列问题:
(l)f元素基态原子的价电子排布式为
(2)a、b、c的第一电离能由大到小的顺序
(3)与b元素单质分子互为等电子体的阴离子为
(4)下图为a元素某种氧化物的晶胞,其分子中心原子采用

(5)g元素的最简单氢化物分子的空间构型为
(6)向CuSO4溶液中滴加入b元素最简单氢化物的水溶液,先生成蓝色沉淀,后沉淀逐渐溶解,得到深蓝色透明溶液,加入乙醇析出深蓝色晶体的化学式为
(7)已知b的电负性大于氯,则bC13水解反应方程式为
您最近一年使用:0次
解答题-有机推断题
|
较难(0.4)
名校
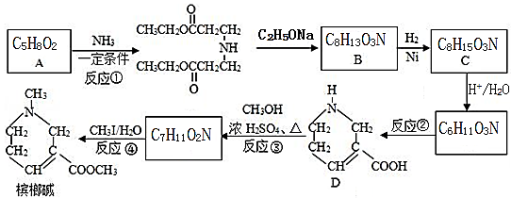
12. 槟榔碱在医疗上常用于治疗青光眼,其一种合成路线如图:
已知:Ⅰ.不饱和化合物与氨(NH3)或胺(R﹣NH2)反应能生成新的胺类化合物如:R1﹣CH=CH2+R2﹣NH2 R1﹣CH2﹣CH2﹣NH﹣R2;
R1﹣CH2﹣CH2﹣NH﹣R2;
Ⅱ.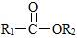 +
+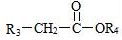
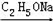
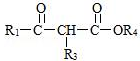 + R2OH。
+ R2OH。
(1)B的含氧官能团名称为____________ ,D分子中最多有_____ 个碳原子共平面。
(2)反应①④的反应类型分别为________ 、___________ ,反应②的反应条件为___________ 。
(3)反应③的化学方程式为_____________________________________ 。
(4)C的结构简式为____________________________ 。
(5)A的同分异构体中满足下列条件的有_______________ 种。
a.含有能与NaHCO3溶液反应放出CO2气体的官能团;
b.能使溴的CCl4溶液褪色。
(6)结合题中信息,以乙二醇为主要原料,其他无机试剂任选,写出合成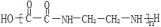 的最简单路线
的最简单路线____________________________ 。
已知:Ⅰ.不饱和化合物与氨(NH3)或胺(R﹣NH2)反应能生成新的胺类化合物如:R1﹣CH=CH2+R2﹣NH2
 R1﹣CH2﹣CH2﹣NH﹣R2;
R1﹣CH2﹣CH2﹣NH﹣R2;Ⅱ.
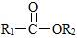 +
+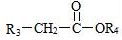
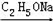
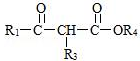 + R2OH。
+ R2OH。(1)B的含氧官能团名称为
(2)反应①④的反应类型分别为
(3)反应③的化学方程式为
(4)C的结构简式为
(5)A的同分异构体中满足下列条件的有
a.含有能与NaHCO3溶液反应放出CO2气体的官能团;
b.能使溴的CCl4溶液褪色。
(6)结合题中信息,以乙二醇为主要原料,其他无机试剂任选,写出合成
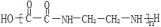 的最简单路线
的最简单路线
您最近一年使用:0次
试卷分析
整体难度:适中
考查范围:常见无机物及其应用、有机化学基础、化学与STSE、认识化学科学、化学实验基础、化学反应原理、物质结构与性质
试卷题型(共 12题)
题型
数量
单选题
7
解答题
5
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.65 | 二氧化硫的漂白性 乙烯的用途 化学科学对人类文明发展的意义 | |
| 2 | 0.65 | 阿伏加德罗常数的求算 结合氧化还原反应知识与NA相关推算 | |
| 3 | 0.65 | 仪器使用与实验安全 配制一定物质的量浓度的溶液实验的仪器 物质分离、提纯综合应用 蒸馏与分馏 | |
| 4 | 0.4 | 氯气与水的反应 二氧化硫的化学性质 过氧化钠 | |
| 5 | 0.65 | 有机物的分类-根据官能团分类 含碳碳双键物质的性质的推断 多官能团有机物的结构与性质 | |
| 6 | 0.65 | 原电池电极反应式书写 新型电池 原电池、电解池综合考查 | |
| 7 | 0.4 | 难溶电解质的溶解平衡 溶度积 溶度积常数相关计算 | |
| 二、解答题 | |||
| 8 | 0.4 | 氯气的实验室制法 氯气与金属单质的反应 物质制备的探究 综合实验设计与评价 | 实验探究题 |
| 9 | 0.4 | 沉淀的溶解与生成 物质分离、提纯综合应用 常见无机物的制备 物质制备的探究 | 工业流程题 |
| 10 | 0.65 | 盖斯定律及其有关计算 化学平衡的移动及其影响因素 化学平衡常数 电解池电极反应式及化学方程式的书写与判断 | 原理综合题 |
| 11 | 0.65 | 元素周期表提供的元素信息 电离能变化规律 元素性质与电负性的关系 晶胞的有关计算 | 无机推断题 |
| 12 | 0.4 | 同分异构体的数目的确定 根据题给物质选择合适合成路线 有机推断综合考查 胺的性质与应用 | 有机推断题 |



