8. 铅的单质、氧化物、盐在现代工业中有着重要用途。
I.(1)铅能形成多种氧化物,如碱性氧化物PbO、酸性氧化的PbO
2、还有组成类似Fe
3O
4的Pb
3O
4,请将Pb
3O
4改写成简单氧化物的形式:
_________。
II.以废旧铅酸电池中的含铅废料铅膏(Pb、PbO、PbO
2、PbSO
4等)为原料,制备超细PbO,实现铅的再生利用。其工作流程如下:
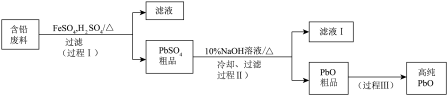
(2)步骤①的目的是“脱硫”,即将PbSO
4转化PbSO
3,反应的离子方程式为
_______________________。
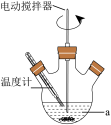
“脱硫过程”可在如图所示的装置中进行,实验条件为:转化温度为35℃,液固比为5:1,转化时间为2h.。
①仪器a的名称是
__________;转化温度为35℃,采用的合适加热方式是
________。
②步骤②中H
2O
2的作用是
__________________(用化学方程式表示)。
(3)草酸铅受热分解生成PbO时,还有CO和CO
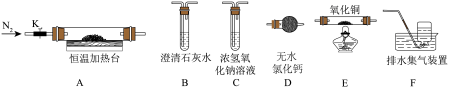
2生成,为检验这两种气体,用下图所示装置(可重复选用)进行实验。实验装置中,依次连接的合理顺序为A
_____________(填装置字母代号),证明产物中有CO气体的实验现象是
________________。
(4)测定草酸铅样品纯度:称取2.5g样品,酸溶后配制成250mL溶液,然后量取25.00mL该溶液,用0.05000mol•L
-1的EDTA(Na
2H
2Y)标准溶液滴定其中的Pb
2+(反应方程式为Pb
2++H
2Y
2-= PbY
2-+2H
+,杂质不反应),平行滴定三次,平均消耗EDTA标准溶液14.52mL
①若滴定管未用EDT A标准液润洗,测定结果将
_________(填“偏高”“偏低”或“不变”)。
②草酸铅的纯度为
__________(保留四位有效数字)。