10. NH
3、NO
2、SO
2处理不当易造成环境污染,如果对这些气体加以利用就可以变废为宝,既减少了对环境的污染,又解决了部分能源危机问题。
(1)硝酸厂常用催化还原方法处理尾气。CH
4在催化条件下可以NO
2将还原为N
2。已知:
CH
4 (g)+2O
2(g)=CO
2(g)+2H
2O(l) △H
1=-890.3kJ•mol
-1①
N
2 (g) +2O
2(g)=2 NO
2 (g) △H
2=+67.7kJ•mol
-1②
则反应CH
4 (g)+2NO
2(g)=CO
2(g)+ N
2 (g)+ 2H
2O(l) △H=
_____________ 。
(2)工业上利用氨气生产氢氰酸(HCN)的反应为:CH
4 (g)+ NH
3 (g)

HCN(g)+ 3H
2 (g) △H>0
①在一定温度条件下,向2L恒容密闭容器中加入2mol CH
4和2mol NH
3,平衡时NH
3体积分数为30%,所用时间为10min,则该时间段内用CH
4的浓度变化表示的反应速率为
__________________mol•L
-1•min
-1,该温度下平衡常数K=
_________。若保持温度不变,再向容器中加入CH
4和H
2各1mol,则此时v
正=
________ (填“>”“=”或“<”)v
逆。
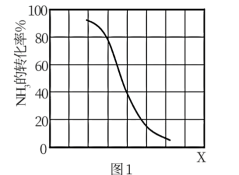
②其他条件一定,达到平衡时NH
3转化率随外界条件X 变化的关系如图1所示,X 代表
__________(填字母代号)
A.温度
B.
压强
C. 原料中CH
4与NH
3的体积比
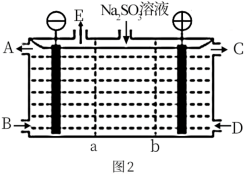
(3)某研究小组用NaOH 溶液吸收尾气中的二氧化碳,将得到的Na
2SO
3进行电解生产硫酸,其中阴、阳膜组合电解装置如图2所示,电极材料为石墨,A~E分别代表生产中的原料或产品,b表示
_____(填“阴”或“阳”)离子交换膜,阳极的电极反应式为
________。