17. 氢气作为清洁能源有着广泛的应用前景,采用天然气制备氢气的流程如下。请回答下列问题:
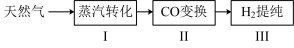
I.蒸汽转化:在催化剂的作用下,水蒸气将CH
4氧化,结合图表信息回答问题。

(1)该过程的热化学方程式是
_______________________。
(2)平衡混合物中CO的体积分数与压强的关系如图所示,判断T
1和T
2的大小关系:T
1__________T
2(选填“>”“<”或“=”),并说明理由:
______________。
(3)一定温度下,在1 L恒容的密闭容器中充入1 mol CH
4和1 mol水蒸气充分反应达到平衡后,测得反应前后容器中气体的物质的量之比是3:4,计算该条件下反应的平衡常数为
__________。
II.CO变换:500℃时,CO进一步与水反应生成CO
2和H
2。反应的方程式如下:CO(g)+H
2O(g)

CO
2(g)+H
2(g) △
H=-41 k/mol,在一定温度下的容积固定的密闭容器中进行上述反应。
(4)写出一种可以提高CO转化率的措施:
__________________,下列说法可以证明该反应已达到平衡状况的是
__________。
A.断裂2 mol H-O键的同时断裂1 mol H-H键
B.容器内气体压强不再改变
C.H
2的浓度不再改变
D.CO
2和H
2的浓度之比为1:1
III.模拟H
2提纯工艺:将CO
2和H
2分离得到H
2的过程如下。
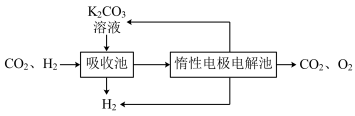
依据图示信息回答:
(5)吸收池中发生反应的离子方程式是
_____________________。
(6)写出电解池中阳极发生的电极反应式:
_____________________。