H2S是石油化工行业广泛存在的污染性气体,但同时也是重要的氢源和硫源,工业上可以采取多种方式处理。
Ⅰ.干法脱硫
(1)已知H2S的燃烧热为akJ∙mol-1,S的燃烧热为bkJ∙mol-1,则常温下空气直接氧化脱除H2S的反应:2H2S(g)+O2(g)=2S(s)+2H2O(l) △H=______ kJ∙mol-1。
(2)常用脱硫剂的脱硫效果及反应条件如下表,最佳脱硫剂为_________ 。
Ⅱ.热分解法脱硫
在密闭容器中,充入一定量的H2S气体,发生热分解反应H2S(g)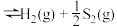 控制不同的温度和压强进行实验,结果如图(a)。
控制不同的温度和压强进行实验,结果如图(a)。
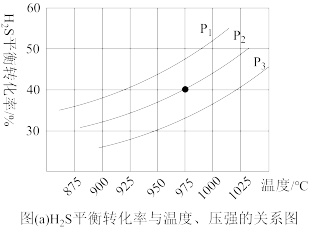
(3)图(a)中压强关系p1、p2、p3由大到小的顺序为______ ,该反应为____ (填“吸热”或“放热”)反应,若要进一步提高H2S的平衡转化率,除了改变温度和压强外,还可以采取的措施有_______ 。
(4)若压强为p、温度为975℃时, 的平衡常数K=0.04,则起始浓度c=
的平衡常数K=0.04,则起始浓度c=______ mol∙Lˉ1,若向容器中再加入1molH2S气体,相同温度下再次达到平衡时,K_____ 0.04(填“>”1 “<”或“=”)。
Ⅲ.间接电解法脱硫
间接电解法是通过FeCl3溶液吸收并氧化H2S气体,将反应后溶液通过电解再生,实现循环使用,该法处理过程如下图(b)。
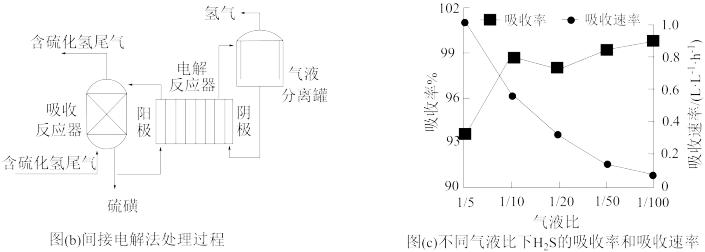
(5)电解反应器总反应的离子方程式为________ 。
(6)气液比为气体与液体的流速比,吸收反应器内液体流速固定。测定吸收器中相同时间内不同气液比下H2S的吸收率和吸收速率,结果如图(c)所示,随着气液比减小,H2S的吸收速率逐渐降低,而吸收率呈上升趋势的原因为____________ 。
Ⅰ.干法脱硫
(1)已知H2S的燃烧热为akJ∙mol-1,S的燃烧热为bkJ∙mol-1,则常温下空气直接氧化脱除H2S的反应:2H2S(g)+O2(g)=2S(s)+2H2O(l) △H=
(2)常用脱硫剂的脱硫效果及反应条件如下表,最佳脱硫剂为
| 脱硫剂 | 出口硫(mg·m-3) | 脱硫温度(℃) | 操作压力(MPa) | 再生条件 |
| 一氧化碳 | <1.33 | 300~400 | 0~3.0 | 蒸气再生 |
| 活性炭 | <1.33 | 常温 | 0~3.0 | 蒸气再生 |
| 氧化锌 | <1.33 | 350~400 | 0~5.0 | 不再生 |
| 锰矿 | <3.99 | 400 | 0~2.0 | 不再生 |
Ⅱ.热分解法脱硫
在密闭容器中,充入一定量的H2S气体,发生热分解反应H2S(g)
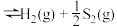 控制不同的温度和压强进行实验,结果如图(a)。
控制不同的温度和压强进行实验,结果如图(a)。
(3)图(a)中压强关系p1、p2、p3由大到小的顺序为
(4)若压强为p、温度为975℃时,
 的平衡常数K=0.04,则起始浓度c=
的平衡常数K=0.04,则起始浓度c=Ⅲ.间接电解法脱硫
间接电解法是通过FeCl3溶液吸收并氧化H2S气体,将反应后溶液通过电解再生,实现循环使用,该法处理过程如下图(b)。

(5)电解反应器总反应的离子方程式为
(6)气液比为气体与液体的流速比,吸收反应器内液体流速固定。测定吸收器中相同时间内不同气液比下H2S的吸收率和吸收速率,结果如图(c)所示,随着气液比减小,H2S的吸收速率逐渐降低,而吸收率呈上升趋势的原因为
更新时间:2020-04-12 21:44:47
|
相似题推荐
解答题-原理综合题
|
较难
(0.4)
名校
【推荐1】“十三五”期间中国应对气候变化工作取得显著成效,并向国际社会承诺2030年“碳达峰”,2060年实现“碳中和”。CO2的的回收及综合利用越来越受到国际社会的重视,将CO2转化为高附加值化学品已成为有吸引力的解决方案。
I.CO2合成二甲醚(DME):
(1)合成二甲醚反应:2CO2(g)+6H2(g)⇌CH3OCH3(g)+3H2O(g)。
已知:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ΔH1=-49kJ/mol
2CH3OH(g)⇌CH3OCH3(g)+H2O(g) ΔH2=-25kJ/mol
则合成二甲醚的反应的ΔH=_______ kJ/mol。
(2)将1 mol CO2、3mol H2通入容积为1L的恒容密闭容器中合成二甲醚,200℃时容器内CO2的物质的量随时间的变化如表所示:
①0~40min内,消耗H2的平均反应速率为_______ mol·L-1·min-1
②能说明反应已达平衡状态的是_______ (填标号)
a.c(CO2):c(H2O)=1:6 b.混合气体的密度不变 c.2v正(H2)=v逆(H2O) d.密闭容器内压强不变
(3)在不同温度和不同氢碳比时,合成二甲醚反应CO2的平衡转化率如图1所示,则图中氢碳比由大到小的关系是_______ (用a、b、c、d表示)。
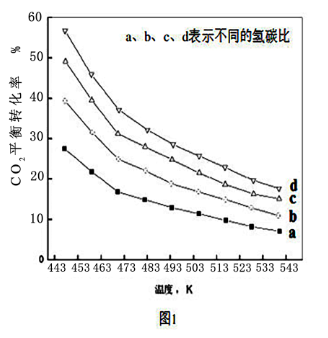
(4)在503K时,当以氢碳比为0.9时合成二甲醚(如图2),则化学平衡常数Kp=_______ MPa-4(用气体的平衡分压代替物质的量浓度计算压强平衡常数Kp,气体分压=气体总压×各气体的体积分数,列出表达式)。
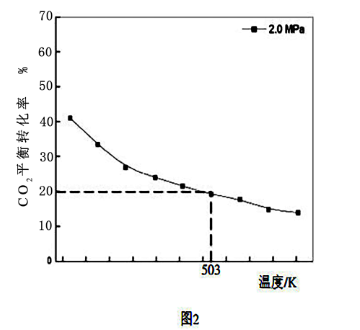
II.CO2合成甲醇(MT):
(5)合成甲醇反应:I.CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ΔH=-49kJ/mol
逆水煤气反应:II.CO2(g)+H2(g)⇌CO(g)+H2O(g) ΔH=+41.17kJ/mol
CO合成甲醇反应:Ⅲ.CO(g)+2H2(g)⇌CH3OH(g) ΔH=-90.18kJ/mol
在不同条件下CO2平衡转化率和甲醇的平衡产率如图所示:
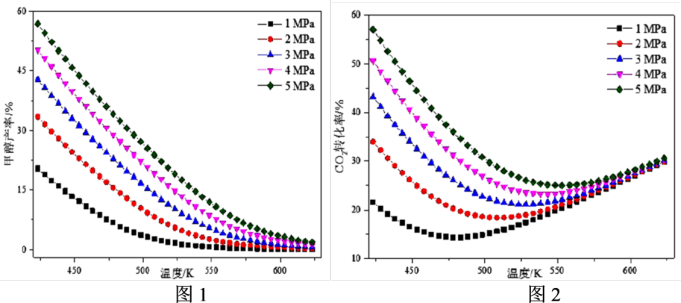
①图1中甲醇的平衡产率随温度升高而降低的原因是_______ 。
②由图2可知,不同压强下CO2的平衡转化率在550℃后趋于相等,原因是_______ 。
I.CO2合成二甲醚(DME):
(1)合成二甲醚反应:2CO2(g)+6H2(g)⇌CH3OCH3(g)+3H2O(g)。
已知:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ΔH1=-49kJ/mol
2CH3OH(g)⇌CH3OCH3(g)+H2O(g) ΔH2=-25kJ/mol
则合成二甲醚的反应的ΔH=
(2)将1 mol CO2、3mol H2通入容积为1L的恒容密闭容器中合成二甲醚,200℃时容器内CO2的物质的量随时间的变化如表所示:
| 时间/min-1 | 10 | 20 | 30 | 40 | 50 | 60 |
| n(CO2)mol | 0.31 | 0.53 | 0.40 | 0.30 | 0.20 | 0.20 |
①0~40min内,消耗H2的平均反应速率为
②能说明反应已达平衡状态的是
a.c(CO2):c(H2O)=1:6 b.混合气体的密度不变 c.2v正(H2)=v逆(H2O) d.密闭容器内压强不变
(3)在不同温度和不同氢碳比时,合成二甲醚反应CO2的平衡转化率如图1所示,则图中氢碳比由大到小的关系是

(4)在503K时,当以氢碳比为0.9时合成二甲醚(如图2),则化学平衡常数Kp=

II.CO2合成甲醇(MT):
(5)合成甲醇反应:I.CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ΔH=-49kJ/mol
逆水煤气反应:II.CO2(g)+H2(g)⇌CO(g)+H2O(g) ΔH=+41.17kJ/mol
CO合成甲醇反应:Ⅲ.CO(g)+2H2(g)⇌CH3OH(g) ΔH=-90.18kJ/mol
在不同条件下CO2平衡转化率和甲醇的平衡产率如图所示:

①图1中甲醇的平衡产率随温度升高而降低的原因是
②由图2可知,不同压强下CO2的平衡转化率在550℃后趋于相等,原因是
您最近一年使用:0次
【推荐2】甲醇、乙醇来源丰富、价格低廉、运输贮存方便,都是重要的化工原料,有着重要的用途和应用前景,可以用多种方法合成。
I.用CO2生产甲醇、乙醇
(1)已知:H2的燃烧热为-285.8 kJ/mol,CH3OH(l)的燃烧热为-725.8kJ/mol,CH3OH(g)=CH3OH(l) △H= -37.3 kJ/mol,则CO2(g)+3H2(g)=CH3OH(g)+ H2O(1) △H=____ kJ/mol。
(2)将CO2和H2按物质的量之比1:3充入体积为2.0L的恒容密闭容器中反应[生成 H2O(g)],如图1表示压强为0.1 MPa和5.0 MPa下CO2转化率随温度的变化关系。
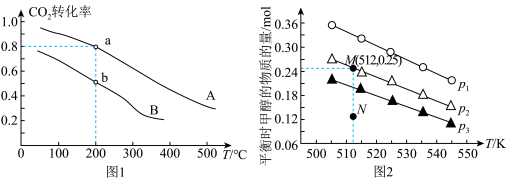
①a、b两点化学反应速率分别用Va、Vb,表示,则Va___ Vb(填“大于”、“小于”或“等于”)。
②列出a点对应的平衡常数表达式K=____________________ 。
(3)在1.0 L恒容密闭容器中投入1 mol CO2和2.75 mol H2发生反应:CO2(g)+3H2(g) CH3OH (g)+H2O(g),实验测得不同温度及压强下,平衡时甲醇的物质的量变化如图2所示,下列说法正确的是
CH3OH (g)+H2O(g),实验测得不同温度及压强下,平衡时甲醇的物质的量变化如图2所示,下列说法正确的是_____ 。
A.该反应的正反应为放热反应
B.压强大小关系为p1<p2<p3
C.M点对应的平衡常数K的值约为1.04×10-2
D.在p2及512 K时,图中N点υ(正)<υ(逆)
(4)CO2催化加氢合成乙醇的反应为:2CO2(g)+6H2(g) C2H5OH(g) +3H2O(g) △H;m代表起始时的投料比,即m=
C2H5OH(g) +3H2O(g) △H;m代表起始时的投料比,即m=

①图3中投料比相同,温度T3>T2>T1,则该反应的焓变△H____ 0(填“>”、“<”)。
②m=3时,该反应达到平衡状态后p(总)=20a MPa,恒压条件下各物质的物质的量分数与温度的关系如图4所示,则曲线b代表的物质为_________ (填化学式),T4温度时,反应达到平衡时物质d的分压p(d)=___________ 。
Ⅱ.甲醇的应用
(5)以甲醇为主要原料,电化学合成碳酸二甲酯的工作原理如图5所示。
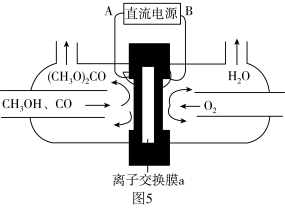
离子交换膜a为_____ (填“阳膜”、“阴膜”),阳极的电极反应式为______________ 。
I.用CO2生产甲醇、乙醇
(1)已知:H2的燃烧热为-285.8 kJ/mol,CH3OH(l)的燃烧热为-725.8kJ/mol,CH3OH(g)=CH3OH(l) △H= -37.3 kJ/mol,则CO2(g)+3H2(g)=CH3OH(g)+ H2O(1) △H=
(2)将CO2和H2按物质的量之比1:3充入体积为2.0L的恒容密闭容器中反应[生成 H2O(g)],如图1表示压强为0.1 MPa和5.0 MPa下CO2转化率随温度的变化关系。

①a、b两点化学反应速率分别用Va、Vb,表示,则Va
②列出a点对应的平衡常数表达式K=
(3)在1.0 L恒容密闭容器中投入1 mol CO2和2.75 mol H2发生反应:CO2(g)+3H2(g)
 CH3OH (g)+H2O(g),实验测得不同温度及压强下,平衡时甲醇的物质的量变化如图2所示,下列说法正确的是
CH3OH (g)+H2O(g),实验测得不同温度及压强下,平衡时甲醇的物质的量变化如图2所示,下列说法正确的是A.该反应的正反应为放热反应
B.压强大小关系为p1<p2<p3
C.M点对应的平衡常数K的值约为1.04×10-2
D.在p2及512 K时,图中N点υ(正)<υ(逆)
(4)CO2催化加氢合成乙醇的反应为:2CO2(g)+6H2(g)
 C2H5OH(g) +3H2O(g) △H;m代表起始时的投料比,即m=
C2H5OH(g) +3H2O(g) △H;m代表起始时的投料比,即m=

①图3中投料比相同,温度T3>T2>T1,则该反应的焓变△H
②m=3时,该反应达到平衡状态后p(总)=20a MPa,恒压条件下各物质的物质的量分数与温度的关系如图4所示,则曲线b代表的物质为
Ⅱ.甲醇的应用
(5)以甲醇为主要原料,电化学合成碳酸二甲酯的工作原理如图5所示。

离子交换膜a为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐3】水煤气变换[CO(g)+H2O(g)
 CO2(g)+H2(g)]是重要的化工过程,主要用于合成氨、制氢以及合成气加工等工业领域中。回答下列问题:
CO2(g)+H2(g)]是重要的化工过程,主要用于合成氨、制氢以及合成气加工等工业领域中。回答下列问题:
(1)我国学者结合实验与计算机模拟结果,研究了在金催化剂表面上水煤气变换的反应历程,如图所示,其中吸附在金催化剂表面上的物种用 标注。
标注。
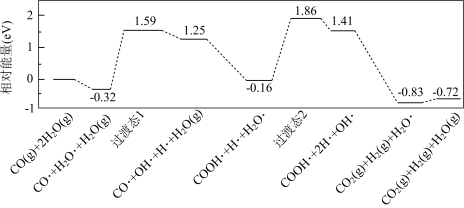
该历程中决速步骤的化学方程式为__ (方程式两边若有相同物料不用约简)。水煤气变换反应的热化学方程式为__ 。
(2)t1℃时,密闭容器中,通入一定量的CO和H2O,发生水煤气变换反应,容器中各物质浓度(单位:mol·L-1)变化如下表所示:
①一定处于平衡状态的时间段为__ 。
②5~6min时间段内,平衡移动方向为__ (填“向左移动”或“向右移动”),根据表中数据判断,平衡移动的原因是__ (填字母编号)。
a.增加了H2O(g)的量 b.增加氢气浓度 c.使用催化剂 d.降低温度
③t2℃时(t2>t1),在相同条件下发生上述反应,达平衡时,CO浓度__ c1(填“>”“<”或“=”)。
(3)已知反应Fe(s)+CO2(g) FeO(s)+CO(g)的平衡常数随温度变化情况如图所示:
FeO(s)+CO(g)的平衡常数随温度变化情况如图所示:

①该反应是__ (填“吸热”或“放热”)反应。
②若T1时水煤气变换反应的平衡常数等于0.5,则T1时FeO(s)+H2(g) Fe(s)+H2O(g)的平衡常数为
Fe(s)+H2O(g)的平衡常数为__ 。
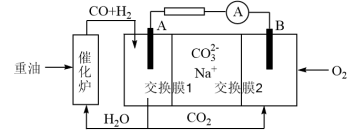
(4)水煤气可做燃料电池的燃料。一种熔融碳酸盐燃料电池的工作原理如图所示。电极A上H2参与的电极反应为__ 。假设催化炉产生的CO与H2物质的量之比为1︰2。电极A处产生的CO2有部分参与循环利用,其利用率为__ 。

 CO2(g)+H2(g)]是重要的化工过程,主要用于合成氨、制氢以及合成气加工等工业领域中。回答下列问题:
CO2(g)+H2(g)]是重要的化工过程,主要用于合成氨、制氢以及合成气加工等工业领域中。回答下列问题:(1)我国学者结合实验与计算机模拟结果,研究了在金催化剂表面上水煤气变换的反应历程,如图所示,其中吸附在金催化剂表面上的物种用
 标注。
标注。
该历程中决速步骤的化学方程式为
(2)t1℃时,密闭容器中,通入一定量的CO和H2O,发生水煤气变换反应,容器中各物质浓度(单位:mol·L-1)变化如下表所示:
| 时间(min) | CO | H2O | CO2 | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | c1 | c2 | c3 | c3 |
| 4 | c1 | c2 | c3 | c3 |
| 5 | 0.116 | 0.216 | 0.084 | |
| 6 | 0.096 | 0.266 | 0.104 |
②5~6min时间段内,平衡移动方向为
a.增加了H2O(g)的量 b.增加氢气浓度 c.使用催化剂 d.降低温度
③t2℃时(t2>t1),在相同条件下发生上述反应,达平衡时,CO浓度
(3)已知反应Fe(s)+CO2(g)
 FeO(s)+CO(g)的平衡常数随温度变化情况如图所示:
FeO(s)+CO(g)的平衡常数随温度变化情况如图所示:
①该反应是
②若T1时水煤气变换反应的平衡常数等于0.5,则T1时FeO(s)+H2(g)
 Fe(s)+H2O(g)的平衡常数为
Fe(s)+H2O(g)的平衡常数为(4)水煤气可做燃料电池的燃料。一种熔融碳酸盐燃料电池的工作原理如图所示。电极A上H2参与的电极反应为

您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐1】利用 合成甲醇、二甲醚技术是有效利用
合成甲醇、二甲醚技术是有效利用 资源,实现“碳中和”目标的重要途径。
资源,实现“碳中和”目标的重要途径。
(1)开发 直接催化加氢合成二甲醚技术是很好的一个研究方向。
直接催化加氢合成二甲醚技术是很好的一个研究方向。
主反应: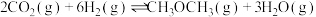

副反应:

①已知25℃和101kPa下,H2(g)、CO(g)的燃烧热 分别为-285.8kJ/mol、-283.0kJ/mol,
分别为-285.8kJ/mol、-283.0kJ/mol,
 ,则
,则
_______ kJ/mol。
②其他条件相同时,反应温度对 平衡转化率影响如图所示。温度低于280℃时,
平衡转化率影响如图所示。温度低于280℃时, 平衡转化率随温度的升高而减小的原因可能是
平衡转化率随温度的升高而减小的原因可能是_______ 。 ,反应平衡时测得
,反应平衡时测得 的转化率为20%,二甲醚的选择性为80%(已知二甲醚的选择性
的转化率为20%,二甲醚的选择性为80%(已知二甲醚的选择性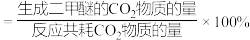 ),则副反应
),则副反应 的
的
_______ (保留两位有效数字,用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(2)利用 合成甲醇也是有效利用
合成甲醇也是有效利用 资源的重要途径。将原料气
资源的重要途径。将原料气 充入某一恒容密闭容器中,只发生
充入某一恒容密闭容器中,只发生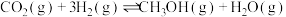
 ,在不同催化剂作用下,反应
,在不同催化剂作用下,反应 时
时 的转化率随温度的变化如图所示。
的转化率随温度的变化如图所示。_______ 。
A.使用催化剂Ⅰ时,d点已达到平衡
B. 的平衡常数大于
的平衡常数大于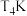 的平衡常数
的平衡常数
C.若a点时, ,则此条件下反应已达到最大限度
,则此条件下反应已达到最大限度
D.c点转化率比a点低的原因一定是催化剂活性降低
②若图中a点时反应已达平衡,现原料气按 充入同一恒容密闭容器中,在催化剂Ⅰ的作用下发生反应。请在图中用实线画出
充入同一恒容密闭容器中,在催化剂Ⅰ的作用下发生反应。请在图中用实线画出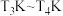 之间
之间 的平衡转化率变化曲线
的平衡转化率变化曲线______ 。
(3)水煤气变换反应的机理被广泛研究,其中有一种为羧基机理,某催化剂催化 (*表示吸附态、
(*表示吸附态、 表示活化能)步骤如下:
表示活化能)步骤如下:
Ⅰ.

Ⅱ._______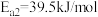
Ⅲ.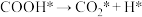

Ⅳ._______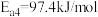
①请补充其中的一个反应式:Ⅱ_______ 。
②反应 的决速步骤是
的决速步骤是_______ (填序号)。
 合成甲醇、二甲醚技术是有效利用
合成甲醇、二甲醚技术是有效利用 资源,实现“碳中和”目标的重要途径。
资源,实现“碳中和”目标的重要途径。(1)开发
 直接催化加氢合成二甲醚技术是很好的一个研究方向。
直接催化加氢合成二甲醚技术是很好的一个研究方向。主反应:
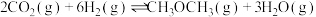

副反应:


①已知25℃和101kPa下,H2(g)、CO(g)的燃烧热
 分别为-285.8kJ/mol、-283.0kJ/mol,
分别为-285.8kJ/mol、-283.0kJ/mol,
 ,则
,则
②其他条件相同时,反应温度对
 平衡转化率影响如图所示。温度低于280℃时,
平衡转化率影响如图所示。温度低于280℃时, 平衡转化率随温度的升高而减小的原因可能是
平衡转化率随温度的升高而减小的原因可能是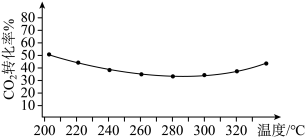
 ,反应平衡时测得
,反应平衡时测得 的转化率为20%,二甲醚的选择性为80%(已知二甲醚的选择性
的转化率为20%,二甲醚的选择性为80%(已知二甲醚的选择性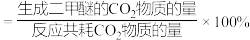 ),则副反应
),则副反应 的
的
(2)利用
 合成甲醇也是有效利用
合成甲醇也是有效利用 资源的重要途径。将原料气
资源的重要途径。将原料气 充入某一恒容密闭容器中,只发生
充入某一恒容密闭容器中,只发生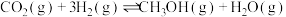
 ,在不同催化剂作用下,反应
,在不同催化剂作用下,反应 时
时 的转化率随温度的变化如图所示。
的转化率随温度的变化如图所示。
A.使用催化剂Ⅰ时,d点已达到平衡
B.
 的平衡常数大于
的平衡常数大于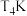 的平衡常数
的平衡常数C.若a点时,
 ,则此条件下反应已达到最大限度
,则此条件下反应已达到最大限度D.c点转化率比a点低的原因一定是催化剂活性降低
②若图中a点时反应已达平衡,现原料气按
 充入同一恒容密闭容器中,在催化剂Ⅰ的作用下发生反应。请在图中用实线画出
充入同一恒容密闭容器中,在催化剂Ⅰ的作用下发生反应。请在图中用实线画出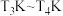 之间
之间 的平衡转化率变化曲线
的平衡转化率变化曲线(3)水煤气变换反应的机理被广泛研究,其中有一种为羧基机理,某催化剂催化
 (*表示吸附态、
(*表示吸附态、 表示活化能)步骤如下:
表示活化能)步骤如下:Ⅰ.


Ⅱ._______
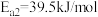
Ⅲ.
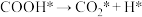

Ⅳ._______
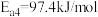
①请补充其中的一个反应式:Ⅱ
②反应
 的决速步骤是
的决速步骤是
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐2】以CH3OH(g)和CO2(g)为原料在一定条件下可制备HCOOCH3(g),发生的主要反应如下:
I.CH3OH(g)+CO2(g)⇌HCOOH(g)+HCHO(g) ΔH1=+757kJ·mol-1
Ⅱ.HCOOH(g)+CH3OH(g)⇌HCOOCH3(g)+H2O(g) ΔH2=+316kJ·mol-1
Ⅲ.2HCHO(g)⇌HCOOCH3(g) ΔH3=-162kJ·mol-1
回答下列问题:
(1)反应4CH3OH(g)+2CO2(g)⇌3HCOOCH3(g)+2H2O(g)的ΔH=___________ (用含ΔH1、ΔH2、ΔH3符号的表达式表示)
(2)已知:压强平衡常数(Kp)与温度(T)之间存在定量关系: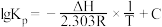 (其中R、C为常数,ΔH为反应的焓变)。反应I、Ⅱ、Ⅲ的lgKp与
(其中R、C为常数,ΔH为反应的焓变)。反应I、Ⅱ、Ⅲ的lgKp与 之间均为线性关系,如图1所示。其中反应Ⅱ对应的曲线为
之间均为线性关系,如图1所示。其中反应Ⅱ对应的曲线为___________ (选填“a”、“b”或“c”)。

(3)T℃时,向体积为VL的恒容密闭容器中充入2molCH3OH(g)和1molCO2(g),发生反应I、Ⅱ、Ⅲ达到平衡时测得容器中n(HCHO)、n(HCOOH)和n(HCOOCH3)分别为0.1mol、0.1mol和1.2mol。
①CH3OH(g)的平衡转化率为___________ 。
②T℃时,反应Ⅱ的平衡常数K=___________ 。
③当温度高于T℃时,HCOOCH3(g)的产率随温度的升高而下降的原因为___________ 。
(4)利用金属Ti的氧化物作催化剂也可实现由CH3OH(g)和CO2(g)合成HCOOCH3(g),其反应机理如图2所示。

①该反应的总反应为:___________ 。
②T℃时,将 的混合气体以aL·h-1的流速通过装有催化剂的反应器,试计算当HCOOCH3(g)的产率为90%时,其生成速率v(HCOOCH3)=
的混合气体以aL·h-1的流速通过装有催化剂的反应器,试计算当HCOOCH3(g)的产率为90%时,其生成速率v(HCOOCH3)=___________ L·h-1。
③若向反应体系中通入适量H2,可大大提高总反应速率,其原因可能为___________ 。
I.CH3OH(g)+CO2(g)⇌HCOOH(g)+HCHO(g) ΔH1=+757kJ·mol-1
Ⅱ.HCOOH(g)+CH3OH(g)⇌HCOOCH3(g)+H2O(g) ΔH2=+316kJ·mol-1
Ⅲ.2HCHO(g)⇌HCOOCH3(g) ΔH3=-162kJ·mol-1
回答下列问题:
(1)反应4CH3OH(g)+2CO2(g)⇌3HCOOCH3(g)+2H2O(g)的ΔH=
(2)已知:压强平衡常数(Kp)与温度(T)之间存在定量关系:
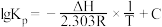 (其中R、C为常数,ΔH为反应的焓变)。反应I、Ⅱ、Ⅲ的lgKp与
(其中R、C为常数,ΔH为反应的焓变)。反应I、Ⅱ、Ⅲ的lgKp与 之间均为线性关系,如图1所示。其中反应Ⅱ对应的曲线为
之间均为线性关系,如图1所示。其中反应Ⅱ对应的曲线为
(3)T℃时,向体积为VL的恒容密闭容器中充入2molCH3OH(g)和1molCO2(g),发生反应I、Ⅱ、Ⅲ达到平衡时测得容器中n(HCHO)、n(HCOOH)和n(HCOOCH3)分别为0.1mol、0.1mol和1.2mol。
①CH3OH(g)的平衡转化率为
②T℃时,反应Ⅱ的平衡常数K=
③当温度高于T℃时,HCOOCH3(g)的产率随温度的升高而下降的原因为
(4)利用金属Ti的氧化物作催化剂也可实现由CH3OH(g)和CO2(g)合成HCOOCH3(g),其反应机理如图2所示。

①该反应的总反应为:
②T℃时,将
 的混合气体以aL·h-1的流速通过装有催化剂的反应器,试计算当HCOOCH3(g)的产率为90%时,其生成速率v(HCOOCH3)=
的混合气体以aL·h-1的流速通过装有催化剂的反应器,试计算当HCOOCH3(g)的产率为90%时,其生成速率v(HCOOCH3)=③若向反应体系中通入适量H2,可大大提高总反应速率,其原因可能为
您最近一年使用:0次
【推荐3】Ⅰ.氨是工业生产硝酸的重要原料,请根据以下工业制硝酸的原理示意图回答含氮化合物相关的问题:

(1)工业用甲烷制取氢气作为合成氨的原料,已知以下的热化学反应方程式:
①2CO(g)+O2(g)=2CO2(g)∆H=-566kJ/mol
②2H2(g)+O2(g)=2H2O(g)∆H=-484kJ/mol
③CH4(g)+2O2(g)=CO2(g)+2H2O(g)∆H=-890kJ/mol
则:CH4(g)+CO2(g)=2CO(g)+2H2(g)∆H=__ kJ/mol。
(2)一定温度下,将N2与H2以体积比1:2置于2L的密闭容器中发生反应:N2(g)+3H2(g) 2NH3(g),下列能说明反应达到平衡状态的是
2NH3(g),下列能说明反应达到平衡状态的是___ 。
A.体系压强保持不变
B.混合气体颜色保持不变
C.N2与H2的物质的量之比保持不变
D.每消耗2molNH3的同时消耗1molN2
(3)“吸收塔”尾部会有含NO、NO2等氮氧化物的尾气排出,为消除它们对环境的破坏作用,通常用氨转化法处理:已知7mol氨恰好能将含NO和NO2共6mol的混合气体完全转化为N2,则混合气体中NO和NO2的物质的量之比为__ 。
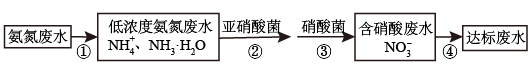
Ⅱ.氮肥厂的废水直接排放会造成污染,目前氨氮废水处理方法主要有吹脱法、化学沉淀法、生物硝化反硝化法等。某氮肥厂的氨氮废水中氮元素多以NH 和NH3•H2O的形式存在。该厂技术团队设计该废水处理方案流程如图:
和NH3•H2O的形式存在。该厂技术团队设计该废水处理方案流程如图:
(4)检验某溶液中是否含有NH 的方法
的方法___ (写出所需试剂、操作及现象)。
(5)过程②、③:在微生物亚硝酸菌和硝酸菌作用下实现NH →NO
→NO →NO
→NO 的转化,称为硝化反应。1molNH
的转化,称为硝化反应。1molNH 可被
可被___ L(标准状况)O2最终氧化成NO 。
。
(6)过程④:在一定条件下向废水中加入甲醇(CH3OH)实现HNO2→N2转化,称为反硝化反应。此过程中甲醇(C元素-2价)转化为CO2,写出此过程的化学方程式___ 。

(1)工业用甲烷制取氢气作为合成氨的原料,已知以下的热化学反应方程式:
①2CO(g)+O2(g)=2CO2(g)∆H=-566kJ/mol
②2H2(g)+O2(g)=2H2O(g)∆H=-484kJ/mol
③CH4(g)+2O2(g)=CO2(g)+2H2O(g)∆H=-890kJ/mol
则:CH4(g)+CO2(g)=2CO(g)+2H2(g)∆H=
(2)一定温度下,将N2与H2以体积比1:2置于2L的密闭容器中发生反应:N2(g)+3H2(g)
 2NH3(g),下列能说明反应达到平衡状态的是
2NH3(g),下列能说明反应达到平衡状态的是A.体系压强保持不变
B.混合气体颜色保持不变
C.N2与H2的物质的量之比保持不变
D.每消耗2molNH3的同时消耗1molN2
(3)“吸收塔”尾部会有含NO、NO2等氮氧化物的尾气排出,为消除它们对环境的破坏作用,通常用氨转化法处理:已知7mol氨恰好能将含NO和NO2共6mol的混合气体完全转化为N2,则混合气体中NO和NO2的物质的量之比为
Ⅱ.氮肥厂的废水直接排放会造成污染,目前氨氮废水处理方法主要有吹脱法、化学沉淀法、生物硝化反硝化法等。某氮肥厂的氨氮废水中氮元素多以NH
 和NH3•H2O的形式存在。该厂技术团队设计该废水处理方案流程如图:
和NH3•H2O的形式存在。该厂技术团队设计该废水处理方案流程如图:
(4)检验某溶液中是否含有NH
 的方法
的方法(5)过程②、③:在微生物亚硝酸菌和硝酸菌作用下实现NH
 →NO
→NO →NO
→NO 的转化,称为硝化反应。1molNH
的转化,称为硝化反应。1molNH 可被
可被 。
。(6)过程④:在一定条件下向废水中加入甲醇(CH3OH)实现HNO2→N2转化,称为反硝化反应。此过程中甲醇(C元素-2价)转化为CO2,写出此过程的化学方程式
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐1】CO2的资源化利用一直是科学研究的热点领域。回答下列问题
(1)CO2的甲烷化反应为:CO2(g)+4H2(g) CH4(g)+2H2O(g) △H,该反应又称Sabatier反应。相关的化学键键能数据如表,上述反应的△H=
CH4(g)+2H2O(g) △H,该反应又称Sabatier反应。相关的化学键键能数据如表,上述反应的△H=______ kJ•mol-1。
(2)以CO2和H2为原料合成甲醇(CH3OH)。300℃时,将6molCO2和8molH2的气态混合物充入2L密闭容器中发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H<0,该容器中n(H2)随时间变化如图中实线所示:
CH3OH(g)+H2O(g) △H<0,该容器中n(H2)随时间变化如图中实线所示:
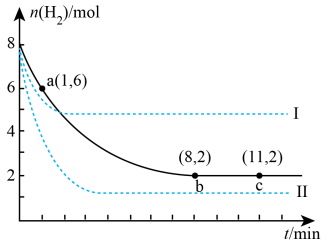
①从反应开始到a点,用CO2表示的反应速率为v(CO2)=______ (保留2位有效数字),此时H2的转化率为______ 。
②根据图中平衡状态计算该反应的平衡常数______ 。
③图中虚线______ (填“I”或“Ⅱ”)表示的是该反应升温时n(H2)随时间变化的曲线,判断依据______ 。
(3)以CO2、NaCl和NH3为原料可以制备NaHCO3。如图为某实验测得NaHCO3溶液的pH随温度的变化曲线(不考虑水挥发)。
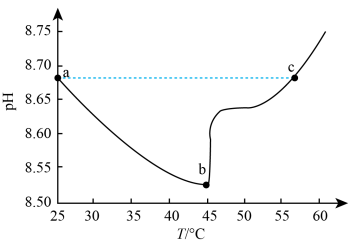
溶液中的c(OH-):a点______ c点(填“>”“<”或“=”)。
(1)CO2的甲烷化反应为:CO2(g)+4H2(g)
 CH4(g)+2H2O(g) △H,该反应又称Sabatier反应。相关的化学键键能数据如表,上述反应的△H=
CH4(g)+2H2O(g) △H,该反应又称Sabatier反应。相关的化学键键能数据如表,上述反应的△H=| 化学键 | H-H | H-O | C-H | C=O |
| E(kJ•mol-1) | 436 | 463 | 413 | 803 |
 CH3OH(g)+H2O(g) △H<0,该容器中n(H2)随时间变化如图中实线所示:
CH3OH(g)+H2O(g) △H<0,该容器中n(H2)随时间变化如图中实线所示:
①从反应开始到a点,用CO2表示的反应速率为v(CO2)=
②根据图中平衡状态计算该反应的平衡常数
③图中虚线
(3)以CO2、NaCl和NH3为原料可以制备NaHCO3。如图为某实验测得NaHCO3溶液的pH随温度的变化曲线(不考虑水挥发)。

溶液中的c(OH-):a点
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐2】以银锰精矿(主要含 、
、 、
、 )和氧化锰矿(主要含
)和氧化锰矿(主要含 )为原料联合提取银和锰的一种流程示意图如下。
)为原料联合提取银和锰的一种流程示意图如下。
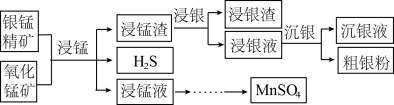
已知:酸性条件下, 的氧化性强于
的氧化性强于 。
。
(1)“浸锰”过程是在 溶液中使矿石中的锰元素浸出,同时去除
溶液中使矿石中的锰元素浸出,同时去除 ,有利于后续银的浸出,矿石中的银以
,有利于后续银的浸出,矿石中的银以 的形式残留于浸锰渣中。“浸锰”过程中,发生了反应
的形式残留于浸锰渣中。“浸锰”过程中,发生了反应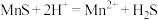 ,其平衡常数K与
,其平衡常数K与 、
、 、
、 的代数关系式为
的代数关系式为
_______ 。
(2)“浸银”时,使用过量 、
、 和
和 的混合液作为浸出剂,将
的混合液作为浸出剂,将 中的银以
中的银以 形式浸出。
形式浸出。
①“浸银”反应的离子方程式为_______ 。
②结合平衡移动原理,解释浸出剂中 、
、 的作用是
的作用是_______ 。
(3)“沉银”过程中需要过量的铁粉作为还原剂。
①“沉银”过程中主要反应的离子方程式为_______ 。
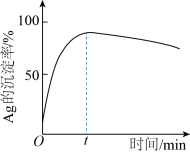
②一定温度下, 的沉淀率随反应时间的变化如图所示。解释t分钟后
的沉淀率随反应时间的变化如图所示。解释t分钟后 的沉淀率逐渐减小的原因是
的沉淀率逐渐减小的原因是_______ 。
(4)“浸锰”过程中产生的 可用于“浸银”,生产中需要测定
可用于“浸银”,生产中需要测定 的浓度来确定其用量。测定方法:准确量取20.00
的浓度来确定其用量。测定方法:准确量取20.00 浸取液置于250
浸取液置于250 锥形瓶中,加入适量稀硫酸,滴加稍过量的
锥形瓶中,加入适量稀硫酸,滴加稍过量的 溶液(
溶液( 将
将 还原为
还原为 ),充分反应后,除去过量的
),充分反应后,除去过量的 。用
。用
 溶液滴定至终点(滴定过程中
溶液滴定至终点(滴定过程中 与
与 反应生成
反应生成 和
和 ),消耗
),消耗 溶液12.00
溶液12.00 。计算浸取液中
。计算浸取液中 的浓度
的浓度_______ (写出计算过程)。
 、
、 、
、 )和氧化锰矿(主要含
)和氧化锰矿(主要含 )为原料联合提取银和锰的一种流程示意图如下。
)为原料联合提取银和锰的一种流程示意图如下。
已知:酸性条件下,
 的氧化性强于
的氧化性强于 。
。(1)“浸锰”过程是在
 溶液中使矿石中的锰元素浸出,同时去除
溶液中使矿石中的锰元素浸出,同时去除 ,有利于后续银的浸出,矿石中的银以
,有利于后续银的浸出,矿石中的银以 的形式残留于浸锰渣中。“浸锰”过程中,发生了反应
的形式残留于浸锰渣中。“浸锰”过程中,发生了反应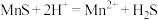 ,其平衡常数K与
,其平衡常数K与 、
、 、
、 的代数关系式为
的代数关系式为
(2)“浸银”时,使用过量
 、
、 和
和 的混合液作为浸出剂,将
的混合液作为浸出剂,将 中的银以
中的银以 形式浸出。
形式浸出。①“浸银”反应的离子方程式为
②结合平衡移动原理,解释浸出剂中
 、
、 的作用是
的作用是(3)“沉银”过程中需要过量的铁粉作为还原剂。
①“沉银”过程中主要反应的离子方程式为
②一定温度下,
 的沉淀率随反应时间的变化如图所示。解释t分钟后
的沉淀率随反应时间的变化如图所示。解释t分钟后 的沉淀率逐渐减小的原因是
的沉淀率逐渐减小的原因是
(4)“浸锰”过程中产生的
 可用于“浸银”,生产中需要测定
可用于“浸银”,生产中需要测定 的浓度来确定其用量。测定方法:准确量取20.00
的浓度来确定其用量。测定方法:准确量取20.00 浸取液置于250
浸取液置于250 锥形瓶中,加入适量稀硫酸,滴加稍过量的
锥形瓶中,加入适量稀硫酸,滴加稍过量的 溶液(
溶液( 将
将 还原为
还原为 ),充分反应后,除去过量的
),充分反应后,除去过量的 。用
。用
 溶液滴定至终点(滴定过程中
溶液滴定至终点(滴定过程中 与
与 反应生成
反应生成 和
和 ),消耗
),消耗 溶液12.00
溶液12.00 。计算浸取液中
。计算浸取液中 的浓度
的浓度
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐3】工业废水中常含有一定量的 ,会危害生态系统,必须进行处理。常将
,会危害生态系统,必须进行处理。常将 转化为纺织印染中的媒染剂
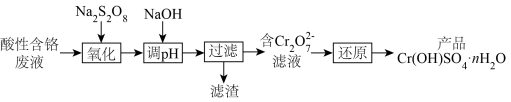
转化为纺织印染中的媒染剂 ,变废为宝。该法用酸性含铬废液(含
,变废为宝。该法用酸性含铬废液(含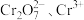 及少量
及少量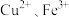 等)制备
等)制备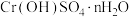 晶体,工艺流程如下:
晶体,工艺流程如下:
常温下, 金属离子形成氢氧化物沉淀的
金属离子形成氢氧化物沉淀的 范围如表。已知:
范围如表。已知:
回答下列问题
(1)“氧化”时,
①将 先氧化为
先氧化为 的目的是
的目的是_______ 。
②加入的 (
( 为+6价)中,
为+6价)中,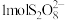 含有过氧键数目为
含有过氧键数目为_______ 。
③完成下列离子方程式:_______ 。

(2)“调 ”时,加入
”时,加入 至溶液呈碱性,但
至溶液呈碱性,但 不能大于9的原因是
不能大于9的原因是_______ ;
(3)“过滤”时,滤渣的主要成分是_______ 。(填化学式)
(4)“还原”时,还原剂将 还原为
还原为 ,最适合的还原剂是_______。
,最适合的还原剂是_______。
(5)从 溶液得到
溶液得到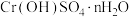 晶体,需进行的操作为:蒸发浓缩、_______、过滤、洗涤、干燥。
晶体,需进行的操作为:蒸发浓缩、_______、过滤、洗涤、干燥。
 ,会危害生态系统,必须进行处理。常将
,会危害生态系统,必须进行处理。常将 转化为纺织印染中的媒染剂
转化为纺织印染中的媒染剂 ,变废为宝。该法用酸性含铬废液(含
,变废为宝。该法用酸性含铬废液(含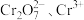 及少量
及少量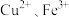 等)制备
等)制备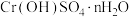 晶体,工艺流程如下:
晶体,工艺流程如下:
常温下,
 金属离子形成氢氧化物沉淀的
金属离子形成氢氧化物沉淀的 范围如表。已知:
范围如表。已知:
| 离子 | 开始沉淀的 | 完全沉淀的 |
 | 1.4 | 3.0 |
 | 4.2 | 6.7 |
 | 4.0 | 6.8 |
(1)“氧化”时,
①将
 先氧化为
先氧化为 的目的是
的目的是②加入的
 (
( 为+6价)中,
为+6价)中,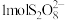 含有过氧键数目为
含有过氧键数目为③完成下列离子方程式:

(2)“调
 ”时,加入
”时,加入 至溶液呈碱性,但
至溶液呈碱性,但 不能大于9的原因是
不能大于9的原因是(3)“过滤”时,滤渣的主要成分是
(4)“还原”时,还原剂将
 还原为
还原为 ,最适合的还原剂是_______。
,最适合的还原剂是_______。A. | B. | C. | D. |
(5)从
 溶液得到
溶液得到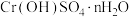 晶体,需进行的操作为:蒸发浓缩、_______、过滤、洗涤、干燥。
晶体,需进行的操作为:蒸发浓缩、_______、过滤、洗涤、干燥。
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐1】脱除工业废气中的氮氧化物(主要是指NO和NO2)可以净化空气、改善环境,是环境保护的主要课题。
(1)早期是利用NH3还原法,可将NOx还原为N2进行脱除。
已知:①4NH3(g)+5O2(g) 4NO(g)+6H2O(g) ΔH=-905.9kJ·mol-1
4NO(g)+6H2O(g) ΔH=-905.9kJ·mol-1
②N2(g)+O2(g) 2NO(g) ΔH=+180kJ·mol-1
2NO(g) ΔH=+180kJ·mol-1
③H2O(g) H2O(l) ΔH=-44kJ·mol-1
H2O(l) ΔH=-44kJ·mol-1
写出常温下,NH3还原NO反应的热化学方程式__ 。
(2)以漂粉精溶液为吸收剂可以有效脱除烟气中的NO。
①漂粉精溶液的主要成分是Ca(ClO)2,若吸收过程中,消耗的Ca(ClO)2与吸收的NO的物质的量之比为3∶4,则脱除后NO转化为__ 。
②某一兴趣小组研究不同温度下相同浓度漂粉精溶液对NO脱除率的影响,结果如图所示。图中,40~60℃NO脱除率上升可能的原因为__ ;60~80℃NO脱除率下降可能的原因为__ 。

(3)过硫酸钠(Na2S2O8)氧化去除NO
第一步:NO在碱性环境中被Na2S2O8氧化为NaNO2
第二步:NaNO2继续被氧化为NaNO3,反应为 +
+ +2OH-
+2OH-
 +2
+2 +H2O。
+H2O。
不同温度下,平衡时 的脱除率与过硫酸钠(Na2S2O8)初始浓度(指第二步反应的初始浓度)的关系如图所示。
的脱除率与过硫酸钠(Na2S2O8)初始浓度(指第二步反应的初始浓度)的关系如图所示。
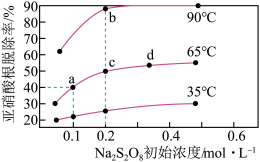
①a、b、c、d四点平衡常数K由大到小的顺序为__ ,原因是__ 。
②若a点(0.1,40%)时, 的初始浓度为amol·L-1,平衡时pH=13,则65℃时,第二步反应的平衡常数K=
的初始浓度为amol·L-1,平衡时pH=13,则65℃时,第二步反应的平衡常数K=__ 。(用含a的代数式表示,已知65℃时Kw=1.0×10-13)
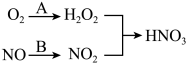
(4)利用新型材料光催化脱除NO法如图所示。
某电化学小组将过程A、B设计成酸性电解池反应,则该反应中阴极反应方程式为___ 。
(1)早期是利用NH3还原法,可将NOx还原为N2进行脱除。
已知:①4NH3(g)+5O2(g)
 4NO(g)+6H2O(g) ΔH=-905.9kJ·mol-1
4NO(g)+6H2O(g) ΔH=-905.9kJ·mol-1②N2(g)+O2(g)
 2NO(g) ΔH=+180kJ·mol-1
2NO(g) ΔH=+180kJ·mol-1③H2O(g)
 H2O(l) ΔH=-44kJ·mol-1
H2O(l) ΔH=-44kJ·mol-1写出常温下,NH3还原NO反应的热化学方程式
(2)以漂粉精溶液为吸收剂可以有效脱除烟气中的NO。
①漂粉精溶液的主要成分是Ca(ClO)2,若吸收过程中,消耗的Ca(ClO)2与吸收的NO的物质的量之比为3∶4,则脱除后NO转化为
②某一兴趣小组研究不同温度下相同浓度漂粉精溶液对NO脱除率的影响,结果如图所示。图中,40~60℃NO脱除率上升可能的原因为

(3)过硫酸钠(Na2S2O8)氧化去除NO
第一步:NO在碱性环境中被Na2S2O8氧化为NaNO2
第二步:NaNO2继续被氧化为NaNO3,反应为
 +
+ +2OH-
+2OH-
 +2
+2 +H2O。
+H2O。不同温度下,平衡时
 的脱除率与过硫酸钠(Na2S2O8)初始浓度(指第二步反应的初始浓度)的关系如图所示。
的脱除率与过硫酸钠(Na2S2O8)初始浓度(指第二步反应的初始浓度)的关系如图所示。
①a、b、c、d四点平衡常数K由大到小的顺序为
②若a点(0.1,40%)时,
 的初始浓度为amol·L-1,平衡时pH=13,则65℃时,第二步反应的平衡常数K=
的初始浓度为amol·L-1,平衡时pH=13,则65℃时,第二步反应的平衡常数K=(4)利用新型材料光催化脱除NO法如图所示。
某电化学小组将过程A、B设计成酸性电解池反应,则该反应中阴极反应方程式为

您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐2】近年来CO2变废为宝,改善环境是科学研究的重要课题,对于实现废气资源的再利用及碳循环经济技术的发展都具有重要意义。
Ⅰ.已知CO2、C2H6为原料合成C2H4涉及的主要反应如下:
①C2H6(g) CH4(g)+H2(g)+C(s)△H1=+9kJ·mol-1
CH4(g)+H2(g)+C(s)△H1=+9kJ·mol-1
②C2H4(g)+H2(g) C2H6(g)△H2=-136kJ·mol-1
C2H6(g)△H2=-136kJ·mol-1
③H2(g)+CO2(g) H2O(g)+CO(g)△H3=+41kJ·mol-1
H2O(g)+CO(g)△H3=+41kJ·mol-1
④CO2(g)+C2H6(g) C2H4(g)+H2O(g)+CO(g)△H4
C2H4(g)+H2O(g)+CO(g)△H4
(1)△H4=___ ,0.1MPa时向密闭容器中充入CO2和C2H6,发生反应④,温度对催化剂K—Fe—Mn/Si性能的影响如图:
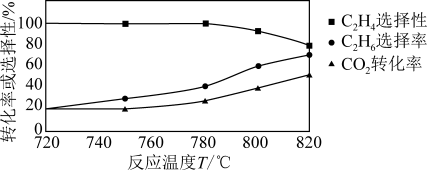
工业生产综合各方面的因素,根据图中的信息判断反应的最佳温度是__ ℃。
(2)在800℃时,n(CO2):n(C2H6)=1:3,充入一定体积的密闭容器中,在有催化剂存在的条件下,发生反应④,初始压强为p0,一段时间后达到平衡,产物的总物质的量与剩余反应物的总物质的量相等,则该温度下反应的平衡常数Kp=___ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数,用最简分式表示)。
Ⅱ.科学家利用Li4SiO4吸附CO2有着重要的现实意义。CO2的回收及材料再生的原理如图所示:

(1)“吸附”过程中主要反应的化学方程式为___ 。
(2)为了探究Li4SiO4的吸附效果,在刚性容器中放入1000g的Li4SiO4,通入10mol不同比例的N2和CO2混合气体,控制反应时间均为2小时,得到Li4SiO4吸附CO2后固体样品质量分数与温度的关系如图所示。
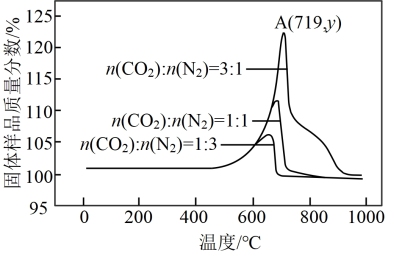
①该反应为___ 反应(填“吸热”或“放热”)。
②保持A点的温度不变,若所用刚性容器体积变为原来的一半,则平衡时c(CO2)较原平衡___ (填“增大”、“减小”或“不变”)。
③若在A点CO2的吸收率为70%,A点的纵坐标y的值为___ 。
Ⅰ.已知CO2、C2H6为原料合成C2H4涉及的主要反应如下:
①C2H6(g)
 CH4(g)+H2(g)+C(s)△H1=+9kJ·mol-1
CH4(g)+H2(g)+C(s)△H1=+9kJ·mol-1②C2H4(g)+H2(g)
 C2H6(g)△H2=-136kJ·mol-1
C2H6(g)△H2=-136kJ·mol-1③H2(g)+CO2(g)
 H2O(g)+CO(g)△H3=+41kJ·mol-1
H2O(g)+CO(g)△H3=+41kJ·mol-1④CO2(g)+C2H6(g)
 C2H4(g)+H2O(g)+CO(g)△H4
C2H4(g)+H2O(g)+CO(g)△H4(1)△H4=

工业生产综合各方面的因素,根据图中的信息判断反应的最佳温度是
(2)在800℃时,n(CO2):n(C2H6)=1:3,充入一定体积的密闭容器中,在有催化剂存在的条件下,发生反应④,初始压强为p0,一段时间后达到平衡,产物的总物质的量与剩余反应物的总物质的量相等,则该温度下反应的平衡常数Kp=
Ⅱ.科学家利用Li4SiO4吸附CO2有着重要的现实意义。CO2的回收及材料再生的原理如图所示:

(1)“吸附”过程中主要反应的化学方程式为
(2)为了探究Li4SiO4的吸附效果,在刚性容器中放入1000g的Li4SiO4,通入10mol不同比例的N2和CO2混合气体,控制反应时间均为2小时,得到Li4SiO4吸附CO2后固体样品质量分数与温度的关系如图所示。

①该反应为
②保持A点的温度不变,若所用刚性容器体积变为原来的一半,则平衡时c(CO2)较原平衡
③若在A点CO2的吸收率为70%,A点的纵坐标y的值为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
【推荐3】汽车尾气是否为导致空气质量问题的主要原因,由此引发的“汽车限行”争议,是当前备受关注的社会性科学议题。
(1)反应
 可有效降低汽车尾气污染物的排放。
可有效降低汽车尾气污染物的排放。
①探究温度、压强(2MPa、5MPa)对该反应的影响,如图所示,表示5MPa的是________ (填标号)。
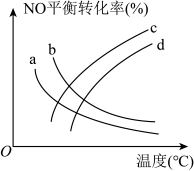
在一定温度下,将2mol CO气体和2mol NO通入恒容密闭容器中,发生以上反应。
②下列不能说明反应达到平衡的是________ 。
A.混合气体的压强不再改变的状态
B.混合气体的密度不再改变的状态
C.单位时间内生成2mol NO同时消耗
D.混合气体的平均相对分子质量不再改变的状态
(2)用 可以消除NO污染:
可以消除NO污染:
 。在体积为1L的恒容密闭容器中加入
。在体积为1L的恒容密闭容器中加入 和5mol NO,在200℃时发生上述反应,测得
和5mol NO,在200℃时发生上述反应,测得 和
和 的物质的量随时间变化如图。
的物质的量随时间变化如图。
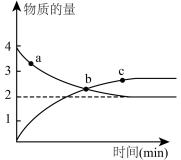
a点的正反应速率________ c点的逆反应速率(填“大于”、“小于”或“等于”);测得平衡时体系压强为P0,则该反应温度下Kp________ (用含P0的式子表示,只列式不用化简。用各气体物质的分压替代浓度计算的平衡常数叫压强平衡常数Kp,某气体的分压=气体总压强×该气体的物质的量分数)。
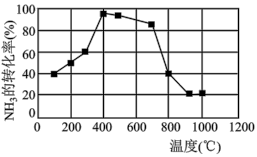
(3)若在相同时间内测得 的转化率随温度的变化曲线如下图,200℃~700℃之间
的转化率随温度的变化曲线如下图,200℃~700℃之间 的转化率先升高又降低的原因是
的转化率先升高又降低的原因是________ ;800℃反应达到平衡后,再向反应体系中加入2mol NO和 ,平衡
,平衡________ (填“正向移动”、“逆向移动”或“不移动”)。
(1)反应

 可有效降低汽车尾气污染物的排放。
可有效降低汽车尾气污染物的排放。①探究温度、压强(2MPa、5MPa)对该反应的影响,如图所示,表示5MPa的是

在一定温度下,将2mol CO气体和2mol NO通入恒容密闭容器中,发生以上反应。
②下列不能说明反应达到平衡的是
A.混合气体的压强不再改变的状态
B.混合气体的密度不再改变的状态
C.单位时间内生成2mol NO同时消耗

D.混合气体的平均相对分子质量不再改变的状态
(2)用
 可以消除NO污染:
可以消除NO污染:
 。在体积为1L的恒容密闭容器中加入
。在体积为1L的恒容密闭容器中加入 和5mol NO,在200℃时发生上述反应,测得
和5mol NO,在200℃时发生上述反应,测得 和
和 的物质的量随时间变化如图。
的物质的量随时间变化如图。
a点的正反应速率
(3)若在相同时间内测得
 的转化率随温度的变化曲线如下图,200℃~700℃之间
的转化率随温度的变化曲线如下图,200℃~700℃之间 的转化率先升高又降低的原因是
的转化率先升高又降低的原因是 ,平衡
,平衡
您最近一年使用:0次



