马日夫盐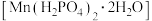 用于钢铁制品,特别是大型机械设备的磷化处理,可起到防锈效果。以软锰矿(主要成分为
用于钢铁制品,特别是大型机械设备的磷化处理,可起到防锈效果。以软锰矿(主要成分为 及少量的FeO、
及少量的FeO、 和
和 )为原料制备马日夫盐的主要工艺流程如图:
)为原料制备马日夫盐的主要工艺流程如图:
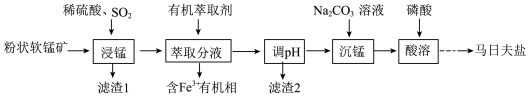
(1)“浸锰”过程中,FeO参与氧化还原反应的离子方程式为_______________ 。
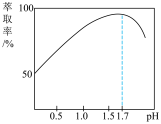
(2) 的萃取率与溶液的pH的关系如图所示,当
的萃取率与溶液的pH的关系如图所示,当 时,
时, 的萃取率急剧下降的原因可能为
的萃取率急剧下降的原因可能为_______________ (用化学用语表示)。
(3)“调pH”的最大范围为________ 。
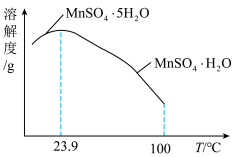
(4)如图为硫酸锰水合物的溶解度曲线,若要用“调pH”所得滤液制备 ,需要控制温度在80℃~90℃之间的原因是
,需要控制温度在80℃~90℃之间的原因是_____ ,采用水浴加热,经蒸发浓缩、_____ (填操作名称)、用80℃~90℃的蒸馏水洗涤2~3次,放在真空干燥箱中低温干燥获得。
(5)写出检验“沉锰”是否已完成的实验操作_________ 。
(6)常温下,马日夫盐溶液显________ 性(填“酸”或“碱”),理由是:____________ 。(写出计算过程并结合必要的文字说明。已知: 的电离常数
的电离常数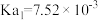 ,
,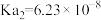 ,
,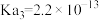 )
)
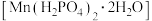 用于钢铁制品,特别是大型机械设备的磷化处理,可起到防锈效果。以软锰矿(主要成分为
用于钢铁制品,特别是大型机械设备的磷化处理,可起到防锈效果。以软锰矿(主要成分为 及少量的FeO、
及少量的FeO、 和
和 )为原料制备马日夫盐的主要工艺流程如图:
)为原料制备马日夫盐的主要工艺流程如图:
(1)“浸锰”过程中,FeO参与氧化还原反应的离子方程式为
(2)
 的萃取率与溶液的pH的关系如图所示,当
的萃取率与溶液的pH的关系如图所示,当 时,
时, 的萃取率急剧下降的原因可能为
的萃取率急剧下降的原因可能为
(3)“调pH”的最大范围为
| 金属离子 | 开始沉淀的pH | 完全沉淀的pH |
 | l. 8 | 3.2 |
 | 3.0 | 5.0 |
 | 5.8 | 8.8 |
 | 7.8 | 9.8 |
(4)如图为硫酸锰水合物的溶解度曲线,若要用“调pH”所得滤液制备
 ,需要控制温度在80℃~90℃之间的原因是
,需要控制温度在80℃~90℃之间的原因是
(5)写出检验“沉锰”是否已完成的实验操作
(6)常温下,马日夫盐溶液显
 的电离常数
的电离常数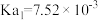 ,
,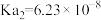 ,
,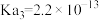 )
)
更新时间:2020-06-12 10:02:18
|
相似题推荐
【推荐1】以含铝、铁烧渣(主要成分为Al2O3、Fe2O3,含少量FeO、SiO2)为原料制备聚合碱式硫酸铝铁{[FeaAlb(OH)x(SO4)y]n}或明矾[KAl(SO4)2·12H2O]的流程如图所示:
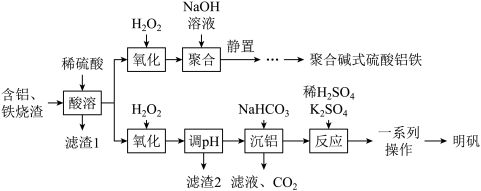
回答下列问题:
(1)滤渣1的用途为______ (任写一种)。
(2)“酸溶”后溶液中含有的阳离子为_____ 。
(3)“氧化”时发生反应的离子方程式为______ 。
(4)“调pH”的目的是______ 。
(5)“沉铝”中加入NaHCO3的目的是将Al3+转化为Al(OH)3,写出该反应的离子方程式:_____ 。
(6)根据不同温度KAl(SO4)2·12H2O的溶解度(如表),“一系列操作”应包括蒸发浓缩、_____ 、过滤、洗涤、干燥等。

回答下列问题:
(1)滤渣1的用途为
(2)“酸溶”后溶液中含有的阳离子为
(3)“氧化”时发生反应的离子方程式为
(4)“调pH”的目的是
(5)“沉铝”中加入NaHCO3的目的是将Al3+转化为Al(OH)3,写出该反应的离子方程式:
(6)根据不同温度KAl(SO4)2·12H2O的溶解度(如表),“一系列操作”应包括蒸发浓缩、
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 60 | 80 | 90 |
| KAl(SO4)2·12H2O/g | 3.00 | 3.99 | 5.90 | 8.39 | 11.7 | 24.8 | 71.0 | 109 |
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】某Al2O3样品中含有一定量的Cu、Fe,以及少量的Fe2O3。现通过下列生产过程,从该样品中回收铁红。流程如图:
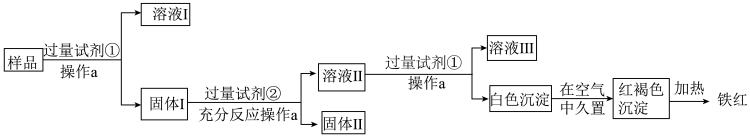
(1)操作a需要的玻璃仪器有烧杯、漏斗、____ 。
(2)溶液Ⅰ中除OH-外还含有大量的阴离子是____ 。
(3)试剂②是____ ,加入试剂②后发生的化学方程式为____ 。
(4)白色沉淀的成分是____ ;写出白色沉淀转化为红褐色沉淀的化学方程式:____ 。
(5)溶液Ⅱ中铁元素的存在形式是____ (填离子符号),如何用实验证明:____ 。

(1)操作a需要的玻璃仪器有烧杯、漏斗、
(2)溶液Ⅰ中除OH-外还含有大量的阴离子是
(3)试剂②是
(4)白色沉淀的成分是
(5)溶液Ⅱ中铁元素的存在形式是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】某油脂厂废弃的镍催化剂主要含量金属Ni、Al、Fe及其氧化物,还有少量其他不溶性物质。采用如图工艺流程回收镍制备硫酸镍晶体(NiSO4•7H2O)。
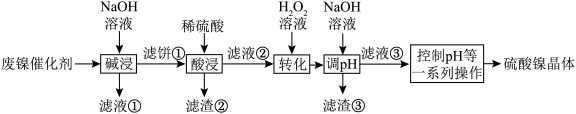
(1)提高“碱浸”速率的有效措施有________ (任写一种即可)。
(2)“滤液②”中含有的金属离子有_______ ,滤渣③的化学式是_______ 。
(3)为回收金属,控制稀硫酸用量将“滤液①”转化为沉淀,写出该反应的离子方程式_______ 。
(4)“转化”过程中温度不宜过高的原因是________ 。
(5)将“滤液③”经过控制pH、蒸发浓缩、________ 、________ 、洗涤、干燥等一系列操作可得到硫酸镍晶体。
(6)硫酸镍在强碱条件下用NaClO氧化,可沉淀出能用作镍镉电池正极材料的NiOOH。该反应的离子方程式为________ 。

(1)提高“碱浸”速率的有效措施有
(2)“滤液②”中含有的金属离子有
(3)为回收金属,控制稀硫酸用量将“滤液①”转化为沉淀,写出该反应的离子方程式
(4)“转化”过程中温度不宜过高的原因是
(5)将“滤液③”经过控制pH、蒸发浓缩、
(6)硫酸镍在强碱条件下用NaClO氧化,可沉淀出能用作镍镉电池正极材料的NiOOH。该反应的离子方程式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】碳氧化物、氮氧化物、二氧化硫的处理与利用是世界各国研究的热点问题。
消除汽车尾气中的NO、CO,有利于减少PM2.5的排放。已知如下信息:
2CO(g)+2NO(g) 2CO2(g)+N2(g) ΔH1=-748kJ·mol-1
2CO2(g)+N2(g) ΔH1=-748kJ·mol-1
2CO(g)+O2(g)===2CO2(g) ΔH2=-565kJ·mol-1
(1)在一定条件下N2和O2会转化为NO,写出该反应的热化学方程式:_________ 。
(2)为研究不同条件对反应的影响,在恒温条件下,向2L恒容密闭容器中加入0.2molNO和0.4mol CO,在催化剂存在的条件下发生反应,10min时反应达到平衡,测得10min内v(NO)=7.5×10-3mol·L-1·min-1,则平衡后n(CO)=________ mol,关于该平衡的下列说法正确的是________ 。
a.增大压强,平衡一定向右移动
b.其他条件不变,升高温度,化学反应速率一定增大
c.其他条件不变,若改为在恒压容器中进行,CO的平衡转化率比恒容条件下大
d.达到平衡后v正(NO)=2v逆(N2)
(3)其他条件相同,t min时不同温度下测得NO的转化率如图所示。
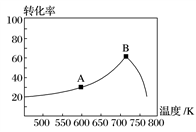
A点的反应速度v正________ (填“>”、“<”或“=”)v逆,A、B两点反应的平衡常数较大的是________ (填“A”或“B”)。
(4)已知HNO2的电离常数Ka=7.1×10-4mol·L-1;
NH3·H2O的电离常数Kb=1.7×10-5mol·L-1
则0.1mol·L-1NH4NO2溶液中离子浓度由大到小的顺序是____________________________ ,
常温下NO2-水解反应的平衡常数Kh=________ (保留两位有效数字)。
消除汽车尾气中的NO、CO,有利于减少PM2.5的排放。已知如下信息:
2CO(g)+2NO(g)
 2CO2(g)+N2(g) ΔH1=-748kJ·mol-1
2CO2(g)+N2(g) ΔH1=-748kJ·mol-12CO(g)+O2(g)===2CO2(g) ΔH2=-565kJ·mol-1
(1)在一定条件下N2和O2会转化为NO,写出该反应的热化学方程式:
(2)为研究不同条件对反应的影响,在恒温条件下,向2L恒容密闭容器中加入0.2molNO和0.4mol CO,在催化剂存在的条件下发生反应,10min时反应达到平衡,测得10min内v(NO)=7.5×10-3mol·L-1·min-1,则平衡后n(CO)=
a.增大压强,平衡一定向右移动
b.其他条件不变,升高温度,化学反应速率一定增大
c.其他条件不变,若改为在恒压容器中进行,CO的平衡转化率比恒容条件下大
d.达到平衡后v正(NO)=2v逆(N2)
(3)其他条件相同,t min时不同温度下测得NO的转化率如图所示。

A点的反应速度v正
(4)已知HNO2的电离常数Ka=7.1×10-4mol·L-1;
NH3·H2O的电离常数Kb=1.7×10-5mol·L-1
则0.1mol·L-1NH4NO2溶液中离子浓度由大到小的顺序是
常温下NO2-水解反应的平衡常数Kh=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】完成下列问题。
(1)①已知:HCN的Ka=4.9×10-10、CH3COOH的Ka=1.7×10-5,等浓度的NaCN溶液和CH3COONa溶液比较pH (NaCN)___________ pH (CH3COONa) (填“>”“<”或“=”)。
②常温下若CH3COONa和CH3COOH的混合溶液中c(Na+) =c(CH3COO-),则该溶液呈___________ 性。(填“酸”“碱”或“中”)
③已知100 ℃时,0.01 mol·L-1 NaHSO4溶液中由水电离的c(H+)=10-10 mol·L-1,该温度下将pH=8的Ba(OH)2溶液V1 L与pH=5的NaHSO4溶液 V2 L混合,所得溶液pH=7,则V1∶V2___________
(2)将下列固体物质溶于水,再将其溶液加热、蒸发结晶,再灼烧,得到化学组成与原固体物质相同的是___________ (填序号)。
①胆矾、②氯化铝、③硫酸铝、④氯化铜、⑤硫酸亚铁、⑥碳酸钠、⑦亚硫酸钠、⑧NH4Cl、⑨KMnO4、⑩Ca(HCO3)2
(3)已知某温度时,Kw=1.0×10-12,Na2CO3溶液的水解常数Kh=2.0×10-3,则当溶液中c( )∶c(
)∶c( )=2∶1时,试求该溶液的pH=
)=2∶1时,试求该溶液的pH=___________ 。
(4)下列事实,其中与盐类的水解有关的是___________ (填序号)。
①NaHSO4溶液呈酸性 ②长期使用(NH4)2SO4化肥会使土壤酸性增大,发生板结
③配制CuCl2溶液,用稀盐酸溶解CuCl2固体 ④实验室盛放纯碱溶液的试剂瓶不能用磨口玻璃塞
⑤加热FeCl3·6H2O晶体,往往得不到FeCl3固体
(5)已知:H2CO3:Ka1=4.5×10-7,Ka2=4.7×10-11,NH3·H2O:Kb=1.8×10-5现有常温下0.1 mol·L-1的(NH4)2CO3溶液,该溶液中各微粒浓度之间的关系式错误的是________ (填字母)。
A.c( )+c(H+)=c(
)+c(H+)=c( )+c(OH-)+c(
)+c(OH-)+c( )
)
B.c( )+c(NH3·H2O)=2c(
)+c(NH3·H2O)=2c( )+2c(
)+2c( )+2c(H2CO3)
)+2c(H2CO3)
C.c( )+c(
)+c( )+c(H2CO3)=0.1 mol·L-1
)+c(H2CO3)=0.1 mol·L-1
D.c(H+)+c( )+c(H2CO3)=c(OH-)+c(NH3·H2O)
)+c(H2CO3)=c(OH-)+c(NH3·H2O)
E.c( )>c(
)>c( )>c(
)>c( )>c(NH3·H2O)
)>c(NH3·H2O)
(1)①已知:HCN的Ka=4.9×10-10、CH3COOH的Ka=1.7×10-5,等浓度的NaCN溶液和CH3COONa溶液比较pH (NaCN)
②常温下若CH3COONa和CH3COOH的混合溶液中c(Na+) =c(CH3COO-),则该溶液呈
③已知100 ℃时,0.01 mol·L-1 NaHSO4溶液中由水电离的c(H+)=10-10 mol·L-1,该温度下将pH=8的Ba(OH)2溶液V1 L与pH=5的NaHSO4溶液 V2 L混合,所得溶液pH=7,则V1∶V2
(2)将下列固体物质溶于水,再将其溶液加热、蒸发结晶,再灼烧,得到化学组成与原固体物质相同的是
①胆矾、②氯化铝、③硫酸铝、④氯化铜、⑤硫酸亚铁、⑥碳酸钠、⑦亚硫酸钠、⑧NH4Cl、⑨KMnO4、⑩Ca(HCO3)2
(3)已知某温度时,Kw=1.0×10-12,Na2CO3溶液的水解常数Kh=2.0×10-3,则当溶液中c(
 )∶c(
)∶c( )=2∶1时,试求该溶液的pH=
)=2∶1时,试求该溶液的pH=(4)下列事实,其中与盐类的水解有关的是
①NaHSO4溶液呈酸性 ②长期使用(NH4)2SO4化肥会使土壤酸性增大,发生板结
③配制CuCl2溶液,用稀盐酸溶解CuCl2固体 ④实验室盛放纯碱溶液的试剂瓶不能用磨口玻璃塞
⑤加热FeCl3·6H2O晶体,往往得不到FeCl3固体
(5)已知:H2CO3:Ka1=4.5×10-7,Ka2=4.7×10-11,NH3·H2O:Kb=1.8×10-5现有常温下0.1 mol·L-1的(NH4)2CO3溶液,该溶液中各微粒浓度之间的关系式错误的是
A.c(
 )+c(H+)=c(
)+c(H+)=c( )+c(OH-)+c(
)+c(OH-)+c( )
)B.c(
 )+c(NH3·H2O)=2c(
)+c(NH3·H2O)=2c( )+2c(
)+2c( )+2c(H2CO3)
)+2c(H2CO3)C.c(
 )+c(
)+c( )+c(H2CO3)=0.1 mol·L-1
)+c(H2CO3)=0.1 mol·L-1 D.c(H+)+c(
 )+c(H2CO3)=c(OH-)+c(NH3·H2O)
)+c(H2CO3)=c(OH-)+c(NH3·H2O)E.c(
 )>c(
)>c( )>c(
)>c( )>c(NH3·H2O)
)>c(NH3·H2O)
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】物质在水中可能存在电离平衡和盐类水解平衡,它们都可以看作化学平衡。根据所学的知识,回答下列问题:
(1)已知25℃时, 的电离常数:
的电离常数: 、
、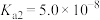 ;
; 的电离常数:
的电离常数: 、
、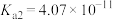 。
。
①该温度下 的水溶液显
的水溶液显_______ (填“酸性”“碱性”或“中性”)。
②若向 溶液中加入少量的
溶液中加入少量的 ,则溶液中
,则溶液中 将
将_______ (填“增大”“减小”或“不变”)。
③足量的 溶液和
溶液和 溶液发生反应的主要离子方程式为
溶液发生反应的主要离子方程式为_______ 。
(2)常温下,向 溶液中滴加
溶液中滴加 的
的 溶液,得到的溶液
溶液,得到的溶液 与
与 溶液体积的关系曲线如图所示。
溶液体积的关系曲线如图所示。
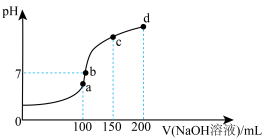
①图中 、
、 、
、 、
、 四个点中水的电离程度最大的是
四个点中水的电离程度最大的是_______ 。
② 点溶液中各离子浓度由大到小的排列顺序是
点溶液中各离子浓度由大到小的排列顺序是_______ 。
(3)25℃时,向含有 的溶液中滴加
的溶液中滴加 氨水后溶液呈中性,则滴加氨水的过程中水的电离平衡将
氨水后溶液呈中性,则滴加氨水的过程中水的电离平衡将_______ (填“正向”“不”或“逆向”)移动,所滴加氨水的浓度为_______  。(25℃时,
。(25℃时, 的电离平衡常数为
的电离平衡常数为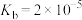 )。
)。
(1)已知25℃时,
 的电离常数:
的电离常数: 、
、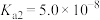 ;
; 的电离常数:
的电离常数: 、
、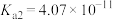 。
。①该温度下
 的水溶液显
的水溶液显②若向
 溶液中加入少量的
溶液中加入少量的 ,则溶液中
,则溶液中 将
将③足量的
 溶液和
溶液和 溶液发生反应的主要离子方程式为
溶液发生反应的主要离子方程式为(2)常温下,向
 溶液中滴加
溶液中滴加 的
的 溶液,得到的溶液
溶液,得到的溶液 与
与 溶液体积的关系曲线如图所示。
溶液体积的关系曲线如图所示。
①图中
 、
、 、
、 、
、 四个点中水的电离程度最大的是
四个点中水的电离程度最大的是②
 点溶液中各离子浓度由大到小的排列顺序是
点溶液中各离子浓度由大到小的排列顺序是(3)25℃时,向含有
 的溶液中滴加
的溶液中滴加 氨水后溶液呈中性,则滴加氨水的过程中水的电离平衡将
氨水后溶液呈中性,则滴加氨水的过程中水的电离平衡将 。(25℃时,
。(25℃时, 的电离平衡常数为
的电离平衡常数为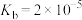 )。
)。
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】碳酸锰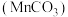 是制造电信器材软磁铁氧体的重要原料。工业上用硫锰矿(主要成分为
是制造电信器材软磁铁氧体的重要原料。工业上用硫锰矿(主要成分为 ,还含少量
,还含少量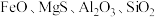 等)制备高纯
等)制备高纯 的流程如下:
的流程如下: 如下表:
如下表:
②室温下, 。回答下列问题:
。回答下列问题:
(1)为了提高硫锰矿在空气中“煅烧”的反应速率,可采取的措施是___________ (任写一种),“尾气”中含有由“煅烧”生成的有害气体的化学式为___________ 。
(2)加入 主要是氧化酸性溶液中的
主要是氧化酸性溶液中的 ,发生反应的离子方程式为
,发生反应的离子方程式为___________ 。
(3)加入氨水调节溶液 为5.0,则溶液中
为5.0,则溶液中
___________ (填“>”“<”或“=”)c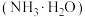 ;溶液中能够完全沉淀的金属离子为
;溶液中能够完全沉淀的金属离子为___________ (填离子符号,金属离子浓度 时,视为沉淀完全)。
时,视为沉淀完全)。
(4)室温下“沉镁”时,离子反应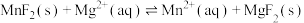 的化学平衡常数
的化学平衡常数
___________ 。
(5)加入 “沉锰”时发生反应的离子方程式为
“沉锰”时发生反应的离子方程式为___________ 。
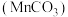 是制造电信器材软磁铁氧体的重要原料。工业上用硫锰矿(主要成分为
是制造电信器材软磁铁氧体的重要原料。工业上用硫锰矿(主要成分为 ,还含少量
,还含少量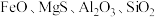 等)制备高纯
等)制备高纯 的流程如下:
的流程如下:
 如下表:
如下表:| 物质 |  |  |  |  |  |
 | 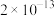 | 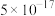 | 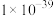 | 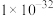 |  |
 。回答下列问题:
。回答下列问题:(1)为了提高硫锰矿在空气中“煅烧”的反应速率,可采取的措施是
(2)加入
 主要是氧化酸性溶液中的
主要是氧化酸性溶液中的 ,发生反应的离子方程式为
,发生反应的离子方程式为(3)加入氨水调节溶液
 为5.0,则溶液中
为5.0,则溶液中
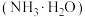 ;溶液中能够完全沉淀的金属离子为
;溶液中能够完全沉淀的金属离子为 时,视为沉淀完全)。
时,视为沉淀完全)。(4)室温下“沉镁”时,离子反应
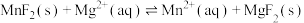 的化学平衡常数
的化学平衡常数
(5)加入
 “沉锰”时发生反应的离子方程式为
“沉锰”时发生反应的离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】一种从钼镍废催化剂(主要含MoS2、NiS、Al2O3、SiO2以及C)中回收镍和钼的工艺流程如下:

回答下列问题:
(1)写出“培烧”时产生的CO2的电子式:_______ 。
(2)“焙烧”时,MoS2首先转化为MoO3,写出该反应的化学方程式:_______ 。
(3)写出滤液中溶质的一种工业用途:_______ ;“净化2”时,发生反应的离子方程式为_______ 。
(4)已知常温下,Ksp(CaMoO4)=1.46×10-8;Ksp(CaCO3)=3.36×10-9,由CaMoO4制备Na2MoO4的方法是_______ 。
(5)已知NiO是不溶于水的碱性氧化物,由浸渣“除铝”所用的试剂是_______ ;“酸溶”得到的溶液制备NiSO4·7H2O的操作方法是_______ 、过滤、洗涤、干燥。
(6)若废催化剂中含160 g MoS2,上,述工艺中获得CaMoO4的质量为190 g,则CaMoO4的产率为_______ 。

回答下列问题:
(1)写出“培烧”时产生的CO2的电子式:
(2)“焙烧”时,MoS2首先转化为MoO3,写出该反应的化学方程式:
(3)写出滤液中溶质的一种工业用途:
(4)已知常温下,Ksp(CaMoO4)=1.46×10-8;Ksp(CaCO3)=3.36×10-9,由CaMoO4制备Na2MoO4的方法是
(5)已知NiO是不溶于水的碱性氧化物,由浸渣“除铝”所用的试剂是
(6)若废催化剂中含160 g MoS2,上,述工艺中获得CaMoO4的质量为190 g,则CaMoO4的产率为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】钛是一种重要的金属,以钛铁矿[主要成分为钛酸亚铁(FeTiO3),还含有少量Fe2O3]为原料制备钛的工艺流程如图所示:
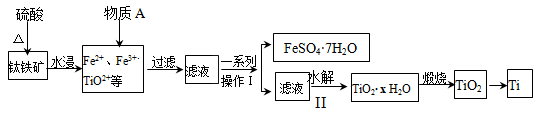
(1)钛铁矿与硫酸反应的化学方程式为___________________________ 。
(2)加入的物质A为_____________ 。
(3)步骤Ⅱ中发生反应的离子方程式为____________________ ;水解过程中需要升高温度,其目的是:①加快反应水解速率 ②______________________________ 。
(4)由TiO2获得金属Ti可用以下两种方法。
①电解法:以石墨为阳极,TiO2为阴极,熔融CaO为电解质,其阴极的电极反应式为________ 。
②热还原法:首先将TiO2、氯气和过量焦炭混合,高温反应生成TiCl4;然后用Mg还原TiCl4即可制取Ti。生成TiCl4的反应中,氧化剂与还原剂的物质的量之比为_______ ;生成Ti的反应需在Ar气氛中,其原因为___________________________ 。

(1)钛铁矿与硫酸反应的化学方程式为
(2)加入的物质A为
(3)步骤Ⅱ中发生反应的离子方程式为
(4)由TiO2获得金属Ti可用以下两种方法。
①电解法:以石墨为阳极,TiO2为阴极,熔融CaO为电解质,其阴极的电极反应式为
②热还原法:首先将TiO2、氯气和过量焦炭混合,高温反应生成TiCl4;然后用Mg还原TiCl4即可制取Ti。生成TiCl4的反应中,氧化剂与还原剂的物质的量之比为
您最近一年使用:0次



