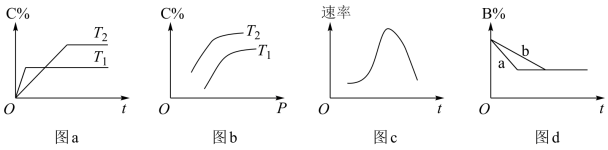
某化学研究小组探究外界条件对化学反应mA(g)+nB(g) pC(g)的速率和平衡的影响,图像如下,下列判断正确的是
pC(g)的速率和平衡的影响,图像如下,下列判断正确的是
 pC(g)的速率和平衡的影响,图像如下,下列判断正确的是
pC(g)的速率和平衡的影响,图像如下,下列判断正确的是
| A.图d中,若m+n=p,则曲线a一定增大了压强 |
| B.图c是绝热条件下速率和时间的图像,由此说明该反应吸热 |
| C.由图b可知,该反应m+n<p |
| D.由图a可知,T1>T2,该反应的逆反应为吸热反应 |
20-21高二上·内蒙古赤峰·阶段练习 查看更多[3]
内蒙古自治区赤峰二中2020-2021学年高二上学期第一次月考化学试题(已下线)练习8 化学平衡的移动-2020-2021学年【补习教材·寒假作业】高二化学(苏教版)广东省深圳市龙华中学2021-2022学年高二上学期第一次考试化学试题
更新时间:2020-10-20 20:02:55
|
相似题推荐
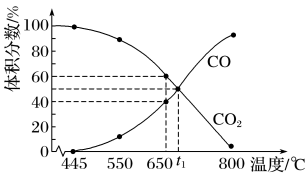
【推荐1】一定量的CO2与足量的C在恒压密闭容器中发生反应:C(s)+CO2(g) 2CO(g) ΔH,若压强为p kPa,平衡时体系中气体体积分数与温度的关系如图所示,下列说法正确的是
2CO(g) ΔH,若压强为p kPa,平衡时体系中气体体积分数与温度的关系如图所示,下列说法正确的是
 2CO(g) ΔH,若压强为p kPa,平衡时体系中气体体积分数与温度的关系如图所示,下列说法正确的是
2CO(g) ΔH,若压强为p kPa,平衡时体系中气体体积分数与温度的关系如图所示,下列说法正确的是
| A.该反应ΔH<0 |
| B.650℃时CO2的平衡转化率为30% |
| C.t1℃时达平衡后若再充入等物质的量的CO和CO2气体,则平衡向逆向移动 |
| D.若密闭容器中混合气体密度不再变化时,该反应处于平衡状态 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】对于反应:C(S) + H2O(g) CO(g) + H2(g) △H>0,为了提高C(S)的转化率,可采取的措施是
CO(g) + H2(g) △H>0,为了提高C(S)的转化率,可采取的措施是
 CO(g) + H2(g) △H>0,为了提高C(S)的转化率,可采取的措施是
CO(g) + H2(g) △H>0,为了提高C(S)的转化率,可采取的措施是| A.升高反应温度 | B.降低反应温度 |
| C.增大压强 | D.再加入一些C(S) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】下列实验事实不能用平衡移动原理解释的是
| A.升高温度水的离子积增大 | B.镁条与氯化铵溶液反应生成氢气 |
| C.制备 H2 时用粗锌比纯锌的速率快 | D.压缩 NO2 的体积,气体的颜色先加深后逐渐变浅 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】有反应CO(g)+H2O(g) CO2(g)+H2(g) ΔH<0,在其他条件不变的情况下
CO2(g)+H2(g) ΔH<0,在其他条件不变的情况下
 CO2(g)+H2(g) ΔH<0,在其他条件不变的情况下
CO2(g)+H2(g) ΔH<0,在其他条件不变的情况下| A.加入催化剂,改变了反应的途径,反应的ΔH也随之改变 |
| B.改变压强,平衡不发生移动,反应放出的热量不变 |
| C.升高温度,反应速率加快,反应放出的热量不变 |
| D.增大反应物浓度,反应的ΔH也随之改变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】甲醇脱氢可制取甲醛,反应原理为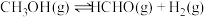 ,甲醇的平衡转化率随温度的变化曲线如图所示(已知反应在1L的密闭容器中进行,甲醇的初始物质的量为1mol)。下列有关说法正确的是
,甲醇的平衡转化率随温度的变化曲线如图所示(已知反应在1L的密闭容器中进行,甲醇的初始物质的量为1mol)。下列有关说法正确的是

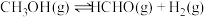 ,甲醇的平衡转化率随温度的变化曲线如图所示(已知反应在1L的密闭容器中进行,甲醇的初始物质的量为1mol)。下列有关说法正确的是
,甲醇的平衡转化率随温度的变化曲线如图所示(已知反应在1L的密闭容器中进行,甲醇的初始物质的量为1mol)。下列有关说法正确的是
A.脱氢反应的 |
B.600K时,Y点: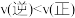 |
| C.要实现从Y点到Z点的变化可通过增大压强的方法 |
D.在 时,该反应的平衡常数为8.1 时,该反应的平衡常数为8.1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】工业上利用焦炭与水蒸气生产H2的反应原理为C(s)+H2O(g)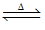 CO(g)+H2(g) ΔH>0;CO(g)+H2O(g)
CO(g)+H2(g) ΔH>0;CO(g)+H2O(g)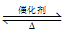 CO2(g)+H2(g) ΔH<0;第二步生产的原料CO来源于第一步的产物。为提高原料的利用率及H2的日产量,下列措施中不可取的是( )
CO2(g)+H2(g) ΔH<0;第二步生产的原料CO来源于第一步的产物。为提高原料的利用率及H2的日产量,下列措施中不可取的是( )
①第一步产生的混合气直接作为第二步的反应物
②第二步生产应采用适当的温度和催化剂
③第一、二步生产中均充入足量水蒸气
④第二步应在低温下进行
⑤第二步生产采用高压
⑥第二步生产中增大CO的浓度
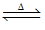 CO(g)+H2(g) ΔH>0;CO(g)+H2O(g)
CO(g)+H2(g) ΔH>0;CO(g)+H2O(g)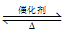 CO2(g)+H2(g) ΔH<0;第二步生产的原料CO来源于第一步的产物。为提高原料的利用率及H2的日产量,下列措施中不可取的是( )
CO2(g)+H2(g) ΔH<0;第二步生产的原料CO来源于第一步的产物。为提高原料的利用率及H2的日产量,下列措施中不可取的是( )①第一步产生的混合气直接作为第二步的反应物
②第二步生产应采用适当的温度和催化剂
③第一、二步生产中均充入足量水蒸气
④第二步应在低温下进行
⑤第二步生产采用高压
⑥第二步生产中增大CO的浓度
| A.①③⑤ | B.②④⑥ |
| C.②③⑤ | D.①④⑤⑥ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列图示与对应的叙述相符的是


A.图一表示反应:mA(s)+nB(g)  pC(g) △H>O,在一定温度下,平衡时B的体积分数(B%)与压强变化的关系如图所示,反应速率x点比y点时的慢 pC(g) △H>O,在一定温度下,平衡时B的体积分数(B%)与压强变化的关系如图所示,反应速率x点比y点时的慢 |
B.图二是可逆反应:A(g)+B(s)  C(s)+D(g) △H>O的速率时间图象,在t1时刻改变条件一定是加入催化剂 C(s)+D(g) △H>O的速率时间图象,在t1时刻改变条件一定是加入催化剂 |
C.图三表示对于化学反应mA(g)+nB(g)  pC(g)+qD(g),A的百分含量与温度(T)的变化情况,则该反应的ΔH>0 pC(g)+qD(g),A的百分含量与温度(T)的变化情况,则该反应的ΔH>0 |
| D.图四所示图中的阴影部分面积的含义是(v正-v逆) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】一定温度下,将1 mol气体A和1 mol气体B充入2 L某密闭容器中,发生反应: ,
, 时达到平衡。在
时达到平衡。在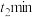 、
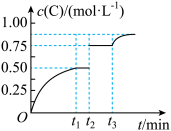
、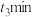 时刻分别改变反应的一个条件,测得容器中气体C的浓度随时间变化的曲线如图所示。下列说法正确的是
时刻分别改变反应的一个条件,测得容器中气体C的浓度随时间变化的曲线如图所示。下列说法正确的是
 ,
, 时达到平衡。在
时达到平衡。在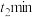 、
、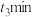 时刻分别改变反应的一个条件,测得容器中气体C的浓度随时间变化的曲线如图所示。下列说法正确的是
时刻分别改变反应的一个条件,测得容器中气体C的浓度随时间变化的曲线如图所示。下列说法正确的是
A.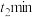 时改变的条件是使用催化剂 时改变的条件是使用催化剂 |
B.反应的化学方程式中, |
C.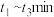 间该反应的平衡常数均为5 间该反应的平衡常数均为5 |
D. 时改变的条件是移去少量物质D 时改变的条件是移去少量物质D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】已知某可逆反应aA(g) +bB(g)⇌pC(g) +qD(g) ΔH=Q kJ·mol-1,生成物C的物质的量百分数与时间的关系如图所示,下列判断正确的是
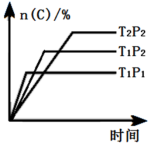

| A.T1>T2 Q>0 | B.T1<T2 Q<0 |
| C.P1>P2 a+b<p+q | D.P1<P2 a+b>p+q |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】在 ℃,
℃, 下,向1L的密闭容器中充入1mol
下,向1L的密闭容器中充入1mol 和一定物质的量的
和一定物质的量的 发生反应:
发生反应: ,平衡时
,平衡时 的物质的量分数与初始投料比
的物质的量分数与初始投料比 的关系如图所示。下列说法错误的是
的关系如图所示。下列说法错误的是
 ℃,
℃, 下,向1L的密闭容器中充入1mol
下,向1L的密闭容器中充入1mol 和一定物质的量的
和一定物质的量的 发生反应:
发生反应: ,平衡时
,平衡时 的物质的量分数与初始投料比
的物质的量分数与初始投料比 的关系如图所示。下列说法错误的是
的关系如图所示。下列说法错误的是
A.随着 的增大, 的增大, 的转化率逐渐增大 的转化率逐渐增大 |
B.e点: |
C.a点时,该反应的平衡常数为 |
D.a点,平衡后再投入1mol 和1mol 和1mol ,达到新平衡时, ,达到新平衡时,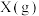 的产率增大 的产率增大 |
您最近一年使用:0次


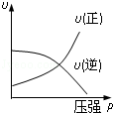


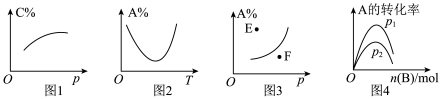
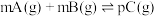 中平衡时C的百分含量与压强的关系,说明m+n>p
中平衡时C的百分含量与压强的关系,说明m+n>p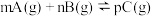 ,当其他条件一定时A的百分含量随压强变化的图像,其中E点v正>v逆
,当其他条件一定时A的百分含量随压强变化的图像,其中E点v正>v逆 在一定条件下,向含有一定量A的容器中逐渐加入B时的图像,压强p1>p2
在一定条件下,向含有一定量A的容器中逐渐加入B时的图像,压强p1>p2

