CO2和CH4是两种重要的温室气体,通过CH4和CO2反应制造更高价值的化学品是目前的研究方向。
(1)已知:CH4(g) + 2O2(g)=CO2(g) + 2H2O(g) ΔH1=akJ·mol−1
CO(g) + H2O (g)=CO2(g) + H2(g) ΔH2=bkJ·mol−1
2CO(g) + O2(g)=2CO2(g) ΔH3=ckJ·mol−1
反应CO2(g) + CH4(g)=2CO(g) + 2H2(g) 的ΔH=__ kJ·mol−1。
(2)以二氧化钛表面覆盖Cu2Al2O4为催化剂,可以将CO2和CH4直接转化成乙酸。
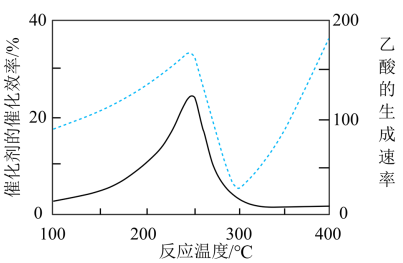
①在不同温度下,催化剂的催化效率与乙酸的生成速率如图所示。250~300℃时,温度升高而乙酸的生成速率降低的原因可能是___ 。
②为了提高该反应中CH4的转化率,可以采取的措施是___ 。
(3)以CO2为原料可以合成多种物质。
①利用FeO吸收CO2的化学方程式为:6FeO + CO2=2Fe3O4 + C,则反应中每生成1 mol Fe3O4,转移电子的物质的量为___ mol。
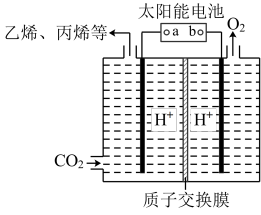
②以稀硫酸为电解质溶液,利用太阳能将CO2转化为低碳烯烃,工作原理如图所示,b是电源的________ (填“正极”或“负极”),写出生成丙烯的电极反应式___ 。
(1)已知:CH4(g) + 2O2(g)=CO2(g) + 2H2O(g) ΔH1=akJ·mol−1
CO(g) + H2O (g)=CO2(g) + H2(g) ΔH2=bkJ·mol−1
2CO(g) + O2(g)=2CO2(g) ΔH3=ckJ·mol−1
反应CO2(g) + CH4(g)=2CO(g) + 2H2(g) 的ΔH=
(2)以二氧化钛表面覆盖Cu2Al2O4为催化剂,可以将CO2和CH4直接转化成乙酸。

①在不同温度下,催化剂的催化效率与乙酸的生成速率如图所示。250~300℃时,温度升高而乙酸的生成速率降低的原因可能是
②为了提高该反应中CH4的转化率,可以采取的措施是
(3)以CO2为原料可以合成多种物质。
①利用FeO吸收CO2的化学方程式为:6FeO + CO2=2Fe3O4 + C,则反应中每生成1 mol Fe3O4,转移电子的物质的量为
②以稀硫酸为电解质溶液,利用太阳能将CO2转化为低碳烯烃,工作原理如图所示,b是电源的

更新时间:2020-11-24 18:53:10
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
【推荐1】将烟气中的 选择性还原为单质硫是一种具有经济效益和社会效益的脱硫方法。
选择性还原为单质硫是一种具有经济效益和社会效益的脱硫方法。
Ⅰ.氢气还原法: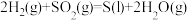
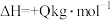 ……反应a
……反应a
(1)下图中曲线表示了反应a在有、无催化剂条件下反应过程中体系的能量变化。

①曲线_______ (填“m”或“n”)表示的是有催化剂参与的过程;
②图中括号内应该填写_______ 。
(2)已知:ⅰ.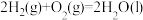

ⅱ.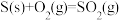

ⅲ._______ 
利用 、
、 、
、 可计算出反应a的焓变。将过程ⅲ补写完整。
可计算出反应a的焓变。将过程ⅲ补写完整。
Ⅱ.一氧化碳还原法: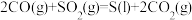
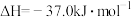 ……反应b
……反应b
(3)向恒温恒容密闭容器中充入一定量的 和
和 ,发生反应b。下列描述可判断该反应达到平衡状态的是
,发生反应b。下列描述可判断该反应达到平衡状态的是_______ 。
A.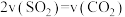
B. 气体的浓度不再变化
气体的浓度不再变化
C.容器内的总压强不再变化
D.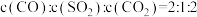
E.混合气体的密度不再变化
(4)某温度时,向2L的密闭容器中充入
 和
和
 ,发生反应b,
,发生反应b, 时反应达平衡状态,测得
时反应达平衡状态,测得 的平衡转化率为80%。
的平衡转化率为80%。
①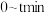 内,
内,
_______  (用含t的代数式表示);
(用含t的代数式表示);
②该温度下,反应b的平衡常数
_______  ;
;
③ 后,向该密闭容器中再充入
后,向该密闭容器中再充入
 和
和
 ,此时v正
,此时v正_______ v逆(填“>”、“<”或“=”)。
(5)向两个密闭容器中分别充入
 和
和
 ,发生反应b,在不同的温度和压强下(物质状态未发生改变),
,发生反应b,在不同的温度和压强下(物质状态未发生改变), 的平衡转化率(
的平衡转化率( )如下表所示,其中
)如下表所示,其中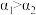 ,则
,则
_______  (填“>”、“<”或“=”),判断的理由是
(填“>”、“<”或“=”),判断的理由是_______ 。
Ⅲ.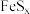 化水煤气(
化水煤气( 、
、 )还原
)还原
(6)该方法的部分反应过程如图所示。下列说法合理的是_______ 。

A. 和
和 为中间产物
为中间产物
B.可能存在反应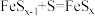
C.生成S的所有反应中,S均为还原产物
D.寻找更高效催化剂可提高S单质平衡回收率
 选择性还原为单质硫是一种具有经济效益和社会效益的脱硫方法。
选择性还原为单质硫是一种具有经济效益和社会效益的脱硫方法。Ⅰ.氢气还原法:
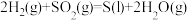
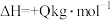 ……反应a
……反应a(1)下图中曲线表示了反应a在有、无催化剂条件下反应过程中体系的能量变化。

①曲线
②图中括号内应该填写
(2)已知:ⅰ.
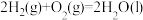

ⅱ.
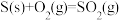

ⅲ.

利用
 、
、 、
、 可计算出反应a的焓变。将过程ⅲ补写完整。
可计算出反应a的焓变。将过程ⅲ补写完整。Ⅱ.一氧化碳还原法:
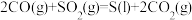
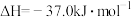 ……反应b
……反应b(3)向恒温恒容密闭容器中充入一定量的
 和
和 ,发生反应b。下列描述可判断该反应达到平衡状态的是
,发生反应b。下列描述可判断该反应达到平衡状态的是A.
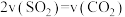
B.
 气体的浓度不再变化
气体的浓度不再变化C.容器内的总压强不再变化
D.
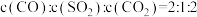
E.混合气体的密度不再变化
(4)某温度时,向2L的密闭容器中充入

 和
和
 ,发生反应b,
,发生反应b, 时反应达平衡状态,测得
时反应达平衡状态,测得 的平衡转化率为80%。
的平衡转化率为80%。①
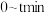 内,
内,
 (用含t的代数式表示);
(用含t的代数式表示);②该温度下,反应b的平衡常数

 ;
;③
 后,向该密闭容器中再充入
后,向该密闭容器中再充入
 和
和
 ,此时v正
,此时v正(5)向两个密闭容器中分别充入

 和
和
 ,发生反应b,在不同的温度和压强下(物质状态未发生改变),
,发生反应b,在不同的温度和压强下(物质状态未发生改变), 的平衡转化率(
的平衡转化率( )如下表所示,其中
)如下表所示,其中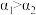 ,则
,则
 (填“>”、“<”或“=”),判断的理由是
(填“>”、“<”或“=”),判断的理由是| 压强/MPa | P | 2P |
| 温度/℃ |  |  |
 的平衡转化率 的平衡转化率 /% /% | 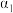 | 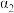 |
Ⅲ.
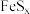 化水煤气(
化水煤气( 、
、 )还原
)还原
(6)该方法的部分反应过程如图所示。下列说法合理的是

A.
 和
和 为中间产物
为中间产物B.可能存在反应
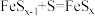
C.生成S的所有反应中,S均为还原产物
D.寻找更高效催化剂可提高S单质平衡回收率
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】氮氧化物是目前的主要空气污染物之一,它的转化和综合利用既有利于节约资源,又有利于保护环境。
(1) 的消除。可以用碳酸钠溶液来进行吸收,在产生
的消除。可以用碳酸钠溶液来进行吸收,在产生 的同时,会生成
的同时,会生成 ,
, 是工业盐的主要成分,在漂白、电镀等方面应用广泛。
是工业盐的主要成分,在漂白、电镀等方面应用广泛。
①写出碳酸钠溶液消除 的化学方程式:
的化学方程式:________________ 。
②写出两种能提高 消除率的措施:
消除率的措施:________________ 。
③经过一系列后续操作可以得到产品 ,但一般会混有一定量
,但一般会混有一定量________ 的杂质。
(2) 的消除。空气中
的消除。空气中 主要来自于汽车尾气的排放和硝酸工厂废气的排放,利用强氧化剂过硫酸钠(
主要来自于汽车尾气的排放和硝酸工厂废气的排放,利用强氧化剂过硫酸钠( )氧化脱除
)氧化脱除 可以消除污染,其流程如下:
可以消除污染,其流程如下:

①反应1的离子方程式为________________ 。
②反应2中 的初始浓度为
的初始浓度为 ,反应为
,反应为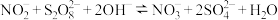 。不同温度下,达到平衡时
。不同温度下,达到平衡时 的脱除率与过硫酸钠(
的脱除率与过硫酸钠( )初始浓度的关系如下图所示。
)初始浓度的关系如下图所示。
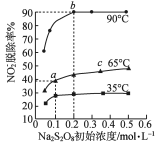
图中点a和点b的平衡常数K的大小关系为________________ 。判断依据是________________ 。
(1)
 的消除。可以用碳酸钠溶液来进行吸收,在产生
的消除。可以用碳酸钠溶液来进行吸收,在产生 的同时,会生成
的同时,会生成 ,
, 是工业盐的主要成分,在漂白、电镀等方面应用广泛。
是工业盐的主要成分,在漂白、电镀等方面应用广泛。①写出碳酸钠溶液消除
 的化学方程式:
的化学方程式:②写出两种能提高
 消除率的措施:
消除率的措施:③经过一系列后续操作可以得到产品
 ,但一般会混有一定量
,但一般会混有一定量(2)
 的消除。空气中
的消除。空气中 主要来自于汽车尾气的排放和硝酸工厂废气的排放,利用强氧化剂过硫酸钠(
主要来自于汽车尾气的排放和硝酸工厂废气的排放,利用强氧化剂过硫酸钠( )氧化脱除
)氧化脱除 可以消除污染,其流程如下:
可以消除污染,其流程如下:
①反应1的离子方程式为
②反应2中
 的初始浓度为
的初始浓度为 ,反应为
,反应为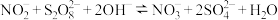 。不同温度下,达到平衡时
。不同温度下,达到平衡时 的脱除率与过硫酸钠(
的脱除率与过硫酸钠( )初始浓度的关系如下图所示。
)初始浓度的关系如下图所示。
图中点a和点b的平衡常数K的大小关系为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】肼( )常用于火箭或原电池的燃料。已知:
)常用于火箭或原电池的燃料。已知:
①N2(g)+2O2(g)=2NO2(g) ∆H= + 67.7kJ/mol
② ∆H= - 534kJ/mol
∆H= - 534kJ/mol
③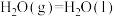 ∆H= - 44kJ/mol
∆H= - 44kJ/mol
回答下列问题:
(1)反应2N2H4(g)+2NO2(g)=3N2(g)+4H2O(l) ∆H=_______ kJ/mol
(2)一定温度下,将N2H4与NO2以体积比1:1置于10L密闭容器中发生上述反应2N2H4(g)+2NO2(g)=3N2(g)+4H2O(l),下列选项不能说明反应达到平衡状态的是_______
a.混合气体密度保持不变 b.混合气体颜色保持不变
c. 与
与 体积之比保持不变 d.体系压强保持不变
体积之比保持不变 d.体系压强保持不变
(3)下列示意图能正确表示反应①过程中能量变化的是_______。

(4)为了提高燃料的利用率以惰性材料作电极将反应②设计为燃料电池,并用以此为电源进行电解实验,装置如图所示,回答相关问题。

①写出甲池中通入N2H4一极的电极反应式_______ ;工作一段时间后,KOH溶液的pH将_______ 。(填“增大”,“减小”或“不变”)
②乙池中若X电极材料为石墨,Y为Fe,电解液A为饱和NaCl溶液,则X极上的电极反应式为_______ ;一段时间后电解质溶液中出现白色沉淀;当Y(Fe)极的质量减少5.60g时,甲池中理论上消耗O2_______ mL。(标准状况)
 )常用于火箭或原电池的燃料。已知:
)常用于火箭或原电池的燃料。已知:①N2(g)+2O2(g)=2NO2(g) ∆H= + 67.7kJ/mol
②
 ∆H= - 534kJ/mol
∆H= - 534kJ/mol③
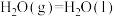 ∆H= - 44kJ/mol
∆H= - 44kJ/mol回答下列问题:
(1)反应2N2H4(g)+2NO2(g)=3N2(g)+4H2O(l) ∆H=
(2)一定温度下,将N2H4与NO2以体积比1:1置于10L密闭容器中发生上述反应2N2H4(g)+2NO2(g)=3N2(g)+4H2O(l),下列选项不能说明反应达到平衡状态的是
a.混合气体密度保持不变 b.混合气体颜色保持不变
c.
 与
与 体积之比保持不变 d.体系压强保持不变
体积之比保持不变 d.体系压强保持不变(3)下列示意图能正确表示反应①过程中能量变化的是_______。

(4)为了提高燃料的利用率以惰性材料作电极将反应②设计为燃料电池,并用以此为电源进行电解实验,装置如图所示,回答相关问题。

①写出甲池中通入N2H4一极的电极反应式
②乙池中若X电极材料为石墨,Y为Fe,电解液A为饱和NaCl溶液,则X极上的电极反应式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】Ⅰ.铁及铁的氧化物广泛应于生产、生活、航天、科研领域。
(1)铁的氧化物循环分解水制H2
已知:H2O(l)=H2(g)+1/2 O2(g) ΔH1=a kJ•mol-1
6FeO(s)+O2(g)=2Fe3O4(s) ΔH2=b kJ•mol-1
则:3FeO(s)+H2O(l)=H2(g)+Fe3O4(s) ΔH3=_______
(2)Fe2O3与CH4反应可制备“纳米级”金属铁。已知,恒温恒容时,加入Fe2O3与CH4发生反应:3CH4(g)+Fe2O3(s)⇌2Fe(s)+6H2(g)+3CO(g)
①此反应的化学平衡常数表达式为_______
②下列条件能判断该反应达到平衡状态的是_______
a.消耗1molFe2O3的同时,消耗3molCO
b.容器内气体的颜色不再改变
c.容器内压强不再改变
d.v正(CH4)=2v逆(H2)
Ⅱ.用CH4还原NO2的反应为CH4(g)+2NO2(g)⇌N2(g)+CO2(g)+2H2O(g),向两个容积均为2L温度分别为T1、T2的恒温恒容密闭容器中分别加入1mol CH4和2mol NO2,测得各容器中n(NO2)随反应时间t的变化如图所示:
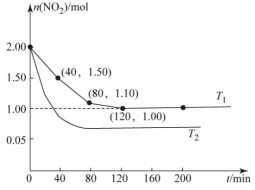
①T1_______ T2(填“>”或“<”)。
②T1时,40~80 min内,用N2的浓度变化表示的平均反应速率为v(N2)=_______
③T1下,200 min时,向容器中再加入CH4、NO2和H2O(g)各l mol,化学平衡_______ 移动(填“正向”“逆向”或“不”)。
Ⅲ.CaSO4微溶于水和酸,可加入氢氧化钠并通入CO2使其转化为CaCO3,然后加酸浸泡除去,反应的离子方程式为CaSO4+CO =CaCO3+SO
=CaCO3+SO ,室温下,该反应的化学平衡常数为
,室温下,该反应的化学平衡常数为_______ (室温下,Ksp(CaCO3)=3×10-9,Ksp(CaSO4)=9×10-6)。
(1)铁的氧化物循环分解水制H2
已知:H2O(l)=H2(g)+1/2 O2(g) ΔH1=a kJ•mol-1
6FeO(s)+O2(g)=2Fe3O4(s) ΔH2=b kJ•mol-1
则:3FeO(s)+H2O(l)=H2(g)+Fe3O4(s) ΔH3=
(2)Fe2O3与CH4反应可制备“纳米级”金属铁。已知,恒温恒容时,加入Fe2O3与CH4发生反应:3CH4(g)+Fe2O3(s)⇌2Fe(s)+6H2(g)+3CO(g)
①此反应的化学平衡常数表达式为
②下列条件能判断该反应达到平衡状态的是
a.消耗1molFe2O3的同时,消耗3molCO
b.容器内气体的颜色不再改变
c.容器内压强不再改变
d.v正(CH4)=2v逆(H2)
Ⅱ.用CH4还原NO2的反应为CH4(g)+2NO2(g)⇌N2(g)+CO2(g)+2H2O(g),向两个容积均为2L温度分别为T1、T2的恒温恒容密闭容器中分别加入1mol CH4和2mol NO2,测得各容器中n(NO2)随反应时间t的变化如图所示:

①T1
②T1时,40~80 min内,用N2的浓度变化表示的平均反应速率为v(N2)=
③T1下,200 min时,向容器中再加入CH4、NO2和H2O(g)各l mol,化学平衡
Ⅲ.CaSO4微溶于水和酸,可加入氢氧化钠并通入CO2使其转化为CaCO3,然后加酸浸泡除去,反应的离子方程式为CaSO4+CO
 =CaCO3+SO
=CaCO3+SO ,室温下,该反应的化学平衡常数为
,室温下,该反应的化学平衡常数为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】氮氧化物是形成酸雨、水体富营养化、光化学烟雾等环境问题的主要原因。
已知:反应Ⅰ.2NO(g)+O2(g) 2NO2(g) ΔH1=-112 kJ/mol;
2NO2(g) ΔH1=-112 kJ/mol;
反应Ⅱ.2NO2(g) N2O4(g) ΔH2=-24.2 kJ/mol;
N2O4(g) ΔH2=-24.2 kJ/mol;
反应Ⅲ.3O2(g) 2O3(g) ΔH3=+144.6 kJ/mol;
2O3(g) ΔH3=+144.6 kJ/mol;
(1)大气层中O3氧化NO的热化学方程式为3NO(g)+O3(g) 3NO2(g) ΔH4=
3NO2(g) ΔH4=________ 。
(2)某温度下,向1L刚性容器中投入1mol O2发生反应Ⅲ,5min时压强变为原来的0.9倍后不再变化。
①5min内O3的生成速率v(O3)=______________________ 。
②平衡时O2的转化率α(O2)________ 30%(填“>”“=”或“<”)。
(3)常温下,向压强为pkPa的恒压容器中充入2molNO和1molO2,发生反应Ⅰ和反应Ⅱ。平衡时NO和NO2的物质的量分别为0.2mol和1mol,则常温下反应Ⅱ的平衡常数Kp=____________ kPa-1(已知气体中某成分的分压p(分)=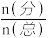 ×p(总),用含p的式子表示)。
×p(总),用含p的式子表示)。
(4)工业上常用氨气去除一氧化氮的污染,反应原理为:4NH3(g)+6NO(g) 5N2(g)+6H2O(g)。测得该反应的平衡常数与温度的关系为:lg Kp=5.0+
5N2(g)+6H2O(g)。测得该反应的平衡常数与温度的关系为:lg Kp=5.0+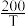 (T为开氏温度)。
(T为开氏温度)。
①该反应ΔH_______________ 0(填“>”“=”或“<”)。
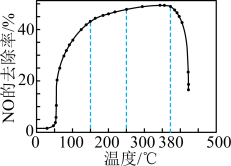
②一定温度下,按进料比n(NH3)∶n(NO)=1∶1,匀速通入装有锰、镁氧化物作催化剂的反应器中反应。反应相同时间,NO的去除率随反应温度的变化曲线如上图。NO的去除率先迅速上升后上升缓慢的主要原因是______________________ ;当反应温度高于380 ℃时,NO的去除率迅速下降的原因可能是____________________ 。
已知:反应Ⅰ.2NO(g)+O2(g)
 2NO2(g) ΔH1=-112 kJ/mol;
2NO2(g) ΔH1=-112 kJ/mol;反应Ⅱ.2NO2(g)
 N2O4(g) ΔH2=-24.2 kJ/mol;
N2O4(g) ΔH2=-24.2 kJ/mol;反应Ⅲ.3O2(g)
 2O3(g) ΔH3=+144.6 kJ/mol;
2O3(g) ΔH3=+144.6 kJ/mol;(1)大气层中O3氧化NO的热化学方程式为3NO(g)+O3(g)
 3NO2(g) ΔH4=
3NO2(g) ΔH4=(2)某温度下,向1L刚性容器中投入1mol O2发生反应Ⅲ,5min时压强变为原来的0.9倍后不再变化。
①5min内O3的生成速率v(O3)=
②平衡时O2的转化率α(O2)
(3)常温下,向压强为pkPa的恒压容器中充入2molNO和1molO2,发生反应Ⅰ和反应Ⅱ。平衡时NO和NO2的物质的量分别为0.2mol和1mol,则常温下反应Ⅱ的平衡常数Kp=
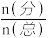 ×p(总),用含p的式子表示)。
×p(总),用含p的式子表示)。(4)工业上常用氨气去除一氧化氮的污染,反应原理为:4NH3(g)+6NO(g)
 5N2(g)+6H2O(g)。测得该反应的平衡常数与温度的关系为:lg Kp=5.0+
5N2(g)+6H2O(g)。测得该反应的平衡常数与温度的关系为:lg Kp=5.0+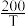 (T为开氏温度)。
(T为开氏温度)。①该反应ΔH

②一定温度下,按进料比n(NH3)∶n(NO)=1∶1,匀速通入装有锰、镁氧化物作催化剂的反应器中反应。反应相同时间,NO的去除率随反应温度的变化曲线如上图。NO的去除率先迅速上升后上升缓慢的主要原因是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】碳排放进入平台期后,进入平稳下降阶段称为“碳达峰”,与“碳中和”一起,简称“双碳”。以CO2为原料合成CH3OH依然是“双碳”环境下的科研热点,相关反应如下:
主反应:
 ;
;
副反应1:
 ;
;
副反应2:
 。
。
回答下列问题:
(1)部分键能的数据如下表所示,则主反应的
___________ ;
___________ (填“>”或“<”)0,原因为___________ 。
(2)化合物M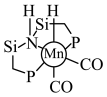 [
[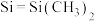 ,
,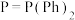 ,Ph代表苯基]可作为CO2合成甲醇的催化剂。化合物M使反应
,Ph代表苯基]可作为CO2合成甲醇的催化剂。化合物M使反应 的速率大大提高,对其逆反应活化能的影响为
的速率大大提高,对其逆反应活化能的影响为___________ 。
(3)某工厂控制条件,建立了存在上述主反应和副反应1的体系,保持其他条件不变,测定温度对合成甲醇过程的影响所得曲线如图1、图2所示(甲醇选择性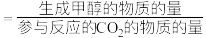 ,CO2转化率在指定时间段内测得),结合图1曲线变化趋势分析图2中温度对甲醇产率的影响:
,CO2转化率在指定时间段内测得),结合图1曲线变化趋势分析图2中温度对甲醇产率的影响:___________ ,242℃时甲醇产率为___________ %(保留三位有效数字)。 ,
, ,达到平衡时CH3OH产率为50%,总压强为p kPa,
,达到平衡时CH3OH产率为50%,总压强为p kPa, ,主反应的平衡常数
,主反应的平衡常数
___________ (保留两位有效数字);达到平衡用时5 min,则0~5 min内,用CH3OH分压表示的平均反应速率为___________ 。
主反应:

 ;
;副反应1:

 ;
;副反应2:

 。
。回答下列问题:
(1)部分键能的数据如下表所示,则主反应的


| 共价键 | H-H | C=O | C-H | C-O | O-H |
键能/( ) ) | 436 | 803 | 414 | 326 | 464 |
(2)化合物M
 [
[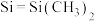 ,
,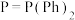 ,Ph代表苯基]可作为CO2合成甲醇的催化剂。化合物M使反应
,Ph代表苯基]可作为CO2合成甲醇的催化剂。化合物M使反应 的速率大大提高,对其逆反应活化能的影响为
的速率大大提高,对其逆反应活化能的影响为(3)某工厂控制条件,建立了存在上述主反应和副反应1的体系,保持其他条件不变,测定温度对合成甲醇过程的影响所得曲线如图1、图2所示(甲醇选择性
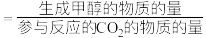 ,CO2转化率在指定时间段内测得),结合图1曲线变化趋势分析图2中温度对甲醇产率的影响:
,CO2转化率在指定时间段内测得),结合图1曲线变化趋势分析图2中温度对甲醇产率的影响: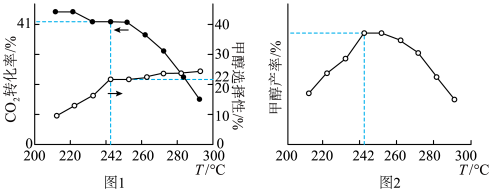
 ,
, ,达到平衡时CH3OH产率为50%,总压强为p kPa,
,达到平衡时CH3OH产率为50%,总压强为p kPa, ,主反应的平衡常数
,主反应的平衡常数
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】雾霾主要成分为灰尘、 、
、 、有机碳氢化合物等粒子。烟气脱硝是治理雾霾的方法之一。
、有机碳氢化合物等粒子。烟气脱硝是治理雾霾的方法之一。
(1)以氨气为脱硝剂时,可将 还原为
还原为 。
。
已知:
ⅰ.
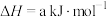
ⅱ.
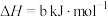
则反应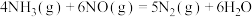 的
的
_______  。
。
(2)臭氧也是理想的烟气脱硝剂,其脱硝反应之一为: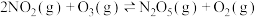
 。某温度时,在体积为1L的刚性密闭容器中充入2mol
。某温度时,在体积为1L的刚性密闭容器中充入2mol  和1mol
和1mol  发生反应。
发生反应。
①在恒温恒容条件下,下列事实能够证明该反应已经达到平衡的是_______ (填标号)。
A. 的消耗速率与
的消耗速率与 的消耗速率相等 B.混合气体压强不再改变
的消耗速率相等 B.混合气体压强不再改变
C.混合气体的平均相对分子质量保持不变 D. 与
与 的物质的量浓度相等
的物质的量浓度相等
②欲增加 的平衡转化率,可采取的措施有
的平衡转化率,可采取的措施有_______ (填标号)。
A.充入氦气 B.升高温度
C.充入2mol D.充入2mol
D.充入2mol  和1mol
和1mol 
③达到平衡时,混合气体总压为p, 的浓度为0.5
的浓度为0.5 ,则
,则 的转化率为
的转化率为_______ ,平衡常数
_______ (以分压表示,分压=总压×物质的量分数)。
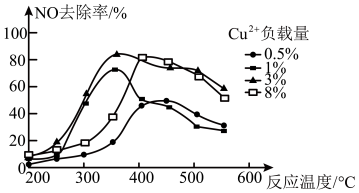
(3)乙烯也可用于烟气脱硝。为研究温度、催化剂中 负载量对NO去除率的影响,控制其它条件一定,实验结果如图所示。为达到最高的NO去除率,应选择的反应温度约为
负载量对NO去除率的影响,控制其它条件一定,实验结果如图所示。为达到最高的NO去除率,应选择的反应温度约为_______ , 负载量为
负载量为_______ 。
 、
、 、有机碳氢化合物等粒子。烟气脱硝是治理雾霾的方法之一。
、有机碳氢化合物等粒子。烟气脱硝是治理雾霾的方法之一。(1)以氨气为脱硝剂时,可将
 还原为
还原为 。
。已知:
ⅰ.

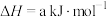
ⅱ.

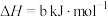
则反应
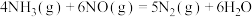 的
的
 。
。(2)臭氧也是理想的烟气脱硝剂,其脱硝反应之一为:
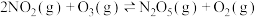
 。某温度时,在体积为1L的刚性密闭容器中充入2mol
。某温度时,在体积为1L的刚性密闭容器中充入2mol  和1mol
和1mol  发生反应。
发生反应。①在恒温恒容条件下,下列事实能够证明该反应已经达到平衡的是
A.
 的消耗速率与
的消耗速率与 的消耗速率相等 B.混合气体压强不再改变
的消耗速率相等 B.混合气体压强不再改变C.混合气体的平均相对分子质量保持不变 D.
 与
与 的物质的量浓度相等
的物质的量浓度相等②欲增加
 的平衡转化率,可采取的措施有
的平衡转化率,可采取的措施有A.充入氦气 B.升高温度
C.充入2mol
 D.充入2mol
D.充入2mol  和1mol
和1mol 
③达到平衡时,混合气体总压为p,
 的浓度为0.5
的浓度为0.5 ,则
,则 的转化率为
的转化率为
(3)乙烯也可用于烟气脱硝。为研究温度、催化剂中
 负载量对NO去除率的影响,控制其它条件一定,实验结果如图所示。为达到最高的NO去除率,应选择的反应温度约为
负载量对NO去除率的影响,控制其它条件一定,实验结果如图所示。为达到最高的NO去除率,应选择的反应温度约为 负载量为
负载量为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】乙酸制氢具有重要意义,发生的反应如下:
热裂解反应:CH3COOH(g)=2CO(g)+2H2(g) ΔH=+213.7 kJ·mol-1
脱羧基反应:CH3COOH(g)=CH4(g)+CO2(g) ΔH=-33.5 kJ·mol-1
(1)请写出CO与H2反应生成甲烷的热化学方程式:___________ 。
(2)在密闭容器中,利用乙酸制氢,选择的压强为___________ (填“高压”或“常压”)。其中温度与气体产率的关系如图:
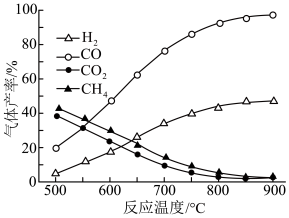
①约650 ℃之前,脱羧基反应活化能低,速率快,故氢气产率低于甲烷;650 ℃之后氢气产率高于甲烷,理由是随着温度升高,热裂解反应速率加快,同时___________ 。
②保持其他条件不变,在乙酸气中掺杂一定量水,氢气产率显著提高而CO的产率下降,请分析原因:___________ 。
(3)若利用合适的催化剂控制其他副反应,温度为T ℃时达到平衡,总压强为p kPa,热裂解反应消耗乙酸30%,脱羧基反应消耗乙酸50%,H2体积分数为___________ ;脱羧基反应的平衡常数Kp为___________ kPa(Kp为以分压表示的平衡常数,分压=总压×体积分数,计算结果用最简式表示)。
热裂解反应:CH3COOH(g)=2CO(g)+2H2(g) ΔH=+213.7 kJ·mol-1
脱羧基反应:CH3COOH(g)=CH4(g)+CO2(g) ΔH=-33.5 kJ·mol-1
(1)请写出CO与H2反应生成甲烷的热化学方程式:
(2)在密闭容器中,利用乙酸制氢,选择的压强为

①约650 ℃之前,脱羧基反应活化能低,速率快,故氢气产率低于甲烷;650 ℃之后氢气产率高于甲烷,理由是随着温度升高,热裂解反应速率加快,同时
②保持其他条件不变,在乙酸气中掺杂一定量水,氢气产率显著提高而CO的产率下降,请分析原因:
(3)若利用合适的催化剂控制其他副反应,温度为T ℃时达到平衡,总压强为p kPa,热裂解反应消耗乙酸30%,脱羧基反应消耗乙酸50%,H2体积分数为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】以下是部分共价键的键能数据:H—S 364 kJ·mol-1,S—S 266 kJ·mol-1,O=O496 kJ·mol-1,H—O 463 kJ·mol-1.已知热化学方程式:
2H2S(g)+O2(g)=2S(g)+2H2O(g) ΔH1
2H2S(g)+3O2(g)=2SO2(g)+2H2O(g) ΔH2=-1 000 kJ·mol-1
反应产物中的S实为S8分子,是一个八元环状分子(如图所示)。
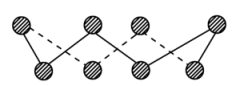
(1)试根据上述数据计算,ΔH1=___________ kJ·mol-1。
(2)将a mol H2S与b mol O2混合进行上述反应,当a>2b时,反应放热___________ kJ;将a mol H2S与b mol O2混合进行上述反应,当3a<2b时,反应放热___________ kJ。
(3)二氧化碳催化加氢制甲醇,有利于减少温室气体二氧化碳。回答下列问题:
二氧化碳加氢制甲醇的总反应可表示为:CO2(g)+3H2(g)=CH3OH(g)+H2O(g) ΔH=-49kJ·mol-1该反应一般认为通过如下步骤来实现:
①CO2(g)+H2(g)=CO(g)+H2O(g) ΔH1=a kJ·mol-1
②CO(g)+2H2(g)=CH3OH(g) ΔH2=-90 kJ·mol-1
若反应①为慢反应,下列示意图中能体现上述反应能量变化的是___________ (填标号),判断的理由是___________ 。
a. B.
B.
C. D.
D.
(4)对于反应CaO(s)+CO2(g) CaCO3(s) K;保持温度不变,若平衡时再充入CO2,使其浓度增大到原来的2倍,则平衡向
CaCO3(s) K;保持温度不变,若平衡时再充入CO2,使其浓度增大到原来的2倍,则平衡向___________ (填“正反应”或“逆反应”)方向移动;当重新平衡后,CO2浓度___________ (填“变大”“变小”或“不变”)。
2H2S(g)+O2(g)=2S(g)+2H2O(g) ΔH1
2H2S(g)+3O2(g)=2SO2(g)+2H2O(g) ΔH2=-1 000 kJ·mol-1
反应产物中的S实为S8分子,是一个八元环状分子(如图所示)。

(1)试根据上述数据计算,ΔH1=
(2)将a mol H2S与b mol O2混合进行上述反应,当a>2b时,反应放热
(3)二氧化碳催化加氢制甲醇,有利于减少温室气体二氧化碳。回答下列问题:
二氧化碳加氢制甲醇的总反应可表示为:CO2(g)+3H2(g)=CH3OH(g)+H2O(g) ΔH=-49kJ·mol-1该反应一般认为通过如下步骤来实现:
①CO2(g)+H2(g)=CO(g)+H2O(g) ΔH1=a kJ·mol-1
②CO(g)+2H2(g)=CH3OH(g) ΔH2=-90 kJ·mol-1
若反应①为慢反应,下列示意图中能体现上述反应能量变化的是
a.
 B.
B.
C.
 D.
D.
(4)对于反应CaO(s)+CO2(g)
 CaCO3(s) K;保持温度不变,若平衡时再充入CO2,使其浓度增大到原来的2倍,则平衡向
CaCO3(s) K;保持温度不变,若平衡时再充入CO2,使其浓度增大到原来的2倍,则平衡向
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】采用废铁屑还原软锰矿(软锰矿主要成分是 ,还含有
,还含有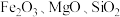 和
和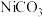 杂质)来制备
杂质)来制备 的工艺流程如图所示。
的工艺流程如图所示。
 。
。
已知:生成氢氧化物的 见下表
见下表
(1)“酸浸”前将原料粉碎的目的是_______ 。
(2)加入量 的目的是
的目的是_______ ,其反应的离子方程式为_______ 。
(3)常温下,已知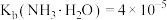 ,则0.1mol/L的
,则0.1mol/L的 的
的 约为
约为_______ 。( )。
)。
(4)“调节 ”操作中
”操作中 控制范围为
控制范围为_______ 。
(5)“沉锰”过程中的离子方程式为_______ ,其过程中温度和 对
对 和
和 沉淀率的影响如图所示,由图可知,“沉锰”的合适条件是
沉淀率的影响如图所示,由图可知,“沉锰”的合适条件是_______ 。

(6)该流程中可循环利用的物质是_______ 。
 ,还含有
,还含有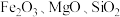 和
和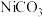 杂质)来制备
杂质)来制备 的工艺流程如图所示。
的工艺流程如图所示。 。
。已知:生成氢氧化物的
 见下表
见下表| 离子 |  |  |  |  |  |
开始沉淀的 | 7.5 | 2.7 | 8.1 | 7.7 | 8.3 |
完全沉淀的 | 9.7 | 3.7 | 9.4 | 8.4 | 9.8 |
(2)加入量
 的目的是
的目的是(3)常温下,已知
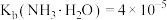 ,则0.1mol/L的
,则0.1mol/L的 的
的 约为
约为 )。
)。(4)“调节
 ”操作中
”操作中 控制范围为
控制范围为(5)“沉锰”过程中的离子方程式为
 对
对 和
和 沉淀率的影响如图所示,由图可知,“沉锰”的合适条件是
沉淀率的影响如图所示,由图可知,“沉锰”的合适条件是
(6)该流程中可循环利用的物质是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】某兴趣小组的同学用下图所示装置研究有关电化学的问题(甲、乙、丙三池中溶质足量), 当闭合该装置的电键 K 时,观察到电流计的指针发生了偏转。请回答下列问题:
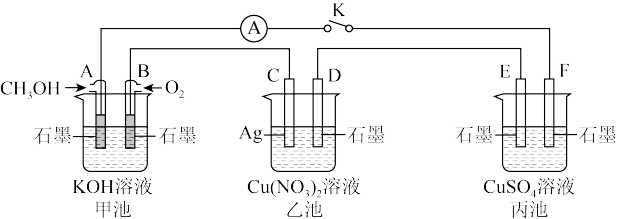
(1)乙池为_____ (填“原电池”、“电解池”或“电镀池”),B 电极的电极反应式为____ 。
(2)丙池中 E 电极为____ (填“正极”、“负极”、“阴极”或“阳极”),电极的电极反应式为____ 。该池总反应的化学方程式为____ 。
(3)当乙池中 C 极质量减轻 54 g 时,甲池中 B 电极理论上消耗 O2的为____ L(标准状况)。
(4)一段时间后,断开电键 K,下列物质能使丙池恢复到反应前浓度的是____ (填选项字母)。
A Cu B CuO C Cu(OH)2 D Cu2(OH)2CO3

(1)乙池为
(2)丙池中 E 电极为
(3)当乙池中 C 极质量减轻 54 g 时,甲池中 B 电极理论上消耗 O2的为
(4)一段时间后,断开电键 K,下列物质能使丙池恢复到反应前浓度的是
A Cu B CuO C Cu(OH)2 D Cu2(OH)2CO3
您最近一年使用:0次
【推荐3】氨是一种重要的化工原料,工业上利用氮气和氢气催化合成氨是人工固氮的主要手段,对人类生存、社会进步和经济发展都有着重大意义。请回答下列问题:
(1)合成氨的反应历程和能量变化如图所示:
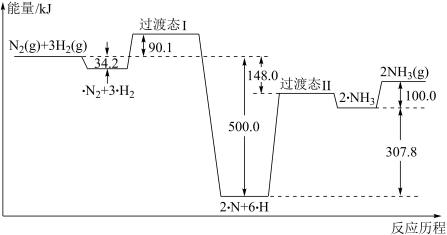
①合成氨反应的热化学方程式为_______ 。
②对总反应速率影响较大的步骤的能垒(活化能)为_______ kJ,该步骤的化学方程式为_______ 。
(2)按照n(N2):n(H2)=1:3投料,发生合成氨反应,NH3的平衡体积分数φ(NH3)在不同压强下随温度变化如图所示。
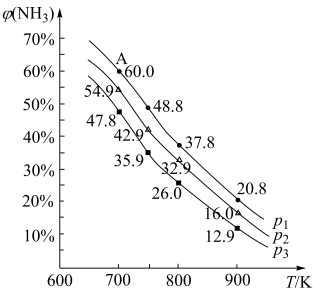
①判断压强从小到大的顺序为_______ ,理由是_______ 。
②A点(700K,0.5MPa)的压强平衡常数Kp=_______ ,此时的平衡转化率α(N2)=_______ 。
(3)常温常压下,以N2和H2O为原料的电化学合成氨是极具应用前途的绿色合成氨过程。在阳极室、阴极室中加入Na2SO4电解液,以镍的有机配位化合物与炭黑合成的物质以及铂为电极,实验室模拟氨的电化学合成过程如图所示。
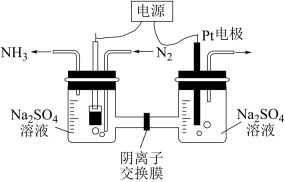
①阳极的电极反应式为_______ 。
②电路上转移1.5mol电子时,阴极收集到的气体体积小于11.2L(标准状况),可能的原因为_______ 。
(1)合成氨的反应历程和能量变化如图所示:

①合成氨反应的热化学方程式为
②对总反应速率影响较大的步骤的能垒(活化能)为
(2)按照n(N2):n(H2)=1:3投料,发生合成氨反应,NH3的平衡体积分数φ(NH3)在不同压强下随温度变化如图所示。

①判断压强从小到大的顺序为
②A点(700K,0.5MPa)的压强平衡常数Kp=
(3)常温常压下,以N2和H2O为原料的电化学合成氨是极具应用前途的绿色合成氨过程。在阳极室、阴极室中加入Na2SO4电解液,以镍的有机配位化合物与炭黑合成的物质以及铂为电极,实验室模拟氨的电化学合成过程如图所示。

①阳极的电极反应式为
②电路上转移1.5mol电子时,阴极收集到的气体体积小于11.2L(标准状况),可能的原因为
您最近一年使用:0次



