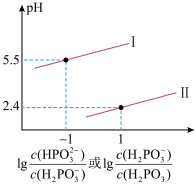
已知亚磷酸( )是二元弱酸,常温下,向某浓度的亚磷酸溶液中逐滴加入一定浓度的NaOH溶液,混合溶液的pH与离子浓度的关系如图所示:
)是二元弱酸,常温下,向某浓度的亚磷酸溶液中逐滴加入一定浓度的NaOH溶液,混合溶液的pH与离子浓度的关系如图所示:
(1)请写出 的电离方程式
的电离方程式_______ 。
(2)向 溶液中滴加NaOH溶液至过量,滴加过程中水的电离程度
溶液中滴加NaOH溶液至过量,滴加过程中水的电离程度_______ 。
(3)当NaOH与 等物质的量混合时,溶液中的电荷守恒式为
等物质的量混合时,溶液中的电荷守恒式为_______ ,溶液中各离子浓度由大到小的顺序_______ 。
(4)由图分析,表示pH与 的变化关系是曲线
的变化关系是曲线_______ (填“I”或“II”)。
(5) 溶液中存在水解反应
溶液中存在水解反应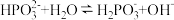 ,常温下该反应的化学平衡常数为
,常温下该反应的化学平衡常数为_______  。
。
 )是二元弱酸,常温下,向某浓度的亚磷酸溶液中逐滴加入一定浓度的NaOH溶液,混合溶液的pH与离子浓度的关系如图所示:
)是二元弱酸,常温下,向某浓度的亚磷酸溶液中逐滴加入一定浓度的NaOH溶液,混合溶液的pH与离子浓度的关系如图所示:
(1)请写出
 的电离方程式
的电离方程式(2)向
 溶液中滴加NaOH溶液至过量,滴加过程中水的电离程度
溶液中滴加NaOH溶液至过量,滴加过程中水的电离程度(3)当NaOH与
 等物质的量混合时,溶液中的电荷守恒式为
等物质的量混合时,溶液中的电荷守恒式为(4)由图分析,表示pH与
 的变化关系是曲线
的变化关系是曲线(5)
 溶液中存在水解反应
溶液中存在水解反应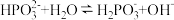 ,常温下该反应的化学平衡常数为
,常温下该反应的化学平衡常数为 。
。
更新时间:2020/12/18 19:48:30
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】已知25℃时,部分弱电解质的电离平衡常数数据如下表:
回答下列问题:
(1)等物质的量浓度的a.CH3COONa、b.NaCN、c.Na2CO3、d.NaHCO3溶液的 由小到大的顺序为
由小到大的顺序为___________ (填字母序号)。
(2)常温下,0.1mol/L醋酸溶液加水稀释过程中,下列表达式的数据减小的是___________(填字母序号)。
(3)25℃时,将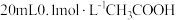 溶液和
溶液和 溶液分别与
溶液分别与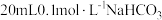 溶液混合,实验测得产生的气体体积(V)随时间(t)变化如图1所示:反应初始阶段两种溶液产生
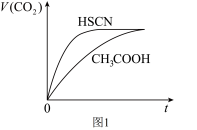
溶液混合,实验测得产生的气体体积(V)随时间(t)变化如图1所示:反应初始阶段两种溶液产生 气体的速率存在明显差异的原因是
气体的速率存在明显差异的原因是___________ 反应结束后所得两溶液中,c(SCN-)_________ c(CH3COO-)(填“>”“<”或“=”)。
(4)体积均为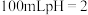 的
的 与一元酸
与一元酸 ,加水稀释过程中
,加水稀释过程中 与溶液体积的关系如图2所示,则
与溶液体积的关系如图2所示,则 的电离平衡常数
的电离平衡常数___________ (填“大于”、“小于”或“等于”) 的电离平衡常数。
的电离平衡常数。

(5)25℃时,在 与
与 的混合溶液中,若测得
的混合溶液中,若测得 ,则溶液中
,则溶液中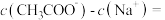
________ mol/L(填精确值),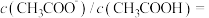
___________ 。
| 弱酸化学式 |  |  |  |  |
| 电离平衡常数 | 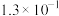 |  |  | 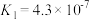 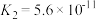 |
(1)等物质的量浓度的a.CH3COONa、b.NaCN、c.Na2CO3、d.NaHCO3溶液的
 由小到大的顺序为
由小到大的顺序为(2)常温下,0.1mol/L醋酸溶液加水稀释过程中,下列表达式的数据减小的是___________(填字母序号)。
A. | B. |
C.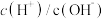 | D. |
(3)25℃时,将
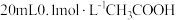 溶液和
溶液和 溶液分别与
溶液分别与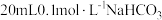 溶液混合,实验测得产生的气体体积(V)随时间(t)变化如图1所示:反应初始阶段两种溶液产生
溶液混合,实验测得产生的气体体积(V)随时间(t)变化如图1所示:反应初始阶段两种溶液产生 气体的速率存在明显差异的原因是
气体的速率存在明显差异的原因是
(4)体积均为
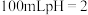 的
的 与一元酸
与一元酸 ,加水稀释过程中
,加水稀释过程中 与溶液体积的关系如图2所示,则
与溶液体积的关系如图2所示,则 的电离平衡常数
的电离平衡常数 的电离平衡常数。
的电离平衡常数。
(5)25℃时,在
 与
与 的混合溶液中,若测得
的混合溶液中,若测得 ,则溶液中
,则溶液中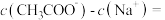
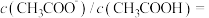
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】在室温下,下列六种溶液:
①0.1 mol/L NH4Cl;②0.1 mol/L CH3COONH4;⑧0.1 mol/L NH4HSO4;④pH = 12的NH3·H2O和pH = 2 HCl等体积混合液:⑤0.1 mol/L NH3·H2O;⑥0.1 mol/L (NH4)2CO3
请根据要求填写下列空白:
(1)溶液①、③呈酸性的原因不同,分别用方程式解释__________ ;___________ 。
(2)室温下,测得溶液②的pH=7 ,则 CH3COO-与 NH4+浓度的大小关系是:c(CH3COO-)________ c( )(填“>”,“<”或“=”)。
)(填“>”,“<”或“=”)。
(3)比较溶液①、②、③、⑤中c( )的大小关系
)的大小关系_________ 。
(4)写出溶液④中离子浓度的大小关系_______ 。
(5)写出溶液⑥的电荷守恒_________________ 。
①0.1 mol/L NH4Cl;②0.1 mol/L CH3COONH4;⑧0.1 mol/L NH4HSO4;④pH = 12的NH3·H2O和pH = 2 HCl等体积混合液:⑤0.1 mol/L NH3·H2O;⑥0.1 mol/L (NH4)2CO3
请根据要求填写下列空白:
(1)溶液①、③呈酸性的原因不同,分别用方程式解释
(2)室温下,测得溶液②的pH=7 ,则 CH3COO-与 NH4+浓度的大小关系是:c(CH3COO-)
 )(填“>”,“<”或“=”)。
)(填“>”,“<”或“=”)。(3)比较溶液①、②、③、⑤中c(
 )的大小关系
)的大小关系(4)写出溶液④中离子浓度的大小关系
(5)写出溶液⑥的电荷守恒
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】已知某溶液中只存在OH-、H+、NH4+、Cl-四种离子,某同学推测该溶液中各离子浓度大小顺序可能有如下四种关系:
A.c(Cl-)>c(NH4+)>c(H+)>c(OH-) B.c(Cl-)>c(NH4+)>c(OH-)>c(H+)
C.c(Cl-)>c(H+)>c(NH4+)>c(OH-) D.c(NH4+)>c(Cl-)>c(OH-)>c(H+)
(1)若溶液中只溶解了一种溶质,该溶质的名称是________________ ,上述离子浓度大小顺序关系中正确的是(选填序号)____________ 。
(2)若上述关系中C是正确的,则溶液中溶质的化学式是____________ 。
(3)若该溶液中由体积相等的稀盐酸和氨水混合而成,且恰好呈中性,则混合前c(HCl)________ c(NH3·H2O)(填“>”、“<”、或“=”)。
A.c(Cl-)>c(NH4+)>c(H+)>c(OH-) B.c(Cl-)>c(NH4+)>c(OH-)>c(H+)
C.c(Cl-)>c(H+)>c(NH4+)>c(OH-) D.c(NH4+)>c(Cl-)>c(OH-)>c(H+)
(1)若溶液中只溶解了一种溶质,该溶质的名称是
(2)若上述关系中C是正确的,则溶液中溶质的化学式是
(3)若该溶液中由体积相等的稀盐酸和氨水混合而成,且恰好呈中性,则混合前c(HCl)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】常温下,浓度均为0.1mol·L-1的下列4种溶液:
①NaCN溶液 ②NaOH溶液 ③CH3COONa溶液 ④NaHCO3溶液
(1)①中各离子浓度由大到小的顺序是___ 。
(2)④的水解平衡常数Kh=___ 。
(3)若向等体积的③和④中滴加盐酸至呈中性,则消耗盐酸的体积③___ ④(填“>”、“<"、“=”)
(4)向NaCN溶液中通入少量CO2,则发生反应的离子方程式为:__ 。
①NaCN溶液 ②NaOH溶液 ③CH3COONa溶液 ④NaHCO3溶液
| HCN | H2CO3 | CH3COOH |
| Ka=4.9×10-10 | Ka1=4×10-7;Ka2=5.6×10-11 | Ka=1.7×10-5 |
(1)①中各离子浓度由大到小的顺序是
(2)④的水解平衡常数Kh=
(3)若向等体积的③和④中滴加盐酸至呈中性,则消耗盐酸的体积③
(4)向NaCN溶液中通入少量CO2,则发生反应的离子方程式为:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】常温下,将某一元酸HA(甲、乙、丙、丁代表不同的一元酸)和NaOH溶液等体积混合,两种溶液的物质的量浓度和混合溶液的pH如下表所示:
(1)从甲组情况分析,如何判断HA是强酸还是弱酸?__________________________________________________ 。
(2)乙组混合溶液中粒子浓度c(A-)和c(Na+)的大小关系________ 。
A.前者大 B.后者大
C.两者相等 D.无法判断
(3)从丙组实验结果分析,该混合溶液中离子浓度由大到小的顺序是__________________
(4)分析丁组实验数据,写出混合溶液中下列算式的精确结果(列式):c(Na+)-c(A-)=________ mol·L-1。
| 实验 编号 | HA物质的量 浓度/(mol·L-1) | NaOH物质的量 浓度/(mol·L-1) | 混合后溶 液的pH |
| 甲 | 0.1 | 0.1 | pH=a |
| 乙 | 0.12 | 0.1 | pH=7 |
| 丙 | 0.2 | 0.1 | pH>7 |
| 丁 | 0.1 | 0.1 | pH=10 |
(1)从甲组情况分析,如何判断HA是强酸还是弱酸?
(2)乙组混合溶液中粒子浓度c(A-)和c(Na+)的大小关系
A.前者大 B.后者大
C.两者相等 D.无法判断
(3)从丙组实验结果分析,该混合溶液中离子浓度由大到小的顺序是
(4)分析丁组实验数据,写出混合溶液中下列算式的精确结果(列式):c(Na+)-c(A-)=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】NH4Al(SO4)2是一种食品添加剂,用于焙烤食品;NH4HSO4在分析化学、制药工业中用途广泛。请回答下列问题:
(1)NH4Al(SO4)2可作净水剂,其理由是___________________________________________________ (用必要的化学用语和相关文字说明)。
(2)相同温度下,浓度均为0.1 mol/L 的下列溶液中的c( )由大到小
)由大到小_____ (填序号)。
①NH4Al(SO4)2 ②CH3COONH4 ③ NH4HSO4 ④NH3·H2O ⑤NH4Cl
(3)如图1是0.1 mol/L电解质溶液的pH随温度变化的图象。其中符合0.1 mol/L NH4Al(SO4)2溶液的pH随温度变化的曲线是_____ (填写字母)。
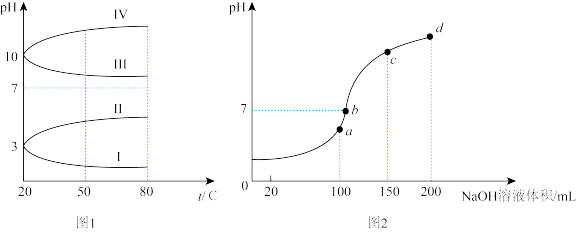
(4)室温时,向100 mL 0.1 mol/L的NH4HSO4溶液中滴加0.1 mol/L NaOH溶液,所得溶液的pH与所加NaOH溶液体积的关系曲线如图2所示。试分析图中a、b、c、d四个点,水的电离程度最大的是_____ ;在b点,溶液中各离子浓度由大到小的排列顺序是______ ;在cd段发生反应的离子方程式________________ 。
(1)NH4Al(SO4)2可作净水剂,其理由是
(2)相同温度下,浓度均为0.1 mol/L 的下列溶液中的c(
 )由大到小
)由大到小①NH4Al(SO4)2 ②CH3COONH4 ③ NH4HSO4 ④NH3·H2O ⑤NH4Cl
(3)如图1是0.1 mol/L电解质溶液的pH随温度变化的图象。其中符合0.1 mol/L NH4Al(SO4)2溶液的pH随温度变化的曲线是

(4)室温时,向100 mL 0.1 mol/L的NH4HSO4溶液中滴加0.1 mol/L NaOH溶液,所得溶液的pH与所加NaOH溶液体积的关系曲线如图2所示。试分析图中a、b、c、d四个点,水的电离程度最大的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】下表是常温下,浓度为0.01mol/L的NaOH溶液与几种酸或盐混合后的情况:
回答下列问题:
(1)①组混合液中,HA、A-、Na+三种粒子浓度由大到小的顺序为________ ,若pH=8,则c(Na+)-c(A-)=________ mol/L(填具体数字)。
(2)由②组混合液pH=7可推知,V1____ V2。
(3)③组混合液中,pH>7的原因是______________________ 。
(4)0.01mol/LNaHD溶液中,水的电离度=_________ 。(已知:水的电离度=[已电离的水分子的个数/水分子总数]×100%)
(5)仅凭上述结果,一定能确定HA、HB、H2C、H2D四种酸中属于弱酸的是_________ 。
| 混合组别 | 混合前酸或盐的总浓度 | 混合比例及混合溶液性质 |
| ① | c(HA)=0.02mol/L | 等体积混合,pH>7 |
| ② | HB溶液的pH=2 | V1 mLNaOH溶液与V2mLHB溶液,pH=7 |
| ③ | c(H2C)=0.01mol/L | 等体积混合,pH>7 |
| ④ | c(NaHD)=0.01mol/L | 等体积混合,pH=7 |
(1)①组混合液中,HA、A-、Na+三种粒子浓度由大到小的顺序为
(2)由②组混合液pH=7可推知,V1
(3)③组混合液中,pH>7的原因是
(4)0.01mol/LNaHD溶液中,水的电离度=
(5)仅凭上述结果,一定能确定HA、HB、H2C、H2D四种酸中属于弱酸的是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】某研究性学习小组为了探究醋酸的电离情况,进行了如下实验。
探究浓度对醋酸电离程度的影响:用pH计测定25℃时不同浓度的醋酸的pH,其结果如下:
回答下列问题:
(1)若用pH试纸测醋酸的pH,实验操作为:_______ 。
(2)根据表中数据,可以得出醋酸是弱电解质的结论,你认为得出此结论的依据是:_______ 。
(3)从表中的数据,还可以得出另一结论:随着醋酸浓度的减小,醋酸的电离程度_______ (填增大、减小或不变)
(4) 俗称纯碱,因
俗称纯碱,因 水解而使其水溶液呈碱性(忽略第二步水解),已知25℃时,
水解而使其水溶液呈碱性(忽略第二步水解),已知25℃时,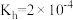 ,则当溶液中
,则当溶液中 时,溶液的pH=
时,溶液的pH=_______ 。
探究浓度对醋酸电离程度的影响:用pH计测定25℃时不同浓度的醋酸的pH,其结果如下:
| 醋酸浓度(mol/L) | 0.0010 | 0.0100 | 0.0200 | 0.1000 | 0.2000 | |
| pH | 3.88 | 3.38 | 3.23 | 2.88 | 2.73 |
回答下列问题:
(1)若用pH试纸测醋酸的pH,实验操作为:
(2)根据表中数据,可以得出醋酸是弱电解质的结论,你认为得出此结论的依据是:
(3)从表中的数据,还可以得出另一结论:随着醋酸浓度的减小,醋酸的电离程度
(4)
 俗称纯碱,因
俗称纯碱,因 水解而使其水溶液呈碱性(忽略第二步水解),已知25℃时,
水解而使其水溶液呈碱性(忽略第二步水解),已知25℃时,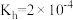 ,则当溶液中
,则当溶液中 时,溶液的pH=
时,溶液的pH=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】常温下,有浓度均为 的下列4种溶液:①
的下列4种溶液:① 溶液 ②
溶液 ② 溶液 ③
溶液 ③ 溶液 ④
溶液 ④ 溶液
溶液
(1)这4种溶液 由大到小的顺序是
由大到小的顺序是______ (填序号)。
(2)①中各离子浓度由大到小的顺序是______ 。
(3)④的水解平衡常数
______  。
。
(4)若向等体积的③和④中滴加盐酸至呈中性,则消耗盐酸的体积③______ ④(填“﹥”、“﹤”、“=”)。
(5)25℃时,测得 和
和 的混合溶液的
的混合溶液的 ,则
,则 约为
约为______ 。向 溶液中通入少量
溶液中通入少量 ,则发生反应的离子方程式为:
,则发生反应的离子方程式为:______ 。
 的下列4种溶液:①
的下列4种溶液:① 溶液 ②
溶液 ② 溶液 ③
溶液 ③ 溶液 ④
溶液 ④ 溶液
溶液 |  |  |
 |   |  |
 由大到小的顺序是
由大到小的顺序是(2)①中各离子浓度由大到小的顺序是
(3)④的水解平衡常数

 。
。(4)若向等体积的③和④中滴加盐酸至呈中性,则消耗盐酸的体积③
(5)25℃时,测得
 和
和 的混合溶液的
的混合溶液的 ,则
,则 约为
约为 溶液中通入少量
溶液中通入少量 ,则发生反应的离子方程式为:
,则发生反应的离子方程式为:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】下表是几种常见弱酸的电离平衡常数(25 ℃)。
回答下列各题:
(1)在温度相同时,各弱酸的K值不同,那么K值的大小与酸性的相对强弱有何关系?___________________ 。
(2)若把CH3COOH、H2CO3、HCO 、H2S、HS-、H3PO4、H2PO
、H2S、HS-、H3PO4、H2PO 、HPO
、HPO 都看作是酸,其中酸性最强的是
都看作是酸,其中酸性最强的是________ ,最弱的是________ 。
(3)多元弱酸是分步电离的,每一步都有相应的电离平衡常数。对于同一种多元弱酸的K1、K2、K3之间存在着数量上的规律,此规律是________ ,产生此规律的原因是___________________________ 。
(4)用食醋浸泡有水垢的水壶,可以清除其中的水垢,这是利用醋酸的________ 。通过该事实________ (填“能”或“不能”)比较醋酸与碳酸的酸性强弱,请设计一个简单的实验方案验证醋酸与碳酸的酸性强弱。
方案:____________________________________ 。
酸 | 电离方程式 | 电离平衡常数K |
CH3COOH | CH3COOH | 1.75×10-5 |
H2CO3 | H2CO3 HCO | K1=4.4×10-7 K2=4.7×10-11 |
H2S | H2S HS- | K1=1.3×10-7 K2=7.1×10-15 |
H3PO4 | H3PO4 H2PO HPO | K1=7.1×10-3 K2=6.3×10-8 K3=4.2×10-13 |
回答下列各题:
(1)在温度相同时,各弱酸的K值不同,那么K值的大小与酸性的相对强弱有何关系?
(2)若把CH3COOH、H2CO3、HCO
 、H2S、HS-、H3PO4、H2PO
、H2S、HS-、H3PO4、H2PO 、HPO
、HPO 都看作是酸,其中酸性最强的是
都看作是酸,其中酸性最强的是(3)多元弱酸是分步电离的,每一步都有相应的电离平衡常数。对于同一种多元弱酸的K1、K2、K3之间存在着数量上的规律,此规律是
(4)用食醋浸泡有水垢的水壶,可以清除其中的水垢,这是利用醋酸的
方案:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】已知常温下CH3COOH的电离常数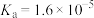 ,该温度下,1
,该温度下,1 CH3COOH溶液pH约为
CH3COOH溶液pH约为___________ (保留小数点后一位)。
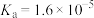 ,该温度下,1
,该温度下,1 CH3COOH溶液pH约为
CH3COOH溶液pH约为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】回答下列问题:
(1)碳氢化合物完全燃烧生成CO2和H2O.常温常压下,空气中的CO2溶于水,达到平衡时,溶液中c(H+)=2.5 10-6mol/L,c(H2CO3)=1.25
10-6mol/L,c(H2CO3)=1.25 10-5mol/L。则H2CO3⇌HCO
10-5mol/L。则H2CO3⇌HCO +H+的电离平衡常数Ka1=
+H+的电离平衡常数Ka1=_______ 。
(2)现有下列物质:①50 ②25
②25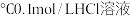 ,③25
,③25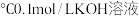 ④25
④25 0.1mol/LBa(OH)2溶液。
0.1mol/LBa(OH)2溶液。
i:这些物质与25 纯水相比,其中水的电离得到促进的是
纯水相比,其中水的电离得到促进的是_______ (填序号,下同),其中水的电离被抑制的是_______ ,水电离的c(OH-)等于溶液中c(OH-)的是_______ ,水电离的c(H+)等于溶液中c(H+)的是_______ 。
ii:从②和③溶液中水的电离程度相等,进而可推出的结论是:同一温度下,当_______ 时,水的电离程度相等。
(1)碳氢化合物完全燃烧生成CO2和H2O.常温常压下,空气中的CO2溶于水,达到平衡时,溶液中c(H+)=2.5
 10-6mol/L,c(H2CO3)=1.25
10-6mol/L,c(H2CO3)=1.25 10-5mol/L。则H2CO3⇌HCO
10-5mol/L。则H2CO3⇌HCO +H+的电离平衡常数Ka1=
+H+的电离平衡常数Ka1=(2)现有下列物质:①50
 ②25
②25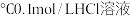 ,③25
,③25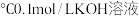 ④25
④25 0.1mol/LBa(OH)2溶液。
0.1mol/LBa(OH)2溶液。i:这些物质与25
 纯水相比,其中水的电离得到促进的是
纯水相比,其中水的电离得到促进的是ii:从②和③溶液中水的电离程度相等,进而可推出的结论是:同一温度下,当
您最近一年使用:0次

 CH3COO-+H+
CH3COO-+H+



