Ⅰ.蕴藏在海底的可燃冰是高压下形成外观像冰的甲烷水合物固体,被称之为“未来能源”。对燃煤废气进行脱硝处理时,常利用甲烷催化还原氮氧化物,如:
CH4(g)+4NO2(g) 4NO(g)+CO2(g)+2H2O(g) △H1 =-574 kJ·mol-1 K1
4NO(g)+CO2(g)+2H2O(g) △H1 =-574 kJ·mol-1 K1
CH4(g)+4NO(g) 2N2(g)+CO2(g)+2H2O(g) △H2 =-1160 kJ·mol-1 K2
2N2(g)+CO2(g)+2H2O(g) △H2 =-1160 kJ·mol-1 K2
则CH4(g)将NO2(g)还原为N2(g)的热化学方程式为___________ ,且该反应的平衡常数K=___________ (用含K1、K2的代数式表示)。
Ⅱ.水煤气是重要燃料和化工原料,可用水蒸气通过炽热的碳层制得:C (s) + H2O(g) CO (g) +H2 (g) △H=+131.3 kJ•mol-1
CO (g) +H2 (g) △H=+131.3 kJ•mol-1
(1) 该反应的化学平衡常数表达式K=___________ ,若某温度下,K值的大小为0.5,此时向体积为1L的密闭容器中加入1mol H2O(g)和足量C(s),H2O(g)的平衡转化率为 ___________ ;
(2) 对于该反应,一定可以提高平衡体系中H2的百分含量,又能加快化学反应速率的措施是___________ ;
a.升高温度 b.增大水蒸气的浓度 c.加入催化剂 d.降低压强
(3) 上述反应达到平衡后,移走体系中部分C(s),平衡___________ ,将产生的CO全部移走,平衡___________ (以上两空选填“向左移”、“向右移”、“不移动”);
(4) 上述反应在t0时刻达到平衡(如下图),若在t1时刻改变某一条件,请在下图中继续画出t1时刻之后升高温度反应速率(ν)随时间的变化趋势___________ 。

CH4(g)+4NO2(g)
 4NO(g)+CO2(g)+2H2O(g) △H1 =-574 kJ·mol-1 K1
4NO(g)+CO2(g)+2H2O(g) △H1 =-574 kJ·mol-1 K1CH4(g)+4NO(g)
 2N2(g)+CO2(g)+2H2O(g) △H2 =-1160 kJ·mol-1 K2
2N2(g)+CO2(g)+2H2O(g) △H2 =-1160 kJ·mol-1 K2则CH4(g)将NO2(g)还原为N2(g)的热化学方程式为
Ⅱ.水煤气是重要燃料和化工原料,可用水蒸气通过炽热的碳层制得:C (s) + H2O(g)
 CO (g) +H2 (g) △H=+131.3 kJ•mol-1
CO (g) +H2 (g) △H=+131.3 kJ•mol-1(1) 该反应的化学平衡常数表达式K=
(2) 对于该反应,一定可以提高平衡体系中H2的百分含量,又能加快化学反应速率的措施是
a.升高温度 b.增大水蒸气的浓度 c.加入催化剂 d.降低压强
(3) 上述反应达到平衡后,移走体系中部分C(s),平衡
(4) 上述反应在t0时刻达到平衡(如下图),若在t1时刻改变某一条件,请在下图中继续画出t1时刻之后升高温度反应速率(ν)随时间的变化趋势

更新时间:2021-02-20 19:35:08
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】中国是世界上最大的钨储藏国,超细钨粉是生产硬质合金所必须的原料,是重要的战略物资。自然界中钨主要存在于黑钨矿中,其主要成分是铁和锰的钨酸盐(FeWO4、MnWO4),还含少量Si、As的化合物。由黑钨矿冶炼钨的工艺流程如图所示:

已知:①“滤渣1”的主要成分是Fe2O3、MnO2。
②上述流程中,钨的化合价只有在最后一步发生改变。
③常温下钨酸难溶于水。
回答下列问题:
(1)钨酸盐(FeWO4、MnWO4)中钨元素的化合价为+6,请写出FeWO4在熔融条件下发生碱分解反应生成Fe2O3的化学方程式_______ 。
(2)从中制备出黄钨(WO3)后,工业上可以采用铝热还原法生产钨铁合金,已知:
①WO3(s)+2Al(s)═W(s)+Al2O3(s) △H1
②3Fe3O4(s)+8Al(s)=9Fe(s)+4Al2O3(s) △H2
则四氧化三铁与钨反应的热化学方程式为_______ (反应热写为△H3并用含△H1、△H2的代数式表示)。
(3)工业上也可以用H2逐级还原:WO3→WO2.90→WO2.72→WO2→W,总反应为3H2(g)+WO3(s)═W(s)+3H2O(g) △H,实验测得一定条件下,平衡时H2的体积分数曲线如图所示:

①由图可知,a点处反应将向_______ (填“左”或“右”)进行。
②如果上述反应在体积不变的密闭容器中达到平衡,下列说法正确的是_______ (填字母)。
A.v消耗(H2)=v生成(H2O)时,一定达到平衡状态
B.混合气体的平均相对分子质量不变时,一定达到平衡状态
C.容器内气体的密度不变时,一定达到平衡状态
D.容器内压强不变时,一定达到平衡状态
③由图可知900K时,该反应的平衡常数K=_______ 。
④已知在高温下,氧化钨会与水蒸气反应生成一种挥发性极强的水钨化合物WO2(OH)2,因此在反应中要适当加快氢气的流速,原因是_______ 。
⑤若该反应的正、逆反应速率表达式分别为v正=k正•c3(H2),v逆=k逆•c3(H2O),k正,k逆为反应速率常数。其他条件不变升高温度,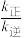 的值将
的值将_______ (填“增大”“减小”或“不变”)。

已知:①“滤渣1”的主要成分是Fe2O3、MnO2。
②上述流程中,钨的化合价只有在最后一步发生改变。
③常温下钨酸难溶于水。
回答下列问题:
(1)钨酸盐(FeWO4、MnWO4)中钨元素的化合价为+6,请写出FeWO4在熔融条件下发生碱分解反应生成Fe2O3的化学方程式
(2)从中制备出黄钨(WO3)后,工业上可以采用铝热还原法生产钨铁合金,已知:
①WO3(s)+2Al(s)═W(s)+Al2O3(s) △H1
②3Fe3O4(s)+8Al(s)=9Fe(s)+4Al2O3(s) △H2
则四氧化三铁与钨反应的热化学方程式为
(3)工业上也可以用H2逐级还原:WO3→WO2.90→WO2.72→WO2→W,总反应为3H2(g)+WO3(s)═W(s)+3H2O(g) △H,实验测得一定条件下,平衡时H2的体积分数曲线如图所示:

①由图可知,a点处反应将向
②如果上述反应在体积不变的密闭容器中达到平衡,下列说法正确的是
A.v消耗(H2)=v生成(H2O)时,一定达到平衡状态
B.混合气体的平均相对分子质量不变时,一定达到平衡状态
C.容器内气体的密度不变时,一定达到平衡状态
D.容器内压强不变时,一定达到平衡状态
③由图可知900K时,该反应的平衡常数K=
④已知在高温下,氧化钨会与水蒸气反应生成一种挥发性极强的水钨化合物WO2(OH)2,因此在反应中要适当加快氢气的流速,原因是
⑤若该反应的正、逆反应速率表达式分别为v正=k正•c3(H2),v逆=k逆•c3(H2O),k正,k逆为反应速率常数。其他条件不变升高温度,
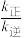 的值将
的值将
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】我国提出争取在2030年前实现碳峰值,2060年实现碳中和,这对改善环境、实现绿色发展至关重要。以含碳物质为原料的“碳-化学”将处于化学产业的核心,成为科学家研究的重要课题。请回答下列问题:
(1)已知CO、H2、 的燃烧热分别为:
的燃烧热分别为: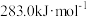 、
、 、
、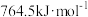 。则反应:
。则反应:
_______ 。
(2)在一容积可变的密闭容器中充入 和
和 ,发生反应
,发生反应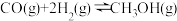 ,CO的平衡转化率(
,CO的平衡转化率( )与温度(T)、压强(p)的关系如图所示。
)与温度(T)、压强(p)的关系如图所示。
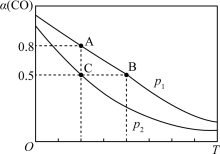
则压强
_______ (填“<”“=”或“>”) ;A、B、C三点的平衡常数
;A、B、C三点的平衡常数 、
、 、
、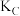 的大小关系为
的大小关系为_______ (用“<”“=”或“>”表示)。
(3) 经催化加氢可合成低碳烯烃:
经催化加氢可合成低碳烯烃: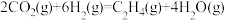 。在
。在 时,按
时,按 投料,如图所示为不同温度(T)下,平衡时四种气态物质的物质的量(n)关系。
投料,如图所示为不同温度(T)下,平衡时四种气态物质的物质的量(n)关系。
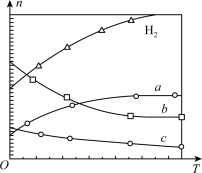
则:
①该反应的
_______ (填“>”或“<”)0。
②曲线c表示的物质为_______ 。
(4)在 、
、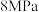 下,将
下,将 和
和 按物质的量之比1∶3通入一密闭容器中发生反应:
按物质的量之比1∶3通入一密闭容器中发生反应: ,达到平衡时,测得
,达到平衡时,测得 的平衡转化率为50%,则该反应条件下的平衡常数
的平衡转化率为50%,则该反应条件下的平衡常数
_______ 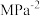 (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(1)已知CO、H2、
 的燃烧热分别为:
的燃烧热分别为: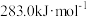 、
、 、
、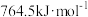 。则反应:
。则反应:
(2)在一容积可变的密闭容器中充入
 和
和 ,发生反应
,发生反应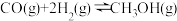 ,CO的平衡转化率(
,CO的平衡转化率( )与温度(T)、压强(p)的关系如图所示。
)与温度(T)、压强(p)的关系如图所示。
则压强

 ;A、B、C三点的平衡常数
;A、B、C三点的平衡常数 、
、 、
、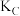 的大小关系为
的大小关系为(3)
 经催化加氢可合成低碳烯烃:
经催化加氢可合成低碳烯烃: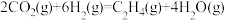 。在
。在 时,按
时,按 投料,如图所示为不同温度(T)下,平衡时四种气态物质的物质的量(n)关系。
投料,如图所示为不同温度(T)下,平衡时四种气态物质的物质的量(n)关系。
则:
①该反应的

②曲线c表示的物质为
(4)在
 、
、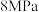 下,将
下,将 和
和 按物质的量之比1∶3通入一密闭容器中发生反应:
按物质的量之比1∶3通入一密闭容器中发生反应: ,达到平衡时,测得
,达到平衡时,测得 的平衡转化率为50%,则该反应条件下的平衡常数
的平衡转化率为50%,则该反应条件下的平衡常数
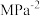 (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
您最近一年使用:0次
【推荐3】直接排放含SO2的烟气会形成酸雨,危害环境。工业上常采用催化还原法和碱吸收法处理SO2气体。
(1)下图所示:1mol CH4完全燃烧生成气态水的能量变化和1mol S(g)燃烧的能量变化。
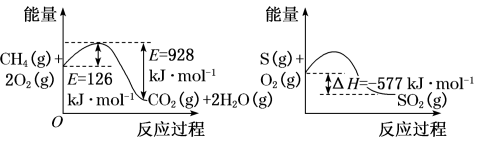
在催化剂作用下,CH4可以还原SO2生成单质S(g)、H2O(g)和CO2,写出该反应的热化学方程式________________________________________________________ 。
(2)焦炭催化还原二氧化硫的化学方程式为2C(s)+2SO2(g) S2(g)+2CO2(g)。一定压强下,向1L密闭容器中充入足量的焦炭和1molSO2发生反应,测得SO2的生成速率与S2(g)的生成速率随温度变化的关系如图所示:
S2(g)+2CO2(g)。一定压强下,向1L密闭容器中充入足量的焦炭和1molSO2发生反应,测得SO2的生成速率与S2(g)的生成速率随温度变化的关系如图所示:
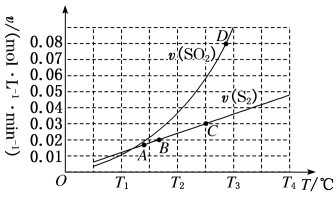
①A、B、C、D四点对应的状态中,达到平衡状态的有_____________ (填字母)。
②该反应的△H_____ 0(填“>”“<”或“=”)。
③下列措施能够增大SO2平衡转化率的是______________ 。
A.降低温度 B.增加C的量 C.减小容器体积 D.添加高效催化剂
(3)用氨水吸收SO2。25℃时,将含SO2的烟气通入一定浓度的氨水中,当溶液显中性时,溶液中的 =
=_____________ 。(已知25℃,Ka1(H2SO3)=1.3×10-2,Ka2(H2SO3)=6.2×10-8 )
(4)当吸收液失去吸收能力后通入O2可得到NH4HSO4溶液,用如图所示装置电解所得NH4HSO4溶液可制得强氧化剂(NH4)2S2O8,请写出电解NH4HSO4溶液的化学方程式_______________ 。

(1)下图所示:1mol CH4完全燃烧生成气态水的能量变化和1mol S(g)燃烧的能量变化。

在催化剂作用下,CH4可以还原SO2生成单质S(g)、H2O(g)和CO2,写出该反应的热化学方程式
(2)焦炭催化还原二氧化硫的化学方程式为2C(s)+2SO2(g)
 S2(g)+2CO2(g)。一定压强下,向1L密闭容器中充入足量的焦炭和1molSO2发生反应,测得SO2的生成速率与S2(g)的生成速率随温度变化的关系如图所示:
S2(g)+2CO2(g)。一定压强下,向1L密闭容器中充入足量的焦炭和1molSO2发生反应,测得SO2的生成速率与S2(g)的生成速率随温度变化的关系如图所示:
①A、B、C、D四点对应的状态中,达到平衡状态的有
②该反应的△H
③下列措施能够增大SO2平衡转化率的是
A.降低温度 B.增加C的量 C.减小容器体积 D.添加高效催化剂
(3)用氨水吸收SO2。25℃时,将含SO2的烟气通入一定浓度的氨水中,当溶液显中性时,溶液中的
 =
=(4)当吸收液失去吸收能力后通入O2可得到NH4HSO4溶液,用如图所示装置电解所得NH4HSO4溶液可制得强氧化剂(NH4)2S2O8,请写出电解NH4HSO4溶液的化学方程式

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】下图所示装置是某化学小组模拟工业生产制取 ,其中a为一个可持续鼓入空气的橡皮球。
,其中a为一个可持续鼓入空气的橡皮球。
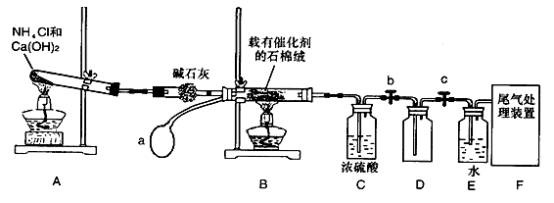
请回答下列问题:
(1)写出装置B中发生反应的化学方程式______ 。
(2)已知 1mol 与液态水反应生成
与液态水反应生成 溶液和NO气体放出热量46kJ写出该反应的热化学方程式
溶液和NO气体放出热量46kJ写出该反应的热化学方程式______ ;该反应是一个可逆反应,欲要提高 的转化率,可采取的措施是
的转化率,可采取的措施是 ______ (填序号)。
A.升高温度 B.降低温度 C.增大压强 D.减小压强
(3)装置C中浓硫酸的作用是______ 。
(4)实验结束后,关闭止水夹b、c,将装置D浸入冰水中,现象是______ 。
(5)实验室制取 也可以用浓氨水与生石灰反应,反应的化学方程式为
也可以用浓氨水与生石灰反应,反应的化学方程式为______ 。
(6)干燥管中的碱石灰用于干燥 ,某同学想用无水氯化钙代替碱石灰,并设计如图所示装置(仪器固定装置未画)进行验证。实验步骤如下:
,某同学想用无水氯化钙代替碱石灰,并设计如图所示装置(仪器固定装置未画)进行验证。实验步骤如下:
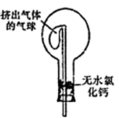
①用烧瓶收集满干燥的氨气,立即塞上如图所示的橡胶塞
②正立烧瓶,使无水氯化钙固体滑入烧瓶底部,摇动,可以观察到的现象是______ ,由此该同学得出结论:不能用 代替碱石灰来干燥氨气。
代替碱石灰来干燥氨气。
 ,其中a为一个可持续鼓入空气的橡皮球。
,其中a为一个可持续鼓入空气的橡皮球。
请回答下列问题:
(1)写出装置B中发生反应的化学方程式
(2)已知 1mol
 与液态水反应生成
与液态水反应生成 溶液和NO气体放出热量46kJ写出该反应的热化学方程式
溶液和NO气体放出热量46kJ写出该反应的热化学方程式 的转化率,可采取的措施是
的转化率,可采取的措施是 A.升高温度 B.降低温度 C.增大压强 D.减小压强
(3)装置C中浓硫酸的作用是
(4)实验结束后,关闭止水夹b、c,将装置D浸入冰水中,现象是
(5)实验室制取
 也可以用浓氨水与生石灰反应,反应的化学方程式为
也可以用浓氨水与生石灰反应,反应的化学方程式为(6)干燥管中的碱石灰用于干燥
 ,某同学想用无水氯化钙代替碱石灰,并设计如图所示装置(仪器固定装置未画)进行验证。实验步骤如下:
,某同学想用无水氯化钙代替碱石灰,并设计如图所示装置(仪器固定装置未画)进行验证。实验步骤如下:
①用烧瓶收集满干燥的氨气,立即塞上如图所示的橡胶塞
②正立烧瓶,使无水氯化钙固体滑入烧瓶底部,摇动,可以观察到的现象是
 代替碱石灰来干燥氨气。
代替碱石灰来干燥氨气。
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】甲醇是一种可再生的清洁能源,具有广阔的开发和应用前景。
(1)已知①CH3OH(g)+H2O(l)=CO2(g)+3H2(g) ΔH=+93.0kJ·mol-1
②CH3OH(g)+ O2(g)=CO2(g)+2H2(g) ΔH=-192.9 kJ·mol-1
O2(g)=CO2(g)+2H2(g) ΔH=-192.9 kJ·mol-1
③CH3OH(g)=CH3OH(l) ΔH=−38.19kJ/mol
写出表示甲醇CH3OH(l)燃烧热的热化学方程式___________ 。
(2)甲醇可采用煤的气化、液化制取(CO+2H2 CH3OH ΔH<0)。在T1℃时,体积为2L的恒容容器中充入物质的量之和为3mol的H2和CO,反应达到平衡时CH3OH的体积分数(V%)与
CH3OH ΔH<0)。在T1℃时,体积为2L的恒容容器中充入物质的量之和为3mol的H2和CO,反应达到平衡时CH3OH的体积分数(V%)与 的关系如图所示。
的关系如图所示。
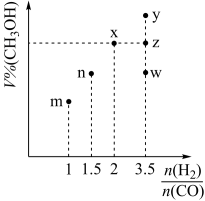
①当起始 =2,经过5min达到平衡,0~5min内平均反应速率v(H2) = 0.1mol⋅L-1⋅min-1,则该条件CO的平衡转化率为
=2,经过5min达到平衡,0~5min内平均反应速率v(H2) = 0.1mol⋅L-1⋅min-1,则该条件CO的平衡转化率为___________ ;若其它条件不变,在T2℃(T2>T1)下达到平衡时CO的体积分数可能是___________ (填标号)
A.33% B.30% C.25% D.20%
②当 =3.5时,达到平衡状态后,CH3OH的体积分数可能是图象中的
=3.5时,达到平衡状态后,CH3OH的体积分数可能是图象中的___________ 点(选填“y”、“z”或“w”)。
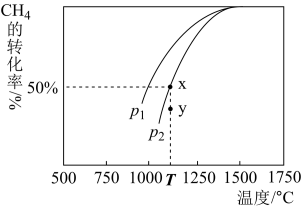
(3)制甲醇的CO和H2可用天然气来制取: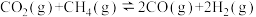 。在某一密闭容器中有浓度均为0.1mol·L−1的CH4和CO2,在一定条件下反应,测得CH4的平衡转化率与温度及压强的关系如图所示,则该反应的ΔH
。在某一密闭容器中有浓度均为0.1mol·L−1的CH4和CO2,在一定条件下反应,测得CH4的平衡转化率与温度及压强的关系如图所示,则该反应的ΔH___________ 0.(选填>、<或=,下同).当压强为p2时,在y点:V(正)___________ V(逆)。若p2=1.2Mpa,则T℃时该反应的平衡常数Kp=___________ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(4)研究表明:CO2和H2在一定条件下也可以合成甲醇,反应方程式为 [反应Ⅰ]。
[反应Ⅰ]。
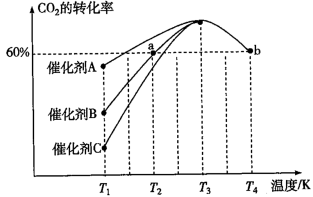
①一定条件下,往2L恒容密闭容器中充入2.0mol CO2和4.0mol H2,在不同催化剂作用下合成甲醇,相同时间内CO2的转化率随温度变化如下图所示,其中活化能最低的反应所用的催化剂是___________ (填“A”、“B”或“C”)。
②在某催化剂作用下,CO2和H2除发生反应①外,还发生如下反应 [反应Ⅱ]。维持压强不变,按固定初始投料比将CO2和H2按一定流速通过该催化剂,经过相同时间测得实验数据:
[反应Ⅱ]。维持压强不变,按固定初始投料比将CO2和H2按一定流速通过该催化剂,经过相同时间测得实验数据:
注:甲醇的选择性是指发生反应的CO2中转化为甲醇的百分比。
表中数据说明,升高温度,CO2的实际转化率提高而甲醇的选择性降低,其原因是________ 。
(1)已知①CH3OH(g)+H2O(l)=CO2(g)+3H2(g) ΔH=+93.0kJ·mol-1
②CH3OH(g)+
 O2(g)=CO2(g)+2H2(g) ΔH=-192.9 kJ·mol-1
O2(g)=CO2(g)+2H2(g) ΔH=-192.9 kJ·mol-1③CH3OH(g)=CH3OH(l) ΔH=−38.19kJ/mol
写出表示甲醇CH3OH(l)燃烧热的热化学方程式
(2)甲醇可采用煤的气化、液化制取(CO+2H2
 CH3OH ΔH<0)。在T1℃时,体积为2L的恒容容器中充入物质的量之和为3mol的H2和CO,反应达到平衡时CH3OH的体积分数(V%)与
CH3OH ΔH<0)。在T1℃时,体积为2L的恒容容器中充入物质的量之和为3mol的H2和CO,反应达到平衡时CH3OH的体积分数(V%)与 的关系如图所示。
的关系如图所示。
①当起始
 =2,经过5min达到平衡,0~5min内平均反应速率v(H2) = 0.1mol⋅L-1⋅min-1,则该条件CO的平衡转化率为
=2,经过5min达到平衡,0~5min内平均反应速率v(H2) = 0.1mol⋅L-1⋅min-1,则该条件CO的平衡转化率为A.33% B.30% C.25% D.20%
②当
 =3.5时,达到平衡状态后,CH3OH的体积分数可能是图象中的
=3.5时,达到平衡状态后,CH3OH的体积分数可能是图象中的(3)制甲醇的CO和H2可用天然气来制取:
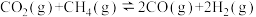 。在某一密闭容器中有浓度均为0.1mol·L−1的CH4和CO2,在一定条件下反应,测得CH4的平衡转化率与温度及压强的关系如图所示,则该反应的ΔH
。在某一密闭容器中有浓度均为0.1mol·L−1的CH4和CO2,在一定条件下反应,测得CH4的平衡转化率与温度及压强的关系如图所示,则该反应的ΔH
(4)研究表明:CO2和H2在一定条件下也可以合成甲醇,反应方程式为
 [反应Ⅰ]。
[反应Ⅰ]。①一定条件下,往2L恒容密闭容器中充入2.0mol CO2和4.0mol H2,在不同催化剂作用下合成甲醇,相同时间内CO2的转化率随温度变化如下图所示,其中活化能最低的反应所用的催化剂是

②在某催化剂作用下,CO2和H2除发生反应①外,还发生如下反应
 [反应Ⅱ]。维持压强不变,按固定初始投料比将CO2和H2按一定流速通过该催化剂,经过相同时间测得实验数据:
[反应Ⅱ]。维持压强不变,按固定初始投料比将CO2和H2按一定流速通过该催化剂,经过相同时间测得实验数据:| T(K) | CO2实际转化率(%) | 甲醇选择性(%) |
| 543 | 12.3 | 42.3 |
| 553 | 15.3 | 39.1 |
表中数据说明,升高温度,CO2的实际转化率提高而甲醇的选择性降低,其原因是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】某实验小组通过铁与盐酸反应的实验,研究影响反应速率的因素(铁的质量相等,铁块的形状一样,盐酸均过量),设计实验如下表:
(1)若四组实验均反应1分钟(铁有剩余),则以上实验需要测出的数据是___________ 。
(2)实验___________ 和___________ (填实验编号)是研究盐酸的浓度对该反应速率的影响;实验1和2是研究___________ 对该反应速率的影响。
(3)测定在不同时间产生氢气体积V的数据,绘制出图甲,则曲线c、d分别对应的实验组别可能是___________ 、___________ 。
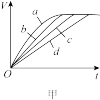
(4)分析其中一组实验,发现产生氢气的速率随时间变化情况如图乙所示。
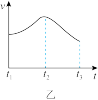
①其中t1~t2速率变化的主要原因是___________ 。
②t2~t3速率变化的主要原因是___________ 。
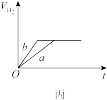
(5)实验1产生氢气的体积如图丙中的曲线a,添加某试剂能使曲线a变为曲线b的是___________(填序号)。
(6)在2 L密闭容器中进行反应:mX(g)+nY(g) pZ(g)+qQ(g),式中m、n、p、q为化学计量数。在0~3 min内,各物质的物质的量的变化如下表所示:
pZ(g)+qQ(g),式中m、n、p、q为化学计量数。在0~3 min内,各物质的物质的量的变化如下表所示:
已知:2 min内v(Q)=0.075 mol/(L·min),v(Z):v(Y)=1:2。
请回答下列问题:
①2 min内Z的反应速率v(Z)=___________ 。
②起始时n(Y)=___________ 、n(Q)=___________ 。
③化学方程式中m=___________ 、n=___________ 、p=___________ 、q=___________ 。
④对于该反应,能增大正反应速率的措施是___________ (填序号)。
A.增大容器容积 B.移走部分Q C.通入大量X D.升高温度
| 实验编号 | 盐酸浓度/(mol/L) | 铁的形态 | 温度/K |
| 1 | 4.00 | 块状 | 293 |
| 2 | 4.00 | 粉末 | 293 |
| 3 | 2.00 | 块状 | 293 |
| 4 | 2.00 | 粉末 | 313 |
(2)实验
(3)测定在不同时间产生氢气体积V的数据,绘制出图甲,则曲线c、d分别对应的实验组别可能是

(4)分析其中一组实验,发现产生氢气的速率随时间变化情况如图乙所示。

①其中t1~t2速率变化的主要原因是
②t2~t3速率变化的主要原因是
(5)实验1产生氢气的体积如图丙中的曲线a,添加某试剂能使曲线a变为曲线b的是___________(填序号)。

| A.CuO粉末 | B.NaNO3固体 | C.NaCl溶液 | D.浓H2SO4 |
 pZ(g)+qQ(g),式中m、n、p、q为化学计量数。在0~3 min内,各物质的物质的量的变化如下表所示:
pZ(g)+qQ(g),式中m、n、p、q为化学计量数。在0~3 min内,各物质的物质的量的变化如下表所示:| 物质 | X | Y | Z | Q |
| n(起始)/mol | 0.7 | 1.0 | ||
| n(2 min末)/mol | 0.8 | 2.7 | 0.8 | 2.7 |
| n(3 min末)/mol | 0.8 |
请回答下列问题:
①2 min内Z的反应速率v(Z)=
②起始时n(Y)=
③化学方程式中m=
④对于该反应,能增大正反应速率的措施是
A.增大容器容积 B.移走部分Q C.通入大量X D.升高温度
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐1】铁及其化合物在生产、生活中有着广泛的应用。
(1)下图是研究海水对铁闸不同部位腐蚀情况的剖面示意图。

在图中A、B、C、D四个部位中,生成铁锈最多的部位________ (填字母)。
(2)已知t℃时,反应FeO(s)+CO(g) Fe(s)+CO2(g)的平衡常数K=0.25。则该反应的平衡常数表达式为K=
Fe(s)+CO2(g)的平衡常数K=0.25。则该反应的平衡常数表达式为K=____________ ;t℃时,反应达到平衡时n(CO):n(CO2) =_______ ;t℃时,若在1L密闭容器中加入0.02 mol FeO(s)、xmol CO,发生反应,当反应达到平衡时FeO(s)的转化率为50%,则x=________ 。
(3)高铁酸钾是一种高效、多功能的水处理剂。工业上常采用NaClO氧化法生产,有关
反应原理为:
3NaClO+2Fe(NO3)3+l0NaOH=2Na2FeO4 ↓+3NaCl+6NaNO3+5H2O
Na2FeO4+2KOH=K2FeO4+2NaOH
实验证明,反应的温度、原料的浓度及配比对高铁酸钾的产率都有影响。图1为不同的温度下,Fe(NO3)3不同质量浓度对K2FeO4生成率的影响;图2为一定温度下,NaClO不同质量浓度对K2FeO4生成率的影响。

①工业生产中,反应进行的适宜温度为_________ ℃;此时Fe(NO3)3与NaClO两种溶液的理想的质量浓度之比是____________ 。
②高铁酸钾做水处理剂时的作用主要有__________________ (答出2条即可)。
(1)下图是研究海水对铁闸不同部位腐蚀情况的剖面示意图。

在图中A、B、C、D四个部位中,生成铁锈最多的部位
(2)已知t℃时,反应FeO(s)+CO(g)
 Fe(s)+CO2(g)的平衡常数K=0.25。则该反应的平衡常数表达式为K=
Fe(s)+CO2(g)的平衡常数K=0.25。则该反应的平衡常数表达式为K=(3)高铁酸钾是一种高效、多功能的水处理剂。工业上常采用NaClO氧化法生产,有关
反应原理为:
3NaClO+2Fe(NO3)3+l0NaOH=2Na2FeO4 ↓+3NaCl+6NaNO3+5H2O
Na2FeO4+2KOH=K2FeO4+2NaOH
实验证明,反应的温度、原料的浓度及配比对高铁酸钾的产率都有影响。图1为不同的温度下,Fe(NO3)3不同质量浓度对K2FeO4生成率的影响;图2为一定温度下,NaClO不同质量浓度对K2FeO4生成率的影响。

①工业生产中,反应进行的适宜温度为
②高铁酸钾做水处理剂时的作用主要有
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】甲醇可作为燃料电池的原料。下列反应制备甲醇:CO(g)+2H2(g) CH3OH(g) △H=﹣90.8 kJ•mol-1,在一容积可变的密闭容器中充入10 mol CO 和20 mol H2,CO的平衡转化率随温度(T)、压强(P)的变化如图所示,当达到平衡状态A时,容器的体积为20 L。
CH3OH(g) △H=﹣90.8 kJ•mol-1,在一容积可变的密闭容器中充入10 mol CO 和20 mol H2,CO的平衡转化率随温度(T)、压强(P)的变化如图所示,当达到平衡状态A时,容器的体积为20 L。

(1)该反应的平衡常数表达式_______ 。若提高温度到T2,达平衡时,K值_______ (填“增大”“减小”或“不变”)。
(2)图中P1_______ P2(填“>”、“<”或“=”)。
(3)已知CO2(g)+H2(g) CO(g)+H2O(g) △H=+41.3 kJ•mol﹣1,试写出由CO2和H2制取气态甲醇和气态水的热化学方程式
CO(g)+H2O(g) △H=+41.3 kJ•mol﹣1,试写出由CO2和H2制取气态甲醇和气态水的热化学方程式_______ 。
 CH3OH(g) △H=﹣90.8 kJ•mol-1,在一容积可变的密闭容器中充入10 mol CO 和20 mol H2,CO的平衡转化率随温度(T)、压强(P)的变化如图所示,当达到平衡状态A时,容器的体积为20 L。
CH3OH(g) △H=﹣90.8 kJ•mol-1,在一容积可变的密闭容器中充入10 mol CO 和20 mol H2,CO的平衡转化率随温度(T)、压强(P)的变化如图所示,当达到平衡状态A时,容器的体积为20 L。
(1)该反应的平衡常数表达式
(2)图中P1
(3)已知CO2(g)+H2(g)
 CO(g)+H2O(g) △H=+41.3 kJ•mol﹣1,试写出由CO2和H2制取气态甲醇和气态水的热化学方程式
CO(g)+H2O(g) △H=+41.3 kJ•mol﹣1,试写出由CO2和H2制取气态甲醇和气态水的热化学方程式
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】科学家利用反应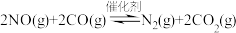 对汽车尾气进行无害化处理,一定条件下,在
对汽车尾气进行无害化处理,一定条件下,在 密闭容器中充入
密闭容器中充入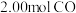 和
和 ,一段时间后测得
,一段时间后测得 、
、 浓度随时间变化如图1所示,
浓度随时间变化如图1所示, 的平衡转化率与温度、起始投料比m的关系如图2所示,图中起始投料比
的平衡转化率与温度、起始投料比m的关系如图2所示,图中起始投料比 。
。
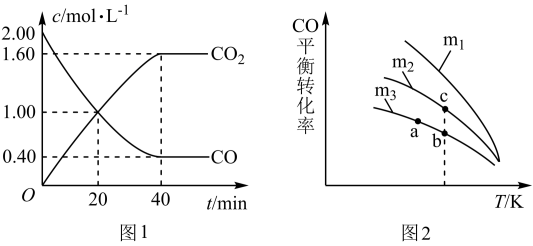
完成下列填空:
(1)氮原子最外层电子排布式为_______ ,氧原子核外能量最高的电子有_______ 个。
(2)根据图1,用 表示该反应达平衡过程中的平均反应速率是
表示该反应达平衡过程中的平均反应速率是_______ (保留小数后两位小数)。
(3)该反应的化学平衡常数表达式是_______ ,该反应的正反应是_______ 反应(填“吸热”或“放热”)。
(4)图2中a、b、c三点对应的平衡常数 、
、 、
、 相对大小关系是
相对大小关系是_______ 。
(5)关于该可逆反应的说法正确的是_______ 。
a.加入催化剂可提高 的平衡转化率
的平衡转化率
b.当体系中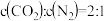 时,该反应达到平衡状态
时,该反应达到平衡状态
c.保持其他条件不变,若充入 ,则达到新平衡时,正、逆反应速率均增大
,则达到新平衡时,正、逆反应速率均增大
d.投料比: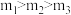
(6)随着温度的升高,不同投料比下CO的平衡转化率趋于相近的原因为_______ 。
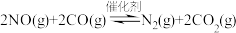 对汽车尾气进行无害化处理,一定条件下,在
对汽车尾气进行无害化处理,一定条件下,在 密闭容器中充入
密闭容器中充入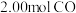 和
和 ,一段时间后测得
,一段时间后测得 、
、 浓度随时间变化如图1所示,
浓度随时间变化如图1所示, 的平衡转化率与温度、起始投料比m的关系如图2所示,图中起始投料比
的平衡转化率与温度、起始投料比m的关系如图2所示,图中起始投料比 。
。
完成下列填空:
(1)氮原子最外层电子排布式为
(2)根据图1,用
 表示该反应达平衡过程中的平均反应速率是
表示该反应达平衡过程中的平均反应速率是(3)该反应的化学平衡常数表达式是
(4)图2中a、b、c三点对应的平衡常数
 、
、 、
、 相对大小关系是
相对大小关系是(5)关于该可逆反应的说法正确的是
a.加入催化剂可提高
 的平衡转化率
的平衡转化率b.当体系中
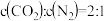 时,该反应达到平衡状态
时,该反应达到平衡状态c.保持其他条件不变,若充入
 ,则达到新平衡时,正、逆反应速率均增大
,则达到新平衡时,正、逆反应速率均增大d.投料比:
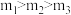
(6)随着温度的升高,不同投料比下CO的平衡转化率趋于相近的原因为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】甲醇是一种重要的可再生能源。已知:①2CH4(g)+O2(g)=2CO(g)+4H2(g)△H=akJ/mol,②CO(g)+2H2(g)=CH3OH(g)△H=bkJ/mol。
(1)写出由CH4和O2制取CH3OH(g)的热化学方程式:__ 。
(2)在80℃时,将0.4mol的四氧化二氮气体充入2L已抽空的固定容积的密闭容器中,隔一段时间对该容器内的物质进行分析,得到如下数据:
反应进行至100s后将反应混合物的温度降低,发现气体的颜色变浅。该反应的化学方程式为N2O4 2NO2。
2NO2。
①0→20s内N2O4的平均反应速率为___ 。
②该反应的平衡时的N2O4转化率为___ ,在80℃时该反应的平衡常数K值为___ (保留2位小数)。
③下列说法正确的是___ 。
A.温度越高,K值越大,N2O4的转化率越高
B.加压,平衡逆向移动,气体颜色变浅
C.增大N2O4的浓度,新平衡建立过程中正反应速率不断加快
D.起始条件相同,将等物质的量的N2O4分别在A、B两个相同的容器中反应建立平衡,A保持恒温、恒容;B保持恒温、恒压,达到平衡后,A中的N2O4平衡转化率小于B
④反应平衡后压强是反应开始压强的__ 倍、与反应开始相比,到平衡时容器中平均相对分子质量___ 。(填增大或减小或不变)
(1)写出由CH4和O2制取CH3OH(g)的热化学方程式:
(2)在80℃时,将0.4mol的四氧化二氮气体充入2L已抽空的固定容积的密闭容器中,隔一段时间对该容器内的物质进行分析,得到如下数据:
| 时间(s) | 0 | 20 | 40 | 60 | 80 | 100 |
| c(N2O4) | 0.20 | a | 0.10 | c | d | e |
| c(NO2) | 0.00 | 0.12 | b | 0.22 | 0.22 | 0.22 |
 2NO2。
2NO2。①0→20s内N2O4的平均反应速率为
②该反应的平衡时的N2O4转化率为
③下列说法正确的是
A.温度越高,K值越大,N2O4的转化率越高
B.加压,平衡逆向移动,气体颜色变浅
C.增大N2O4的浓度,新平衡建立过程中正反应速率不断加快
D.起始条件相同,将等物质的量的N2O4分别在A、B两个相同的容器中反应建立平衡,A保持恒温、恒容;B保持恒温、恒压,达到平衡后,A中的N2O4平衡转化率小于B
④反应平衡后压强是反应开始压强的
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】某学习小组同学研究过氧化氢溶液与氢碘酸的反应,查到一组室温时的实验数据如表所示。
(1)过氧化氢溶液与氢碘酸反应的化学方程式为_______ 。
(2)由表中编号为①②③的实验数据得到的结论是_______ 。
(3)若该反应的速率方程可表示为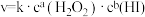 ,对比表中数据可知
,对比表中数据可知
_______ ,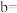
_______ 。
(4)资料显示编号①的反应进行至 时,测得氢碘酸的浓度为
时,测得氢碘酸的浓度为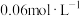 ,此时
,此时 的转化率为
的转化率为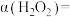
_______  。
。
(5)该小组同学将实验编号④的温度升高,发现到一定温度时,溶液出现棕黄色所需时间变长,可能的原因_______ 。
| 实验编号 | ① | ② | ③ | ④ | ⑤ |
 | 0.1 | 0.1 | 0.1 | 0.2 | 0.3 |
 | 0.1 | 0.2 | 0.3 | 0.1 | 0.1 |
从混合至溶液出现棕黄色的时间 | 13 | 6.5 | 4.3 | 6.6 | 4.4 |
(2)由表中编号为①②③的实验数据得到的结论是
(3)若该反应的速率方程可表示为
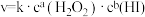 ,对比表中数据可知
,对比表中数据可知
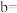
(4)资料显示编号①的反应进行至
 时,测得氢碘酸的浓度为
时,测得氢碘酸的浓度为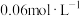 ,此时
,此时 的转化率为
的转化率为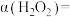
 。
。(5)该小组同学将实验编号④的温度升高,发现到一定温度时,溶液出现棕黄色所需时间变长,可能的原因
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】以煤为原料可合成一系列燃料。回答下列问题:
(1)向1L恒容密闭容器中加入2mol CO、4mol H2,在适当的催化剂作用下,发生反应:2CO(g)+4H2(g) CH3OCH3(l)+H2O(l) △H=+71kJ·mol-l
CH3OCH3(l)+H2O(l) △H=+71kJ·mol-l
①该反应_______ 自发进行(填“能”、“不能”或“无法判断”);
②下列叙述能说明此反应达到平衡状态的是_______ 。
a.混合气体的平均相对分子质量保持不变
b.CO和H2的转化率相等
c.CO和H2的体积分数保持不变
d.混合气体的密度保持不变
e.1mol CO生成的同时有1mol O-H 键断裂
(2)CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H<0,在一定条件下,某反应过程中部分数据如下表:
CH3OH(g)+H2O(g) △H<0,在一定条件下,某反应过程中部分数据如下表:
①0~10min内,用H2O(g)表示的化学反应速率v(H2O)=_______ mol/(L ·min)。
②T1℃,该反应的平衡常数K=_______ (用分数表示),平衡时H2的转化率是_______ 。
③在其它条件不变的情况下,若30min时改变温度为T2℃,再次平衡时H2的物质的量为3.2mol,则T1_______ T2(填“>”“<”或“=”),理由是_______ ; 在其他条件不变的情况下,若30min时向容器中再充入1mol CO2(g)和1mol H2O(g),则平衡_______ 移动(填“正向”、“逆向”或“不”)。
(1)向1L恒容密闭容器中加入2mol CO、4mol H2,在适当的催化剂作用下,发生反应:2CO(g)+4H2(g)
 CH3OCH3(l)+H2O(l) △H=+71kJ·mol-l
CH3OCH3(l)+H2O(l) △H=+71kJ·mol-l①该反应
②下列叙述能说明此反应达到平衡状态的是
a.混合气体的平均相对分子质量保持不变
b.CO和H2的转化率相等
c.CO和H2的体积分数保持不变
d.混合气体的密度保持不变
e.1mol CO生成的同时有1mol O-H 键断裂
(2)CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H<0,在一定条件下,某反应过程中部分数据如下表:
CH3OH(g)+H2O(g) △H<0,在一定条件下,某反应过程中部分数据如下表:| 反应条件 | 反应时间 | CO2/mol | H2/mol | CH3OH/mol | H2O/mol |
| 恒温恒容(T1℃、2L) | 0min | 2 | 6 | 0 | 0 |
| 10min | 4.5 | ||||
| 20min | 1 | ||||
| 30min | 1 |
②T1℃,该反应的平衡常数K=
③在其它条件不变的情况下,若30min时改变温度为T2℃,再次平衡时H2的物质的量为3.2mol,则T1
您最近一年使用:0次



