某实验小组通过铁与盐酸反应的实验,研究影响反应速率的因素(铁的质量相等,铁块的形状一样,盐酸均过量),设计实验如下表:
(1)若四组实验均反应1分钟(铁有剩余),则以上实验需要测出的数据是___________ 。
(2)实验___________ 和___________ (填实验编号)是研究盐酸的浓度对该反应速率的影响;实验1和2是研究___________ 对该反应速率的影响。
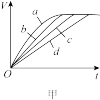
(3)测定在不同时间产生氢气体积V的数据,绘制出图甲,则曲线c、d分别对应的实验组别可能是___________ 、___________ 。
(4)分析其中一组实验,发现产生氢气的速率随时间变化情况如图乙所示。
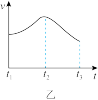
①其中t1~t2速率变化的主要原因是___________ 。
②t2~t3速率变化的主要原因是___________ 。
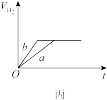
(5)实验1产生氢气的体积如图丙中的曲线a,添加某试剂能使曲线a变为曲线b的是___________(填序号)。
(6)在2 L密闭容器中进行反应:mX(g)+nY(g) pZ(g)+qQ(g),式中m、n、p、q为化学计量数。在0~3 min内,各物质的物质的量的变化如下表所示:
pZ(g)+qQ(g),式中m、n、p、q为化学计量数。在0~3 min内,各物质的物质的量的变化如下表所示:
已知:2 min内v(Q)=0.075 mol/(L·min),v(Z):v(Y)=1:2。
请回答下列问题:
①2 min内Z的反应速率v(Z)=___________ 。
②起始时n(Y)=___________ 、n(Q)=___________ 。
③化学方程式中m=___________ 、n=___________ 、p=___________ 、q=___________ 。
④对于该反应,能增大正反应速率的措施是___________ (填序号)。
A.增大容器容积 B.移走部分Q C.通入大量X D.升高温度
| 实验编号 | 盐酸浓度/(mol/L) | 铁的形态 | 温度/K |
| 1 | 4.00 | 块状 | 293 |
| 2 | 4.00 | 粉末 | 293 |
| 3 | 2.00 | 块状 | 293 |
| 4 | 2.00 | 粉末 | 313 |
(2)实验
(3)测定在不同时间产生氢气体积V的数据,绘制出图甲,则曲线c、d分别对应的实验组别可能是

(4)分析其中一组实验,发现产生氢气的速率随时间变化情况如图乙所示。

①其中t1~t2速率变化的主要原因是
②t2~t3速率变化的主要原因是
(5)实验1产生氢气的体积如图丙中的曲线a,添加某试剂能使曲线a变为曲线b的是___________(填序号)。

| A.CuO粉末 | B.NaNO3固体 | C.NaCl溶液 | D.浓H2SO4 |
 pZ(g)+qQ(g),式中m、n、p、q为化学计量数。在0~3 min内,各物质的物质的量的变化如下表所示:
pZ(g)+qQ(g),式中m、n、p、q为化学计量数。在0~3 min内,各物质的物质的量的变化如下表所示:| 物质 | X | Y | Z | Q |
| n(起始)/mol | 0.7 | 1.0 | ||
| n(2 min末)/mol | 0.8 | 2.7 | 0.8 | 2.7 |
| n(3 min末)/mol | 0.8 |
请回答下列问题:
①2 min内Z的反应速率v(Z)=
②起始时n(Y)=
③化学方程式中m=
④对于该反应,能增大正反应速率的措施是
A.增大容器容积 B.移走部分Q C.通入大量X D.升高温度
更新时间:2022-09-17 08:44:59
|
相似题推荐
【推荐1】将二氧化碳转化为绿色液体燃料甲醇(CH3OH)是实现碳中和的一个重要途径。
I.我国科学家在含铂高效催化剂作用下把二氧化碳高效转化为清洁液态燃料――甲醇。
(1)该法利用CO₂制取甲醇的有关化学反应如下:
①CO2(g)+3H2(g) CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)  =-178kJ/mol
=-178kJ/mol
②2CO(g)+O2(g) 2CO2(g)
2CO2(g)  =-566kJ/mol
=-566kJ/mol
③2H2(g)+O2(g) 2H2O(g)
2H2O(g)  =-483.6kJ/mol
=-483.6kJ/mol
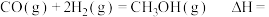
_____ 
Ⅱ.甲醇的制备原理为:CO2(g)+3H2(g) CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)  =-178kJ/mol
=-178kJ/mol
(2)对于该反应,可以同时提高反应速率和CH3OH产率的措施有_____(填字母序号)。
(3)为探究CO2(g)+3H2(g) CH3OH(g)+H2O(g)的反应原理,进行如下实验:在一恒温,体积为2L恒容密闭容器中,充入1molCO2和4molH2,初始压强为8MPa,进行该反应(不考虑其它副反应)。10min时测得体系的压强为6.4MPa且不再随时间变化。回答下列问题:
CH3OH(g)+H2O(g)的反应原理,进行如下实验:在一恒温,体积为2L恒容密闭容器中,充入1molCO2和4molH2,初始压强为8MPa,进行该反应(不考虑其它副反应)。10min时测得体系的压强为6.4MPa且不再随时间变化。回答下列问题:
①反应开始到10min时,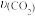 =
= _____ 。
②10min时,体系中CH₃OH的物质的量分数为_____ %。
③该温度下的压强平衡常数
_____ 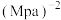 (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(4)某科研小组研究不同催化剂对反应CO2(g)+3H2(g) CH3OH(g)+H2O(g)的影响,按:n(CO2):n(H2)=1:3投料,不同催化剂作用下,反应tmin时,CH3OH的产率随温度的变化如图所示:
CH3OH(g)+H2O(g)的影响,按:n(CO2):n(H2)=1:3投料,不同催化剂作用下,反应tmin时,CH3OH的产率随温度的变化如图所示:
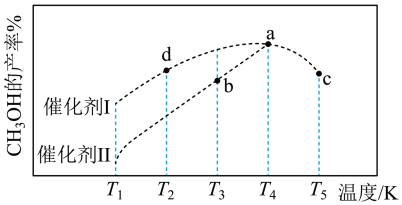
①催化剂效果最佳的是_____ (填“催化剂I”、“催化剂Ⅱ”),理由是_____ 。
②d点 (逆)
(逆)_____ a点 (逆)(填“>”、“<”或“=”)。
(逆)(填“>”、“<”或“=”)。
I.我国科学家在含铂高效催化剂作用下把二氧化碳高效转化为清洁液态燃料――甲醇。
(1)该法利用CO₂制取甲醇的有关化学反应如下:
①CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)  =-178kJ/mol
=-178kJ/mol ②2CO(g)+O2(g)
 2CO2(g)
2CO2(g)  =-566kJ/mol
=-566kJ/mol ③2H2(g)+O2(g)
 2H2O(g)
2H2O(g)  =-483.6kJ/mol
=-483.6kJ/mol 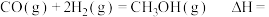

Ⅱ.甲醇的制备原理为:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)  =-178kJ/mol
=-178kJ/mol(2)对于该反应,可以同时提高反应速率和CH3OH产率的措施有_____(填字母序号)。
| A.升高反应温度 | B.使用高效催化剂 |
| C.增大体系压强 | D.移走CH3OH |
(3)为探究CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)的反应原理,进行如下实验:在一恒温,体积为2L恒容密闭容器中,充入1molCO2和4molH2,初始压强为8MPa,进行该反应(不考虑其它副反应)。10min时测得体系的压强为6.4MPa且不再随时间变化。回答下列问题:
CH3OH(g)+H2O(g)的反应原理,进行如下实验:在一恒温,体积为2L恒容密闭容器中,充入1molCO2和4molH2,初始压强为8MPa,进行该反应(不考虑其它副反应)。10min时测得体系的压强为6.4MPa且不再随时间变化。回答下列问题:①反应开始到10min时,
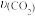 =
= ②10min时,体系中CH₃OH的物质的量分数为
③该温度下的压强平衡常数

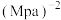 (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。(4)某科研小组研究不同催化剂对反应CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)的影响,按:n(CO2):n(H2)=1:3投料,不同催化剂作用下,反应tmin时,CH3OH的产率随温度的变化如图所示:
CH3OH(g)+H2O(g)的影响,按:n(CO2):n(H2)=1:3投料,不同催化剂作用下,反应tmin时,CH3OH的产率随温度的变化如图所示:
①催化剂效果最佳的是
②d点
 (逆)
(逆) (逆)(填“>”、“<”或“=”)。
(逆)(填“>”、“<”或“=”)。
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】酸碱中和滴定、氧化还原滴定和沉淀滴定法在科研和工业生产中都很重要。
I.为了测定草酸(H2C2O4)溶液的浓度,进行如下实验:取25.00mL草酸溶液于锥形瓶内,加入适量稀H2SO4,用0.0100mol/LKMnO4溶液滴定。发生的反应:2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O。试回答:
(1)滴定终点时的现象:_______ 。
(2)若在接近滴定终点时,用少量蒸馏水将锥形瓶内壁冲洗一下,再继续滴至终点,则所测得c(H2C2O4)_______ (填“偏大”、“偏小”或“无影响”)。
(3)在滴定过程中若用去KMnO4溶液体积V数据如下,则所配制的草酸溶液的物质的量浓度为_______ mol/L。
(4)若将KMnO4与稍过量的草酸溶液直接混合,发现开始时变色不明显,但一会后突然Ag2CrO4褪色,猜测其原因是:_______ 。
II.莫尔法是一种沉淀滴定法,以K2CrO4为指示剂,用标准硝酸银溶液滴定待测液,进行测定溶液中Cl-的浓度。已知常温下Ksp数值如下表。回答下列问题:
(5)当溶液中的Cl-恰好沉淀完全(浓度为1.0×10-5mol/L)时,溶液中的c(Ag+)=_______ mol/L,c(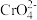 )=
)=_______ mol/L。
(6)若用AgNO3溶液滴定NaSCN溶液,可选为滴定指示剂的是_______。
I.为了测定草酸(H2C2O4)溶液的浓度,进行如下实验:取25.00mL草酸溶液于锥形瓶内,加入适量稀H2SO4,用0.0100mol/LKMnO4溶液滴定。发生的反应:2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2↑+8H2O。试回答:
(1)滴定终点时的现象:
(2)若在接近滴定终点时,用少量蒸馏水将锥形瓶内壁冲洗一下,再继续滴至终点,则所测得c(H2C2O4)
(3)在滴定过程中若用去KMnO4溶液体积V数据如下,则所配制的草酸溶液的物质的量浓度为
| 实验编号 | V始(mL) | V终(mL) | V(mL) |
| 1 | 1.00 | 13.05 | ? |
| 2 | 0.50 | 12.45 | ? |
| 3 | 0.70 | 15.70 | ? |
II.莫尔法是一种沉淀滴定法,以K2CrO4为指示剂,用标准硝酸银溶液滴定待测液,进行测定溶液中Cl-的浓度。已知常温下Ksp数值如下表。回答下列问题:
| AgCl | AgBr | AgCN | Ag2CrO4 | AgSCN | |
| 颜色 | 白色 | 浅黄色 | 白色 | 砖红色 | 白色 |
| Ksp | 1.8×10-10 | 5.4×10-13 | 1.2×10-16 | 9.0×10-12 | 1.0×10-12 |
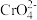 )=
)=(6)若用AgNO3溶液滴定NaSCN溶液,可选为滴定指示剂的是_______。
| A.NaCl | B.KBr | C.Na2CrO4 | D.NaCN |
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】尿素[CO(NH2)2],又称碳酰胺,是目前含氨量较高的氮肥,适用于各种土壤和植物。
已知:
①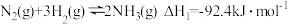
②
③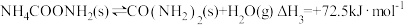
(1)请写出由N2、H2和CO2合成尿素的热化学方程式:_______ 。
(2)相比③,若②的反应速率更快,下列示意图_______(填标号)最能体现②③反应过程的能量变化。
(3)在某温度下,将NH3和CO2以物质的量之比2∶1置于一恒容密闭容器中反应: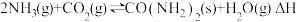 ,NH3的转化率随时间变化关系如图所示。t1时反应达到平衡,此时的压强为p MPa。
,NH3的转化率随时间变化关系如图所示。t1时反应达到平衡,此时的压强为p MPa。
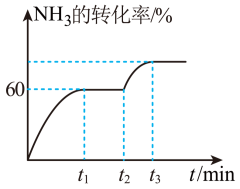
①下列说法能判断该反应达到平衡状态的是_______ (填标号)。
A.容器压强不变
B.消耗1 mol CO2时,生成1 mol H2O
C.容器内n(C)与n(N)的比值不发生变化
D.混合气体的平均摩尔质量不变
②t1时反应达到平衡,CO2的体积分数为_______ (保留三位有效数字),c(NH3):c(CO2):c(H2O)=_______ ;平衡常数Kp=_______ 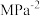 (Kp为以分压表示的平衡常数,分压=总压×物质的量分数)。
(Kp为以分压表示的平衡常数,分压=总压×物质的量分数)。
③向平衡后的反应体系中再通入2 molNH3,Kp将_______ (填“增大”、“减小”或“不变”)。
④图中t2时,NH3的转化率发生改变,此时改变的反应条件是_______ (请写出任意一条)。
已知:
①
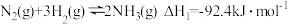
②

③
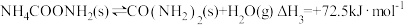
(1)请写出由N2、H2和CO2合成尿素的热化学方程式:
(2)相比③,若②的反应速率更快,下列示意图_______(填标号)最能体现②③反应过程的能量变化。
A.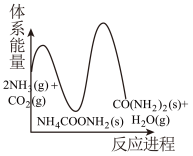 | B.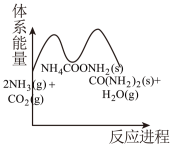 |
C.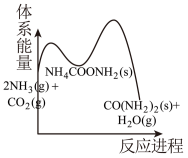 | D.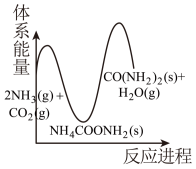 |
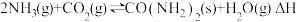 ,NH3的转化率随时间变化关系如图所示。t1时反应达到平衡,此时的压强为p MPa。
,NH3的转化率随时间变化关系如图所示。t1时反应达到平衡,此时的压强为p MPa。
①下列说法能判断该反应达到平衡状态的是
A.容器压强不变
B.消耗1 mol CO2时,生成1 mol H2O
C.容器内n(C)与n(N)的比值不发生变化
D.混合气体的平均摩尔质量不变
②t1时反应达到平衡,CO2的体积分数为
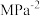 (Kp为以分压表示的平衡常数,分压=总压×物质的量分数)。
(Kp为以分压表示的平衡常数,分压=总压×物质的量分数)。③向平衡后的反应体系中再通入2 molNH3,Kp将
④图中t2时,NH3的转化率发生改变,此时改变的反应条件是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】I.请回答下列问题:把A、B、C、D四种金属按表中装置进行实验。
(1)根据表中信息判断四种金属活动性由大到小的顺序是_______ ;写出装置乙中正极的电极反应式:_______ 。
(2)若甲池中电极A为Zn、电极B为Cu、该装置工作时, 向
向_______ (填“A”或“B”极移动,经过一段时间后,若导线中转移了0.4mol电子,则产生的气体在标准状况下的体积为_______ L。如果该反应太剧烈,为了减缓反应速率而又不减少产生氢气的量,该同学在烧杯中分别加入等体积的下列液体,你认为可行的是_______ (填字母)。
A.蒸馏水 B.NaCl溶液 C.Na2CO3溶液 D.KNO3溶液
II.某温度时,在2L恒容密闭容器中,发生反应2M(g)+N(g) 2R(g),A、B气体的物质的量随时间变化的曲线如图,回答下列问题:
2R(g),A、B气体的物质的量随时间变化的曲线如图,回答下列问题:
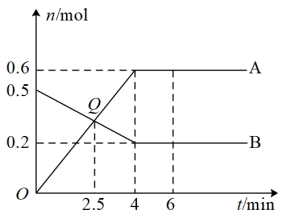
(3)B为_______ (填“M”“N”或“R”)。
(4)Q点时,正、逆反应速率的大小关系为
_______ (填“>”“<”或“=”) 。
。
(5)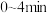 内,该反应的平均反应速率
内,该反应的平均反应速率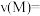
_______  。
。
(6)平衡时N的转化率为_______
(7)在某绝热恒容密闭反应器中入2molM、1molN,发生反应2M(g)+N(g) 2R(g),反应速率随时间的变化的曲线如图。
2R(g),反应速率随时间的变化的曲线如图。

①由图可推知,该反应是_______ (填“吸热”或“放热”)反应。
②t2后反应速率降低的原因是_______ 。
| 装置 | 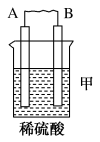 | 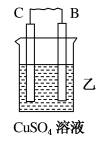 | 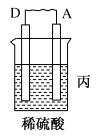 |
| 电子从A到B | C电极的质量增加 | 二价金属D不断溶解 |
(2)若甲池中电极A为Zn、电极B为Cu、该装置工作时,
 向
向A.蒸馏水 B.NaCl溶液 C.Na2CO3溶液 D.KNO3溶液
II.某温度时,在2L恒容密闭容器中,发生反应2M(g)+N(g)
 2R(g),A、B气体的物质的量随时间变化的曲线如图,回答下列问题:
2R(g),A、B气体的物质的量随时间变化的曲线如图,回答下列问题:
(3)B为
(4)Q点时,正、逆反应速率的大小关系为

 。
。(5)
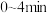 内,该反应的平均反应速率
内,该反应的平均反应速率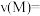
 。
。(6)平衡时N的转化率为
(7)在某绝热恒容密闭反应器中入2molM、1molN,发生反应2M(g)+N(g)
 2R(g),反应速率随时间的变化的曲线如图。
2R(g),反应速率随时间的变化的曲线如图。
①由图可推知,该反应是
②t2后反应速率降低的原因是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】Ⅰ.如图表示在密闭容器中反应:


(1)达到平衡时,由于条件改变而引起反应速率和化学平衡的变化情况,ab过程中改变的条件可能是___________ ;bc过程中改变条件可能是___________ 。
Ⅱ.某温度时,在2 L容器中X、Y、Z三种物质的量随时间的变化关系曲线如图所示。

(2)由图中的数据分析,该反应的化学方程式为___________ 。
(3)反应开始至2min、5min时Z的平均反应速率为___________ 、___________ 。
(4)5min后Z的生成速率比5min末Z的生成速率___________ (填“大”、“小”或“相等)



(1)达到平衡时,由于条件改变而引起反应速率和化学平衡的变化情况,ab过程中改变的条件可能是
Ⅱ.某温度时,在2 L容器中X、Y、Z三种物质的量随时间的变化关系曲线如图所示。

(2)由图中的数据分析,该反应的化学方程式为
(3)反应开始至2min、5min时Z的平均反应速率为
(4)5min后Z的生成速率比5min末Z的生成速率
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】一定温度下,在2 L恒容密闭容器中投入一定量A、B,发生反应:3A(g)+bB(g)  cC(g),12 s时生成0.8 mol C,A、B物质的量变化如下图。
cC(g),12 s时生成0.8 mol C,A、B物质的量变化如下图。
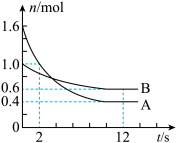
(1)反应进行至2s时,反应向________ 进行。(填“正向”或“逆向”),用A物质浓度变化来表示化学反应速率为________ 。
(2)平衡后向容器中充入Ne,反应速率________ 。(填“增大”、“减小”或“不变”)
(3)反应进行至12s时,正反应速率________ 逆反应速率(填“>”、“<”或“=”)
(4)请计算系数b的值为________ 。
(5)若混合气体密度不变时能说明该反应达平衡状态了吗?________ (填“能”或“不能”)
 cC(g),12 s时生成0.8 mol C,A、B物质的量变化如下图。
cC(g),12 s时生成0.8 mol C,A、B物质的量变化如下图。
(1)反应进行至2s时,反应向
(2)平衡后向容器中充入Ne,反应速率
(3)反应进行至12s时,正反应速率
(4)请计算系数b的值为
(5)若混合气体密度不变时能说明该反应达平衡状态了吗?
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐1】合成氨技术的创立开辟了人工固氮的重要途径,通常用以铁为主的催化剂在400~500℃和10~30MPa的条件下,由氮气和氢气直接合成氨。
(1)“哈伯法”合成氨的反应: △H,相关键能数据如下表:
△H,相关键能数据如下表:
①△H=_______ kJ・mol-1。
②在恒温恒容密闭容器中进行的工业合成氨反应,下列能表示达到平衡状态的是_______ (填序号)。
A.单位时间内断开3a个H—H键的同时形成6a个N—H键
B.混合气体的平均相对分子质量不再发生变化
C.混合气体的密度不再发生变化
D.反应容器中N2、NH3的物质的量的比值不再发生变化
③工业生产必须对原料气进行净化的目的是_______
④向密闭容器中按1:3体积比通入N2和H2,反应达平衡时NH3的体积分数为25.0%,则N2的平衡转化率α(N2)=_______ 。
(2)“球磨法”是在温和的条件下(45℃和1bar,1bar≈100kPa)合成氨,氨的最终体积分数可高达82.5%。该法分为两个步骤(如下图):第一步,铁粉在球磨过程中被反复剧烈碰撞而活化,产生高密度的缺陷,氮分子被吸附在这些缺陷上([Fe(N*)]),有助于氮分子的解离。第二步,N*发生加氢反应得到NHx*(x=1~3),剧烈碰撞中,NHx*从催化剂表面脱附得到产物氨。

①“球磨法”与“哈伯法”相比较,下列说法中正确的是_______ (选填标号)。
A.催化剂(Fe)缺陷密度越高,N2的吸附率越高
B.“哈伯法”采用高温主要用于解离氮氮三键,而“球磨法”不用解离氮氮三键
C.“球磨法”中“剧烈碰撞”仅仅为了产生“活化缺陷”
D.“球磨法”不采用高压,是因为低压产率已经较高,加压会增大成本
②机械碰撞有助于催化剂缺陷的形成,而摩擦生热会使体系温度升高。如图是N2吸附量、体系温度随球磨转速变化曲线,则应选择的最佳转速约_______ 转/min。

(1)“哈伯法”合成氨的反应:
 △H,相关键能数据如下表:
△H,相关键能数据如下表:化学键 | N≡N | H-H | N-H |
| 键能(kJ∙mol-1) | 946.0 | 436.0 | 390.8 |
②在恒温恒容密闭容器中进行的工业合成氨反应,下列能表示达到平衡状态的是
A.单位时间内断开3a个H—H键的同时形成6a个N—H键
B.混合气体的平均相对分子质量不再发生变化
C.混合气体的密度不再发生变化
D.反应容器中N2、NH3的物质的量的比值不再发生变化
③工业生产必须对原料气进行净化的目的是
④向密闭容器中按1:3体积比通入N2和H2,反应达平衡时NH3的体积分数为25.0%,则N2的平衡转化率α(N2)=
(2)“球磨法”是在温和的条件下(45℃和1bar,1bar≈100kPa)合成氨,氨的最终体积分数可高达82.5%。该法分为两个步骤(如下图):第一步,铁粉在球磨过程中被反复剧烈碰撞而活化,产生高密度的缺陷,氮分子被吸附在这些缺陷上([Fe(N*)]),有助于氮分子的解离。第二步,N*发生加氢反应得到NHx*(x=1~3),剧烈碰撞中,NHx*从催化剂表面脱附得到产物氨。

①“球磨法”与“哈伯法”相比较,下列说法中正确的是
A.催化剂(Fe)缺陷密度越高,N2的吸附率越高
B.“哈伯法”采用高温主要用于解离氮氮三键,而“球磨法”不用解离氮氮三键
C.“球磨法”中“剧烈碰撞”仅仅为了产生“活化缺陷”
D.“球磨法”不采用高压,是因为低压产率已经较高,加压会增大成本
②机械碰撞有助于催化剂缺陷的形成,而摩擦生热会使体系温度升高。如图是N2吸附量、体系温度随球磨转速变化曲线,则应选择的最佳转速约

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】工业合成氨是人类科学技术的一项重大突破,我国目前氨的生产能力位居世界首位。其合成原理为:
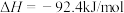
 。
。
(1)合成氨及其衍生工业是化工生产的重要门类,某工厂用下图流程合成氨及其含氮产物:
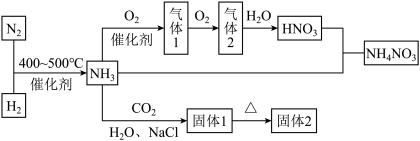
上流程中气体2为___________ ,在饱和 溶液中先通入过量
溶液中先通入过量 再通入过量
再通入过量 可得到固体
可得到固体___________ ;
(2)合成氨反应在常温下___________ (填“能”或“不能”)自发;
(3)在恒温恒容密闭容器中充入
 和
和
 进行合成氨的反应,下列能说明该反应已达平衡状态的是
进行合成氨的反应,下列能说明该反应已达平衡状态的是___________ ;
a.断裂
 同时生成
同时生成

b.容器内压强保持不变
c.混合气体密度保持不变
d。容器内 、
、 、
、 物质的量之比为1:3:2
物质的量之比为1:3:2
e. 的百分含量保持不变
的百分含量保持不变
(4)研究表明,合成氨反应在Fe催化剂上可能通过下图机理进行(*表示催化剂表面吸附位, 表示被吸附于催化剂表面的
表示被吸附于催化剂表面的 )。
)。
(ⅰ)
(ⅱ)
(ⅲ)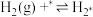
(ⅳ)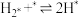
(ⅴ)
……
(…)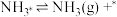
判断上述反应机理中,速率控制步骤(即速率最慢步骤)为___________ (填步骤前的标号),理由是___________ 。
(5)基于 载氮体的碳基化学链合成氨技术示反应如下:
载氮体的碳基化学链合成氨技术示反应如下:
吸氮反应:
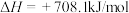
释氮反应:
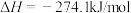
在温度为T、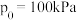 恒压条件下进行吸氮反应,平衡时氮气转化率为50%,分压平衡常数
恒压条件下进行吸氮反应,平衡时氮气转化率为50%,分压平衡常数
___________  。
。

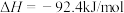
 。
。(1)合成氨及其衍生工业是化工生产的重要门类,某工厂用下图流程合成氨及其含氮产物:

上流程中气体2为
 溶液中先通入过量
溶液中先通入过量 再通入过量
再通入过量 可得到固体
可得到固体(2)合成氨反应在常温下
(3)在恒温恒容密闭容器中充入

 和
和
 进行合成氨的反应,下列能说明该反应已达平衡状态的是
进行合成氨的反应,下列能说明该反应已达平衡状态的是a.断裂

 同时生成
同时生成

b.容器内压强保持不变
c.混合气体密度保持不变
d。容器内
 、
、 、
、 物质的量之比为1:3:2
物质的量之比为1:3:2e.
 的百分含量保持不变
的百分含量保持不变(4)研究表明,合成氨反应在Fe催化剂上可能通过下图机理进行(*表示催化剂表面吸附位,
 表示被吸附于催化剂表面的
表示被吸附于催化剂表面的 )。
)。(ⅰ)

(ⅱ)

(ⅲ)
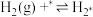
(ⅳ)
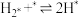
(ⅴ)

……
(…)
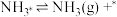
判断上述反应机理中,速率控制步骤(即速率最慢步骤)为
(5)基于
 载氮体的碳基化学链合成氨技术示反应如下:
载氮体的碳基化学链合成氨技术示反应如下:吸氮反应:

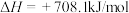
释氮反应:

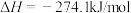
在温度为T、
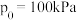 恒压条件下进行吸氮反应,平衡时氮气转化率为50%,分压平衡常数
恒压条件下进行吸氮反应,平衡时氮气转化率为50%,分压平衡常数
 。
。
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】按要求回答问题:
(1)乙烷(C2H6)燃料电池是一种高效无污染的清洁电池,以稀H2SO4为电解质溶液形成的燃料电池中:
① 向
向_______ 极移动(填“正”或“负”)。
②写出燃料电池负极反应方程式是_______ 。
③下列装置中能够组成原电池的是_______ (填序号)。

(2)如图是1molNO2(g)和1molCO(g)反应生成1molCO2(g)和1molNO(g)过程中能量变化示意图。
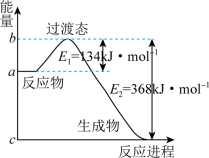
则该反应生成1molNO_______ (填“吸收”或“放出”)_______ kJ热量。
(3)一定温度下,在固定容积为2L的密闭容器中进行反应:aN(g)⇌bM(g)+cP(g),M、N、P的物质的量随时间变化的曲线如图所示:
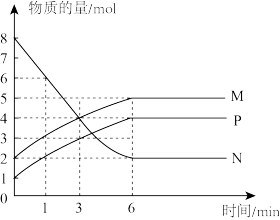
①反应化学方程式中各物质的系数比为a︰b︰c=_______ 。
②1min到3min这段时刻,以M的浓度变化表示的平均反应速率为_______ ,平衡时混合气体中M的体积分数为_______ (保留三位有效数字)。
③下列各项中说明上述反应达到化学平衡状态的是_______ (填字母)。
A.混合气体的密度不变 B.容器内的压强保持不变
C.P的浓度保持不变 D.生成1molN和同时生成0.5molM
(1)乙烷(C2H6)燃料电池是一种高效无污染的清洁电池,以稀H2SO4为电解质溶液形成的燃料电池中:
①
 向
向②写出燃料电池负极反应方程式是
③下列装置中能够组成原电池的是

(2)如图是1molNO2(g)和1molCO(g)反应生成1molCO2(g)和1molNO(g)过程中能量变化示意图。

则该反应生成1molNO
(3)一定温度下,在固定容积为2L的密闭容器中进行反应:aN(g)⇌bM(g)+cP(g),M、N、P的物质的量随时间变化的曲线如图所示:

①反应化学方程式中各物质的系数比为a︰b︰c=
②1min到3min这段时刻,以M的浓度变化表示的平均反应速率为
③下列各项中说明上述反应达到化学平衡状态的是
A.混合气体的密度不变 B.容器内的压强保持不变
C.P的浓度保持不变 D.生成1molN和同时生成0.5molM
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】五氧化二氮(N2O5)是一种绿色硝化剂,在军用炸药、火箭推进剂、医药等工业中得到广泛应用。常温下N2O5为白色固体,可溶于二氯甲烷等氯代烃溶剂,微溶于水且与水反应生成硝酸,高于室温时不稳定。回答下列问题:
(1)1840年,Devill将干燥的氯气通入无水硝酸银中,首次制得了固体N2O5。该反应的氧化产物为空气中的主要成分之一,写出反应的化学方程式:_______ 。
(2)某化学兴趣小组设计用臭氧(O3)氧化法制备N2O5,反应原理为 N2O4+O3→N2O5+O2。实验装置如下图:
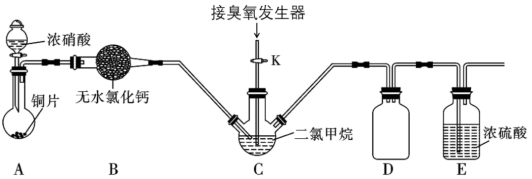
装置B的仪器名称是_______ ;装置E的作用是_______ 。实验时,先将三口烧瓶C浸入_______ (填字母编号)中,打开装置A中分液漏斗的活塞,随即关闭。一段时间后C中液体变为红棕色。然后打开活塞K,通过臭氧发生器向三口烧瓶中通入含有臭氧的氧气。
a.热水 b.冰水 c.自来水 d.饱和食盐水
(3)C中二氯甲烷(CH2Cl2)的作用是_______ (填字母编号)。判断C中反应已结束的简单方法是_______ 。
a.溶解反应物NO2 b.充分混合反应物使其反应更加充分 c.控制O3的通入速度 d.溶解生成物N2O5
(4)该装置存在一处明显缺陷,请指出_______ 。
(5)N2O5粗产品中常含有N2O4。该兴趣小组用滴定法测定N2O5粗产品的纯度。取2.0g粗产品,加入20.00mL 0.1250mol·L-1酸性高锰酸钾溶液。充分反应后,用0.1000mol·L-1 H2O2溶液滴定剩余的高锰酸钾,达到滴定终点时,消耗H2O2溶液17.50mL。已知:N2O4与KMnO4发生反应的离子方程式为5N2O4+2MnO +2H2O→Mn2++10NO
+2H2O→Mn2++10NO +4H+,H2O2与KMnO4发生反应的离子方程式为5H2O2+2MnO
+4H+,H2O2与KMnO4发生反应的离子方程式为5H2O2+2MnO +6H+→2Mn2++5O2↑+8H2O,H2O2与HNO3不反应且不考虑其分解。判断滴定到达终点的方法是
+6H+→2Mn2++5O2↑+8H2O,H2O2与HNO3不反应且不考虑其分解。判断滴定到达终点的方法是_______ 。粗产品的纯度为_______ (结果保留三位有效数字)。
(1)1840年,Devill将干燥的氯气通入无水硝酸银中,首次制得了固体N2O5。该反应的氧化产物为空气中的主要成分之一,写出反应的化学方程式:
(2)某化学兴趣小组设计用臭氧(O3)氧化法制备N2O5,反应原理为 N2O4+O3→N2O5+O2。实验装置如下图:

装置B的仪器名称是
a.热水 b.冰水 c.自来水 d.饱和食盐水
(3)C中二氯甲烷(CH2Cl2)的作用是
a.溶解反应物NO2 b.充分混合反应物使其反应更加充分 c.控制O3的通入速度 d.溶解生成物N2O5
(4)该装置存在一处明显缺陷,请指出
(5)N2O5粗产品中常含有N2O4。该兴趣小组用滴定法测定N2O5粗产品的纯度。取2.0g粗产品,加入20.00mL 0.1250mol·L-1酸性高锰酸钾溶液。充分反应后,用0.1000mol·L-1 H2O2溶液滴定剩余的高锰酸钾,达到滴定终点时,消耗H2O2溶液17.50mL。已知:N2O4与KMnO4发生反应的离子方程式为5N2O4+2MnO
 +2H2O→Mn2++10NO
+2H2O→Mn2++10NO +4H+,H2O2与KMnO4发生反应的离子方程式为5H2O2+2MnO
+4H+,H2O2与KMnO4发生反应的离子方程式为5H2O2+2MnO +6H+→2Mn2++5O2↑+8H2O,H2O2与HNO3不反应且不考虑其分解。判断滴定到达终点的方法是
+6H+→2Mn2++5O2↑+8H2O,H2O2与HNO3不反应且不考虑其分解。判断滴定到达终点的方法是
您最近一年使用:0次
【推荐2】甲醇是一种新型的汽车动力燃料,工业上可通过CO和H2化合来制备甲醇。
(1)已知H2(g)、CO(g)、CH3OH(l)的燃烧热分别为285.8kJ/mol、283.0kJ/mol和726.5kJ/mol,则甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为___ 。
(2)某研究性学习小组在容积固定为2L的密闭容器内充入1molCO和2molH2,加入合适催化剂(体积可以忽略不计)后进行反应CO(g)+2H2(g)=CH3OH(g) ΔH<0。
①下列措施中有利于增大该反应的反应速率且提高转化率的是__ (填字母序号)
A.随时将CH3OH与反应混合物分离 B.降低反应温度
C.使用高效催化剂 D.增大体系压强
②实验过程中用压力计监测容器内压强的变化如下:
则从反应开始到20min时,以H2表示的平均反应速率=__ mol/(L·min),该温度下平衡常数k=__ 。
③若在恒温恒压条件下进行上述反应,达到平衡后,往体系中通入一定量的稀释剂(水蒸气),CO的转化率__ (填"增大"、"减小"或"不变")。
(3)现在容积均为1L的a、b、c三个密闭容器中分别充入1molCO和2molH2的混合气体,控制温度,进行反应,测得相关数据的关系如图所示。b中甲醇体积分数大于a中的原因是__ 。达到平衡时,a、b、c中CO的转化率大小关系为__ 。

(1)已知H2(g)、CO(g)、CH3OH(l)的燃烧热分别为285.8kJ/mol、283.0kJ/mol和726.5kJ/mol,则甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式为
(2)某研究性学习小组在容积固定为2L的密闭容器内充入1molCO和2molH2,加入合适催化剂(体积可以忽略不计)后进行反应CO(g)+2H2(g)=CH3OH(g) ΔH<0。
①下列措施中有利于增大该反应的反应速率且提高转化率的是
A.随时将CH3OH与反应混合物分离 B.降低反应温度
C.使用高效催化剂 D.增大体系压强
②实验过程中用压力计监测容器内压强的变化如下:
| 反应时间/min | 0 | 5 | 10 | 15 | 20 | 25 |
| 压强/MPa | 12.6 | 10.8 | 9.5 | 8.7 | 8.4 | 8.4 |
则从反应开始到20min时,以H2表示的平均反应速率=
③若在恒温恒压条件下进行上述反应,达到平衡后,往体系中通入一定量的稀释剂(水蒸气),CO的转化率
(3)现在容积均为1L的a、b、c三个密闭容器中分别充入1molCO和2molH2的混合气体,控制温度,进行反应,测得相关数据的关系如图所示。b中甲醇体积分数大于a中的原因是

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】二甲醚(CH3OCH3)重整制取H2,具有无毒、无刺激性等优点。回答下列问题:
(1) CH3OCH3和O2发生反应I:CH3OCH3(g)+1/2O2(g)=2CO(g)+3H2(g) △H
已知:CH3OCH3(g) CO(g)+H2(g)+CH4 (g) △H1
CO(g)+H2(g)+CH4 (g) △H1
CH4 (g)+3/2O2(g)=CO(g)+2H2O (g) △H2
H2(g)+1/2O2(g)=H2O (g) △H3
①则反应I的△H=____ (用含△H1、△H2、△H3的代数式表示)。
②保持温度和压强不变,分别按不同进料比通入CH3OCH3和O2,发生反应I。测得平衡时H2的体积百分含量与进料气中n(O2)/n(CH3OCH3)的关系如图所示。当n(O2)/n(CH3OCH3)>0.6时,H2的体积百分含量快速降低,其主要原因是____ (填标号)。

A.过量的O2起稀释作用
B.过量的O2与H2发生副反应生成H2O
C .n(O2)/n(CH3OCH3)>0.6平衡向逆反应方向移动
(2)T℃时,在恒容密闭容器中通入CH3OCH3,发生反应II:CH3OCH3(g) CO(g)+H2(g)+CH4(g),测得容器内初始压强为41.6 kPa,反应过程中反应速率v(CH3OCH3)时间t与CH3OCH3分压P(CH3OCH3)的关系如图所示。
CO(g)+H2(g)+CH4(g),测得容器内初始压强为41.6 kPa,反应过程中反应速率v(CH3OCH3)时间t与CH3OCH3分压P(CH3OCH3)的关系如图所示。
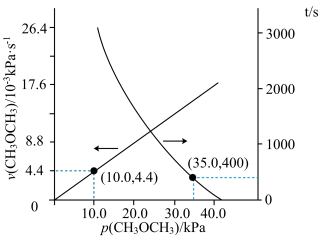
①t=400 s时,CH3OCH3的转化率为____ (保留2位有效数字);反应速率满足v(CH3OCH3)=kPn(CH3OCH3),k=_____ s-1;400 s时v(CH3OCH3)=_____ kPa.s-1。
②达到平衡时,测得体系的总压强P总= 121.6 kPa,则该反应的平衡常数Kp=________________ kPa2(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
③该温度下,要缩短达到平衡所需的时间,除改进催化剂外,还可采取的措施是____ ,其理由是____ 。
(1) CH3OCH3和O2发生反应I:CH3OCH3(g)+1/2O2(g)=2CO(g)+3H2(g) △H
已知:CH3OCH3(g)
 CO(g)+H2(g)+CH4 (g) △H1
CO(g)+H2(g)+CH4 (g) △H1CH4 (g)+3/2O2(g)=CO(g)+2H2O (g) △H2
H2(g)+1/2O2(g)=H2O (g) △H3
①则反应I的△H=
②保持温度和压强不变,分别按不同进料比通入CH3OCH3和O2,发生反应I。测得平衡时H2的体积百分含量与进料气中n(O2)/n(CH3OCH3)的关系如图所示。当n(O2)/n(CH3OCH3)>0.6时,H2的体积百分含量快速降低,其主要原因是

A.过量的O2起稀释作用
B.过量的O2与H2发生副反应生成H2O
C .n(O2)/n(CH3OCH3)>0.6平衡向逆反应方向移动
(2)T℃时,在恒容密闭容器中通入CH3OCH3,发生反应II:CH3OCH3(g)
 CO(g)+H2(g)+CH4(g),测得容器内初始压强为41.6 kPa,反应过程中反应速率v(CH3OCH3)时间t与CH3OCH3分压P(CH3OCH3)的关系如图所示。
CO(g)+H2(g)+CH4(g),测得容器内初始压强为41.6 kPa,反应过程中反应速率v(CH3OCH3)时间t与CH3OCH3分压P(CH3OCH3)的关系如图所示。
①t=400 s时,CH3OCH3的转化率为
②达到平衡时,测得体系的总压强P总= 121.6 kPa,则该反应的平衡常数Kp=
③该温度下,要缩短达到平衡所需的时间,除改进催化剂外,还可采取的措施是
您最近一年使用:0次



