法是工业上消除氮氧化物的常用方法,反应如下:
法是工业上消除氮氧化物的常用方法,反应如下:主反应:

副反应:

相同条件下,在甲、乙两种催化剂作用下进行上述反应,下列说法错误的是
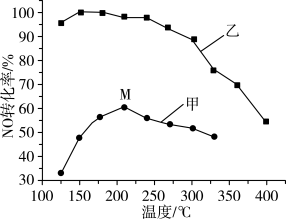
| A.工业上选择催化剂乙的原因是低温下有很强的催化活性 |
B.投料比一定时有利于提高 平衡转化率的反应条件是降低温度、减少压强 平衡转化率的反应条件是降低温度、减少压强 |
C.图中M点处(对应温度为210℃) 的转化率一定不是该温度下的平衡转化率 的转化率一定不是该温度下的平衡转化率 |
D.相同条件下选择高效催化剂,可以提高 的平衡转化率 的平衡转化率 |
2021·山东济宁·一模 查看更多[11]
山东省济宁市2021届高三3月模拟(一模)化学试题山东省济南市2021届高三4月阶段性检测化学试题(已下线)押山东卷第14题 化学反应速率和平衡-备战2021年高考化学临考题号押题(山东卷)(已下线)考点18 化学平衡状态 化学平衡移动-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点18 化学平衡状态 化学平衡移动-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)专题09 反应速率、化学平衡-备战2022年高考化学真题及地市好题专项集训【山东专用】(已下线)专题10 化学反应速率与化学平衡-备战2022年高考化学学霸纠错(全国通用)(已下线)考点22 化学平衡状态与化学平衡移动-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)考点25 化学反应速率与平衡图象-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第27练 化学平衡-2023年高考化学一轮复习小题多维练(全国通用)(已下线)考点25 化学反应速率与平衡图象(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)
更新时间:2021-03-12 09:09:05
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】对于平衡体系:aA(g)+bB(g) cC(g)+dD(g) △H<0,下列判断其中不正确的是
cC(g)+dD(g) △H<0,下列判断其中不正确的是
 cC(g)+dD(g) △H<0,下列判断其中不正确的是
cC(g)+dD(g) △H<0,下列判断其中不正确的是| A.若温度不变,容器体积扩大一倍,此时A的浓度是原来的0.45倍,则a+b<c+d |
| B.若从正反应开始,平衡时,A、B的转化率相等,则投入A、B的物质的量之比为a:b |
| C.若平衡体系中共有气体Mmol,再向其中充入bmolB,达到平衡时气体总物质的量为( M+b)mol,则a+b=c+d |
| D.若a+b=c+d,对于体积不变的容器,升高温度,平衡向左移动,容器中气体的压强不变 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】某科学家利用二氧化饰(CeO2)在太阳能作用下将H2O、CO2转变为H2、 CO,其过程如下所示:
mCeO2 (m-x)CeO2·xCe+xO2
(m-x)CeO2·xCe+xO2
(m-x)CeO2·xCe+x H2O+xCO2 mCeO2+xH2+xCO2
mCeO2+xH2+xCO2
下列说法不正确的是
mCeO2
 (m-x)CeO2·xCe+xO2
(m-x)CeO2·xCe+xO2(m-x)CeO2·xCe+x H2O+xCO2
 mCeO2+xH2+xCO2
mCeO2+xH2+xCO2下列说法不正确的是
| A.该过程中CeO2是H2O、CO2转变为H2、CO反应的催化剂 |
| B.利用CeO2作催化剂-既可使该转变过程速率提高。亦可减小能量的消 耗,并可提高反应物转化率 |
| C.mmol CeO2参加反应,气体物质的量增加x mol |
| D.以CO和O2构成的碱性燃料电池的负极反应式为CO+4OH - - 2e = CO32- +2H2O |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】气态醋酸中存在平衡:
 。实验测得压强分别
。实验测得压强分别 和
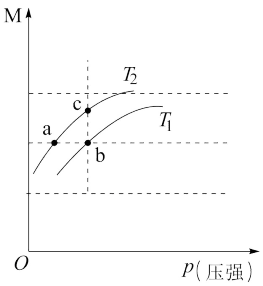
和 时,上述平衡体系中气体的平均摩尔质量(
时,上述平衡体系中气体的平均摩尔质量(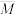 )随温度(T)的变化如下图所示。[已知:(
)随温度(T)的变化如下图所示。[已知:(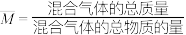 );
); ]
]
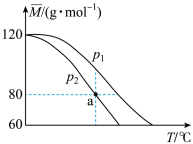
下列说法不正确 的是

 。实验测得压强分别
。实验测得压强分别 和
和 时,上述平衡体系中气体的平均摩尔质量(
时,上述平衡体系中气体的平均摩尔质量(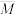 )随温度(T)的变化如下图所示。[已知:(
)随温度(T)的变化如下图所示。[已知:(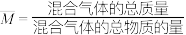 );
); ]
]
下列说法
A. |
B. |
C.a点时,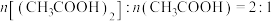 |
D.为了使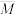 的值接近60,可采取高温、低压的实验条件 的值接近60,可采取高温、低压的实验条件 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】在恒容密闭容器中按物质的量之比 充入
充入 和
和 ,发生反应:
,发生反应: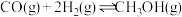 ,测得平衡混合物中
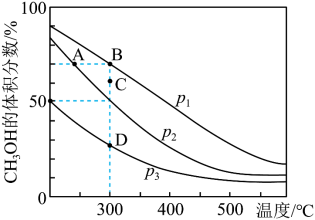
,测得平衡混合物中 的体积分数在不同压强下随温度的变化情况如图所示。下列说法正确的是
的体积分数在不同压强下随温度的变化情况如图所示。下列说法正确的是
 充入
充入 和
和 ,发生反应:
,发生反应: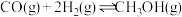 ,测得平衡混合物中
,测得平衡混合物中 的体积分数在不同压强下随温度的变化情况如图所示。下列说法正确的是
的体积分数在不同压强下随温度的变化情况如图所示。下列说法正确的是
A.该反应的 | B.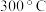 时,该反应的平衡常数 时,该反应的平衡常数 |
C.压强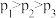 | D.压强为 、温度为 、温度为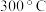 的条件下,C点 的条件下,C点 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列说法不能用勒夏特列原理解释的是
| A.滴有碘水的淀粉溶液中加入少量唾液,蓝色褪去 |
B.对于反应2NO2 N2O4加压稳定后的颜色比原来颜色深 N2O4加压稳定后的颜色比原来颜色深 |
| C.开启可乐瓶,瓶中马上泛起大量气泡 |
| D.利用排液法收集氯气时常用液体为饱和食盐水 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】CH4-CO2催化重整可以得到合成气(CO和H2),有利于减小温室效应,其主要反应为CH4(g)+CO2(g)⇌2CO(g)+2H2(g) ΔH=+247 kJ·mol−1,同时存在以下反应:积碳反应:CH4(g)⇌C(s)+2H2(g) ΔH=+75 kJ·mol−1,消碳反应:CO2(g)+C(s)⇌2CO(g) ΔH=+172 kJ·mol−1,积碳会影响催化剂的活性,一定时间内积碳量和反应温度的关系如图。下列说法正确的是
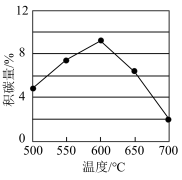

| A.高压利于提高CH4的平衡转化率并减少积碳 |
| B.增大CO2与CH4的物质的量之比有助于减少积碳 |
| C.升高温度,积碳反应的化学平衡常数K减小,消碳反应的K增大 |
| D.温度高于600℃,积碳反应的化学反应速率减慢,消碳反应的化学反应速率加快,积碳量减少 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】列实验方案设计、现象和结论都正确的是
| 目的 | 实验方案设计 | 现象和结论 | |
| A | 探究压强对平衡的影响 | 在针筒中充入一定量的NO2气体,压缩针筒,从针简顶部观察到气体颜色变浅 | 压强增大,平衡向气体体积减小的方向移动 |
| B | 探究浓度对平衡移动的影响 | 向K2Cr2O7溶液中缓慢滴加浓盐酸,黄色变为橙色 | 增大c(H+),平衡向生成 的方向移动 的方向移动 |
| C | 检验某溶液中是否含有Fe2+离子 | 向该溶液中滴加几滴新制氯水, 振荡,再加入少量KSCN溶液 | 溶液变为血红色,则该溶液中含有Fe2+离子 |
| D | 检验乙醇中是否含有水 | 向乙醇中加入一小粒金属钠,产生无色气体 | 乙醇中含有水 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列图示与对应叙述不相符合的是
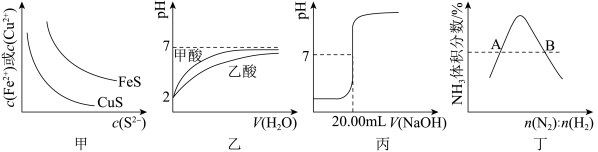

A.图甲表示一定温度下 和 和 的沉淀溶解平衡曲线,则 的沉淀溶解平衡曲线,则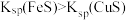 |
B.图乙表示 的甲酸溶液与乙酸溶液稀释时的 的甲酸溶液与乙酸溶液稀释时的 变化曲线,则酸性:甲酸>乙酸 变化曲线,则酸性:甲酸>乙酸 |
C.图丙表示用 溶液滴定 溶液滴定 盐酸的滴定曲线,则 盐酸的滴定曲线,则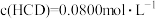 |
D.图丁表示反应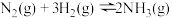 平衡时 平衡时 体积分数随起始 体积分数随起始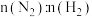 变化的曲线,则 变化的曲线,则 转化率: 转化率: |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】在20 L的密闭容器中按物质的量之比1∶2充入CO和H2,发生:CO(g)+2H2(g)  CH3OH(g) ΔH。测得CO的转化率随温度的变化及不同压强下CO转化率的变化、p2和195 ℃时n(H2)随时间的变化结果如图表所示。下列说法正确的是( )
CH3OH(g) ΔH。测得CO的转化率随温度的变化及不同压强下CO转化率的变化、p2和195 ℃时n(H2)随时间的变化结果如图表所示。下列说法正确的是( )
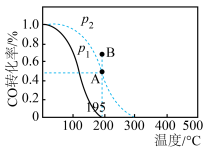
p2和 195℃时,n(H2)
 CH3OH(g) ΔH。测得CO的转化率随温度的变化及不同压强下CO转化率的变化、p2和195 ℃时n(H2)随时间的变化结果如图表所示。下列说法正确的是( )
CH3OH(g) ΔH。测得CO的转化率随温度的变化及不同压强下CO转化率的变化、p2和195 ℃时n(H2)随时间的变化结果如图表所示。下列说法正确的是( )
p2和 195℃时,n(H2)
| t/min | 0 | 1 | 3 | 5 |
| n(H2)/mol | 8 | 5 | 4 | 4 |
| A.0~3 min,平均速率v(CH3OH)=0.8 mol·L-1·min-1 |
| B.p1<p2,ΔH>0 |
| C.在p2和195 ℃时,该反应的平衡常数为25( mol·L-1)-2 |
| D.在B点时,v正>v逆 |
您最近一年使用:0次


 C(g)+3D(g))
C(g)+3D(g)) )在不同温度下随压强的变化曲线如图所示。下列说法正确的
)在不同温度下随压强的变化曲线如图所示。下列说法正确的